
- •Тема 1.1. Основні закони хімії
- •Закон збереження маси речовини
- •Контрольні запитання:
- •Тема 1.2. Оксиди
- •Визначення. Класифікація оксидів.
- •Контрольні запитання:
- •Тема 1.3. Основи
- •Визначення. Класифікація основ.
- •Контрольні запитання:
- •Тема 1.4. Кислоти
- •Визначення. Класифікація кислот.
- •Контрольні запитання:
- •Тема 1.5. Солі
- •Визначення. Класифікація солей.
- •Контрольні запитання:
- •Тема 1.6. Хімічний зв'язок
- •Поняття про хімічний зв'язок. Типи хімічного зв’язку.
- •Контрольні запитання:
- •Тема 1.7. Електролітична дисоціація. Реакції йонного обміну
- •Контрольні запитання:
- •Тема 1.8. Окисно-відновні реакції
- •Контрольні запитання:
- •Тема 2.1. Загальна характеристика металів
- •Контрольні запитання:
- •Тема 2.2. Корозія металів
- •Корозія металів. Види корозії.
- •Контрольні запитання:
- •Тема 2.3. Лужні метали
- •Контрольні запитання:
- •Тема 2.4. Кальцій
- •Кальцій.**
- •Контрольні запитання:
- •Тема 2.5. Сполуки Кальцію
- •Контрольні запитання:
- •Тема 2.6. Алюміній
- •Контрольні запитання:
- •Тема 2.7. Залізо
- •Контрольні запитання:
- •Тема 2.8. Сульфур. Сірка.
- •Контрольні запитання:
- •Тема 2.9. Сполуки Сульфуру
- •Контрольні запитання:
- •Тема 2.10. Сульфатна кислота та її солі
- •Контрольні запитання:
- •Тема 2.11. Нітроген. Азот.
- •Контрольні запитання:
- •Тема 2.12. Аміак. Солі амонію.
- •Контрольні запитання:
- •Тема 2.13. Сполуки Нітрогену
- •Контрольні запитання:
- •Тема 2. 14.Фосфор
- •Фосфор.
- •Контрольні запитання:
- •Тема 2.15. Сполуки Фосфору
- •Контрольні запитання:
- •Тема 2.16. Карбон. Вуглець.
- •Контрольні запитання:
- •Тема 2.16. Сполуки Карбону
- •Контрольні запитання:
- •Тема 2.18. Силіцій.
- •Контрольні запитання:
- •Тема 2.19. Сполуки Силіцію.
- •Контрольні запитання:
- •Тема 3.1. Теорія будови органічних речовин о.М. Бутлерова
- •Контрольні запитання:
- •Тема 3.2. Алкани
- •Контрольні запитання:
- •Тема 3.3. Алкени
- •Контрольні запитання:
- •Тема 3.4. Алкіни
- •Контрольні запитання:
- •Тема 3.5. Алкадієни (дієнові вуглеводні)
- •Контрольні запитання:
- •Тема 3.6. Ароматичні вуглеводні (арени)
- •Контрольні запитання:
- •Тема 3.7. Природні джерела вуглеводнів
- •Контрольні запитання:
- •Тема 4.1. Одноатомні спирти
- •Контрольні запитання:
- •Тема 4.2. Багатоатомні спирти
- •Контрольні запитання:
- •Тема 4.3. Феноли
- •Контрольні запитання:
- •Тема 4.4. Альдегіди
- •Контрольні запитання:
- •Тема 4.5. Карбонові кислоти
- •Контрольні запитання:
- •Тема 4.6. Естери
- •2. Номенклатура:
- •Контрольні запитання:
- •Тема 4.7. Жири. Мило
- •Контрольні запитання:
- •Тема 5.1. Вуглеводи. Глюкоза
- •Контрольні запитання:
- •Тема 5.2. Сахароза
- •Контрольні запитання:
- •Тема 5.3. Крохмаль і целюлоза
- •Контрольні запитання:
- •Тема 5.4. Аміни
- •Контрольні запитання:
- •Тема 5.5. Амінокислоти
- •Контрольні запитання:
- •Тема 5.6. Білки
- •Контрольні запитання:
Контрольні запитання:
-
Які органічні речовини називаються карбоновими кислотами?
-
Як проявляється взаємний вплив атомів в молекулі кислоти?
-
Які хімічні реакції характерні для карбонових кислот?
-
Які особливості будови і властивостей мурашиної кислоти?
-
Скільки грамів мурашиної кислоти потрібно для повної нейтралізації 20 г розчину лугу з масовою часткою натрій гідроксиду 20%?
-
Яку масу етилетаноату можна добути з 120 г оцтової кислоти ї 115 г етанолу, якщо масова частку виходу продукту реакції складає 90% від теоретично можливого?
Література:
-
Данильченко В.Є., Фрадіна Н.В. Хімія. 10 – 11 класи: Навч. посібник. – Х.: Країна мрій™, 2003. - с. 121-122.
-
Хомченко Г.П. Химия. – М.: Высшая школа, 1981. – Ч. ІІІ, Гл. 17, §§ 150-151, с. 154-157.
-
Стахеєв О.Ю. Хімія. Узагальнюючі схеми і таблиці. – Тернопіль.: «Богдан», 1998. – с. 42.
-
Березан О.В. Органічна хімія. – К.: Абрис, 2000. – Р. VІ, §§ 1-6, с. 138-145.
Тема 4.6. Естери
План
-
Визначення та загальна формула класу.
-
Номенклатура.*
-
Ізомерія.*
-
Фізичні властивості.
-
Хімічні властивості.**
-
Добування.*
-
Застосування.
1. Естери (складні ефіри) - це похідні спиртів і карбонових кислот
Загальна формула естерів: R–C=O
|
ОR'
де R–C=O – залишок кислоти, – ОR' – залишок спирту
|
2. Номенклатура:
1) спирт + кислота («ова» → «оат»)
О
||
СН3−С−О–СН3 метилетаноат
2) тривіальна назва
О
||
СН3−С−О–СН3 метиловий естер оцтової кислоти
3. а) Структурна ізомерія карбонового скелета
б) Ізомерія з карбоновими кислотами:
О
||
С2Н5−СООН СН3−С−О–СН3
пропанова кислота метилетаноат
4. Леткі рідини (відсутність водневих зв’язків), малорозчинні у воді, добре розчинні в органічних розчинниках. Мають приємний запах.
5. Хімічні властивості:
І. Гідроліз (реакція каталізується протонами Н+ та гідроксид йонами ОН-):
СН3СООСН3 + Н2О → СН3СООН + СН3ОН
СН3СООСН3 + NaOH → СН3СООNa + СН3ОН
ІІ. Гідрування:
СН3СООСН3 + 2Н2 → С2Н5ОН + СН3ОН
6. Добування: реакція етерифікації
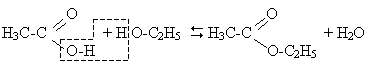
7. Застосування: 1) як розчинник лаків і фарб;
2) для виготовлення штучних фруктових есенцій;
3) у виробництві парфумів;
4) деякі – у виготовленні полімерів (оргскло);
5) виробництво СМЗ і вибухових речовин;
6) у виготовленні штучних волокон (лавсан).
Контрольні запитання:
-
Які органічні речовини називаються естерами?
-
Які види ізомерії характерні для естерів?
-
Які хімічні реакції характерні для скалдних ефірів?
-
Дайте визначення реакції естерифікації.
-
Яку масу оцтової ксилоти можна добути при повному гідролізі пропілацетату масою 120г?
-
Під час нагрівання метанолу масою 2,4 г і оцтової кислоти масою 3,6 г добули метилацетат масою 3,7 г. Визначити вихд естеру.
Література:
-
Данильченко В.Є., Фрадіна Н.В. Хімія. 10 – 11 класи: Навч. посібник. – Х.: Країна мрій™, 2003. - с. 132-133.
-
Хомченко Г.П. Химия. – М.: Высшая школа, 1981. – Ч. ІІІ, Гл. 17, § 152, с. 157-158.
-
Стахеєв О.Ю. Хімія. Узагальнюючі схеми і таблиці. – Тернопіль.: «Богдан», 1998. – с. 43.
-
Березан О.В. Органічна хімія. – К.: Абрис, 2000. – Р. VІІ, § 1, с. 152-153.
