
- •Тема 1.1. Основні закони хімії
- •Закон збереження маси речовини
- •Контрольні запитання:
- •Тема 1.2. Оксиди
- •Визначення. Класифікація оксидів.
- •Контрольні запитання:
- •Тема 1.3. Основи
- •Визначення. Класифікація основ.
- •Контрольні запитання:
- •Тема 1.4. Кислоти
- •Визначення. Класифікація кислот.
- •Контрольні запитання:
- •Тема 1.5. Солі
- •Визначення. Класифікація солей.
- •Контрольні запитання:
- •Тема 1.6. Хімічний зв'язок
- •Поняття про хімічний зв'язок. Типи хімічного зв’язку.
- •Контрольні запитання:
- •Тема 1.7. Електролітична дисоціація. Реакції йонного обміну
- •Контрольні запитання:
- •Тема 1.8. Окисно-відновні реакції
- •Контрольні запитання:
- •Тема 2.1. Загальна характеристика металів
- •Контрольні запитання:
- •Тема 2.2. Корозія металів
- •Корозія металів. Види корозії.
- •Контрольні запитання:
- •Тема 2.3. Лужні метали
- •Контрольні запитання:
- •Тема 2.4. Кальцій
- •Кальцій.**
- •Контрольні запитання:
- •Тема 2.5. Сполуки Кальцію
- •Контрольні запитання:
- •Тема 2.6. Алюміній
- •Контрольні запитання:
- •Тема 2.7. Залізо
- •Контрольні запитання:
- •Тема 2.8. Сульфур. Сірка.
- •Контрольні запитання:
- •Тема 2.9. Сполуки Сульфуру
- •Контрольні запитання:
- •Тема 2.10. Сульфатна кислота та її солі
- •Контрольні запитання:
- •Тема 2.11. Нітроген. Азот.
- •Контрольні запитання:
- •Тема 2.12. Аміак. Солі амонію.
- •Контрольні запитання:
- •Тема 2.13. Сполуки Нітрогену
- •Контрольні запитання:
- •Тема 2. 14.Фосфор
- •Фосфор.
- •Контрольні запитання:
- •Тема 2.15. Сполуки Фосфору
- •Контрольні запитання:
- •Тема 2.16. Карбон. Вуглець.
- •Контрольні запитання:
- •Тема 2.16. Сполуки Карбону
- •Контрольні запитання:
- •Тема 2.18. Силіцій.
- •Контрольні запитання:
- •Тема 2.19. Сполуки Силіцію.
- •Контрольні запитання:
- •Тема 3.1. Теорія будови органічних речовин о.М. Бутлерова
- •Контрольні запитання:
- •Тема 3.2. Алкани
- •Контрольні запитання:
- •Тема 3.3. Алкени
- •Контрольні запитання:
- •Тема 3.4. Алкіни
- •Контрольні запитання:
- •Тема 3.5. Алкадієни (дієнові вуглеводні)
- •Контрольні запитання:
- •Тема 3.6. Ароматичні вуглеводні (арени)
- •Контрольні запитання:
- •Тема 3.7. Природні джерела вуглеводнів
- •Контрольні запитання:
- •Тема 4.1. Одноатомні спирти
- •Контрольні запитання:
- •Тема 4.2. Багатоатомні спирти
- •Контрольні запитання:
- •Тема 4.3. Феноли
- •Контрольні запитання:
- •Тема 4.4. Альдегіди
- •Контрольні запитання:
- •Тема 4.5. Карбонові кислоти
- •Контрольні запитання:
- •Тема 4.6. Естери
- •2. Номенклатура:
- •Контрольні запитання:
- •Тема 4.7. Жири. Мило
- •Контрольні запитання:
- •Тема 5.1. Вуглеводи. Глюкоза
- •Контрольні запитання:
- •Тема 5.2. Сахароза
- •Контрольні запитання:
- •Тема 5.3. Крохмаль і целюлоза
- •Контрольні запитання:
- •Тема 5.4. Аміни
- •Контрольні запитання:
- •Тема 5.5. Амінокислоти
- •Контрольні запитання:
- •Тема 5.6. Білки
- •Контрольні запитання:
Контрольні запитання:
-
Які органічні речовини називаються вуглеводами? Загальна формула вуглеводів.
-
Як класифікують вуглеводи за здатністю до гідролізу?
-
Яка молекулярна, структурна (альдегідна, циклічна) формули глюкози?
-
Як довести наявність в глюкозі альдегідної групи та декількох гідроксильних груп?
-
Обчисліть масу глюкози, добутої з 50 г крохмалю, масова частка домішок в якому складає 20%.
Література:
-
Данильченко В.Є., Фрадіна Н.В. Хімія. 10 – 11 класи: Навч. посібник. – Х.: Країна мрій™, 2003. - с. 138-140.
-
Хомченко Г.П. Химия. – М.: Высшая школа, 1981. – Ч. ІІІ, Гл. 17, § 155, с. 159-161.
-
Березан О.В. Органічна хімія. – К.: Абрис, 2000. – Р. VІІІ, §§ 1-3, с. 171-174.
Тема 5.2. Сахароза
План
-
Склад та будова сахарози.*
-
Фізичні властивості та поширення в природі.
-
Хімічні властивості.**
-
Загальна схема добування цукру.
-
Застосування.
1. Молекулярна формула глюкози – С12Н22О11
С кладається
із залишків циклічної α-глюкози і
фруктози. Має гідроксогрупи і не має
альдегідних та кетонних груп.
кладається
із залишків циклічної α-глюкози і
фруктози. Має гідроксогрупи і не має
альдегідних та кетонних груп.
2. Сахароза - безбарвна кристалічна речовина, добре розчинна у воді, солодка на смак; розплавлена сахароза (tпл = 160ºС) утворює аморфну прозору масу - карамель.
Міститься у багатьох рослинах, здебільшого в їхніх плодах, а також у березовому і кленовому соках. Входить до складу соку цукрового буряку (16 – 20%) та цукрової тростини (14 – 26%).
3. Хімічні властивості:
Н+, tº
1) Гідроліз: С12Н22О11 + Н2О——→ С6Н12О6 + С6Н12О6
глюкоза фруктоза
2) Взаємодія з купрум (ІІ) гідроксидом:
![]()
tº
3) горіння: С12Н22О11 + 12О2 → 12СО2 + 11Н2О
4.
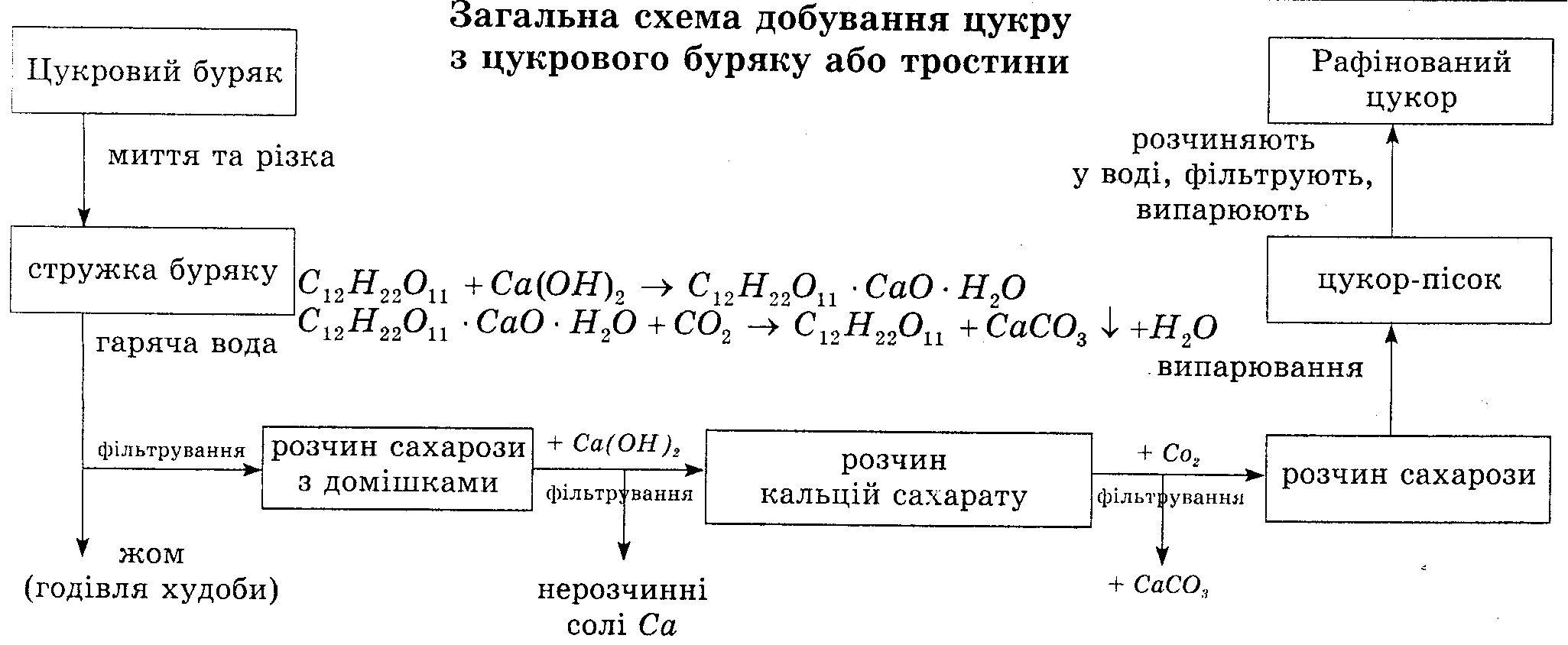
5. Застосування: 1) харчовий продукт;
2) як пластифікатор у виробництві пластмас;
3) для виготовлення деяких ліків, мікстур, сиропів.
Контрольні запитання:
-
Які вуглеводи називаються дисахаридами?
-
Яка молекулярна та структурна формули сахарози?
-
Які хімічні властивості сахарози?
-
Знайдіть масову частку глюкози в розчині, що містить 280 г води та 40 г глюкози.
-
Знайдіть масу сахарози, яку піддали гідролізу, якщо при взаємодії продукту гідролізу з амоніачним розчином аргентум(І) оксиду виділилося 10,8 г срібла?
Література:
-
Данильченко В.Є., Фрадіна Н.В. Хімія. 10 – 11 класи: Навч. посібник. – Х.: Країна мрій™, 2003. - с. 140.
-
Хомченко Г.П. Химия. – М.: Высшая школа, 1981. – Ч. ІІІ, Гл. 17, § 155, с. 161.
-
Березан О.В. Органічна хімія. – К.: Абрис, 2000. – Р. VІІІ, § 4, с. 174-175.
Тема 5.3. Крохмаль і целюлоза
План
-
Склад та будова молекул.*
-
Фізичні властивості та поширення в природі.
-
Хімічні властивості.**
-
Застосування.
1. Молекулярна формула крохмалю та целюлози – (С6Н10О5)n. У крохмалі і целюлозі молекули мономерів сполучені в молекули полімерів за допомогою оксигенових містків.
К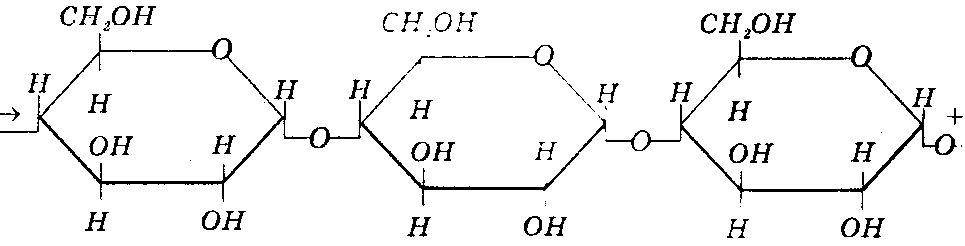 рохмаль
складається з залишків циклічної
α-глюкози. Має досить розгалужену
структуру; значення n
– від сотень до 5000.
рохмаль
складається з залишків циклічної
α-глюкози. Має досить розгалужену
структуру; значення n
– від сотень до 5000.
Ц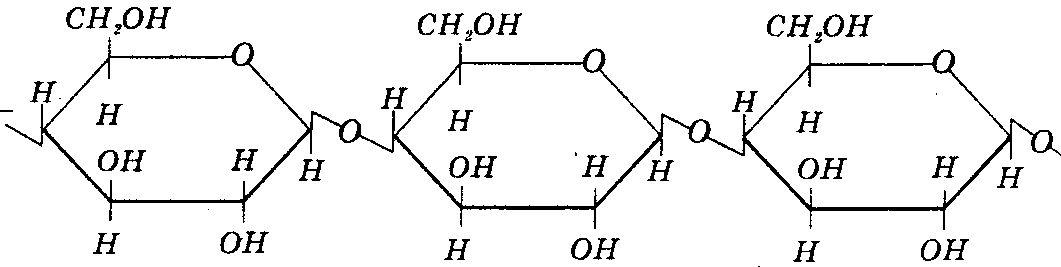 елюлоза
(клітковина)
складається з залишків циклічної
β-глюкози. Має переважно лінійну
структуру; значення n
–до 40000.
елюлоза
(клітковина)
складається з залишків циклічної
β-глюкози. Має переважно лінійну
структуру; значення n
–до 40000.
2. Крохмаль – білий аморфний порошок, не розчиняється в холодній воді, а в гарячій набухає і утворює колоїдний розчин (клейстер). Утворюється в процесі фотосинтезу в листках рослин, відкладається у бульбах, у коренях, зерні.
Целюлоза – біла волокниста речовина, нерозчинна ні у воді, ні в органічних розчинниках; не плавиться, але при 350о обвуглюється. Утворюється в процесі фотосинтезу. Є основною складовою частиною оболонок рослинних клітин. Найбільше її у волокнах бавовни, льону та коноплі.
3. Хімічні властивості:
Н+ , tº
1) Гідроліз: (С6Н10О5)n + nН2О ——→ nС6Н12О6
глюкоза
(С6Н10О5)n ——→ (С6Н10О5)m ——→С12Н22О11 ——→ С6Н12О6
крохмаль декстрини мальтоза глюкоза
2) Повне окиснення:
tº
(С6Н10О5)n + 6nО2 → 6n СО2 + 5nН2О
3) Целюлоза і крохмаль завдяки наявності в їхніх молекулах спиртових гідроксильних груп з кислотами утворюють естери (ефіри крохмалю не мають практичного значення):
[C6H7O2(OH)3]n +3nHNO2→ [C6H7O2(ONO2)3]n + 3nH2O
тринітроцелюлоза
4) Якісна реакція на крохмаль – взаємодія з йодом: крохмаль + I2 → синє забарвлення
4. Крохмаль: 1) харчовий продукт;
2) для одержання патоки (суміші декстринів з глюкозою);
3) для приготування клею, обробки тканин;
4) у виробництві етанолу;
5) у медицині при виготовленні мазей, присипки.
Целюлоза: 1) у складі деревини – у будівництві;
2) у складі волокон – для виготовлення тканин, ниток;
3) виготовлення паперу;
4) у виробництві етанолу, а з нього каучуку;
5) ефіри використовують для виробництва штучних волокон, кіноплівки,
нітролаків, пороху.
