
- •Міністерство освіти і науки України
- •1. Властивості порошків
- •1.1. Хімічні властивості
- •1.2. Фізичні властивості
- •Методи визначення розміру частинок
- •1.3. Технологічні властивості
- •2. Механічні методи отримання порошків
- •2.1. Загальні положення
- •2.2. Характеристика обладнання для подрібнення
- •Він пропонує у цьому виразі замінити поточні напруги на межу міцностіматеріалу, що дозволить визначити роботу, яка виконується під час подрібнення матеріалу об’ємомза один цикл. Ця робота дорівнює:
- •Витрати роботи залежно від етапу руйнування
- •2.4. Вплив рідин та пар на процес подрібнення матеріалів
- •3. Отримання порошків розпиленням розплавів
- •3.1. Загальні положення
- •Математично залежності можна описати емпіричним рівнянням
- •Значення критеріїв Re та Lp для різних умов розпилення
- •3.2. Вплив різних факторів на процес розпилення розплавів газами
- •Гранулометричний склад порошку заліза, одержаного розпиленнямрозплавів сплавів заліза
- •Поверхневий натяг розплавів заліза з киснем, азотом, сіркою та фосфором
- •Коефіцієнт тепловіддачі конвекцією можна визначити за виразом
- •Теплофізичні властивості газів
- •3.3. Розпилення рідиною
- •Значення коефіцієнта тепловіддачі для умов розпилення розплавів водою
- •3.4. Формування складу і структури порошків під час розпилення розплавів
- •3.5. Технологічні особливості отримання порошків розпиленням
- •Режими одержання порошків розпиленням
- •4. Отримання порошків металів і сплавів відновленням з оксидів та інших сполук
- •4.1. Основи термодинаміки відновлювальних процесів
- •4.2. Механізм і кінетика відновлювальних процесів.
- •4.3. Закономірності отримання порошків металів їх
- •4.4.1. Отримання металів відновленням
- •Оксиди відновлюють відповідно до принципу послідовності
- •4.4.2. Магнієтермічне відновлення солей металів
- •4.4.3. Натрієтермічне відновлення солей металів
- •4.5. Отримання порошків сплавів
- •4.5.1. Сумісне відновлення оксидів металів воднем
- •Константи рівноваги
- •4.5.2. Сумісне відновлення сумішів оксидів і металевих порошків
- •4.5.3. Метод термодифузійного насичення з точкових джерел
- •1100 С (протягом 6 год) від їх умісту у вихідній шихті:
- •4.6. Технологічні основи отримання порошків металів та сплавів
- •Відновлення
- •5.1.2. Вплив різноманітних чинників на властивості порошків металів під час їх отримання електролізом водних
- •5.1.3. Особливості отримання порошків сплавів
- •5.1.4. Технологічні основи отримання порошків металів електролізом водних розчинів їх солей
- •11 _ Діафрагма
- •5.2. Електроліз розплавлених середовищ
- •5.2.1. Технологічні основи отримання порошків металів електролізом розплавлених середовищ
- •5.3. Автоклавний метод отримання порошків
- •5.4. Отримання порошків цементацією
- •5.5. Отримання порошків міжкристалевою корозією
- •6. Газові методи отримання порошків
- •6.1. Дисоціація карбонілів
- •7. Отримання порошків безкисневих тугоплавких сполук
- •7.1. Властивості та застосування безкисневих
- •Властивості тугоплавких сполук
- •7.2. Отримання порошків карбідів
- •Фази кінцевого продукту
- •Склад карбідів, одержаних методом свс
- •Характеристики карбіду титану отриманогометодомСвс
- •Умови осадження карбідів з газової фази
- •7.3. Отримання порошків нітридів
- •Умови отримання і склад нітридів, одержаних азотизацією металів
- •Умови осадження нітридів з газової фази
- •7.4. Отримання порошків боридів
- •7.5. Отримання порошків силіцидів
- •Температурні режими отримання силіцидів осадженням з газової фази
- •7.6. Отримання порошків неметалевих тугоплавких сполук
- •Газоподібний утворюваний силіцій, взаємодіючи з вуглецем, утворює силіцію
- •7.7. Отримання порошків литих тугоплавких сполук
- •Вихідні матеріали
- •Хімічний склад плавлених карбідів титана
- •Властивості плавлених карбідів
- •8. Отримання волокон та вусів
- •8.2. Методи отримання волоконта вусів
Умови отримання і склад нітридів, одержаних азотизацією металів
(1 – розрахунковий вміст елементів; 2 – отриманий вміст елементів)
|
Нітрид |
Умови синтезу |
Уміст, % | ||||
|
Температура, ºС |
Тривалість витримки, год |
Ме |
N | |||
|
1 |
2 |
1 |
2 | |||
|
TiN |
1200 |
2...6 |
77,35 |
77,5 |
22,65 |
22,2 |
|
ZrN |
1200 |
1...2 |
86,69 |
86,5 |
13,31 |
13,2 |
|
ZrN |
1400 |
2...4 |
86,69 |
86,80 |
13,31 |
11,8 |
|
HfN |
1200 |
1..2 |
92,78 |
92,85 |
7,28 |
7,1 |
|
VN |
1200 |
3...4 |
78,50 |
78,20 |
21,50 |
20,3 |
|
W3N |
900 |
1 |
90,70 |
90,60 |
9,30 |
8,60 |
|
NbN |
1200 |
3 |
86,90 |
86,90 |
13,10 |
13,10 |
|
Nb2N |
900 |
0,5...1,0 |
92,80 |
97,82 |
3,02 |
6,60 |
|
TaN |
1200 |
1...2 |
92,88 |
92,60 |
7,19 |
7,30 |
|
CrN |
900 |
1...2 |
78,30 |
78,60 |
21, 70 |
21,00 |
|
Cr2N |
1200...1300 |
6 |
88,13 |
88,00 |
11,87 |
11,95 |
|
Mo2N* |
700 |
4 |
- |
- |
- |
- |
|
W2N |
500 |
0,1...1,0 |
- |
- |
- |
- |
* У разі отримання в середовищі аміаку.
Перспективним синтезом нітридів з елементів є метод СВС, суть якого було розглянуто стосовно отримання карбідів. Апаратурне оформлення процесу отримання нітридів аналогічно отриманню карбідів. Як вихідні матеріали використовують зазвичай дисперсні порошки металів і газоподібний азот. При цьому тиск азоту може змінюватися в межах 1...2 ГПа. Наявність одного з реагентів у газоподібному стані дозволяє віднести процес синтезу нітридів до горіння фільтрації. Газ, що реагуює, до зони горіння надходить мимовільно за рахунок різниці тисків у фронті горіння і навколишньому середовищі. Горіння фільтрації складніший тип горіння за СВС, ніж безгазовий. Для його здійснення необхідно дотримувати ряд умов. Це, перш за все, збереження досить високої газопроникності компонента в твердому стані та утвореного в процесі горіння продукту, що необхідно для забезпечення доставляння газоподібного азоту до фронту горіння. Крім того, як і в разі синтезу карбідів, дуже важливо запобігти тепловідведенню в навколишнє середовище.
Одна з найважливіших особливостей горіння фільтрації — наявність двох стадій процесу відповідно до нерівноважної адіабатичної структури хвилі синтезу (рис. 7.6). Під час синтезу нітридів завжди наявні зони горіння і догоряння — об’ємного дореагування шихти, розігрітої хвилею горіння. Наявність двох стадій процесу отримання нітридів зумовлено тим, що спочатку нітрид утворюється на поверхні частинок у вигляді щільної захисної плівки, що перешкоджає дифузійному проникненню азоту вглиб частинки металу, що сильно гальмує процес і призводить до недогоряння. Для отримання в цьому випадку однофазних кінцевих продуктів необхідно забезпечити повноту проходження процесу на стадії догоряння. Труднощі, пов’язані з механізмом фільтрації горіння, особливо характерні для процесів отримання високоазотованих продуктів, коли в зоні горіння майже завжди відчувається брак азоту. Для забезпечення умов синтезу нітридів потрібно застосовувати м’якші режими. Це досягається введенням до складу вихідного порошку металу порошку однойменного нітриду (10...50 %) для зниження температури процесу СВС нітридів перехідних металів, що має не перевищувати 2000 °С.
За оптимальних умов проведення СВС нітридів відбувається повне перетворення вихідних речовин у кінцеві. При цьому кількість непрореагованого матеріалу зазвичай не перевищує 0,01...0,20 %. Ступінь чистоти одержуваних продуктів визначається ступенем чистоти вихідних компонентів, оскільки забруднення в процесі синтезу не відбувається. Основна домішка в нітридах ― кисень, уміст якого в деяких випадках може досягати 0,5 %. Склади деяких нітридів, одержуваних методом СВС, наведено в табл. 7.8.
Для виробництва нітридів дедалі більшого застосування набуває метод плазмохімічного синтезу. Як вихідні речовини при цьому використовують порошки металів, їх галогеніди, оксиди, які вводять або безпосередньо в зону розряду, або у високотемпературний струмінь плазми поза зоною розряду. При цьому процес синтезу нітридів спрощується, оскільки азот, будучи плазмоутворювальним газом, одночасно є і компонентом реакції утворення нітридів. Серед газів, використовуваних як плазмоутворювачі (Аг, Не, Н2, N2, О2), азот має найбільшу питому теплоту згоряння в такому самому інтервалі температур, який підтримують при плазмохімічному синтезі (рис. 7.9). У цьому ж інтервалі температур основний компонент азотної плазми ― це переважно атомарний азот, чим і визначається його висока хімічна активність.
Таблиця 7.8
Склад нітридів, одержаних методом СВС
|
Нітрид
|
Уміст, %
| |||
|
Ме |
N
| |||
|
Розрахунковий
|
Практичний
|
Практичний
|
Практичний
| |
|
TiN ZrN HfN NbN ТаN
|
77,30 86,69 92,73 86,91 92,92
|
77,1 87,5 92,1 87.2 92,2
|
22,62 13,31 7,24 13,09 7,18
|
21,7 12,8 7,2 12,9 7,3
|
В основі процесу утворення нітридів згідно з плазмохімічним методом синтезу, як і в разі отримання їх іншими методами, лежить дифузія азоту вглиб частинок металу. При цьому макроскопічність частинок призводить до зменшення ступеня насичення азотом. Оскільки в умовах дугового розряду швидкості плазмових струменів високі, дифузія не відбувається до кінця, наслідком чого є зазвичай утворення сполук нестехіометричного складу і наявність в кінцевих продуктах вихідних металів, що не прореагували.
Як вихідні матеріали доцільно використовувати галогеніди металів, зокрема хлориди. Якщо вводяться хлориди в плазмовий струмінь, вони розкладаються, утворюючи найдрібніші частинки металів або їх пари. Нітриди утворюються з газової фази в разі взаємодії пари металу з азотом. У результаті розміри утворюваних частинок продукту дорівнюють десяткам нанометрів. Так, наприклад, у разі взаємодії тетрахлориду титану з азотною плазмою можна одержати нітрид титану, склад якого близький до стехіометричного, розмір частинок становить 30 нм, а питома поверхня — 45 м2/г. У процесі його отримання досягається ступінь перетворення хлориду 100 %, а вихід готового продукту становить 98 %.
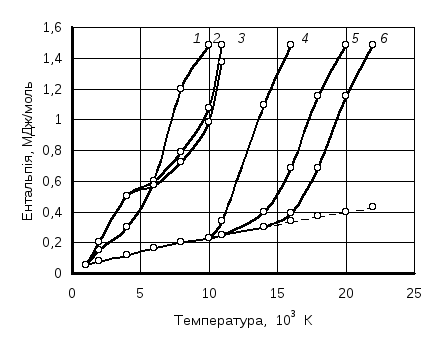
Рис. 7.9. Температурна залежність ентальпії Н деяких газів:
1 – N2; 2 – O2; 3 – Н2; 4 – Аг; 5 – Кг; 6 – Не
Отримання нітридів відновленням оксидів металів твердим відновником у середовищі азоту. Основою процесу є реакція
МеО + Ме (Х) + N2 МеN + МеО (ХО),
де Ме — метал-відновник; Х — неметалевий відновник (вуглець, силіцій, бор).
Найчастіше як відновник використовують вуглець, що разом з утворенням нітридів утворює карбіди відновлюваних металів як неперервний ряд твердих розчинів. Тому цей метод застосовують здебільшого для отримання нітридів технічної чистоти – зазвичай нітридів титану, цирконію, ванадію, ніобію і гафнію.
Для зменшення вмісту вуглецю в одержуваному продукті процес належить провадити за максимально можливих низьких температур, що знижує імовірність утворення карбідів.
На швидкість процесу отримання нітридів істотно впливає газопроникність ущільненої шихти залежно від розміру пор і геометричної форми брикетів. Реакції відновлення з подальшою азотизацією перебігають, головним чином, усередині пор шихти. Тому важливе значення має швидкість відведення із зони реакції СО і доставляння у зворотному напрямі азоту. Якщо швидкість циркуляції цих газів перевищить швидкість реакції утворення нітридів, то процес лімітуватиметься останнім. Уповільнення швидкості відведення оксиду вуглецю із зони реакції зумовить підвищення його парціального тиску в порах і зниження тиску азоту, що, у свою чергу, призведе до утворення карбідів, а отже, й до забруднення продукту вуглецем.
Оптимальні режими отримання нітридів грунтуються на врахуванні рівноважних і кінетичних особливостей перебігу реакцій відновлення і азотування. Так, наприклад, для отримання нітридів титану і ніобію оптимальні температури відповідно 1250 і 1400 °С за тривалості ізотер-мічного витримування для гранульованих шихт 3...4 год, тиску азоту
0,4 МПа і швидкості його подачі 0,18 м/с. У цьому разі нітрид титану містить 0,5...0,7 % вуглецю, а в нітриді ніобію його немає.
Отримання нітридів термічною дисоціацією сполук. Процес отримання нітридів можна провадити в печах опору різного типу, серед яких частіше застосовуються печі періодичної і неперервної (револьверного типу) дії з перемішуванням шару гранульованої шихти вібрацією. Вихідні компоненти (оксид, сажа) змішують і в разі потреби додатково подрібнюють у кульових млинах. Одержану суміш гранулюють або пресують в таблетки невеликих розмірів, використовуючи як пластифікатор водний розчин полівінілового спирту. Підготовлена таким чином шихта має добру рухливість і газопроникність, що забезпечує повний перебіг реакцій відновлення і азотування, неперервність технологічного процесу.
Для проведення процесу в печах револьверного типу застосовуються режими, наведені в табл. 7.9. Одержані при цьому нітриди за складом близькі до розрахункових.
Отримання нітридів осадженням з газової фази. Метод має важливе значення у зв’язку з можливістю отримання продукту високого ступеня чистоти в полі- і монокристалічному стані. Як і в разі отримання інших сполук, за цим методом як вихідні речовини використовують галогеніди відповідних металів. Процес провадять за наявності азоту вищого ступеня очищення або аміаку і водню. Нітриди утворюються за однією зі схем:
МеС14 + NНзMеN + НС1;
МеOCl2 + NНз МеN + Н20 + НС1;
МеС1 + N2 + Н2 МеN + НС1.
Таблиця 7.9
Склад і режими отримання нітридів в печах револьверного типу відновленням оксидів металів вуглецем з одночасною азотизацією
|
Нітрид |
Температура, оС
|
Тривалість витримування, год |
Уміст, % | |||
|
Ме |
N | |||||
|
Розра- хун- ковий
|
Прак- тичний |
Розра- хун- ковий
|
Прак-тичний | |||
|
TiN |
1250 |
1,5 |
87,37 |
78,3…79,0 |
22,63 |
20,0...21,7 |
|
ZrN |
1200 |
2 |
86,69 |
87,0…87,5 |
13,31 |
12,5...13,2 |
|
1200 |
2 |
92,72 |
92,7…93,0 |
7,28 |
6,9...7,3 | |
|
VN |
1250 |
1 |
88,44 |
78,8...80,8 |
21,56 |
18,0...20,5 |
|
NЬN |
1200 |
2 |
86,9 |
86,9...87,7 |
13,10 |
12,3...13,0 |
|
ТаN |
1200 |
1,5 |
92,81 |
92,8…93,2 |
7,19 |
6,7...6,9 |
|
Сг2N |
1200 |
1 |
88,14 |
86,7…87,7 |
11,86 |
10,7...11,3 |
Температурні режими наведено в табл. 7.10.
Апаратурне оформлення процесу осадження нітридів з газової фази подібне до оформлення процесу отримання інших тугоплавких сполук з газової фази. Найчастіше нітриди осідають на нагрітій вольфрамовій нитці. Чим тонша нитка, тим швидше починається реакція. Найчастіше осад нітриду є конгломератами рихлої і пористої структури. Величина утворюваних кристалів залежить від температури нитки. За низьких температур утворюються дрібні кристали. Із підвищенням температури розмір кристалів і міцність їх зчеплення з підкладкою збільшуються. Прискоренню процесу утворення нітридів сприяє розвинена поверхня
нитки. За високої і стабільної температури нитки, що має монокристалічну структуру або складається з витягнутих зерен, утворюються монокристалічні осади. Можливе також отримання нітридів з газової фази у вигляді дисперсних осадів. Так, у разі отримання нітриду титану в основі процесу лежить реакція
2ТiС14 + 2NН3 = 2ТiN + 6НС1 + Сl2,
що перебігає за температури понад 1000 °С. Сутність технології полягає в подачі заздалегідь нагрітих до 700...900 °С тетрахлориду титану й аміаку в кварцову реакційну камеру через форсунку, по внутрішньому каналу якої подається тетрахлорид, а по зовнішньому кільцевому простору — аміак. У газовій фазі необхідно забезпечити співвідношення два-чотири молі аміаку на один моль ТiС14. Середня температура в камері має бути не нижчою 750...950 °С, а безпосередньо на виході—1000...1200 °С, що забезпечить високий ступінь перебігу реакції. Важливим також є забезпечення ламінарних потоків газів у реакційному просторі за швидкості їх руху 2 ... 20 м/с. У цих умовах продукт, що виходить з реакційної камери, складається з тонкої суспензії нітриду в газовому середовищі, що складається з хлору, пари НС1, реагентів, що не прореагували. Цю суміш охолоджують у трубчастих теплообмінниках з подальшим відділенням нітриду електростатичним осадженням і фільтрацією на керамічних фільтрах. Одержаний таким чином нітрид ― порошок з розміром частинок 0,1...0,6 мкм і вмістом азоту 22,2... 22,6 %.
Таблиця 7.10
