
- •Міністерство освіти і науки України
- •1. Властивості порошків
- •1.1. Хімічні властивості
- •1.2. Фізичні властивості
- •Методи визначення розміру частинок
- •1.3. Технологічні властивості
- •2. Механічні методи отримання порошків
- •2.1. Загальні положення
- •2.2. Характеристика обладнання для подрібнення
- •Він пропонує у цьому виразі замінити поточні напруги на межу міцностіматеріалу, що дозволить визначити роботу, яка виконується під час подрібнення матеріалу об’ємомза один цикл. Ця робота дорівнює:
- •Витрати роботи залежно від етапу руйнування
- •2.4. Вплив рідин та пар на процес подрібнення матеріалів
- •3. Отримання порошків розпиленням розплавів
- •3.1. Загальні положення
- •Математично залежності можна описати емпіричним рівнянням
- •Значення критеріїв Re та Lp для різних умов розпилення
- •3.2. Вплив різних факторів на процес розпилення розплавів газами
- •Гранулометричний склад порошку заліза, одержаного розпиленнямрозплавів сплавів заліза
- •Поверхневий натяг розплавів заліза з киснем, азотом, сіркою та фосфором
- •Коефіцієнт тепловіддачі конвекцією можна визначити за виразом
- •Теплофізичні властивості газів
- •3.3. Розпилення рідиною
- •Значення коефіцієнта тепловіддачі для умов розпилення розплавів водою
- •3.4. Формування складу і структури порошків під час розпилення розплавів
- •3.5. Технологічні особливості отримання порошків розпиленням
- •Режими одержання порошків розпиленням
- •4. Отримання порошків металів і сплавів відновленням з оксидів та інших сполук
- •4.1. Основи термодинаміки відновлювальних процесів
- •4.2. Механізм і кінетика відновлювальних процесів.
- •4.3. Закономірності отримання порошків металів їх
- •4.4.1. Отримання металів відновленням
- •Оксиди відновлюють відповідно до принципу послідовності
- •4.4.2. Магнієтермічне відновлення солей металів
- •4.4.3. Натрієтермічне відновлення солей металів
- •4.5. Отримання порошків сплавів
- •4.5.1. Сумісне відновлення оксидів металів воднем
- •Константи рівноваги
- •4.5.2. Сумісне відновлення сумішів оксидів і металевих порошків
- •4.5.3. Метод термодифузійного насичення з точкових джерел
- •1100 С (протягом 6 год) від їх умісту у вихідній шихті:
- •4.6. Технологічні основи отримання порошків металів та сплавів
- •Відновлення
- •5.1.2. Вплив різноманітних чинників на властивості порошків металів під час їх отримання електролізом водних
- •5.1.3. Особливості отримання порошків сплавів
- •5.1.4. Технологічні основи отримання порошків металів електролізом водних розчинів їх солей
- •11 _ Діафрагма
- •5.2. Електроліз розплавлених середовищ
- •5.2.1. Технологічні основи отримання порошків металів електролізом розплавлених середовищ
- •5.3. Автоклавний метод отримання порошків
- •5.4. Отримання порошків цементацією
- •5.5. Отримання порошків міжкристалевою корозією
- •6. Газові методи отримання порошків
- •6.1. Дисоціація карбонілів
- •7. Отримання порошків безкисневих тугоплавких сполук
- •7.1. Властивості та застосування безкисневих
- •Властивості тугоплавких сполук
- •7.2. Отримання порошків карбідів
- •Фази кінцевого продукту
- •Склад карбідів, одержаних методом свс
- •Характеристики карбіду титану отриманогометодомСвс
- •Умови осадження карбідів з газової фази
- •7.3. Отримання порошків нітридів
- •Умови отримання і склад нітридів, одержаних азотизацією металів
- •Умови осадження нітридів з газової фази
- •7.4. Отримання порошків боридів
- •7.5. Отримання порошків силіцидів
- •Температурні режими отримання силіцидів осадженням з газової фази
- •7.6. Отримання порошків неметалевих тугоплавких сполук
- •Газоподібний утворюваний силіцій, взаємодіючи з вуглецем, утворює силіцію
- •7.7. Отримання порошків литих тугоплавких сполук
- •Вихідні матеріали
- •Хімічний склад плавлених карбідів титана
- •Властивості плавлених карбідів
- •8. Отримання волокон та вусів
- •8.2. Методи отримання волоконта вусів
5.1.2. Вплив різноманітних чинників на властивості порошків металів під час їх отримання електролізом водних
розчинів солей
Густина струму. Отриманню розсипчастих, порошкоподібних осадів сприяє висока густина струму електролізу. Одна з причин появи розсипчастих осадів за високої густини струму – співвідношення швидкостей виникнення центрів кристалізації і росту частинок. Чим вища густина струму і менша концентрація електроліту біля поверхні катода, тим менша швидкість зростання зародків нової фази, що швидко з’являються, і тим сприятливіші умови створюються для виникнення розсипчастих осадів. Це зумовлено тим, що за високих густин струму з досягненням граничного значення струму дифузії розряджуваних іонів унаслідок концентраційної поляризації різко знижується їх концентрація в прикатодному прошарку. Знижена конденсація уповільнює ріст граней окремих кристалічних центрів, особливо в поперечному напрямі, і вони ніби пасивуються. Вирівнювання концентрації на пасивованих гранях знову створює умови для кристалізації нових центрів. Поперемінне пасивування і зростання нової фази сприяють утворенню розсипчастої структури виділених осадів та слабкому їх зчепленню з металом катода.
Не виключається вплив на отримання розсипчастих осадів водню, що виділяється в процесі електролізу водних розчинів солей за високої густини струму через перенапругу.
У діапазоні густин струму, що забезпечують виділення порошкоподібних осадів, варто враховувати вплив густини струму та інших параметрів процесу електролізу на вихід за струмом і властивості порошків, передусім на розмір отримуваних частинок.
Вихід за струмом під час електролізу визначають за співвідношенням:
![]()
де Gп – практичний вихід металу; Gт – теоретичний вихід металу, що визначається за законом Фарадея:
![]()
де E – електрохімічний еквівалент металу, що виділяється; К – кількість електрики (К = і , Кл); n – валентність.
Стовідсотковий вихід за струмом досягається в тому випадку, якщо в перенесенні кількості електрики, що визначається струмом електролізу, беруть участь тільки іони елемента, що виділяються. Однак насправді з деяких причин (наприклад, через наявність іонів інших елементів, низьку концентрацію електроліту, високу електронегативність іонів елемента, концентраційну поляризацію, перенапругу тощо) практичний вихід за струмом завжди нижчий за 100 %.
У всіх випадках отримання порошків металів електролізом водних розчинів їх солей збільшення густини струму спричиняє зменшення виходу за струмом (рис. 5.3). Це зумовлено тим, що в процесі електролізу водних розчинів у перенесенні потрібної кількості електрики беруть участь іони водню. У разі проведення електролізу за великих густин цей процес поглиблюється через концентраційну поляризацію і перенапругу. Варто зазначити, що за інших однакових умов вихід за струмом для металів, що мають вищу електронегативність і розміщені в ряду напруг лівіше водню (нижче водню в табл. 5.1), має низькі значення, оскільки потенціал водню опиняється нижче від потенціалу виділення металу. Поряд з вилученням металу відбувається інтенсивне виділення водню. Так, у разі отримання порошкоподібного осаду заліза за електролізом водного розчину його солі (FeSO4) вихід за струмом не перевищує 60 %.
Оскільки процес розряду на катоді іонів металів більшої електронегативності, ніж водень, супроводжується його інтенсивним виділенням, для забезпечення максимального виходу за струмом необхідно знижувати поляризацію (малі Е) для розряду іонів цих металів і підвищувати перенапругу для водню. Один з найефективніших способів зменшення поляризації для розряду іонів таких металів – збільшення їх концентрації в електроліті. Крім того, потрібне введення домішок, що підвищують електричну провідність і стабілізують значення рН розчинів. Так, для отримання порошкоподібного нікелю до складу електроліту вводять до 200 г/л хлористого натрію (NaCl) і до
50 г/л NH4Cl. Уведення NaCl сприяє підвищенню електричної провідності розчину (рис. 5.4.), що дозволяє використовувати високі густини струму для утворення порошкоподібного осаду. Крім того, підвищена концентрація іонів натрію ускладнює доступ іонів нікелю до катода, збіднює нікелем прикатодний прошарок електроліту і тим самим створює умови для порошкоподібного осадження.
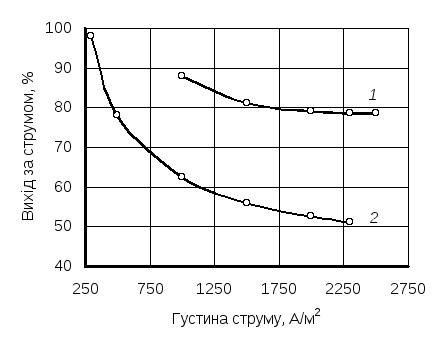
Рис. 5.3. Залежність виходу за струмом від густини
струму для одержання порошку міді (1) та срібла (2)
Значна частка іонів натрію в прикатодній ділянці спричиняє концентраційну поляризацію, що також утруднює розряд іонів нікелю. Усе це разом взяте дозволяє за високої густини струму підвищувати концентрацію іонів нікелю в електроліті, збільшувати вихід за струмом (до 92%), зберігати дисперсну структуру порошкового осаду. Падіння виходу за струмом зі збільшенням густини струму зумовлено здебільшого зростаючим виділенням водню.
Однак підвищення виходу за струмом в цьому разі в процесі електролізу з розчинів з досить високим значенням рН недостатнє для утворення гідроксидів та основних солей.

Рис. 5.4. Залежність електричної провідності електроліту
від концентрації NaCl зі складом електроліту
NiSO4 7H2O – 120 г/л; NH4Cl – 40 г/л
У разі високих рН потрібна для виділення водню перенапруга підвищується і утворюються менш сприятливі умови для його виділення на катоді.
Вихід за струмом під час отримання порошку нікелю залежно від
рН розчину (NiSO47H2O – 109 г/л; NH4Cl – 50г/л; NaCl – 200 г/л; К = 2500 А/м2; t = 55C; = 0,5 год) характеризується такою залежністю, як наведено в табл.5.3
Тобто для досягнення високих виходів металу за струмом значення рН варто підтримувати в межах 6,0…6,5. Однак під час проходження процесів електролізу за високих густин струму внаслідок виділення водню відбувається істотна зміна рН у прикатодній ділянці. У цьому випадку до розчину вводять буферні домішки, що стабілізують рН розчину. Для розглянутого прикладу отримання нікелевого порошку як домішку використано хлористий амоній.
Таблиця 5.3
Вихід нікелю за струмом (т) залежно від рН розчину
|
рН |
2,5 |
3,2 |
3,9 |
4,5 |
4,8 |
5,2 |
5,6 |
6,0 |
6,2 |
6,5 |
|
т, % |
84,4 |
82,5 |
85,2 |
87,5 |
89,0 |
89,3 |
90,1 |
91,2 |
91,5 |
91,9 |
Густина струму в процесі електролізу також істотно впливає на властивості порошків і передусім на їх розміри. Збільшення густини струму, за інших однакових умов, зумовлює зменшення середнього розміру частинок металу і його насипної щільності (рис. 5.5).

Рис. 5.5. Залежність середнього розміру частинок нікелевого порошку та його насипної щільності γнас від густини струму в процесі електролізу з розчинів, що містять NiSO47H2O – 105 г/л; NH4Cl – 50 г/л; NaCl – 20 г/л; pH – 6,3; Т – 55С:
1 – розмір частинок; 2 – насипна щільність
Зменшення розміру частинок зумовлено тим, що чим вища густина струму, тим більше центрів кристалізації формується на одиницю площі поверхні катода, в результаті чого внаслідок перерозподілу виділюваного металу формується порошок з малим розміром частинок. Крім того, збільшення густини струму сприяє підвищенню концентраційної поляризації, що супроводжується зменшенням концентрації іонів металу, що виділяються у прикатодній зоні і теж сприяє зменшенню розміру утворених частинок.
Як видно з рис. 5.5, зменшення розміру частинок з підвищенням густини відбувається із затуханням. Це зумовлено тим, що збільшення густини струму викликає інтенсивніше виділення водню, який сприяє перемішуванню електроліту, збільшенню концентрації іонів металу біля катода, що поліпшує умови живлення іонами металу зростаючих кристалів. Зі збільшенням густини струму помітно змінюється і гранулометричний склад порошку. Збільшення струму зумовлює зменшення вмісту в порошку великих фракцій та зростання вмісту дрібних фракцій (табл. 5.4)
Таблиця 5.4
Гранулометричний склад (%) порошків нікелю , одержаних за різних значень густини струму
|
Розмір частинок, мкм |
А/м2 | ||||
|
2500 |
3000 |
3500 |
5000 |
6000 | |
|
420…500 |
0,1 |
0,2 |
0,1 |
0,1 |
0,0 |
|
150…420 |
33,8 |
28,6 |
25,8 |
22,4 |
16,9 |
|
101…150 |
23,4 |
23,1 |
20,3 |
18,8 |
17,1 |
|
75…101 |
16,8 |
16,6 |
20,2 |
21,6 |
20,4 |
|
53…75 |
11,3 |
7,1 |
10,9 |
10,7 |
14,4 |
|
42…53 |
8,1 |
14,1 |
11,4 |
13,6 |
15,2 |
|
42 |
6,5 |
9,5 |
10,2 |
12,8 |
15,1 |
Концентрація електроліту. Причина утворення порошкоподібних осадів у процесі електролізу – різні швидкості зародження і росту кристалів. Якщо концентрація іонів металу в електроліті низька, між зростаючими кристалами в поперечному напрямі виникають розриви і утворюється розсипчастий порошкоподібний осад. У зв’язку з тим, що в прикатодній ділянці виникає градієнт концентрацій, за малої концентрації електроліту створюються умови для росту дрібних дендритоподібних кристалів, за недостачі іонів металу у прикатодному прошарку грані зростаючих кристалів сильніше розвиваються в глибину розчину.
У міру зростання кристалів у бік об’єму електроліту концентрація іонів поблизу їх вершини збільшується і створюються умови для росту кристалів у поперечному напрямі. Таким чином, формуються розгалужені, дендритоподібні кристали.
Крім того, за зниженням концентрації іонів металу на катоді також виділяється водень, що сприяє розсипанню осаду.
У межах концентрацій, що забезпечують виділення порошкоподібних осадів, збільшення концентрації іонів металу в електроліті зумовлює зменшення концентраційної поляризації, і дифузійне живлення прикатодного простору іонами металу посилюється. У результаті послаблюється процес утворення на катоді дрібних дендритоподібних кристалів і створюються сприятливі умови для формування великих порошків. При цьому підвищується масова частка великих фракцій у порошку, а дендритна, розгалужена форма частинок змінюється на простішу, округлу. Загалом середній розмір частинок збільшується, спрощується форма частинок і збільшується насипна щільність отримуваних порошків.
Концентрація електроліту істотно впливає на вихід металу за струмом. Майже для всіх металів, отриманих електролізом, вихід металу за струмом зі збільшенням концентрації іонів у розчині зростає (рис. 5.6). При цьому найінтенсивніше зростання виходу за струмом спостерігається в зоні малих концентрацій. За подальшого збільшення концентрації темп росту виходу за струмом падає і може досягати насичення, після чого починає виділятися густий осад.
Зростанню виходу за струмом зі зростанням концентрації іонів металу в розчині сприяло їх полегшене доставляння до поверхні катода, що призводить до зниження поляризації і перерозподілу на користь процесу розрядження іонів металу. Концентрація електролітів – основний параметр електролізу, оскільки ефективно впливає як на вихід за струмом, так і на дисперсність порошку.

Рис. 5.6. Залежність виходу за струмом від концентрації
іонів металу для одержання срібла (1) та міді (2)
електролізом водних розчинів їх солей
Кислотність електроліту. Кислотність електроліту впливає як на вихід металу за струмом, так і на розмір утворюваних частинок. Вихід за струмом знижується зі збільшенням концентрації кислоти в розчині. При цьому особливо швидке зменшення виходу за струмом спостерігається в зоні малої концентрації кислоти, як це відбувається в разі отримання електролізом порошку серебра (рис. 5.7). Це зумовлене тим, що в процесі перенесення кількості електрики беруть участь іони водню. Для зменшення впливу цього ефекту потрібно підвищувати перенапругу водню.
Збільшення концентрації кислоти в електроліті також сприяє зростанню дисперності порошків і отриманню розсипчастих осадів через інтенсивне виділення водню. Поряд з чистомеханічним розкришуванням осаду газоподібним воднем, що виділяється, це явище може бути зумовлено виділенням водню, який займає вакантні місця у вузлах гратки зростаючого кристала, на гранях зростаючого кристала під час розрядження іонів металу. Надалі, дифундуючи з кристала, водень залишає вакансії, за високої концентрації яких утворюються порожнини, що й спричиняють розсипання осаду.

Рис. 5.7. Залежність виходу за струмом від концентрації
HNO3 (1) та частоти знімання (2) для отримання
порошку срібла з розчину його солі AgNO3
Однак такий вплив водню на розмір утворюваних частинок не однозначний. Так, за наявності в розчині ПАР, які сприяють отриманню дрібнодисперсних частинок, інтенсивне виділення водню сприяє збільшенню частинок завдяки розриванню плівки ПАР на поверхні частинок, що обмежує їх ріст.
Таким чином, вплив концентрації кислоти на дисперсність частинок, що виділяються, варто розглядати в комплексі з іншими чинниками.
Температура електролізу. Підвищення температури процесу електролізу сприяє збільшенню виходу за струмом, що зумовлено прискоренням дифузійного доставлення іонів металу до катода. Вплив температури ефективний для поліпшення техніко-економічних показників електролізу, оскільки з підвищенням температури не тільки збільшується вихід за струмом, але й істотно знижується напруга на шинах електролізера.
Крім того, збільшення концентрації іонів металу в прикатодному просторі з підвищенням температури сприяє росту частинок порошку.
Підвищення температури може впливати на структуру частинок особливо за наявності ПАР. Це сприяє утворенню дрібних частинок зі слаборозвинутою поверхнею через блокування їх росту адсорбованим на їх поверхні прошарком молекул ПАР. Із підвищенням температури густина адсорбційної плівки зменшується, стає можливою десорбція ПАР, у результаті створюють умови для росту частинок з утворенням жорстких, грубих порошків з розгалуженою поверхнею. Підвищувати температуру електролізу понад 60 оС недоцільно, оскільки створюються шкідливі умови для обслуговування ванн і збільшується швидкість розчинення осадів в електроліті.
Час електролізу. Із виділенням розсипчастого осаду на катоді, його поверхня значно збільшується, в результаті чого дійсна густина струму на катоді стає нижчою за початкову. У разі зниження дійсної густини зменшується швидкість розряду іонів металу і їх концентрація в прикатодному просторі збільшується. В результаті створюються умови для росту утворених частинок і з’являються менш дисперсні частинки з меншим ступенем дендритності.
Зниження катодної густини струму в часі приводить до зменшення концентраційної поляризації і перерозподілу струму між сумісними процесами розряду іонів металу і водню на користь іонів металу. Крім того, утворювані мікродендрити розсипчастого осаду ростуть в глибину розчину, в результаті чого їх живлення розряджуваними іонами поліпшується. Усе це сприяє збільшенню виходу за струмом. Для запобігання коротким замиканням необхідно збільшувати міжелектродний простір, що зумовлює небажане підвищення напруги на ванні. Таким чином, у разі потреби зберігати високу дисперсність отриманих електролізом порошків час їх виділення необхідно обмежувати, що досягається збільшенням частоти їх зняття.
Домішки в електроліті. Домішки в електролітах зазвичай мають штучний характер. Це такі, як ПАР, що вводяться в електроліт, колоїди, пероксид водню. Поверхнево-активні речовини і колоїди створюють адсорбовані мономолекулярні плівки на поверхні осаджених частинок і перешкоджають їх росту та зрощенню, що сприяє отриманню порошкоподібного осаду з частинками малого розміру. Такий самий вплив чинять окисники, створюючи на поверхні частинок катодного осаду оксидних плівок. Як домішки, що обмежують зростання частинок, використовують такі речовини, які можуть утворюватися в процесі електролізу – гідроксиди, солі металу нижчої валентності та ін. Наприклад, для отримання порошку міді до складу електроліту разом з водою вводять іони хлору, які взаємодіють з невеликою кількістю іонів одновалентної міді, що містяться в розчині, і утворюють слаборозчинні сполуки CuCl. Колоїдні частинки CuCl адсорбуються на поверхні виділених частинок міді та сприяють їх розгалуженню.
Варто зазначити, що введенням в електроліт домішок речовин, що обмежують зростання частинок, можна отримати порошкоподібні осади навіть за концентрації розчинів, яка в звичайних умовах зумовлює утворення густих осадів.
