
- •Міністерство освіти і науки України
- •1. Властивості порошків
- •1.1. Хімічні властивості
- •1.2. Фізичні властивості
- •Методи визначення розміру частинок
- •1.3. Технологічні властивості
- •2. Механічні методи отримання порошків
- •2.1. Загальні положення
- •2.2. Характеристика обладнання для подрібнення
- •Він пропонує у цьому виразі замінити поточні напруги на межу міцностіматеріалу, що дозволить визначити роботу, яка виконується під час подрібнення матеріалу об’ємомза один цикл. Ця робота дорівнює:
- •Витрати роботи залежно від етапу руйнування
- •2.4. Вплив рідин та пар на процес подрібнення матеріалів
- •3. Отримання порошків розпиленням розплавів
- •3.1. Загальні положення
- •Математично залежності можна описати емпіричним рівнянням
- •Значення критеріїв Re та Lp для різних умов розпилення
- •3.2. Вплив різних факторів на процес розпилення розплавів газами
- •Гранулометричний склад порошку заліза, одержаного розпиленнямрозплавів сплавів заліза
- •Поверхневий натяг розплавів заліза з киснем, азотом, сіркою та фосфором
- •Коефіцієнт тепловіддачі конвекцією можна визначити за виразом
- •Теплофізичні властивості газів
- •3.3. Розпилення рідиною
- •Значення коефіцієнта тепловіддачі для умов розпилення розплавів водою
- •3.4. Формування складу і структури порошків під час розпилення розплавів
- •3.5. Технологічні особливості отримання порошків розпиленням
- •Режими одержання порошків розпиленням
- •4. Отримання порошків металів і сплавів відновленням з оксидів та інших сполук
- •4.1. Основи термодинаміки відновлювальних процесів
- •4.2. Механізм і кінетика відновлювальних процесів.
- •4.3. Закономірності отримання порошків металів їх
- •4.4.1. Отримання металів відновленням
- •Оксиди відновлюють відповідно до принципу послідовності
- •4.4.2. Магнієтермічне відновлення солей металів
- •4.4.3. Натрієтермічне відновлення солей металів
- •4.5. Отримання порошків сплавів
- •4.5.1. Сумісне відновлення оксидів металів воднем
- •Константи рівноваги
- •4.5.2. Сумісне відновлення сумішів оксидів і металевих порошків
- •4.5.3. Метод термодифузійного насичення з точкових джерел
- •1100 С (протягом 6 год) від їх умісту у вихідній шихті:
- •4.6. Технологічні основи отримання порошків металів та сплавів
- •Відновлення
- •5.1.2. Вплив різноманітних чинників на властивості порошків металів під час їх отримання електролізом водних
- •5.1.3. Особливості отримання порошків сплавів
- •5.1.4. Технологічні основи отримання порошків металів електролізом водних розчинів їх солей
- •11 _ Діафрагма
- •5.2. Електроліз розплавлених середовищ
- •5.2.1. Технологічні основи отримання порошків металів електролізом розплавлених середовищ
- •5.3. Автоклавний метод отримання порошків
- •5.4. Отримання порошків цементацією
- •5.5. Отримання порошків міжкристалевою корозією
- •6. Газові методи отримання порошків
- •6.1. Дисоціація карбонілів
- •7. Отримання порошків безкисневих тугоплавких сполук
- •7.1. Властивості та застосування безкисневих
- •Властивості тугоплавких сполук
- •7.2. Отримання порошків карбідів
- •Фази кінцевого продукту
- •Склад карбідів, одержаних методом свс
- •Характеристики карбіду титану отриманогометодомСвс
- •Умови осадження карбідів з газової фази
- •7.3. Отримання порошків нітридів
- •Умови отримання і склад нітридів, одержаних азотизацією металів
- •Умови осадження нітридів з газової фази
- •7.4. Отримання порошків боридів
- •7.5. Отримання порошків силіцидів
- •Температурні режими отримання силіцидів осадженням з газової фази
- •7.6. Отримання порошків неметалевих тугоплавких сполук
- •Газоподібний утворюваний силіцій, взаємодіючи з вуглецем, утворює силіцію
- •7.7. Отримання порошків литих тугоплавких сполук
- •Вихідні матеріали
- •Хімічний склад плавлених карбідів титана
- •Властивості плавлених карбідів
- •8. Отримання волокон та вусів
- •8.2. Методи отримання волоконта вусів
5.2.1. Технологічні основи отримання порошків металів електролізом розплавлених середовищ
Із технологічного погляду процес отримання металів електролізом розплавлених середовищ можна розділити на чотири етапи:
– безпосередньо електроліз;
– попереднє відокремлення отриманого порошку від застигнутого електроліту;
– вакуумне рафінування отриманого продукту;
– розмелювання та розсіювання.
Для електролізу можна використовувати електролізери двох типів. Так для отримання порошку танталу використовують електролізер, схему якого показано на рис. 5.12. Такий електролізер має катод у вигляді тигля, виготовленого зі сталі або сплаву ніхрому. Як анод застосовують полий перфорований графітовий стрижень, у який завантажують джерело металу (табл. 5.7) – прості та складні комплексні солі, оксиди , сполуки у вигляді кусків розмірами 5...20 мм, гранул або брикетів. Порошок, який виділяється в процесі електролізу, осідає на дні та стінках тигля-катода. Процес провадять до заповнення тигля на 2/3 його об’єму. Потім процес електролізу зупиняють, виймають анод, а розплав охолоджують разом з тиглем . Закристалізований розплав солей з вкрапленими в нього частинками порошку підлягає подальшій переробці.
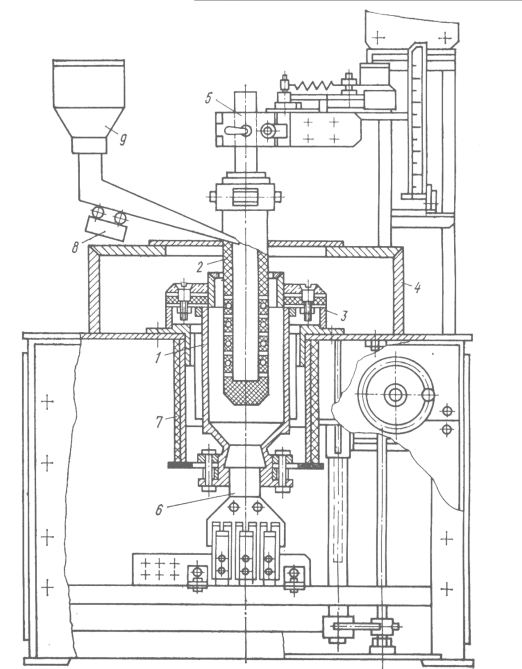
Рис. 5.12 Схема електролізера з трубчастим графітовим анодом:
1 – тигель-катод; 2 – трубчастий перфорований графітовий анод;
3 – теплоізоляційний кожух; 4 – кришка; 5 – кронштейн для закріплення анода; 6 – нижній струмопідвід; 7 – теплоізоляційний стакан;
8 – електромагнітний вібратор; 9 – завантажувальний бункер
Інший варіант електролізу процес з використанням електролізерів, у яких анодом слугує графітовий тигель, а катод виготовляють зі сталі або нікелю (рис. 5.13). Для отримання порошків у таких електролізерах вихідну сировину, наприклад двооксид титану, засипають безпосередньо в електроліт, основу якого складаєCaCl2.Упроцесі електролізу на металевому катоді разом з електролітом створюється катодна«груша». У міру накопичення катодної «груші» її виймають з електролізера і охолоджують в соляній ванні.
Упроцесі електролізу розплавлених соляних середовищдляпідтримання заданих умов коригують склад електроліту,добавляючи в нього матеріал – джерело основного металу.
Отриманий електролізний продукт у вигляді закристалізованих солей-розчинників із вкрапленими частинками порошку розміром 50...70 мкм , наприклад танталу, розмелюють в млинах,які працюють у замкнутому циклі з повітряними сепараторами. Унаслідок цього частина електроліту відділяється і може використовуватись повторно в процесі електролізу. Після розмелювання продукт для більш повного видалення електроліту промивають на концентраційних столах водою. Для зменшення в порошку вмісту домішок металів (заліза, молібдену) та стабілізації поверхні частинок його обробляють гарячим розчином азотної та соляної кислот. Потім порошок промивають водою і сушать у вакуумі.
Можливий інший варіант очищення катодних осадів з використанням вакуумно-термічних установок (рис. 5.14). У них порошок металу відділяють від соляного електроліту його виплавленням у середовищі аргону в спеціальних ретортах, виготовлених з жаростійкого матеріалу. Для цього в реторті (1) розміщують тигель (7) з катодним осадом . Потім реторту вакуумують , заповнюють аргоном і нагрівають до температури 1000 ºС за допомогою електропечі (2), Соляний електроліт плавиться і через гратку в нижній частині тигля стікає в стакан (4). У кінці процесу реторта знову вакуумується для більш повного видалення солей випаровуванням. Унаслідок такого процесу отримують порошок металу у вигляді злегка спечених дендритів, які розмелюють. Таким чином, можна отримувати порошок танталу з умістом основного компонента 99,8…99,9 %.

Рис. 5.13 Схема електролізера з графітовим анодом-тиглем:
1 – гідроциліндр; 2 – камера; 3 – катод; 4 – електрод; 5 – газовідвідна трубка;
6 – графітовий анод; 7 – підвід тетрахлориду титану

Рис. 5.14. Схема вакуумно-термічної установки для очищення катодних осадів:
1 – реторта; 2 – електропіч; 3 – конденсатор; 4 – стакан; 5 – дифузійний вакуумний насос; 6 – система завантаження тигля – катода; 7 – тигель–катод
Таблиця 5.7
Умови отримання порошків деяких металів електролізом розплавлених середовищ
|
Метал |
Склад електроліту, % |
Густина струму, кА/м2 |
Температура, С |
Вихід за струмом, % |
Анод | |
|
Джерело металу |
Розчинник | |||||
|
Титан |
TiCl2 (TiCl3) |
NaCl, NaCl + KCl,
NaCl + KCl + MgCl2 |
ак = 5...15
аа = 1...3 |
809...880 |
90 |
Титановий скрап |
|
Цирконій |
K2ZrF6 (25…30) |
KCl, NaCl (75…70) |
ак= 3,5...4,5
|
750...800 |
88...90 |
Графіт |
|
Залізо |
FeCl2 (11…12) |
NaCl + KCl (96…88) |
ак = 50
аа = 2...4 |
750...900 |
80...90 |
Губчасте залізо |
|
Тантал |
Ta2O5 (3…3,5)
K2TaF7 (25…30) |
NaCl + KCl (60…70) |
ак = 5
аа = 12...16 |
680...720 |
80 |
Скрап, сполуки |
|
Ніобій |
NbCl2, (Nb) ( 5…8) |
NaCl + KCl + NaF |
ак =10 ... 20
|
680...720 |
88...90 |
Скрап, сполуки |
