
- •Розрахунки в середовищі excel Розділ 1. Розрахунок кінетичних параметрів топохімічних реакцій
- •Індивідуальна самостійна робота
- •Розділ 2. Статистична обробка результатів експерименту
- •2.1. Кореляційний аналіз
- •2.2. Довірчий інтервал
- •Контрольні питання
- •Література
- •Розділ 3. Розрахунок кінетичних параметрів хімічних реакцій
- •Література
- •Розділ 4. Оптимізація об'єктів досліджень за моделями другого порядку
- •Література
- •Розділ 5. Розрахунки математичних моделей "склад - властивість"
- •Література
- •Розділ 6. Розрахунок кінетичних параметрів за дериватографічними даними
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Розділ 7. Розрахунок очищення коксового газу від сірководню
- •Алгоритм розрахунку
- •Розділ 8. Розрахунок виробництва водню мембранним методом
- •Алгоритм розрахунку [1]
- •Контрольні питання
- •Розділ 9. Розрахунок паро – повітряної конверсії метану
- •Вихідні дані (додаткові)
- •Контрольні питання
- •Розділ 10. Розрахунок двоступеневої
- •Розділ 11. Розрахунок матеріального балансу синтезу метанолу
- •Розділ 12. Розрахунок матеріального балансу синтезу аміаку
- •Алгоритм розрахунку
- •Контрольні питання
- •Розділ 13. Розрахунок очищення газу від co2 розчином моноетаноламіну
- •Алгоритм розрахунку Розрахунок матеріального балансу виробництва
- •Стадія «тонкого» очищення
- •Стадія «тонкого» очищення
- •Концентрації компонентів суміші с(і)2відповідають даним таблиці 3.
- •2 Розрахунок теплового балансу виробництва
- •Де ∑m(mea)р-ну - сума витрат розчину меа на «грубе» та «тонке» очищення, кг меа/год.
- •3 Розрахунок насадкового абсорбера верхня частина абсорбера («тонке» очищення)
- •Алгоритм розрахунку
- •Швидкість захлинання абсорбера у верхній частині [3]:
- •Робоча швидкість газу у верхній частині абсорбера:
- •Нижня частина абсорбера («грубе» очищення)
- •Алгоритм розрахунку
- •Швидкість захлинання абсорбера у нижній частині [3]:
- •Робоча швидкість газу у нижній частині абсорбера:
- •4 Розрахунок тарілчастого абсорбера
- •Верхня частина абсорбера
- •Алгоритм розрахунку
- •Нижня частина абсорбера
- •Алгоритм розрахунку
- •Промисловий абсорбер має 15 тарілок: 9 в нижній частині і 6 у верхній.
- •Розділ 14. Аналіз статики іонного обміну однозарядних (рівнозарядних) іонів
- •Рівновага іонного обміну рівновалентних іонів
- •Алгоритм розрахунку
- •Контрольні питання
- •Література
- •Розділ 15. Аналіз статики іонного обміну різнозарядних іонів
- •Алгоритм розрахунку
- •Контрольні питання
- •Література
- •Розділ 16. Розрахунок очищення газу від оксиду карбону (IV) гарячим розчином поташу
- •1 Матеріальний розрахунок
- •Алгоритм розрахунку
- •1.1 Розрахунок грубого очищення
- •1.2 Розрахунок тонкого очищення
- •2 Тепловий баланс поташного очищення конвертованого газу
- •Алгоритм розрахунку
- •3 Конструктивні розрахунки насадкового абсорберу
- •3.1 Розрахунок діаметру абсорберу Нижня зона
- •Алгоритм розрахунку
- •Верхня зона
- •Алгоритм розрахунку
- •3.2 Розрахунок висоти насадки
- •Верхня зона
- •Алгоритм розрахунку
- •Нижня зона
- •Алгоритм розрахунку
- •1. Розрахувати реальний вміст компонентів k2co3,kнco3і н2о в розчинах згідно даних таблиці 10. Врахувати стехіометрію реакції
- •Розрахунок матеріального балансу
- •Розрахунок теплового балансу
- •Алгоритм розрахунку
- •Конструктивний розрахунок
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Література
- •Розрахунки в середовищіmathcad розділ 18. Розрахунок рівноваги оборотних реакцій
- •Розділ 19. Розрахунок трубчатого реактора конверсії природного газу
- •Алгоритм розрахунку
- •Розділ 20. Розрахунок рівноваги пароповітряної конверсії метану
- •Розділ 21. Розрахунок окиснення оксиду сульфуру (IV)
- •Контрольні питання
- •Література
- •Розділ 22. Альтернативний розрахунок матеріального балансу синтезу аміаку
- •Контрольні питання
- •Розділ 23. Альтернативний розрахунок матеріального балансу синтезу метанолу
- •Розділ 24. Розрахунок паро-вуглекислотної конверсії природного газу
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Розділ 25. Розрахунок вуглекислотної рівноваги у водних розчинах
- •Алгоритм розрахунку
- •Значення рН буде приймати значення 4, 5, 6, 7, ..... До значення –log(Kw). Важливо! Отримані числові значення параметра не утворюють матрицю, тому з ними не можливі дії, що застосовуються до матриці.
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Розділ 26. Аналіз динаміки іонного обміну однозарядних іонів
- •2 Хвильове рівняння для концентрації
- •3 Рівняння збереження в безрозмірній формі [1]
- •4 Рівняння ізотерми іонного обміну
- •5 Рішення хвильового рівняння методом характеристик [1]
- •6 Розрахунок обміну однозарядних іонів[1]
- •Алгоритм розрахунку
- •Вихідні дані для 1-ої ступені водопідготовки
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Література
- •Розділ 27. Термодинамічний та матеріальний розрахунки газифікації вугілля
- •Розділ 28. Термодинамічний розрахунок газифікації (конверсії) вуглеводнів
- •Алгоритм розрахунку
- •.Індивідуальна самостійна робота
- •Контрольні питання
- •Література
- •Розділ 29. Розрахунок концентрацiй iонiв у вапнованiй та коагульованiй воді
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Література
- •Розділ 30. Аналіз динаміки іонного обміну різнозарядних іонів
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Література
- •Розділ 31. Термодинамічний розрахунок газифікації рідких палив невідомої формули
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Розділ 32.Розрахунок поличних колон синтезу аміаку
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Література
- •Методичні рекомендації до виконання розрахункової роботи
- •Розрахунок матеріального балансу виробництва
- •Розрахунок енергетичного (теплового) балансу виробництва
- •Розрахунок основних реакторів
- •Захист розрахункової роботи
- •Завдання на розрахункову роботу з дисципліни
Розділ 27. Термодинамічний та матеріальний розрахунки газифікації вугілля
Процес газифікації твердого палива можна охарактеризувати як сукупність гетерогенних і гомогенних реакцій, в результаті яких утворюється суміш СО, Н2, СН4, в якості основних паливних компонентів цільового газу. Ці реакції достатньо повно описуються рівняннями, наведеними в таблиці 1 і охоплюють усі стадії різноманітних методів газифікації [1].
Таблиця 1 – Реакції, які проходять при газифікації твердого палива
|
№ реакції |
Реакція |
Тепловий ефект реакції*, ∆Н, кДж/моль |
|
1 |
2 |
3 |
|
Реакції горіння і газифікації | ||
|
1 |
С + О2 → СО2 |
- 393,6 |
|
2 |
С + 0,5О2 ↔ СО |
- 110,6 |
|
3 |
СО + 0,5О2 ↔ СО2 |
- 283,0 |
|
4 |
С + Н2О ↔ СО + Н2 |
+ 131,5 |
|
5 |
С + 2Н2О ↔ СО2 + 2Н2 |
+ 88,8 |
|
6 |
С + СО2 ↔ 2СО |
+ 172,5 |
|
7 |
СО + Н2О ↔ СО2 + Н2 |
- 41,17 |
|
8 |
Н2 + 0,5О2 ↔Н2О |
- 286,0 |
|
9 |
С + 2Н2 ↔ СН4 |
- 74,9 |
|
10 |
СО+3Н2 ↔ СН4 + Н2О |
- 206,4 |
|
11 |
2СО+2Н2 ↔ СН4 + СО2 |
- 247,4 |
|
Побічні процеси | ||
|
12 |
0,5S2 + Н2 ↔ Н2S |
- 20,1 |
Примітка: * Зі знаком (-) – екзотермічний процес, зі знаком (+) – ендотермічний процес.
Власно реакціями газифікації вуглецю твердого палива є сильно ендотермічні реакції (4) та (6). Тому процес газифікації вуглецю твердого палива потребує підведення значної кількості високотемпературного тепла посереднім шляхом (алотермічний процес газифікації), або за рахунок одночасного спалювання частини твердого палива, що підлягає газифікації, до СО2 (автотермічний процес) – реакція повного горіння вуглецю палива (1).
За допомогою трьох реакцій: реакції Будуара (6), реакції парової конверсії СО (7), реакції гідрування вуглецю (9) можна довести термодинамічну залежність всіх інших реакцій.
Залежності констант рівноваги для цих реакцій мають наступний вигляд:

2СО ↔ СО2 + С (6а) ;

С О2
+ Н2
↔ СО + Н2O
(7а)
;
О2
+ Н2
↔ СО + Н2O
(7а)
;
С + 2Н2 ↔ СН4 (9) .
Зауваженн 1. Реакції (6) і (7) переписана навпаки як (6а) і (7а), враховуючи напрям зсуву рівноваги за умов процесу. Це враховано методикою розрахунку, що викладена нижче за текстом.
Константи рівноваги можна визначити з наступних рівнянь:
lgKр1 = – 8947,7 / T + 2,4673 · lgT – 0,0010824 · T + 1,16 · 10-7 · T2 + 2,772;
lgKр2 = -2217,5 / T - 0,297 ∙ lgT - 0,0003525 ∙ T + 5,08 ∙ 10-8 ∙ T2 + 3,26;
lgKр3 = 3348 / T – 5,957 ∙ lgT + 0,00186 ∙ T – 1,095 ∙ 10-7 ∙ T2 + 11,79.
Існуюча методика термодинамічного розрахунку [2 – 5] видає склад генераторного газу, отриманого при газифікації ідеального вугілля, яке на 100% складається з вуглецю. При цьому відсутні відомості про вихід генераторного газу і ступінь газифікації вугілля.
Наступний алгоритм [6, 7] базується на попередньому розрахунку вихідних об’ємів газів, що утворюються при взаємодії вугілля з окисниками згідно умовно незворотної брутто реакції (13) та допоміжних реакцій (14 ‑ 15), які перебігають при газифікації вугілля реального складу:
n1C+n2O2+n3H2O=n4CO+n5H2, (13)
де n1 = 2, n2 = 1, n3 = 0, n4 = 2, n5 = 0 для повітряного дуття;
n1 = 1, n2 = 0, n3 = 1, n4 = 1, n5 = 1 для парового дуття;
n1 = 3, n2 = 1, n3 = 1, n4 = 3, n5 = 1 для паро-киснево-повітряного дуття;
S+H2=H2S; (14)
СО+O2=СO2 для парового дуття. (15)
Цей прийом дозволяє визначити склад вихідного газу, що за оборотними реакціями (6а, 7а, 9) визначає рівноважний склад генераторного газу.
При проведенні повітряної газифікації вугілля, в складі якого наявна сірка, утворюється суміш H2S та SО2. При виконанні термодинамічного розрахунку важко врахувати в якому співвідношенні утворюються ці гази. Враховуючи те, що в складі вугілля присутній водень в такій кількості, якої достатньо для повного зв’язування сірки до H2S, можна припустити, що в генераторному газі буде наявний тільки H2S, а можливістю утворення SО2 можна знехтувати. Для інших видів газифікації враховано утворення лише H2S, оскільки парове дуття призводить до надлишку водню.
Для парового дуття в реакції (13) не передбачена наявність кисню, але кисень може бути наявний в складі вугілля, для такого випадку передбачені розрахунки за реакцією (15).
Щоб визначити рівноважний склад генераторного газу, необхідно розрахувати ступені перетворення: х – по СО, y – по СО2, та z – по Н2 реакцій (6а, 7а, 9), відповідно. Для цього складена система 3-х рівнянь – залежності констант рівноваги від рівноважних концентрацій (парціальних тисків) відповідних компонентів, виражених через їх вихідні об’єми та ступені перетворення. Рівноважний склад генераторного газу можна визначити за наступними рівняннями, м3:
VkCO=V0CO –V0CO∙x + (V0CO∙x/2 + V0CO2)∙y; (16)
VkCO2=V0CO2+V0CO∙x/2– (V0CO∙x/2 + V0CO2)∙y; (17)
VkH2O=V0H2O+(V0CO∙x/2 + V0CO2)∙y; (18)
VkH2=V0H2–V0H2∙z–(V0CO∙x/2+ V0CO2)∙y; (19)
VkCH4=V0CH4+V0H2∙z/2; (20)
VkH2S= V0H2S; (21)
VkN2=V0N2, (22)
де Vki – об’єм компоненту генераторного газу у стані рівноваги;
V0i – об’єм компоненту вихідного газу – визначення цих об’ємів робиться в попередніх розрахунках згідно стехіометрії реакцій (13 – 15) з врахуванням кількості і складу вугілля та дуття.
Оскільки молярна частка компоненту Nki = Vki / ΣVki, a його парціальний тиск Pki = Nki ∙ P (Р – загальний тиск, атм), після ряду перетворень система рівнянь приймає вид:

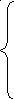

(23)

Система рівнянь (23) є універсальною для всіх видів дуття. Вид дуття впливає на визначення об’ємів компонентів вихідного газу V0i.
Мета роботи: розробити в середовищі MathCad програму розрахунку рівноважного складу газу з врахуванням кількості та складу вугілля, яке піддається пароповітряній або паро-кисневій газифікації.
Вихідні дані
З метою перевірки адекватності математичної моделі і правильності розробленої програми виконати за вищенаведеним алгоритмом розрахунок для ідеального вугілля (100% вуглецю) і стехіометричної кількості пари і кисню (повітря збагачене киснем) в дутті: Х1 = N2:О2 = 1 і Х2= Н2О:О2 = 1.
Маса вугілля, кг: m – 100. Тиск процесу, атм: Р – 20. Температура газифікації, оС: t – 900, Вологість повітря для ідеального випадку Wpov ‑ 0 г/м3.
Зробити аналіз відхилення отриманих результатів від довідкових даних [4]. Звернути увагу на неповне перетворення вугілля (недопал) 19,2 кг за даних умов (визначається як різниця маси вихідних речовин і маси генераторного газу разом з золою. В таблиці 2 надано деякі контрольні цифри для перевірки розрахунків, комірки (-) не заповнюються.
Для термодинамічного розрахунку пароповітряної газифікації вугілля різними окисниками за допомогою програми, що розробляється, необхідно ввести наступні дані:
- значення температури процесу газифікації, ºС;
- значення тиску процесу газифікації, атм.;
- кількість вугілля, для якого необхідно зробити розрахунок, кг;
- елементарний склад вугілля, % мас.;
- об’ємне співвідношення Х1 = N2 : О2 в дутті та об’ємне співвідношення
Х2 = Н2О : О2 в дутті;
- значення вологості повітря, г/м3. Для паро-кисневої газифікації при
Х1 < 1, що відповідає співвідношенню N2 : О2 < 50 : 50 значення вологості приймається рівним нулю.
Далі відбувається попередній розрахунок складу газу (кг, м3), який утворюється згідно реакцій (13 – 15).
1 Маса технологічного кисню або кисню повітря розраховується згідно стехіометрії реакції (13), при цьому врахувати, що за рахунок наявності кисню в складі вугілля кисню дуття необхідно взяти менше. Розрахувати об’єм кисню;
2 Об’єм азоту дуття розраховується за співвідношенням Х1, після чого розрахувати масу азоту. При цьому в загальній кількості азоту, (кг, м3) врахувати азот в складі вугілля.
3 Кількість СО (маса, потім об’єм) розраховується згідно стехіометрії реакції (13).
4 Кількість СО2 (маса, потім об’єм) приймається рівною нулю (розраховується тільки для парового дуття згідно стехіометрії реакції (15)).
5 Кількість H2S (маса, потім об’єм) розраховується згідно стехіометрії реакції (14).
6 Кількість H2 (маса, потім об’єм) розраховується згідно стехіометрії реакції (13), при цьому необхідно врахувати масу водню, що наявна в складі вугілля, а також те, що певна кількість H2 витратиться на перебіг реакції (14).
7 Кількість пари H2О розраховується в залежності від виду дуття:
для пароповітряного дуття – кількість пари визначається за об’ємним співвідношенням Х2 (об’єм, потім маса), враховуючи результати за п. 1. Необхідно врахувати те, що крім пари дуття також наявна волога в складі вугілля, та волога, яка надходить з повітрям дуття, отже необхідно розрахувати надлишкову кількість вологи як різницю загальної кількості пари дуття та пари необхідної згідно стехіометрії реакції (13), розраховане значення буде відповідати кількості пари у вихідній суміші.
для паро-кисневого дуття все теж саме, але не враховується кількість вологи, яка надходить з повітрям.
8 Вихідна кількість метану приймається рівною нулю.
Результати розрахунків зводяться в таблицю складу вихідного газу, в якій для кожного компоненту надані значення маси, кг, масового відсотку, значення об’єму, м3, об’ємного відсотку та значення парціального тиску.
За балансом враховується зола, що надходить в складі вугілля, – відображається в таблиці окремою строчкою, кг.
Далі відбувається термодинамічний розрахунок в такій послідовності:
- здійснити перерахунок температури в абсолютну шкалу;
- розрахувати константи рівноваги реакцій (6а, 7, 9) за відповідними рівняннями при заданому значенні температури;
- для рішення системи рівнянь (23) задати початкові наближеннями ступенів перетворення: х, y та z, наприклад, х=0,5, y=0,1 та z= 0,1). Рішення системи рівнянь відбувається з використанням операторів Given Find. Оператор Given ставиться перед системою рівнянь. Кожне рівняння в системі повинно бути записано через «жирне дорівнює» (Ctrl + =). За допомогою оператора Find виводяться значення розрахованих величин L:=Find(x, y, z). Якщо шукані величини не мають фізико-хімічного сенсу, треба змінити їх початкові наближення.;
- кількість компонентів генераторного газу (об’єм, потім маса) розрахувати згідно рівнянь (16 – 22).
Таблиця 1 – Результати розрахунків рівноважного складу генераторного газу, отриманого з ідеального вугілля
|
Температура 900 °С, тиск 20 атм., об’ємне співвідношення в дутті: N2 : O2 = 1; Н2О : O2= 1 Вологість повітря = 0 г/м3 | ||||||
|
Компонент |
Прихід, кг |
Вихідний газ, кг |
Витрата в стані рівно-ваги, кг |
Рівноважний об’єм, м3. |
Рівноважний склад, % об. |
Довідник. данні, % об. |
|
Вугілля |
100,00 |
- |
19,20 |
- |
- |
- |
|
Пара |
50,00 |
- |
- |
- |
- |
- |
|
О2(збагаче-не повітря) |
88,89 |
- |
- |
- |
- |
- |
|
N2(збагаче-не повітря) |
77,78 |
- |
- |
- |
- |
- |
|
СО2 |
- |
0,00 |
|
|
СО2 |
11,05 |
|
СО |
- |
233,33 |
|
|
СО |
43,10 |
|
Н2 |
- |
5,56 |
|
|
Н2 |
16,10 |
|
СН4 |
- |
0,00 |
|
|
СН4 |
1,04 |
|
N2 |
- |
77,78 |
|
|
N2 |
23,42 |
|
Н2О |
- |
0,00 |
|
|
Н2О |
5,29 |
|
Всього |
316,67 |
316,67 |
|
|
Всього |
100,00 |
Результати розрахунків зводяться в таблицю 1 рівноважного складу продуктів газифікації, в якій для кожного компоненту генераторного газу надати кількісні значення об’єму, м3, об’ємного відсотку, значення маси, кг, масового відсотку, також в таблиці відобразити вміст золи, яка надходить в складі вугілля. Вміст кожного компоненту надати для вологого генераторного газу.
Виконати розрахунок для реального високозольного вугілля – таблиця 2 (на відміну від ідеального вугілля врахувати присутність в складі реального вугілля всіх компонентів) з використанням стехіометричної кількості пари і кисню (повітря збагачене киснем): Х2 = 1, Х1 = 1. Вологість повітря для реального розрахунку Wpov – 17 г/м3.
Таблиця 2– Склад вугілля різного походження
|
Склад низькозольного вугілля, % |
Склад високозольного вугілля, % | ||
|
Вуглець, C |
83,5 |
Вуглець |
57,6 |
|
Водень, H |
2,4 |
Водень |
3,1 |
|
Сірка, S |
2,2 |
Сірка |
0,3 |
|
Азот, N |
1 |
Азот |
0,5 |
|
Кисень, O |
0,9 |
Кисень |
4,7 |
|
Зола, Z |
4,8 |
Зола |
25,8 |
|
Волога, W |
5,2 |
Волога |
8 |
В таблиці 3 надано деякі контрольні цифри для перевірки розрахунків, комірки (-) не заповнюються.
Таблиця 3 – Результати розрахунків рівноважного складу генераторного газу, отриманого з реального високозольного вугілля
|
Тем-ра 900 °С, тиск 20 атм., об’ємне співвідношення в дутті: Х1=N2 : O2 = 1; Х2=Н2О : O2 = 1. Вологість повітря = 17 г/м3 | |||||
|
Компонент |
Прихід, кг |
Вихідна суміш, кг |
Витрата в стані рівноваги, кг |
Рівноважний об’єм, м3. |
Рівноважний склад, % об. |
|
Вугілля, в т.ч. С і зола: |
100 |
- |
- |
- |
- |
|
Вуглець |
57,6 |
- |
6,489 |
- |
- |
|
Зола |
25,8 |
25,8 |
25,8 |
- |
- |
|
Пара |
26,156 |
- |
- |
- |
- |
|
О2(збагачене повітря) |
46,5 |
- |
- |
- |
- |
|
N2 (збагачене повітря) |
40,688 |
- |
- |
- |
- |
|
Волога повітря |
1,1067 |
- |
- |
- |
- |
|
СО2 |
- |
0 |
|
|
|
|
СО |
- |
134,4 |
|
|
|
|
Н2 |
- |
6,281 |
|
|
|
|
СН4 |
- |
0 |
|
|
|
|
N2 |
- |
41,188 |
|
|
|
|
Н2О |
- |
6,463 |
|
|
|
|
H2S |
- |
0,319 |
|
|
|
|
Всього |
214,45 |
214,45 |
214,45 |
193,256 |
100 |
Особливістю запропонованої математичної моделі є можливість складання матеріального балансу, при цьому розраховується необхідна кількість дуття певного складу на задану масу вугілля – стовпчик 2, кількість вихідного газу, що утворюється згідно реакцій (13 – 15) – стовпчик 3, кількість і склад отриманого генераторного газу – стовпчики 4 – 6. При відносно низьких температурах відбувається неповна газифікація вугілля: в стовпчику 4 надано масу вуглецю (недопал), що не прореагував. Недопал визначається як різниця між приходом і масою генераторного газу (витрата в стані рівноваги, кг) разом з золою.
Контрольні запитання
Реакції газифікації твердого палива, склад генераторного газу в залежності від його призначення і складу окислювачів. Способи компенсації ендотермічних ефектів при газифікації. Принцип термодинамічного і матеріального розрахунків процесів газифікації вугілля:
Література
Товажнянський, Л.Л. Технологія зв’язаного азоту: Підручник / Л.Л. Товажнянський, О.Я. Лобойко та ін. – Харків: НТУ «ХПІ», 2007. –
536 с.
Химические вещества из угля. / Под общей редакцией Ю. Фальбе – М.: Химия, 1980. – 616 с.
Шиллинг, Г.Д. Газификация угля. / Шиллинг Г.Д., Бонн Б., Краус У.; Пер с нем и ред.. С.Р. Исламов – М.: Недра, 1986. – с. 175.
Справочник азотчика. / Под редакцией Е. Я. Мельникова. – М.: Химия, 1967. – 492 с.
5. Jarungthammachote, A. Dutta Energy. Thermodynamic equilibrium model and second law analysis of a downdraft waste gasifier. – Field of Study, School of Environment, Resources and Development, Asian Institute of Technology, P.O. Box 4, Klongluang, Pathumthani 12120, Thailand, Received 9 August 2006.– 10р.
6. Концевой, А.Л. Алгоритм и программа термодинамического расчета газификации твердого топлива / А.Л. Концевой, М.В. Голубева – Сборник трудов XXIV Международная научная конференция. Математические методы в технике и технологиях.: в 10 т. Т. 7. Секция 11 / под общ. ред. В.С. Балакирева. – Пенза: пенз. гос. технол. ак-мия, 2011. – 156 с.
7. Концевой, А.Л. Термодинамічні аспекти газифікації вугілля з врахуванням його складу та складу дуття / А.Л. Концевой, М.В. Голубева – ІІІ Всеукраїнський з’їзд екологів з міжнародною участю. Україна, Вінниця, 21 – 24 вересня 2011 р. Збірник наукових статей, т.2, с. 581 – 584.
