
- •Розрахунки в середовищі excel Розділ 1. Розрахунок кінетичних параметрів топохімічних реакцій
- •Індивідуальна самостійна робота
- •Розділ 2. Статистична обробка результатів експерименту
- •2.1. Кореляційний аналіз
- •2.2. Довірчий інтервал
- •Контрольні питання
- •Література
- •Розділ 3. Розрахунок кінетичних параметрів хімічних реакцій
- •Література
- •Розділ 4. Оптимізація об'єктів досліджень за моделями другого порядку
- •Література
- •Розділ 5. Розрахунки математичних моделей "склад - властивість"
- •Література
- •Розділ 6. Розрахунок кінетичних параметрів за дериватографічними даними
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Розділ 7. Розрахунок очищення коксового газу від сірководню
- •Алгоритм розрахунку
- •Розділ 8. Розрахунок виробництва водню мембранним методом
- •Алгоритм розрахунку [1]
- •Контрольні питання
- •Розділ 9. Розрахунок паро – повітряної конверсії метану
- •Вихідні дані (додаткові)
- •Контрольні питання
- •Розділ 10. Розрахунок двоступеневої
- •Розділ 11. Розрахунок матеріального балансу синтезу метанолу
- •Розділ 12. Розрахунок матеріального балансу синтезу аміаку
- •Алгоритм розрахунку
- •Контрольні питання
- •Розділ 13. Розрахунок очищення газу від co2 розчином моноетаноламіну
- •Алгоритм розрахунку Розрахунок матеріального балансу виробництва
- •Стадія «тонкого» очищення
- •Стадія «тонкого» очищення
- •Концентрації компонентів суміші с(і)2відповідають даним таблиці 3.
- •2 Розрахунок теплового балансу виробництва
- •Де ∑m(mea)р-ну - сума витрат розчину меа на «грубе» та «тонке» очищення, кг меа/год.
- •3 Розрахунок насадкового абсорбера верхня частина абсорбера («тонке» очищення)
- •Алгоритм розрахунку
- •Швидкість захлинання абсорбера у верхній частині [3]:
- •Робоча швидкість газу у верхній частині абсорбера:
- •Нижня частина абсорбера («грубе» очищення)
- •Алгоритм розрахунку
- •Швидкість захлинання абсорбера у нижній частині [3]:
- •Робоча швидкість газу у нижній частині абсорбера:
- •4 Розрахунок тарілчастого абсорбера
- •Верхня частина абсорбера
- •Алгоритм розрахунку
- •Нижня частина абсорбера
- •Алгоритм розрахунку
- •Промисловий абсорбер має 15 тарілок: 9 в нижній частині і 6 у верхній.
- •Розділ 14. Аналіз статики іонного обміну однозарядних (рівнозарядних) іонів
- •Рівновага іонного обміну рівновалентних іонів
- •Алгоритм розрахунку
- •Контрольні питання
- •Література
- •Розділ 15. Аналіз статики іонного обміну різнозарядних іонів
- •Алгоритм розрахунку
- •Контрольні питання
- •Література
- •Розділ 16. Розрахунок очищення газу від оксиду карбону (IV) гарячим розчином поташу
- •1 Матеріальний розрахунок
- •Алгоритм розрахунку
- •1.1 Розрахунок грубого очищення
- •1.2 Розрахунок тонкого очищення
- •2 Тепловий баланс поташного очищення конвертованого газу
- •Алгоритм розрахунку
- •3 Конструктивні розрахунки насадкового абсорберу
- •3.1 Розрахунок діаметру абсорберу Нижня зона
- •Алгоритм розрахунку
- •Верхня зона
- •Алгоритм розрахунку
- •3.2 Розрахунок висоти насадки
- •Верхня зона
- •Алгоритм розрахунку
- •Нижня зона
- •Алгоритм розрахунку
- •1. Розрахувати реальний вміст компонентів k2co3,kнco3і н2о в розчинах згідно даних таблиці 10. Врахувати стехіометрію реакції
- •Розрахунок матеріального балансу
- •Розрахунок теплового балансу
- •Алгоритм розрахунку
- •Конструктивний розрахунок
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Література
- •Розрахунки в середовищіmathcad розділ 18. Розрахунок рівноваги оборотних реакцій
- •Розділ 19. Розрахунок трубчатого реактора конверсії природного газу
- •Алгоритм розрахунку
- •Розділ 20. Розрахунок рівноваги пароповітряної конверсії метану
- •Розділ 21. Розрахунок окиснення оксиду сульфуру (IV)
- •Контрольні питання
- •Література
- •Розділ 22. Альтернативний розрахунок матеріального балансу синтезу аміаку
- •Контрольні питання
- •Розділ 23. Альтернативний розрахунок матеріального балансу синтезу метанолу
- •Розділ 24. Розрахунок паро-вуглекислотної конверсії природного газу
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Розділ 25. Розрахунок вуглекислотної рівноваги у водних розчинах
- •Алгоритм розрахунку
- •Значення рН буде приймати значення 4, 5, 6, 7, ..... До значення –log(Kw). Важливо! Отримані числові значення параметра не утворюють матрицю, тому з ними не можливі дії, що застосовуються до матриці.
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Розділ 26. Аналіз динаміки іонного обміну однозарядних іонів
- •2 Хвильове рівняння для концентрації
- •3 Рівняння збереження в безрозмірній формі [1]
- •4 Рівняння ізотерми іонного обміну
- •5 Рішення хвильового рівняння методом характеристик [1]
- •6 Розрахунок обміну однозарядних іонів[1]
- •Алгоритм розрахунку
- •Вихідні дані для 1-ої ступені водопідготовки
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Література
- •Розділ 27. Термодинамічний та матеріальний розрахунки газифікації вугілля
- •Розділ 28. Термодинамічний розрахунок газифікації (конверсії) вуглеводнів
- •Алгоритм розрахунку
- •.Індивідуальна самостійна робота
- •Контрольні питання
- •Література
- •Розділ 29. Розрахунок концентрацiй iонiв у вапнованiй та коагульованiй воді
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Література
- •Розділ 30. Аналіз динаміки іонного обміну різнозарядних іонів
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Література
- •Розділ 31. Термодинамічний розрахунок газифікації рідких палив невідомої формули
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Розділ 32.Розрахунок поличних колон синтезу аміаку
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Література
- •Методичні рекомендації до виконання розрахункової роботи
- •Розрахунок матеріального балансу виробництва
- •Розрахунок енергетичного (теплового) балансу виробництва
- •Розрахунок основних реакторів
- •Захист розрахункової роботи
- •Завдання на розрахункову роботу з дисципліни
Вихідні дані для 1-ої ступені водопідготовки
Лінійна швидкість води: w=10 м/год.
Висота шару іоніту L=2,5 м.
Час роботи фільтра у міжрегенераційний період τ=20 год.
Граничні значення точок Z: Zmin:=0 Zmax:=1,
число
кроків інтегрування Ni:=40 , індекс
![]()
Незалежна
змінна - час в безрозмірній формі t=
τ
w/L. Згідно
цієї формули і вихідних даних tmin:=0; tmax
= 20∙10/2.5 = 80, отже tmax:=80, число кроків
інтегрування Nj:=80, індекс
![]() .
.
Алгоритм розрахунку
В розрахунковому блоці 1 спочатку задається початкове розподілення концентрації вздовж фільтра С(Z). В точках Z починаються характеристики, на яких зберігаються значення C у часі. Друге співвідношення задає хвильову швидкість як функцію концентрації С(Z). Третє співвідношення являється рівнянням характеристики. Подальші обчислення основані на тому, що характеристики являються лініями функції C(Z, t).
В блоці 2 створені набори значень вихідних точок Z , в яких починаються характеристики, і моментів часу t, для яких будуть проводитися розрахунки.
В блоці 3 створена сітка на площині (Z, T) з вузлами, проіндексованими як (i, j) і в цих вузлах розрахована концентрація. При цьому Т =t/tmax – відносний час, що змінюється від 0 до1.



5. Побудувати тривимірні графіки f(Z1, T,C) та f(Z2, T,C).
Для цього на панелі інструментів Graph вибрати 3D Scatter Plot. Для побудови тривимірного графіку у полі, яке з’являться у нижньому лівому кутку області побудови графіка, у дужках зазначаються змінні, відносно яких буде побудовано графік - (Z1, T,C) та (Z2, T,C), відповідно.
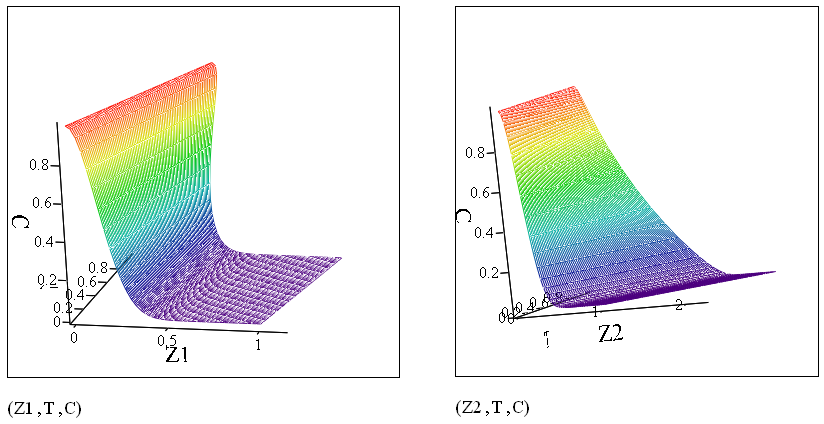
Рисунок 4 – Розподіл концентрації іона, що поглинається, у часі T та за висотою фільтра Z.
Для представлення графік у більш наглядному ракурсі необхідно увійти у вікно побудови графіка та одночасно затискуючи ліву клавішу миші повертати графік (рухами миші), доки не буде досягнуто найбільшої наочності побудованої поверхні.
У вікні “3D Plot Format” (яке відкривається при подвійному кліку лівою клавішею миші на області графіку) у вкладці “General” поставити відмітку “Surface Plot”, у вкладці “Appearance” у полі “Line Options” поставити відмітку в пункті “Colormap” для відображення залежностей у вигляді «веселкової» палітри.
6. Побудувати залежності концентрацій вздовж осі фільтру Сі,0, Сі,40, Сі,80 від Z1i,0, Z1i,40, Z1i,80 (при k1) та Сі,0, Сі,40, Сі,80, від Z2i,0, Z2i,40, Z2i,80 (при k2). Цифри 0, 40, 80 відповідають моментам безрозмірного часу t.

Рисунок 5 – Залежності концентрацій іона, що поглинається, вздовж осі фільтра для різних моментів часу.
7. Проаналізувати графічні залежності розв’язків хвильового рівняння методом характеристик для опуклої та увігнутої ізотерм іонного обміну за матеріалами розділу 7. Визначити ефективність іонного обміну для обох видів ізотерм: порівняти час t, при якому концентрація на виході близька до 0 при значенні координати Z=1.
Додатковий теоретичний матеріал з динаміки іонного обміну [3]
Динаміка іонного обміну може бути описана за допомогою моделі динаміки рівноважної ізотермічної адсорбції.
Приймемо, що між концентраціями адсорбтива (іонів, що поглинаються) та адсорбенту (іоніту) в кожен момент часу та у кожній точці шару існує рівноважне співвідношення. Також виділення теплоти у шарі нескінченно малі, а температури потоку та адсорбенту однакові і процес відбувається за відсутності повздовжньої дифузії.
У відповідності до зроблених припущень процес динаміки сорбції може бути описаний за допомогою системи рівнянь (див. розділ 1):
 .
(16)
.
(16)
Система (16) має два розв’язки: один за наявності кінцевого градієнту концентрацій у колонці (випадок 1), інший – за, так званого, «обривного» фронту (випадок 2) – фронт такої гіпотетичної форми, за якої концентрація адсорбтиву стрибкоподібно змінюється з с = с0 до с = 0. Ці розв’язки записуються наступним чином:
випадок 1:
![]() ,
(17)
,
(17)
випадок 2:
![]() ,
(18)
,
(18)
де Ui
– швидкість руху концентраційної точки
і
шаром адсорбенту,
![]() - похідна ізотерми адсорбції у точціі,
U – швидкість руху усіх точок «обривного»
фронту; с0
— концентрація адсорбтиву у потоці; q0
– рівноважна їй величина адсорбції.
- похідна ізотерми адсорбції у точціі,
U – швидкість руху усіх точок «обривного»
фронту; с0
— концентрація адсорбтиву у потоці; q0
– рівноважна їй величина адсорбції.
Рівняння (17) носить назву закону Вікке, рівняння (18) – закону Вільсона. Дослідимо дію цих законів для різних ізотерм адсорбції.
Опукла ізотерма адсорбції
Ізотерма адсорбції q = f(c) та криві розподілу концентрацій q = q(z) для різних проміжків часу зображені на рисунку 5.
Нехай початковому розподілу відповідає лінія τ0. Оскільки фронт не обривний, то кожна точка цього початкового розподілу буде переміщуватись шаром зі своєю характерною швидкістю, що задається рівнянням (17).
Нехай рух потоку шаром направлений у бік зменшення концентрацій.
а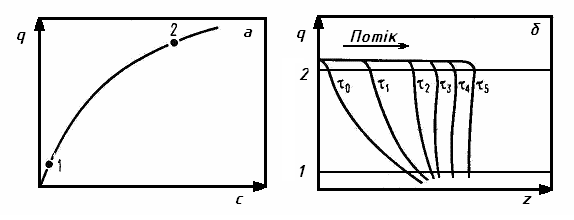 – опукла ізотерма; б – криві розподілу
концентрацій у шарі адсорбенту
– опукла ізотерма; б – криві розподілу
концентрацій у шарі адсорбенту
Рисунок 5 – Опукла ізотерма адсорбції та розподілення концентрацій у шарі адсорбенту при адсорбції.
Виділимо на ізотермі дві точки (1 та 2), зміщення яких по шару від початкового положення τ0 буде предметом аналізу. Для наведеного на рисунку 5 виду ізотерми (dq/dc)1 > (dq/dc)2, тому, згідно з (17), U1 < U2. Це свідчить про те, що відстань між точками 1 та 2, що початково задана розподілом τ0, зменшується – точки зближуються. Таким чином розподіл τ0 трансформується у розподіл τ1, τ2 і т.п. з поступово зростаючим градієнтом концентрацій. За обривного фронту дія закону Вікке зупиняється та всі точки розподілу (τ5 та т.п.) поширюються з однаковою швидкістю U, що визначається законом Вільсона (18 ): U1 < U < U2.
Лінійна ізотерма адсорбції
Для лінійної ізотерми адсорбції рівняння (17) співпадає з рівнянням (18). Тому, незалежно від напрямку руху потоку та виду початкового розподілу точки переміщуються шаром з постійною швидкістю U1 = U = U2 та будь-який початковий розподіл зберігає свою конфігурацію.
Увігнута ізотерма адсорбції
Ізотерма та трансформації розподілів наведені на рисунку 6.
Приймемо, що початковий розподіл такий самий, як і у попередньому випадку.
Згідно з ізотермою, (dq/dc)1 < (dq/dc)2, що, у відповідності з рівнянням (17), дає U1 > U2. Таким чином, у умовах, що розглядаються розподіл концентрацій τ0 має тенденцію до нескінченного «розмивання».
а – увігнута ізотерма; б – криві розподілу
концентрацій у шарі адсорбенту
– увігнута ізотерма; б – криві розподілу
концентрацій у шарі адсорбенту
Рисунок 6 – Увігнута ізотерма адсорбції та розподілення концентрацій у шарі адсорбенту при адсорбції
Наведений розгляд найпростішої динаміки сорбції дозволяє зробити ряд важливих висновків:
1. Форма ізотерми адсорбції, в залежності від початкових умов та напрямку руху потоку, є фактором, яких спричинює затиснення або розширення фронту сорбції, що переміщується зернистим шаром.
2. Переміщення фронту сорбції зернистим шаром може бути явищем стадійним (наприклад «розмитий» розподіл перетворюється в «обривний»), при чому на кожній стадії проявляється дія своїх характерних законів.
