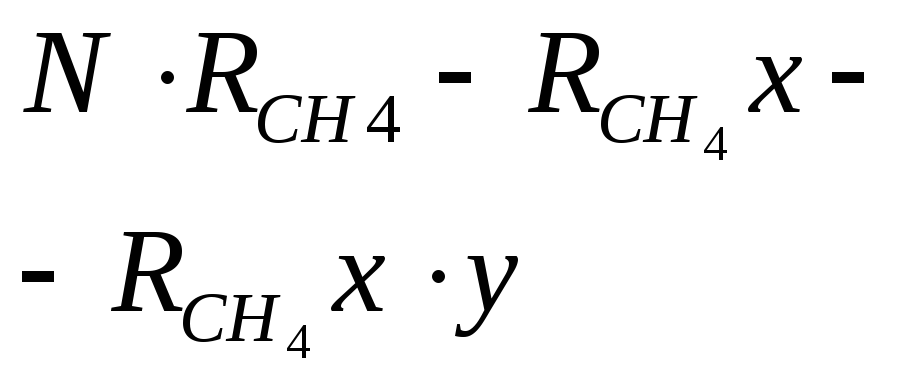- •Розрахунки в середовищі excel Розділ 1. Розрахунок кінетичних параметрів топохімічних реакцій
- •Індивідуальна самостійна робота
- •Розділ 2. Статистична обробка результатів експерименту
- •2.1. Кореляційний аналіз
- •2.2. Довірчий інтервал
- •Контрольні питання
- •Література
- •Розділ 3. Розрахунок кінетичних параметрів хімічних реакцій
- •Література
- •Розділ 4. Оптимізація об'єктів досліджень за моделями другого порядку
- •Література
- •Розділ 5. Розрахунки математичних моделей "склад - властивість"
- •Література
- •Розділ 6. Розрахунок кінетичних параметрів за дериватографічними даними
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Розділ 7. Розрахунок очищення коксового газу від сірководню
- •Алгоритм розрахунку
- •Розділ 8. Розрахунок виробництва водню мембранним методом
- •Алгоритм розрахунку [1]
- •Контрольні питання
- •Розділ 9. Розрахунок паро – повітряної конверсії метану
- •Вихідні дані (додаткові)
- •Контрольні питання
- •Розділ 10. Розрахунок двоступеневої
- •Розділ 11. Розрахунок матеріального балансу синтезу метанолу
- •Розділ 12. Розрахунок матеріального балансу синтезу аміаку
- •Алгоритм розрахунку
- •Контрольні питання
- •Розділ 13. Розрахунок очищення газу від co2 розчином моноетаноламіну
- •Алгоритм розрахунку Розрахунок матеріального балансу виробництва
- •Стадія «тонкого» очищення
- •Стадія «тонкого» очищення
- •Концентрації компонентів суміші с(і)2відповідають даним таблиці 3.
- •2 Розрахунок теплового балансу виробництва
- •Де ∑m(mea)р-ну - сума витрат розчину меа на «грубе» та «тонке» очищення, кг меа/год.
- •3 Розрахунок насадкового абсорбера верхня частина абсорбера («тонке» очищення)
- •Алгоритм розрахунку
- •Швидкість захлинання абсорбера у верхній частині [3]:
- •Робоча швидкість газу у верхній частині абсорбера:
- •Нижня частина абсорбера («грубе» очищення)
- •Алгоритм розрахунку
- •Швидкість захлинання абсорбера у нижній частині [3]:
- •Робоча швидкість газу у нижній частині абсорбера:
- •4 Розрахунок тарілчастого абсорбера
- •Верхня частина абсорбера
- •Алгоритм розрахунку
- •Нижня частина абсорбера
- •Алгоритм розрахунку
- •Промисловий абсорбер має 15 тарілок: 9 в нижній частині і 6 у верхній.
- •Розділ 14. Аналіз статики іонного обміну однозарядних (рівнозарядних) іонів
- •Рівновага іонного обміну рівновалентних іонів
- •Алгоритм розрахунку
- •Контрольні питання
- •Література
- •Розділ 15. Аналіз статики іонного обміну різнозарядних іонів
- •Алгоритм розрахунку
- •Контрольні питання
- •Література
- •Розділ 16. Розрахунок очищення газу від оксиду карбону (IV) гарячим розчином поташу
- •1 Матеріальний розрахунок
- •Алгоритм розрахунку
- •1.1 Розрахунок грубого очищення
- •1.2 Розрахунок тонкого очищення
- •2 Тепловий баланс поташного очищення конвертованого газу
- •Алгоритм розрахунку
- •3 Конструктивні розрахунки насадкового абсорберу
- •3.1 Розрахунок діаметру абсорберу Нижня зона
- •Алгоритм розрахунку
- •Верхня зона
- •Алгоритм розрахунку
- •3.2 Розрахунок висоти насадки
- •Верхня зона
- •Алгоритм розрахунку
- •Нижня зона
- •Алгоритм розрахунку
- •1. Розрахувати реальний вміст компонентів k2co3,kнco3і н2о в розчинах згідно даних таблиці 10. Врахувати стехіометрію реакції
- •Розрахунок матеріального балансу
- •Розрахунок теплового балансу
- •Алгоритм розрахунку
- •Конструктивний розрахунок
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Література
- •Розрахунки в середовищіmathcad розділ 18. Розрахунок рівноваги оборотних реакцій
- •Розділ 19. Розрахунок трубчатого реактора конверсії природного газу
- •Алгоритм розрахунку
- •Розділ 20. Розрахунок рівноваги пароповітряної конверсії метану
- •Розділ 21. Розрахунок окиснення оксиду сульфуру (IV)
- •Контрольні питання
- •Література
- •Розділ 22. Альтернативний розрахунок матеріального балансу синтезу аміаку
- •Контрольні питання
- •Розділ 23. Альтернативний розрахунок матеріального балансу синтезу метанолу
- •Розділ 24. Розрахунок паро-вуглекислотної конверсії природного газу
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Розділ 25. Розрахунок вуглекислотної рівноваги у водних розчинах
- •Алгоритм розрахунку
- •Значення рН буде приймати значення 4, 5, 6, 7, ..... До значення –log(Kw). Важливо! Отримані числові значення параметра не утворюють матрицю, тому з ними не можливі дії, що застосовуються до матриці.
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Розділ 26. Аналіз динаміки іонного обміну однозарядних іонів
- •2 Хвильове рівняння для концентрації
- •3 Рівняння збереження в безрозмірній формі [1]
- •4 Рівняння ізотерми іонного обміну
- •5 Рішення хвильового рівняння методом характеристик [1]
- •6 Розрахунок обміну однозарядних іонів[1]
- •Алгоритм розрахунку
- •Вихідні дані для 1-ої ступені водопідготовки
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Література
- •Розділ 27. Термодинамічний та матеріальний розрахунки газифікації вугілля
- •Розділ 28. Термодинамічний розрахунок газифікації (конверсії) вуглеводнів
- •Алгоритм розрахунку
- •.Індивідуальна самостійна робота
- •Контрольні питання
- •Література
- •Розділ 29. Розрахунок концентрацiй iонiв у вапнованiй та коагульованiй воді
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Література
- •Розділ 30. Аналіз динаміки іонного обміну різнозарядних іонів
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Література
- •Розділ 31. Термодинамічний розрахунок газифікації рідких палив невідомої формули
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Розділ 32.Розрахунок поличних колон синтезу аміаку
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Література
- •Методичні рекомендації до виконання розрахункової роботи
- •Розрахунок матеріального балансу виробництва
- •Розрахунок енергетичного (теплового) балансу виробництва
- •Розрахунок основних реакторів
- •Захист розрахункової роботи
- •Завдання на розрахункову роботу з дисципліни
Розділ 24. Розрахунок паро-вуглекислотної конверсії природного газу
Для одержання вихідного газу і його підготовки для синтезу метанолу використовують паро - вуглекислотну конверсію природного газу. На рисинку 1 надано енерготехнологічну схему агрегату синтезу метанолу, частина якої відноситься до стадії паро-вуглекислотної конверсії. Природний газ із заводського колектора під тиском біля 12 атм проходить загальний витратомір і розподіляється на два потоки. Перший потік змішують з продувними газами синтезу метанолу у співвідношенні приблизно 8 : 1 і направляють в сепаратор 1 для відділення від рідких вуглеводнів. Після сепаратора природний газ поступає на стиснення в відцентровий компресор 3, звідки при температурі 110°С і тиску 30 атм подається у вогневий підігрівач 4. Із підігрівача газ при температурі 400°С поступає на гідрування сіркоорганічних сполук в реактор 5, заповнений алюмо-кобальт-молібденовим каталізатором, а потім на поглинання сірководню у адсорбер 6, заповнений поглиначем на основі оксиду цинку.
Вміст сірковмісних сполук після адсорбера не повинно перевищувати 0,5 мг/м3. Очищений природний газ змішують з двооксидом вуглецю (змішувач на схемі на вказаний) у співвідношенні СО2 : СН4 = 0,2 і з водяною парою у співвідношенні Н2О : СН4 = 4,0. Двооксид вуглецю перед дозуванням в природний газ стискають компресором 8. Водяну пару після спрацьовування в турбінні 37 поступає на конверсію із парового колектора під тиском 40 атм.
Отриману парогазову суміш при температурі 360°С направляють в підігрівач 18, звідки вона при температурі 540°С і тиску 25 атм через розподільчі колектори попадає в реакційні труби, встановлені в радіаційній камері трубчатої печі 19.

Рисунок – Принципова енерготехнологічна схема виробництва синтезу метанолу в агрегаті потужністю 900 т на добу:
1 – сепаратор; 2 – парова турбіна; 3 – турбокомпресор природного газу; 4, 32 – вогневі підігрівачі; 5- реактор гідрування сірковмісних сполук; 6 – адсорбер; 7, 9 – парові турбіни; 8 – компресор вуглекислого газу; 10 – димова труба; 11 – димосос,
12 – підігрівач топкового газу; 13 – економайзер; 14 – трубні пучки пароутворення;
15 – допоміжний котел; 16 – парозбірник; 17 – пароперегрівач; 18 – підігрівач парогазової суміші; 19 – трубчата піч; 20 – горілки трубчатої печі і допоміжного котла; 21 – котел-утилізатор конвертованого газу; 22 – підігрівач деаерованої живильної води; 23 – економайзер; 24 – установка деаерації; 25 – насос питної води; 26 – турбіна насоса питної води; 27 – повітряні конденсатори; 28 – сепаратор синтез-газу; 29 – сепаратор; 30 – повітряний холодильник колони синтезу; 31 – колона синтезу метанолу;
33 - турбокомпресор циркуляційного газу; 34 – підігрівач синтез-газу;
35 – турбокомпресор синтез-газу; 36 – парова турбіна циркуляційного компресора;
37 – парова турбіна компресора синтез-газу.
В реакційних трубах, заповнених нікелевим каталізатором, відбувається паро-вуглекислотна конверсія природного газу. Конвертований газ виходить із шару каталізатора при температурі 850 – 870°С і тиску 18 атм. Вміст залишкового метану і двооксиду вуглецю не перевищує 3 і 12% об. (в перерахунку на сухий газ), стехіометричний показник процесу (Н2 - СО2) : (СО + СО2) = 2,0 – 2,2.
Вологий конвертований газ із трубчатої печі попадає в котел-утилізатор 21, охолоджується приблизно до 280°С, проходить послідовно підігрівач деаерованої води 22 і хімічно очищеної води (перед деаерацією) 23, у яких охолоджується відповідно до 120 і 95°С. Потім газ остаточно охолоджується і відділяється від конденсату у повітряному конденсаторі 27 і сепараторі 28. Сухий очищений синтез-газ при 35-40°С і 18 атм поступає у відцентровий компресор 35, виходить із нього при 55 атм, змішується з циркуляційним газом, що поступає від компресора 33, і через теплообмінник 34 і вогневий підігрівач 32 направляється на синтез метанолу в колону 31.
Другий потік природного газу із заводського колектора після витратоміра змішують з продувними і танковими газами синтезу метанолу у співвідношенні відповідно 1 :2,3 :1 і направляють на спалювання в горілки вогневих підігрівачів 4 і 32, підігрівач топкового газу 12, горілки труб трубчатої печі і допоміжного котла 20, а також пускового котла (на схемі не вказано). Паровий конденсат із сепаратора 28 поступає у відділення хімічної підготовки води, куди подають також конденсат від парових турбін і додаткову свіжу воду. Хімічно очищена води проходить підігрівач 23, установку деаерації 24, насос живильної води 25, підігрівач 22 і при температурі 240°С поступає в економайзер (водопідігрівач) 13, розташований в конвективній камері трубчатої печі.
Із економайзера вода при температурі близько 250°С стікає в парозбірник 16, звідки частина її поступає в котел-утилізатор 21, а залишкова кількість – в пучок пароутворення 14 конвективної камери печі і у допоміжний котел 15. Насичена пара із котла 21, пучка пароутворення 14 і котла 15 повертається в парозбірник 16 при температурі близько 300°С і тиску 100 атм. Пара із парозбірника поступає в пароперегрівач 17, із якого при тиску 104 атм і температурі близько 480°С подається на парову турбіну 37 компресора свіжого синтез-газу. Після турбіни пару тиском 40 ати направляють в загальний колектор, із якого вона далі поступає на парові турбіни 2, 7, 9, 26, 36.
Продукти синтезу через теплообмінник 34 і повітряний холодильник 30 попадають в сепаратор метанолу-сирцю 29. Газ із сепаратора направляють на стиснення в циркуляційний компресор 33. Димові гази із конвективної зони трубчатої печі при температурі не вище 200°С димососом 11 викидаються в атмосферу через димову трубу 10.
Описана схема конверсії і енергопостачання в поєднанні з синтезом метанолу при тиску 50 атм дозволяє різко знизити вартість метанолу порівняно зі старими схемами виробництва.
Основним компонентом природного газу є метан. Тому основні процеси, що перебігають при конверсії, можна описати наступними реакціями:
CH4 + H2O ↔ CO + 3H2 (1)
CO + H2O ↔ CO2 + H2 (2)
CH4 + CO2 ↔2CO + 2H2 (3)
Завдяки реакціям (1) і (3) підтримують необхідне для синтезу метанолу співвідношення CO і H2. З точки зору термодинаміки реакція (3) є залежною - (3) = (1) - (2). і рівновага процесу описується системою 2 рівнянь:

 (4)
(4)
Склад конвертованого газу для синтезу метанолу
задається співвідношенням, що називається функціоналом f :
 (5)
(5)
Початковий і кінцевий склад газової суміші, а також парціальний тиск її компонентів при встановленні рівноваги описуються рівняннями, що наведені в таблиці.
Умовні позначення:
![]() –об’єм
відповідно СН4,
СО2
в вихідному газі, м3.
–об’єм
відповідно СН4,
СО2
в вихідному газі, м3.
N - співвідношення пара/метан на вході; Р - тиск процесу, атм;
x - ступінь перетворення CH4 за реакцією (1), частка;
y - ступінь перетворення СО за реакцією (2), частка.
Таблиця – Розрахункові рівняння складу газової суміші
|
Компонент |
Об’єм, м3 |
Рівноважний тиск компонентів | |
|
вихідний |
рівноважний | ||
|
СН4 |
|
|
|
|
H2О |
|
|
|
|
СО |
- |
|
|
|
СО2 |
|
|
|
|
H2 |
- |
|
|
|
Всього |
Σ |
|
|
З врахуванням виразів парціального тиску з таблиці рівняння
(4) і (5) набувають вигляду:
 (6)
(6)
 (7)
(7)
 (8)
(8)
Значення констант рівноваги К1 и К2 визначаються за формулами:
![]() ;
(9)
;
(9)
![]() .
(10)
.
(10)
Мета роботи: реалізація в середовищі MathCad розрахунку витрати вуглекислого газу, рівноважних (практичних) ступенів перетворення і складу газової суміші.
Вихідні дані
Об’єм
сухого метану, м3:
![]() – 1000. Тиск процесу, атм: Р – 1.
– 1000. Тиск процесу, атм: Р – 1.
Співвідношення пара/метан на вході в конвертор: N – 1.3.
Температура конверсії, К: Т – 1100. Значення функціоналу: f – 1.35.
Алгоритм розрахунку
1. Розрахувати константи К1 и К2 за формулами (9) і (10): Т1=Т2=Т.
2. Задати
начальні наближення x = 0.8, y= 0.1, Rco2
= 0,1.![]() .
.
Вирішити систему рівнянь (6) – (8) відносно x, y і Rco2. за допомогою операторів Given і Find, між якими вводяться ці рівняння
Присвоїти вектору рішення функцію Find: Z:=Find(x, y, Rco2). Привласнити x:=Z0 y:=Z1 Rco2:=Z2. Зауваження: для деяких значень начальних наближень система рішення не має.
Розрахувати рівноважний склад вологого і сухого конвертованого газу (м3, %) за формулами таблиці і представити у матричному вигляді.
Зробити розрахунок для f=2 і значень технологічних параметрів згідно вищенаведеного опису технологічної схеми.