
- •1. Физическая химия: цель, задачи, методы исследования. Основные понятия физической химии.
- •3 .Следствия первого начала термодинамики ( изохорный и изобарный процессы). Способы записи теплот химических реакций.
- •4. Закон Гесса, его следствия. Взаимосвязь между тепловым эффектом химической реакции при постоянном объеме и давлении.
- •7. Зависимость тепловых эффектов химических реакций от температуры. Уравнение Киргоффа. Определение реакции при нестандартной температуре.
- •9. Работа расширения для идеальных газов при адиабатическом процессе. Вывести уравнения адиабат.
- •11. II закон термодинамики для обратимых и необратимых процессов. Свойства энтропии.
- •12.Расчет изменения энтропии для различных физико-химических процессов: нагревание, фазовые переходы, смешение идеальных газов, изобарный, изотермический, изохорныйпроцессы.
- •13. Расчет изменения энтропии реакции при стандартной и нестандартной температурах (на примере реакций с участием неорганических веществ)
- •14.Изохорно-изотермический потенциал, его свойства, применение в качестве критерия направленности процесса.
- •15. Изобарно-изоэнтропийный потенциал, его свойства, применение в качестве критерия направленности процесса.
- •16) Изобарно-изотермический потенциал, его свойства, применение в качестве критерия направленности процесса
- •17. Изохорно-изоэнтропийный потенциал, его свойства, применение в качестве критерия направленности процесса.
- •17. Изохорно-изоэнтропийный потенциал, его свойства, применение в качестве критерия направленности процесса.
- •18) Уравнение Гиббса – Гельмгольца. Определение изменения энергии Гиббса реакции при не стандартной температуре.
- •19) Химический потенциал, определение, условие равновесия в открытых системах. Химический потенциал идеальных и реальных систем (газы, растворы).
- •20) Химическое равновесие, вывод уравнения изотермы химической реакции. Определение стандартного значения константы равновесия реакций.
- •23) Влияние температуры на константу равновесия, вывод уравнения изобары Вант- Гоффа. Принцип Ле- Шателье.
- •25) Расчёт теп.Эф х.Р. На основе изобары Вант-Гоффа (расчётный и граф. Способы).
- •26) Расчёт теп.Эф х.Р. На основе изохоры Вант-Гоффа (расчётный и граф. Способы).
- •27)Фазовые равновесия основные опр-я:
- •28)Равновесие чис-го в-ва в 2-х фазах одноком.Сис-мы.
- •29) Определение теплоты спарение расчетным и графическим способами на основе уравнения Клаузиуса – Клапейрона.
- •30) Гетерогенное равновесие. Бинарные системы. Законы Рауля. Законы Коновалова.
- •31) Основные понятия химической кинетики: скорость, механизм реакции.
- •32) Основной постулат химической кинетики. Гомогенные, гетерогенные реакции. Порядок и молекулярность реакции, отличая между ними.
- •33) Влияние концентрации на скорость химической реакции. Физический смысл, размерность константы скорости.
- •34) Кинетический анализ необратимых реакций первого порядка в закрытых системах.
- •35) Кинетический анализ необратимых реакций второго порядка в закрытых системах.
- •36) Кинетический анализ необратимых реакций нулевого порядка в закрытых системах.
- •37)Реакции 3-ого порядка
- •41. Влияние температуры на скорость химической реакции, правило Вант-Гоффа, закон Аррениуса.
- •42. Энергия активации, ее физический смысл. Методы определения энергии активации.
- •43.Катализ, основные свойства катализатора
- •44. Биогенные каталитические реакции. Кинетический анализ гомогенной каталитической реакции.
- •45. Электрохимия, особенности электрохимических реакций.
- •48. Приближения теории Дебая – Гюккеля, их концентрационные пределы применимости.
- •49) Основы теории электролитической диссоциации
- •50) Основные достоинства и недостатки тэд Аррениуса. Энергия кристаллической решетки, энергия сольватации.
- •51) Свойства буферных растворов, определение их рН, буферная емкость, диаграмма.
- •52) Определение рН гидратообразования и произведения растворимости гирооксидов металлов.
- •53. Удельная электропроводность растворов электролитов, зависимость от температуры и концентрации.
- •54. Молярная электропроводность. Закон Кольрауша. Определение молярной электропроводности при бесконечном разбавлении растворов сильных и электролитов.
- •55. Молярная электропроводность. Влияние температуры и концентрации на молярную электропроводность растворов сильных и слабых электролитов.
- •56. Электролиз, законы электролиза. Электролиз водных растворов солей с инертным анодом (привести пример).
- •57. Определение стандартного значения электродных потенциалов. Уравнение Нернста для определения эдс цепей.
- •58. Классификация электродов, правила записи электродов и цепей.
- •59.Химические цепи(гальванический элемент), их классификация.
- •60.Гальванический элемент. Термодинамика гальванического элемента.
3 .Следствия первого начала термодинамики ( изохорный и изобарный процессы). Способы записи теплот химических реакций.
Химическая термодинамика изучает энергетические эффекты химических процессов; позволяет определить возможность, направление и глубину протекания химического процесса в конкретных условиях. Следствие из I начала термодинамики.
Внутренняя энергия, энтальпия, связь между ними: DH = DU + PDV.
dQV=dU dQP=dH Для изохорного и изобарного процессов теплота процесса приобретает свойства функции состояния. Это положение сформулировано на основании опытных данных Г.И. Гессом и называется законом Гесса. Закон Гесса – математическое следствие I закона термодинамики.
Закон Гесса: тепловой эффект реакции не зависит от пути процесса (промежуточных стадий), а определяется только начальным и конечным состояниями системы, т.е. состоянием исходных веществ и продуктов реакции.
Расчет теплот химических реакций по стандартным теплотам образования и сгорания.
Изохорный процесс (V = const; ΔV = 0).
Поскольку работа расширения равна произведению давления и изменения объема, для изохорного процесса получаем:
![]() (I.1)
(I.1)
![]() (I.2)
(I.2)![]() (I.3)
(I.3)
Следовательно при const=V вся теплота подведенная к системе расходуется на увеличение внутренней энергии или все изменение внутренней энергии обращается в теплоту.
Изобарный процесс (Р = const).
![]() (I.4)
(I.4)
Подставляя полученные выражения для работы различных процессов в уравнение (I.1), для тепловых эффектов этих процессов получим:
![]() (I.5);
(I.5);
![]() (I.6);
(I.6);![]() (I.7)
(I.7)
В уравнении (I.7) сгруппируем переменные с одинаковыми индексами. Получаем:
![]() (I.8)
(I.8)
Введем
новую функцию состояния системы –
энтальпию H, тождественно равную сумме
внутренней энергии и произведения
давления на объем:
![]()
Тогда
выражение (I.8) преобразуется к следующему
виду:
![]() (I.9)
(I.9)
Т.о., тепловой эффект изобарного процесса равен изменению энтальпии системы.
![]() При
этом теплота приобретает св-ва функции
обозначается символом
При
этом теплота приобретает св-ва функции
обозначается символом
![]() (энтальпия)-
эта функция состояния определяется
суммой внутренней энергии и произведением
PV. Из выражения 13 вытекает одна
формулировка 1-ого закона термодинамики.
Когда теплота передается системе при
Р- const она расходуется не только на
увеличение внутренней энергии, но и на
совершение работы расширения системы
т.е. против внешнего давления.
(энтальпия)-
эта функция состояния определяется
суммой внутренней энергии и произведением
PV. Из выражения 13 вытекает одна
формулировка 1-ого закона термодинамики.
Когда теплота передается системе при
Р- const она расходуется не только на
увеличение внутренней энергии, но и на
совершение работы расширения системы
т.е. против внешнего давления.
4. Закон Гесса, его следствия. Взаимосвязь между тепловым эффектом химической реакции при постоянном объеме и давлении.
Как известно, большинство хим. реакций сопровождаются выделением (экзотермические реакции) либо поглощением (эндотермические реакции) теплоты. Первое начало термодинамики дает возможность рассчитать тепловой эффект хим. реакции при различных условиях её проведения.
Тепловой эффект (теплота) химической реакции – количество теплоты, выделившейся либо поглотившейся в ходе реакции. Тепловой эффект относят, как правило, к числу молей прореагировавшего исходного вещества, стехиометрический коэффициент перед которым максимален.
Например, реакцию окисления водорода в хим. термодинамике записывают в виде:
Н2 + 1/2 О2 ––> Н2О
и тепловой эффект рассчитывают на 1 моль водорода.
Теплота образования вещества – тепловой эффект реакции образования 1 моля сложного вещества из простых. Теплоты образования простых в-в принимаются равными нулю.
Теплота сгорания вещества – тепловой эффект реакции окисления 1 моля в-ва в избытке кислорода до высших устойчивых оксидов.
Закон Гесса, является частным случаем первого начала термодинамики:
Тепловой эффект химической реакции, проводимой в изобарно-изотермических или изохорно-изотермических условиях, зависит только от вида и состояния исходных веществ и продуктов реакции и не зависит от пути её протекания.
Закон Гесса: тепловой эффект реакции не зависит от пути процесса (промежуточных стадий), а определяется только начальным и конечным состояниями системы, т.е. состоянием исходных веществ и продуктов реакции.
Выше было показано, что изменение энтальпии ΔН (тепловой эффект изобарного процесса Qp) и изменение внутр. энергии ΔU (тепловой эффект изохорного процесса Qv) не зависят от пути, по которому система переходит из начального состояния в конечное.
Практическое значение закона Гесса состоит в том, что он позволяет рассчитывать тепловые эффекты хим. процессов. Тепловой эффект хим. реакции равен разности сумм теплот образования продуктов реакции и исходных в-в, умноженных на стехиометрические коэффициенты.
Следствия закона Гесса:
![]() (I.20)
(I.20)
Тепловой эффект хим. реакции равен разности сумм теплот сгорания исходных в-в и продуктов реакции, умноженных на стехиометрические коэффициенты.
![]() (I.21)
(I.21)
5. Теплоемкость, виды. Взаимосвязь между теплоемкостью при p=const, V=const (уравнение Майера).
Теплоемкостью называют количество теплоты, которое необходимо сообщить системе для её нагревания на 1 К в условиях отсутствия полезной работы. Различают удельную и молярную теплоемкости. У дельной теплоемкостью С называют количество теплоты, необходимое для нагревания единицы массы вещества на 1К, а молярной теплоемкостью С – количество теплоты, необходимое для нагревания одного моля вещества на 1К.
Различают истинную и среднюю теплоемкости. Под истинной теплоемкостью понимают отношение бесконечно малого количества теплоты, полученного системой, к бесконечно малому приращению температуры, которое при этом наблюдается: C = Q/dT.
Средней молярной теплоемкостью С в интервале температур от Т1 и Т2 называют отношение конечного количества теплоты, подведенного к одному молю вещества, к разности температур Т2-Т1:

Количество
теплоты, переданное телу при постоянном
объеме, равно приращению внутренней
энергии тела
 .
Количество теплоты, переданное телу
припостоянном давлении, равно приращению
энтальпии тела
.
Количество теплоты, переданное телу
припостоянном давлении, равно приращению
энтальпии тела
 .
Отсюдадля
истинной молярной теплоемкости при
постоянном объеме и давлении получаем
выражение:
.
Отсюдадля
истинной молярной теплоемкости при
постоянном объеме и давлении получаем
выражение:

Если постоянство объема или давления указано, то частную производную по температуре можно заменить полной производной и написать (для n молей вещества):
При
V=const QV
= dU = n dT
dT
При
p=const QР
= dH = n dT
dT
В расчетах
 определяют по опытным данным для
определяют по опытным данным для и наоборот. Для этого нужно знать
разность теплоемкостей
и наоборот. Для этого нужно знать
разность теплоемкостей
Для твердых и
жидких тел разность
 мала, так как их объем почти не меняются
от температуры.
мала, так как их объем почти не меняются
от температуры.
Для газов разность
 достаточна
велика и ее нужно учитывать. Внутренняя
энергия идеального газа не зависит от
объема и давления. Продифференциировав
состояние одного моля идеального газа,
получаем соотношение:
достаточна
велика и ее нужно учитывать. Внутренняя
энергия идеального газа не зависит от
объема и давления. Продифференциировав
состояние одного моля идеального газа,
получаем соотношение:
Подставляем полученное выражение, получаем уравнение Майера для идеального газа:
CP - CV = R = 8,314 Дж/(моль*К)
6. Зависимость теплоемкости от температуры. Взаимосвязь между средней и истинной теплоемкостями неорганического вещества p=const (вывод пояснение).
Теплоемкостью называют количество теплоты, которое необходимо сообщить системе для её нагревания на 1 К в условиях отсутствия полезной работы.
Для многих термодинамических расчетов нужно знать значения теплоемкости веществ, участвующих в реакции и зависимость теплоемкости веществ от температуры. Теплоемкости веществ при разных температурах определяются из опыта или вычисляются теоретически. Опытные значения теплоемкости при разных температурах обычно представляют в виде следующих интерполяционных уравнений:

Или

Где a,
b,
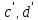 -
коэффициенты.
-
коэффициенты.
Интерполяционные уравнения(1) и (2) пригодны только в том интервале температур, в котором они изучены экспериментально.
Молекулярную
теплоемкость при постоянном объеме
 вычисляют по уравнениям используя
численные значения
вычисляют по уравнениям используя
численные значения ,
найденные по итерполяционным уравнениям
(1) или (2).
,
найденные по итерполяционным уравнениям
(1) или (2).
В термодинамических расчетах часто приходиться вычислять среднюю теплоемкость по данным для истинной теплоемкости при разных температурах и наоборот.
Установим зависимость
между истинной и средней теплоемкостями
при постоянном давлении. Подставляя в
выражение, получаем уравнение для
вычисления средней молярной теплоемкости
в данном интервале температур, зная
истинные теплоемкости
 :
:
 (3)
(3)
 Расчет
Расчет
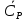 можно провести графически и аналитически,
если известны значения истинной
теплоемкости при нескольких температурах,
то среднюю теплоемкость удобнее
рассчитывать графически. На рисунке
зависимость
можно провести графически и аналитически,
если известны значения истинной
теплоемкости при нескольких температурах,
то среднюю теплоемкость удобнее
рассчитывать графически. На рисунке
зависимость представлена
кривой АВ. Интеграл
представлена
кривой АВ. Интеграл в уравнении (3) представляет собой
площадь
в уравнении (3) представляет собой
площадь под кривой АВ. Средняя теплоемкость
под кривой АВ. Средняя теплоемкость является высотой прямоугольника с
основанием
является высотой прямоугольника с
основанием ,
равновеликого площади
,
равновеликого площади .
Таким образом, измерив площадь
.
Таким образом, измерив площадь под кривой АВ определяем среднюю
теплоемкость
под кривой АВ определяем среднюю
теплоемкость по
уравнению:
по
уравнению:

Где S
– площадь
 .
При этом площадь нужно выразить в
Дж/моль. Аналитическую среднюю
теплоемкость можно рассчитать по (3),
если известна зависимость истинной
теплоемкости от температуры:
.
При этом площадь нужно выразить в
Дж/моль. Аналитическую среднюю
теплоемкость можно рассчитать по (3),
если известна зависимость истинной
теплоемкости от температуры: .
Подставляя уравнение (1) или (2) в (3)
получаем выражения:
.
Подставляя уравнение (1) или (2) в (3)
получаем выражения:

Или

Истинную теплоемкость
можно рассчитать по опытным данным для
средней теплоемкости при разных
температурах. Перепишем равенства (3)
считая температуру
 переменной величиной:
переменной величиной:

Известно, что производная от определенного интеграла по верхнему пределу при постоянном нижнем пределе интегрирования равна подынтегральной функции, поэтому, взяв производную по температуре от уравнения (6), получим:

Средняя теплоемкость
 в интервале температур от
в интервале температур от до
до вычисляется по уравнению:
вычисляется по уравнению:

Где
 -
средние теплоемкости в интервале
температур от 298 К до
-
средние теплоемкости в интервале
температур от 298 К до и от 298 К до
и от 298 К до .
Уравнение (8)
является следствием уравнения (6)
и известного свойства определенного
интеграла:
.
Уравнение (8)
является следствием уравнения (6)
и известного свойства определенного
интеграла:

