
- •1. Физическая химия: цель, задачи, методы исследования. Основные понятия физической химии.
- •3 .Следствия первого начала термодинамики ( изохорный и изобарный процессы). Способы записи теплот химических реакций.
- •4. Закон Гесса, его следствия. Взаимосвязь между тепловым эффектом химической реакции при постоянном объеме и давлении.
- •7. Зависимость тепловых эффектов химических реакций от температуры. Уравнение Киргоффа. Определение реакции при нестандартной температуре.
- •9. Работа расширения для идеальных газов при адиабатическом процессе. Вывести уравнения адиабат.
- •11. II закон термодинамики для обратимых и необратимых процессов. Свойства энтропии.
- •12.Расчет изменения энтропии для различных физико-химических процессов: нагревание, фазовые переходы, смешение идеальных газов, изобарный, изотермический, изохорныйпроцессы.
- •13. Расчет изменения энтропии реакции при стандартной и нестандартной температурах (на примере реакций с участием неорганических веществ)
- •14.Изохорно-изотермический потенциал, его свойства, применение в качестве критерия направленности процесса.
- •15. Изобарно-изоэнтропийный потенциал, его свойства, применение в качестве критерия направленности процесса.
- •16) Изобарно-изотермический потенциал, его свойства, применение в качестве критерия направленности процесса
- •17. Изохорно-изоэнтропийный потенциал, его свойства, применение в качестве критерия направленности процесса.
- •17. Изохорно-изоэнтропийный потенциал, его свойства, применение в качестве критерия направленности процесса.
- •18) Уравнение Гиббса – Гельмгольца. Определение изменения энергии Гиббса реакции при не стандартной температуре.
- •19) Химический потенциал, определение, условие равновесия в открытых системах. Химический потенциал идеальных и реальных систем (газы, растворы).
- •20) Химическое равновесие, вывод уравнения изотермы химической реакции. Определение стандартного значения константы равновесия реакций.
- •23) Влияние температуры на константу равновесия, вывод уравнения изобары Вант- Гоффа. Принцип Ле- Шателье.
- •25) Расчёт теп.Эф х.Р. На основе изобары Вант-Гоффа (расчётный и граф. Способы).
- •26) Расчёт теп.Эф х.Р. На основе изохоры Вант-Гоффа (расчётный и граф. Способы).
- •27)Фазовые равновесия основные опр-я:
- •28)Равновесие чис-го в-ва в 2-х фазах одноком.Сис-мы.
- •29) Определение теплоты спарение расчетным и графическим способами на основе уравнения Клаузиуса – Клапейрона.
- •30) Гетерогенное равновесие. Бинарные системы. Законы Рауля. Законы Коновалова.
- •31) Основные понятия химической кинетики: скорость, механизм реакции.
- •32) Основной постулат химической кинетики. Гомогенные, гетерогенные реакции. Порядок и молекулярность реакции, отличая между ними.
- •33) Влияние концентрации на скорость химической реакции. Физический смысл, размерность константы скорости.
- •34) Кинетический анализ необратимых реакций первого порядка в закрытых системах.
- •35) Кинетический анализ необратимых реакций второго порядка в закрытых системах.
- •36) Кинетический анализ необратимых реакций нулевого порядка в закрытых системах.
- •37)Реакции 3-ого порядка
- •41. Влияние температуры на скорость химической реакции, правило Вант-Гоффа, закон Аррениуса.
- •42. Энергия активации, ее физический смысл. Методы определения энергии активации.
- •43.Катализ, основные свойства катализатора
- •44. Биогенные каталитические реакции. Кинетический анализ гомогенной каталитической реакции.
- •45. Электрохимия, особенности электрохимических реакций.
- •48. Приближения теории Дебая – Гюккеля, их концентрационные пределы применимости.
- •49) Основы теории электролитической диссоциации
- •50) Основные достоинства и недостатки тэд Аррениуса. Энергия кристаллической решетки, энергия сольватации.
- •51) Свойства буферных растворов, определение их рН, буферная емкость, диаграмма.
- •52) Определение рН гидратообразования и произведения растворимости гирооксидов металлов.
- •53. Удельная электропроводность растворов электролитов, зависимость от температуры и концентрации.
- •54. Молярная электропроводность. Закон Кольрауша. Определение молярной электропроводности при бесконечном разбавлении растворов сильных и электролитов.
- •55. Молярная электропроводность. Влияние температуры и концентрации на молярную электропроводность растворов сильных и слабых электролитов.
- •56. Электролиз, законы электролиза. Электролиз водных растворов солей с инертным анодом (привести пример).
- •57. Определение стандартного значения электродных потенциалов. Уравнение Нернста для определения эдс цепей.
- •58. Классификация электродов, правила записи электродов и цепей.
- •59.Химические цепи(гальванический элемент), их классификация.
- •60.Гальванический элемент. Термодинамика гальванического элемента.
23) Влияние температуры на константу равновесия, вывод уравнения изобары Вант- Гоффа. Принцип Ле- Шателье.
1. Влияние температуры на равновесие.
При повышении температуры системы, в которой возможна химическая реакция (системе, находящейся в равновесии, сообщается теплота), согласно принципу Ле Шателье-Брауна усиливается процесс, сопровождающийся поглощением теплоты, т.е. равновесие смещается в сторону эндотермической реакции.Качественные выводы о влиянии температуры на химическое равновесие могут быть получены из общего принципа смещения равновесия, сформулированного Ле-Шателье и Брауном. Этот принцип называется принципом подвижного равновесия: если на систему, находящуюся в устойчивом равновесии, оказывать воздействие извне, изменяя какое-нибудь из условий, определяющих положение равновесия, например, температуру, то в системе усилится то из направлений процесса, протекание которого ослабляет влияние произведенного воздействия. При равенстве энтальпийного и энтропийного факторов ΔН = ТΔS ΔG = 0, что является термодинамическим условием химического равновесия. Скорость реакции (число частиц образующихся в единицу времени в единице объема) в прямом направлении равна скорости реакции в обратном направлении. В этот момент концентрации исходных веществ и продуктов реакции не изменяются во времени и называются равновесными концентрациями. Они обозначаются символом вещества в квадратных скобках.
Константа химического равновесия
При равновесии химической реакции: bB + dD = lL + mM,
![]() или
или
![]()
где pp,L, ppM, pp,D, ppB –равновесные парциальные давления веществ, а [L], [M],[D],[B] –равновесные концентрации веществ; l, m, d, b - показатели степени, равные стехиометрическим коэффициентам.
Из ур-я:
![]() получим
получим![]() (1)
(1)
Продифференцировав выражение (1) по температуре, получаем для зависимости константы равновесия от температуры уравнение (2) – изобару Вант-Гоффа:
![]()
Это изобара равновесия. Она показывает, что константа равновесия экзотермической реакции уменьшается, а эндотермической реакции возрастает с повышением температуры. С увеличением абсолютного значения энтальпии реакции и уменьшением температуры чувствительность константы равновесия (d(lnKp)/dT) к изменению температуры повышается.
2)Характер смещения равновесия можно прогнозировать, применяя принцип французского ученого Ле Шателье:
если на систему, находящуюся в равновесии, оказывается внешнее воздействие, то равновесие смещается в том направлении, которое ослабляет внешнее воздействие.
Принцип Ле Шателье следует из закона действующих масс. Если система находится при постоянной температуре, то константа равновесия при внешних воздействиях остается постоянной. Поэтому любое изменение равновесных концентраций веществ должно приводить к такому изменению равновесных концентраций других веществ, чтобы соблюдалось постоянство константы равновесия. Рассмотрим процесс конверсии метана:
CH4 + 2H2O = CO2 + 4H2, Константа равновесия этого процесса имеет вид:
Кс = [CO2] [H2]4/[CH4] [H2O]2.
1)При увеличении концентрации метана СН4 равновесие системы нарушается, идет прямая реакция. Концентрации продуктов реакции СО2 и Н2 увеличиваются, а концентрации Н2О уменьшается. Процесс будет протекать до тех пор, пока не установится новое равновесие. Новые равновесные концентрации компонентов будут такими, что константа равновесия не изменится. Если увеличить концентрацию СО2, то по принципу Ле Шателье равновесие сместится влево.
2. Если в результате реакции изменяется число молей газообразных веществ, то изменяется общее давление в системе и происходит смещение равновесия. В соответствии с принципом Ле Шателье увеличение общего давления вызывает смещение равновесия в сторону уменьшения числа молей газообразных веществ, т.е. в сторону уменьшения давления. Для рассматриваемой реакции увеличение давления должно смещать равновесие влево (слева- 3 моля, справа – 5 молей).
3. С увеличением температуры равновесие смещается в сторону эндотермических реакций, т.е. реакций протекающих с поглощением теплоты, понижение – в сторону экзотермических реакций.
Принцип Ле Шателье позволяет создавать такие условия протекания реакции, которые обеспечивают максимальный выход продуктов реакции.
Зависимость константы равновесия реакции от температуры описывается уравнением Вант-Гоффа, называемом
изобарой
Вант-Гоффа:
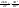 или
или

или
изохорой Вант-Гоффа:
 или
или
 .
.
Знак
теплового эффекта определяется знаком
производной
 в уравнении изобары Вант-Гоффа. Поэтому:
в уравнении изобары Вант-Гоффа. Поэтому:
- если H0 0, т.е. химическая реакция протекает с поглощением тепла. Данная реакция эндотермическая; знак производной будет положительным. Следовательно, константа равновесия возрастает с увеличением температуры;
- если H0 0, т.е. химическая реакция идет с выделением тепла; знак производной будет отрицательным. Следовательно, константа равновесия с увеличением температуры уменьшается;
- если H0 = 0, химическая реакция идет без теплового эффекта, константа равновесия в данном случае не зависит от температуры.
24. Влияние температуры на константу равновесия, вывод ур-я изохоры Вант-Гоффа. Дать обоснование влияния температуры на химическое равновесие на основе анализа уравнения изохоры(изобары) Вант-Гоффа.
1. Влияние температуры на равновесие.
При повышении температуры системы, в которой возможна химическая реакция (системе, находящейся в равновесии, сообщается теплота), согласно принципу Ле Шателье-Брауна усиливается процесс, сопровождающийся поглощением теплоты, т.е. равновесие смещается в сторону эндотермической реакции.Повышение либо понижение температуры означает приобретение либо потерю системой энергии и, следовательно, должно изменять величину константы равновесия. Для выявления зависимости константы равновесия от температуры продифференцируем уравнение изотермы химической реакции (1) по температуре:
![]()
![]() Подставим
полученную производную в уравнение
Гиббса-Гельмгольца:
Подставим
полученную производную в уравнение
Гиббса-Гельмгольца:
![]()
Отсюда:
![]()
После сокращения получаем уравнение, называемое изохорой Вант-Гоффа:
![]() (1)
(1)
Изобара и изохора Вант-Гоффа связывают изменение константы химического равновесия с тепловым эффектом реакции в изобарных и изохорных условиях соответственно. Очевидно, что чем больше по абсолютной величине тепловой эффект химической реакции, тем сильнее влияет температура на величину константы равновесия. Если реакция не сопровождается тепловым эффектом, то константа равновесия не зависит от температуры. Экзотермические реакции: ΔH < 0 (> 0). В этом случае, если температурный коэффициент логарифма константы равновесия отрицателен. Повышение температуры уменьшает величину константы равновесия, т.е. смещает равновесие влево.
Эндотермические реакции: ΔH > 0 (< 0). В этом случае температурный коэффициент логарифма константы равновесия положителен; повышение температуры увеличивает величину константы равновесия (смещает равновесие вправо).
Схематические графики зависимостей константы равновесия от температуры для реакций с различным тепловым эффектом:
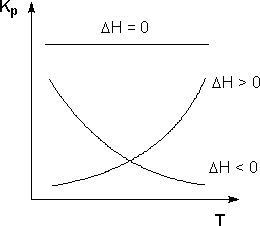 Зависимость
константы равновесия от температуры.
Зависимость
константы равновесия от температуры.
Чтобы рассчитать изменение константы равновесия при изменении температуры, уравнение изобары (изохоры) Вант-Гоффа необходимо проинтегрировать. Если принять, что тепловой эффект реакции не зависит от температуры, что обычно справедливо в достаточно узком интервале температур, то после определённого интегрирования (1) получаем:
![]() При
неопределённом интегрировании изобары
(изохоры) Вант-Гоффа получаем, что
константа равновесия линейно зависит
от обратной температуры (при условии,
что ≠ f(Т)):
При
неопределённом интегрировании изобары
(изохоры) Вант-Гоффа получаем, что
константа равновесия линейно зависит
от обратной температуры (при условии,
что ≠ f(Т)):
![]() .
.
Зависимость константы равновесия от температуры. Уравнения изобары и изохоры Вант-Гоффа
Зависимость константы равновесия реакции от температуры описывается уравнением Вант-Гоффа, называемом
изобарой
Вант-Гоффа:
 или
или

или
изохорой Вант-Гоффа:
 или
или
 .
.
Знак
теплового эффекта определяется знаком
производной
 в уравнении изобары Вант-Гоффа. Поэтому:
в уравнении изобары Вант-Гоффа. Поэтому:
- если H0 0, т.е. химическая реакция протекает с поглощением тепла. Данная реакция эндотермическая; знак производной будет положительным. Следовательно, константа равновесия возрастает с увеличением температуры;
- если H0 0, т.е. химическая реакция идет с выделением тепла; знак производной будет отрицательным. Следовательно, константа равновесия с увеличением температуры уменьшается;
- если H0 = 0, химическая реакция идет без теплового эффекта, константа равновесия в данном случае не зависит от температуры.
