
- •Р. Я. МЕШКОВА
- •Смоленск 1998
- •Содержание
- •Р. Я. МЕШКОВА
- •РУКОВОДСТВО ПО ИММУНОПРОФИЛАКТИКЕ ДЛЯ ВРАЧЕЙ
- •1. ВВЕДЕНИЕ
- •ИММУНОЛОГИЧЕСКИЕ МЕХАНИЗМЫ ПРОТИВОИНФЕКЦИОННОЙ ЗАЩИТЫ
- •2.1. Виды инфекционных агентов и их локализация в организме
- •2.2. Виды иммунного ответа на первичную инфекцию
- •2.2.1. Фазы иммунного ответа
- •2.3. Течение острой инфекции
- •2.3.1. Механизмы разрушения тканей патогенами
- •Прямое разрушение тканей патогенами
- •Непрямое разрушение тканей патогенами
- •2.4. Врожденный иммунитет (неадаптивная защита)
- •2.4.1. Основные клетки врожденного иммунитета
- •2.5. Адаптивный иммунитет
- •2.5.1. Рециркуляция нативных (примитивных) Т-лимфоцитов
- •2.5.2. Адгезивные молекулы
- •А. Суперсемейство иммуноглобулинов
- •Б. Суперсемейство интегринов
- •В. Суперсемейство селектинов
- •Г. Кадгерины
- •Регуляция экспрессии адгезивных молекул
- •2.5.3. Клеточно-опосредованный иммунный ответ
- •Антигенпрезентирующие клетки (APC)
- •Роль эффекторных Т-клеток
- •Механизмы T-клеточно-опосредованной цитоксичности
- •Механизмы эффекторного действия воспалительных CD4 T-клеток (Th1)
- •2.5.4. Гуморальный иммунный ответ
- •Антитела
- •Различия иммуноглобулинов
- •2.5.5. Первичный иммунный ответ
- •2.6. Особенности функционирования иммунной системы у детей
- •2.7. Иммунологические механизмы действия вакцин
- •ВАКЦИНЫ, СОСТАВ, ТЕХНИКА ВАКЦИНАЦИИ, ВАКЦИННЫЕ ПРЕПАРАТЫ. РАЗРАБОТКА НОВЫХ ВИДОВ ВАКЦИН
- •Традиционные вакцины
- •Новое поколение вакцин
- •3.1. Компоненты вакцин
- •Консерванты, стабилизаторы, антибиотики
- •Растворители вакцин
- •Адъюванты
- •3.2. Критерии эффективных вакцин
- •3.3. Условия эффективной вакцинации
- •3.4. Состав отечественных и зарубежных вакцин, используемых для проведения рутинной иммунизации
- •3.4.1. Состав вакцин, входящих в прививочный календарь
- •Отечественные вакцины
- •Импортные вакцины
- •3.4.2. Хранение и транспортировка вакцин
- •3.4.3. Техника вакцинации
- •Пути и техника введения вакцин
- •Общие инструкции
- •Внутримышечные инъекции
- •Внутрикожные инъекции
- •Подкожное введение
- •Одновременная множественная вакцинация
- •Оральное введение вакцин
- •Назальная иммунизация
- •Отклонения от техники вакцинации
- •3.5. Вакцинные препараты
- •3.6. Разработка новых видов вакцин
- •Основные этапы создания вакцин
- •СТРАТЕГИЯ ВАКЦИНАЦИИ В РОССИИ И ДРУГИХ СТРАНАХ МИРА. ГРАФИКИ ИММУНИЗАЦИИ
- •Задачи отдельных этапов реализации РПИ
- •Итоги РПИ-1 и РПИ-2
- •4.1. Пересмотр стратегии вакцинации в 90-х годах XX века
- •4.2. Календарь профилактических прививок в России и графики иммунизации за рубежом
- •4.2.1. Возрастные показания и схемы календарного применения вакцин
- •Отечественные вакцины
- •Импортные вакцины
- •4.2.2. Иммунопрофилактика гепатита B
- •Другие схемы вакцинации детей
- •Вакцинация взрослых
- •4.2.3. Иммунопрофилактика гепатита A
- •4.3. Графики иммунизации за рубежом
- •4.3.1. Графики иммунизации детей, стартующих позднее сверстников
- •4.3.2. Иммунизация подростков
- •Иммунопрофилактика гепатита B
- •Иммунопрофилактика кори, паротита, краснухи (MMR-вакцина). 2-я доза
- •Иммунопрофилактика дифтерии и столбняка (АДС-вакцина)
- •Иммунопрофилактика полиомиелита
- •Иммунопрофилактика гриппа
- •Иммунопрофилактика пневмококковых заболеваний (пневмококковая полисахаридная вакцина)
- •Иммунопрофилактика гепатита A
- •4.3.3. Вакцинация недоношенных новорожденных
- •4.3.4. Вакцинация беременных женщин
- •4.3.5. Кормление грудью и вакцинация
- •4.3.6. Вакцинация пациентов, не имеющих документов о ранее проведенной вакцинации
- •4.4. Интервалы между вводимыми вакцинами
- •4.4.1. Одновременное введение вакцин
- •Календарные вакцины для детей
- •4.5. Интервалы между введением вакцин и препаратов иммуноглобулинов
- •Живые вакцины
- •Убитые вакцины
- •ВАКЦИНАЦИЯ ПАЦИЕНТОВ С ОТЯГОЩЕННЫМ АНАМНЕЗОМ. РЕКОМЕНДУЕМЫЕ ВАКЦИНЫ
- •5.1. Вакцинация пациентов с аллергопатологией
- •5.1.1. Предварительные замечания
- •5.1.2. Рекомендуемые вакцины для детей с аллергопатологией
- •5.1.3. Вакцинация больных, получающих СИТ
- •5.2. Вакцинация пациентов с имунодефицитами (врожденными и приобретенными)
- •5.2.1. Предварительные замечания
- •5.2.2. Вакцинация пациентов со вторичными иммунодефицитами
- •5.2.3. Вакцинация пациентов с врожденными иммунодефицитами
- •5.2.4. Вакцинация ВИЧ-инфицированных пациентов
- •5.3. Вакцинация пациентов с патологией печени.
- •5.4. Вакцинация пациентов с эндокринной патологией.
- •5.5. Вакцинация пациентов с патологией почек
- •5.6. Вакцинация пациентов с патологией ЦНС
- •5.7. Вакцинация детей с патологией крови
- •5.8. Системные заболевания соединительной ткани
- •5.9. Вакцинация детей при некоторых других заболеваниях и состояниях
- •ТАКТИКА ЛЕЧЕНИЯ ДЕТЕЙ С РАЗЛИЧНОЙ ПАТОЛОГИЕЙ ДО И ПОСЛЕ ВАКЦИНАЦИИ
- •6.1. Аллергопатология
- •6.2. Иммунодефициты
- •6.3. Патология ЦНС
- •6.4. Патология почек, печени, поджелудочной железы
- •7. НЕКОТОРЫЕ АСПЕКТЫ ИММУНИЗАЦИИ ВЗРОСЛЫХ
- •8. ПРИВИВОЧНЫЕ РЕАКЦИИ И ОСЛОЖНЕНИЯ
- •8.1. Вероятные механизмы нежелательных реакций иммунизации
- •8.2. Гиперчувствительность к компонентам вакцин
- •8.3. Нежелательные реакции (осложнения) на отдельные вакцины
- •Вакцина БЦЖ
- •Вакцина против полиомиелита
- •ИПВ (инактивированная полиомиелитная вакцина)
- •АКДС-вакцина
- •АДС и АС-анатоксины
- •Вакцина против кори
- •Аллергические реакции
- •Беременность
- •Вакцина против паротита
- •Вакцина против краснухи
- •Вакцина MMR-II (корь, паротит, краснуха)
- •Вакцина против гепатита B
- •Вакцина против пневмококковой инфекции
- •Вакцина против гриппа
- •Вакцина против гемофильной инфекции
- •8.4. Заключения о возможной связи отклонений в состоянии здоровья с вакцинацией
- •9. ПРОТИВОПОКАЗАНИЯ К ВАКЦИНАЦИИ
- •НЕОТЛОЖНЫЕ ЛЕЧЕБНЫЕ МЕРОПРИЯТИЯ ПРИ РАЗВИТИИ ПОСТВАКЦИНАЛЬНЫХ ОСЛОЖНЕНИЙ
- •НЕОТЛОЖНЫЕ ЛЕЧЕБНЫЕ МЕРОПРИЯТИЯ ПРИ РАЗВИТИИ ПОСТВАКЦИНАЛЬНЫХ ОСЛОЖНЕНИЙ
- •СЛОВАРЬ ТЕРМИНОВ
- •Приложение 1
- •МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РФ ПРИКАЗ № 375 от 18.12.97
- •ПРИКАЗЫВАЮ:
- •КАЛЕНДАРЬ ПРОФИЛАКТИЧЕСКИХ ПРИВИВОК
- •КАЛЕНДАРЬ ПРОФИЛАКТИЧЕСКИХ ПРИВИВОК ПРОТИВ ВИРУСНОГО ГЕПАТИТА В
- •КАЛЕНДАРЬ ПРОФИЛАКТИЧЕСКИХ ПРИВИВОК ПРОТИВ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ, ПРОВЕДЕНИЕ КОТОРЫХ НЕОБХОДИМО НА ЭНДЕМИЧНЫХ ИЛИ ЭНЗООТИЧНЫХ ТЕРРИТОРИЯХ И ПО ЭПИДЕМИЧЕСКИМ ПОКАЗАНИЯМ
- •ПЕРЕЧЕНЬ МЕДИЦИНСКИХ ПРОТИВОПОКАЗАНИЙ К ПРОВЕДЕНИЮ ПРОФИЛАКТИЧЕСКИХ ПРИВИВОК
- •ЛОЖНЫЕ ПРОТИВОПОКАЗАНИЯ К ПРОВЕДЕНИЮ ПРОФИЛАКТИЧЕСКИХ ПРИВИВОК
- •ОСНОВНЫЕ ПОЛОЖЕНИЯ ОБ ОРГАНИЗАЦИИ И ПРОВЕДЕНИИ ПРОФИЛАКТИЧЕСКИХ ПРИВИВОК
- •Приложение 2
- •"Об иммунопрофилактике инфекционных болезней"
- •Глава I. Общие положения
- •Статья 1. Основные понятия
- •Статья 2. Законодательство Российской Федерации в области иммунопрофилактики
- •Статья 3. Сфера действия настоящего Федерального закона
- •Глава II. Государственная политика в области иммунопрофилактики. Права и обязанности граждан при осуществлении иммунопрофилактики
- •Статья 4. Государственная политика в области иммунопрофилактики
- •Статья 5. Права и обязанности граждан при осуществлении иммунопрофилактики
- •Глава III. Финансирование иммунопрофилактики
- •Статья 6. Финансирование иммунопрофилактики
- •Статья 7. Поставки медицинских иммунобиологических препаратов
- •Глава IV. Организационные основы деятельности в области иммунопрофилактики
- •Статья 8. Организационные основы деятельности в области иммунопрофилактики
- •Статья 9. Национальный календарь профилактических прививок
- •Статья 10. Профилактические прививки по эпидемическим показаниям
- •Статья 11. Требования к проведению профилактических прививок
- •Статья 12. Требования к медицинским иммунобиологическим препаратам
- •Статья 13. Хранение и транспортировка медицинских иммунобиологических препаратов
- •Статья 14. Государственный контроль медицинских иммунобиологических препаратов
- •Статья 15. Обеспечение медицинскими иммунобиологическими препаратами
- •Статья 16. Особенности лицензирования видов деятельности в области иммунопрофилактики
- •Статья 17. Государственное статистическое наблюдение в области иммунопрофилактики
- •Глава V. Социальная защита граждан при возникновении поствакцинальных осложнений
- •Статья 18. Право граждан на социальную защиту при возникновении поствакцинальных осложнений
- •Статья 19. Государственные единовременные пособия
- •Статья 20. Ежемесячные денежные компенсации
- •Статья 21. Пособия по временной нетрудоспособности
- •Глава VI. Заключительные положения
- •Статья 22. Ответственность за нарушение настоящего Федерального закона
- •Статья 23. Вступление в силу настоящего Федерального закона
диссоциации и, подобно связыванию, в нем могут участвовать сигналы между Т-клетками и АРС, но об этих механизмах в настоящее время известно очень мало.
2.5.3. Клеточно-опосредованный иммунный ответ
Деление на гуморальный и клеточный иммунитет достаточно условно, т.к. в обоих случаях имеет место участие как Т-, так и В-лимфоцитов, а на вторжение инфекционного агента развиваются и гуморальный, и клеточный ответы.
Более того, как внутриклеточные, так и внеклеточные патогены при попадании в организм захватываются антигенпрезентирующими клетками (АРС), чаще всего макрофагами, перерабатываются ими ипредставляются синергичным Т-хелперам и В-лимфоцитам в виде комплексов с молекулами МНС класса I или II.
Антигенпрезентирующие клетки (APC)
Антиген является главным регулятором иммунного ответа [10], поскольку дифференцировка примитивных Т-клеток в те или иные эффекторные клетки зависит от цитокинов, секреция которых регулируется видом захваченного АРС антигена.
В периферических лимфоидных |
органах выделяют 3 типа специализированных АРС: |
|
– |
|
макрофаги; |
– |
дендритные |
клетки; |
– В-лимфоциты. |
|
|
Каждый из этих типов клеток специализируется на переработке и представлении антигенов для примитивных Т-клеток. В свою очередь макрофаги и В-клетки являются также мишенями последующих эффекторных действий Т-клеток.
Только эти 3 типа клеток экспрессируют специализированные ко-стимуляторные молекулы, которые способны затем активировать примитивные Т-клетки. Макрофаги и В-клетки экспрессируют эти молекулы только когда активируются сами вследствие инфицирования.
Макрофаги обнаруживаются во всех зонах лимфоузлов и активно захватывают микробы и другие антигены.
Дендритные клетки, которые в лимфоидных тканях называют интердигитальными ретикулярными клетками – присутствуют только в Т-клеточных зонах лимфоузлов.
В-клетки – присутствуют в лимфоидных фолликулах лимфоузлов и селезенки и особенно эффективны при захватывании растворимых антигенов, таких как бактериальные токсины, с которыми они связываются специфически с помощью поверхностных Ig молекул.
Все специализированные АРС способны экспрессировать оба класса МНС-молекул. АРС представляют пептидные фрагменты захваченного антигена рециркулирующим Т-клеткам.
В результате первого связывания примитивных Т-клеток с антигеном, презентируемым АРС,
реализуется первичный иммунный ответ и генерируется иммунологическая память, которая обеспечивает защиту при последующем реинфицировании.
Роль эффекторных Т-клеток
Для участия в адаптивном иммунном ответе нативные (примитивные) Т-клетки должны быть активированы т.е. индуцированы к пролиферации и последующей дифференцировке в клетки, способные к удалению патогенов. Такие клетки называют эффекторными Т-клетками. Их основным свойством является способность действовать немедленно или очень быстро после связывания с МНС-пептидным комплексом на клетке-мишени.

Генерация эффекторных клеток из примитивных Т-клеток идет несколько дней. В конце этого периода эффекторные Т-клетки покидают лимфоидные органы, возвращаются в кровеносное русло и могут мигрировать в места инфекций. Активация примитивных Т-клеток при первичной встрече с антигеном на поверхности профессиональных АРС называемая праймингом, требует распознавания ими чужеродных пептидных фрагментов, связанных с собственными МНС-молекулами. Кроме того, требуется одновременное поступление ко-стимулирующего сигнала от специализированных профессиональных АРС.
Таким образом, Т-клетки, которые встретили специфический антиген, представленный АРС, активируются, пролиферируют и дифференцируются в эффекторные клетки, а эффекторные Т- клетки оставляют лимфоузлы через эфферентные лимфатические сосуды и входят в циркуляцию.
Эффекторные Т-клетки делят на 3 функциональных класса:
–CD8 Т-клетки – цитотоксические – распознают антигены, происходящие из возбудителей, размножающихся внутри клетки (интрацеллюлярные) и представляемые на клеточную поверхность с помощью молекул МНС класса I. К ним относятся вирусы, микобактерии и т.п. CD8 Т-клетки убивают инфицированную клетку, но при этом сами выживают.
CD4 Т-клетки распознат пептиды, связанные с молекулами МНС-класса II, и в свою очередь разделяются на 2 функциональных типа:
–CD4 (Th1) – воспалительные Т-клетки – вызывают активацию инфицированных макрофагов, что приводит к разрушению внутриклеточных микроорганизмов, синтезируют IFN-γ, ИЛ-2, стимулируют размножение и дифференцировку CD8 Т-клеток, за счет выработки ИЛ-2, стимулируют размножение и усиливают активность NK-клеток. Таким образом, воспалительные CD4 T-клетки специализируются на активации макрофагов, содержащих внутри антигены. После активации воспалительные CD4 T-клетки (Th1) активируют макрофаги, что, в свою очередь, вызывает разрушение интрацеллюлярных микроорганизмов. Th1 секретируют IFN-γ и другие эффекторные молекулы, а также TFN.
–CD4 (Th2) – Т-хелперные – активируют специфические В-лимфоциты, вызывая дифференцировку их в антителопродуцирующие клетки. Хелперные CD4 Т-клетки специализируются на активации В-лимфоцитов. Они секретируют ростовые факторы: IL-4, IL-5, IL- 6, играющие важную роль в активации В-клеток, а также ИЛ-10. Th2-клетки экспрессируют мембран-связанные адгезивные молекулы CD40-ligand, которые, связываясь с CD40 рецептором на В-лимфоцитах, индуцируют пролиферацию В-клеток. Эти процессы лежат в основе гуморального иммунитета.
Однако не все клоны Т-хелперов можно разделить на Th1 и Th2. Есть клетки, которые секретируют все типы цитокинов. Эти клетки обозначают как Т-хелперы тип 0 (Th0). Они могут быть общими прекурсорами Th1 и Th2 клеток или могут быть третьей эффекторной по-пуляцией Т-хелперов.
Всвою очередь, цитокины вовлекаются в регуляцию дифференцировки Th субпопуляций:
–IFN-γ ингибирует пролиферацию Th2 клонов, но не влияет на продукцию ими цитокинов;
–ИЛ-12 – это цитокин, оказывающий мощные эффекты на Th1 клетки. ИЛ-12 продуцируется моноцитами, макрофагами и В-клетками и требуется для оптимальной продукции IFN-γ. Показано, что ИЛ-12 – это обязательный фактор для генерации Th1.
Эти факты свидетельствуют, что IFN-γ и ИЛ-12 можно рассматривать в качестве иммунорегуляторов, способных вмешиваться в клональную экспансию и эффекторные функции Th2 клеток. Кроме того, при нарушении продукции ИЛ-4 Th1 клетками может происходить регуляция развития Th0 клеток в Th2, что приводит к восстановлению продукции ИЛ-4. В итоге, баланс ИЛ-4 и ИЛ-12 обеспечивает дифференцировку Th0 клеток в Th1 и Th2 [89].
Дифференцировка нативных CD4 Т-клеток в эффекторные клетки зависит от цитокинов, индукция которых регулируется главным образом антигеном [89]:
1. Внутриклеточные патогены (в основном вирусы и некоторые бактерии) индуцируют секрецию

макрофагами ИЛ-12, который в свою очередь может активировать NK-клетки и выделение ими IFN-γ. Нативные CD4 Т-клетки, активированные в присутствии ИЛ-12 и IFN-γ, коммитированы к дифференцировке в Th1-клетки. Тh1-лимфоциты стимулируют пролиферацию и дифференцировку CD8-клетoк и превращение их в зрелые Т-киллеры. Так происходит индукция воспалительного или клеточно-опосредованного ответа.
2.Внеклеточные возбудители в основном могут стимулировать другие клетки к выделению ИЛ-4. Нативные CD4 Т-клетки, активирующиеся в присутствии ИЛ-4, коммитированы к дифференцировке в Th2-клетки. Эти клетки выделяют цитокины, опосредующие клональную экспансия и дифференцировку в плазматические клетки стимулированных антигеном В- лимфоцитов. Так происходит индукция гуморального иммунного ответа.
В противоположность, ингибируют генерирование воспалительных Th1 клеток цитокины ИЛ-4 и ИЛ10, а ингибируют пролиферацию хелперных Т-клеток (Th2) – другой цитокин, а именно: IFN-γ.
Клетки, на которые оказывают действие эффекторные Т-клетки, называют клетками-мишенями. Таким образом, цитокины в ранней фазе инфекции влияют на функциональную дифференцировку CD4 Т-клеток. Это главная часть адаптивного иммунного ответа, обеспечивающая в ответ на антиген либо продукцию антител, либо активацию макрофагов и Т-киллеров.
Помимо указанных молекул, все 3 класса эффекторных Т-клеток экспрессируют мембранассоциированные адгезивные эффекторные молекулы, которые, подобно цитокинам, индуци-руются благодаря распознаванию антигена на клетке-мишени и представлены соответственно: Fas-Ligand
на CTL, CD40-Ligand на Th2, TNF на Th1.
Механизмы T-клеточно-опосредованной цитоксичности
Эффекторные функции Т-клеток опосредуются благодаря индукции экспрессии как мембрансвязанных, так и секретируемых молекул. Эффекторные Т-клетки секретируют молекулы, которые разделяются на 2 больших класса:
1.Цитотоксины - которые выделяются CD8 Т-клетками и некоторыми воспалительными (Th1) CD4.
2.Цитокины - которые выделяются всеми эффекторными Т-клетками и являются медиаторами эффекторных действий CD4 Т-клеток.
Цитотоксины не являются специфическими и могут действовать на все виды клеток. Цитокины действуют благодаря специфическим рецепторам к ним на клетке-мишени, а основные эффекторные действия CD4 Т-клеток направлены именно на специализированные клетки, экспрессирующие эти рецепторы.
К цитотоксинам, секретируемым CD8 Т-клетками, относятся: перфорин-1, который создает "дыру" в мембране клетки-мишени; гранзимы, которые представлены протеазой и часто IFN-a. К мембрансвязанным эффекторным молекулам на CD8 Т-клетках относят Fas-ligand, связывание которого с Fas рецептором индуцирует апоптоз клетки-мишени. Апоптоз - это генетически запрограммированная гибель клетки.
Как известно, все вирусы и некоторые бактерии размножаются в цитоплазме инфицированных клеток. Кроме того, вирусы - это патогены, которые не имеют собственных биосинтетических или метаболических аппаратов и могут реплицироваться только внутри клетки. Находясь внутри клеток, эти патогены остаются нечувствительными к антибиотикам и могут быть элиминированы только благодаря разрушению инфицированных клеток.
Таким образом, главная роль CTL - ограничение интрацеллюлярных инфекций, таких как вирусные инфекции и внутрицитоплазматические бактерии, некоторые протозойные инфекции (например токсоплазмоз).
В основе механизмов Т-клеточной цитотоксичности лежат следующие процессы (рис. 2а):
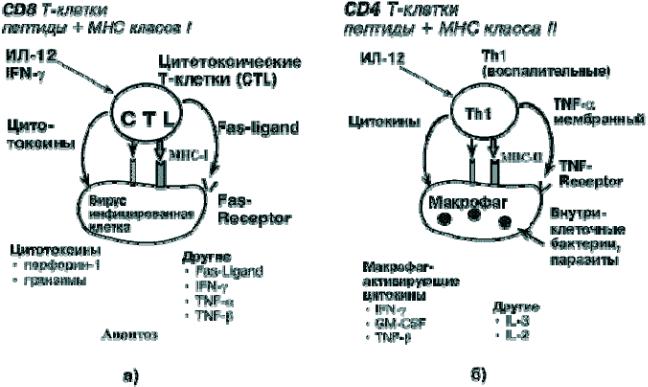
–специфическое разпознавание антигена;
–соединение CTL и клеток-мишеней благодаря механизмам адгезии (Fas-ligand и Fas-рецептор - это связывание приводит к индукции апоптоза клетки-мишени);
–выделение перфорина-1 - протеина, который вызывает "дыру" в мембране клетки-мишени, через которую внутрь клетки входят фрагментины (протеазы, гранзимы). Фрагментины так же способны индуцировать апоптоз клеток-мишеней;
–CD8 Т-клетки продуцируют IFN-γ, который ингибирует репликацию вирусов, а также важен для индукции экспрессии молекул МНС класса 1 и активации макрофагов.
CTL убивают клетки-мишени с высокой точностью, с минимальным вредом для соседних клеток. Эта точность - гарантия минимизации разрушения тканей.
Рис. 2. Индукция клеточно-опосредованного иммунного ответа: а) роль CD8 T-лимфоцитов; б) роль CD4 (Th1)-лимфоцитов
Механизмы эффекторного действия воспалительных CD4 T-клеток (Th1)
Макрофаги активируются благодаря воспалительным CD4 Т-клеткам. Некоторые микроорганизмы, такие как микобактерии (туберкулез, лепра) - это интрацеллюлярные патогены, которые находятся в везикулах, называемых фаголизосомы, макрофагов, где они недоступны для действия как антител, так и CTL.
Эти микробы обычно сохраняют себя внутри фагоцита благодаря ингибиции слияния лизосомы с фаголизосомой, в которой они растут, или благодаря предупреждению излияния этих везикул, для чего требуется активация лизосомальных протеаз. Такие микроорганизмы элиминируются, когда происходит активация макрофагов с помощью воспалительных CD4 Т-клеток, т.е. воспалительные CD4 Т-клетки координируют ответ к интрацеллюлярным бактериям и паразитам.
Зрелые CD4 Т-клетки (Th1) координируют иммунный ответ на эти интрацеллюлярные патогены благодаря синтезу и секреции комплекса цитокинов, которые действуют как локально, так и дистанционно.
