
- •Влияние различных факторов на црп Влияние температуры
- •Влияние концентрации инициатора
- •Влияние концентрации мономера
- •Влияние давления
- •Влияние примесей
- •Роль кислорода при црп
- •Ионная полимеризация (ип)
- •Катионная полимеризация (кп)
- •Механизм кп
- •Кинетика катионной полимеризации
- •Анионная полимеризация
- •Механизм ап
- •I Инициирование ап
- •II Рост цепи
- •III Способы дезактивации активного центра (ограничение роста цепи)
- •Влияние различных факторов на аП
- •Ионно-координационная полимеризация (икп)
- •Оксидно-металлические катализаторы (омк)
- •Сополимеризация
- •Свободнорадикальная сополимеризация
- •Ионная сополимеризация
- •Ступенчатая (миграционная) полимеризация
- •Другие примеры мп
- •Полимеризация циклов
- •Полимеризация циклов в присутствии активаторов
- •Влияние концентрации активатора на скорость полимеризации и молекулярную массу полимера
- •Влияние температуры на скорость полимеризации и молекулярную массу полимера
- •Ионная полимеризация циклов
- •Катионнная полимеризация циклов
- •Полимеризация циклических простых эфиров
- •Анионная полимеризация циклов
- •Поликонденсация (пк)
- •Некотрые важнейшие примеры пк
- •Влияние строения мономеров на способность к пк см. В курсе «СиРсм»
- •Равновесная пк
- •Молекулярно-массовое распределение при пк
- •Поликонденсационное равновесие
- •Влияние различных факторов на скорость пк и молекулярную массу полимера Влияние концентрации и соотношения мономеров
- •Влияние примесей монофункциоанльных соединений
- •Влияние температуры
- •Влияние катализатора
- •Способы проведения равновесной пк
- •Неравновесная пк
- •Способы проведения мфпк
- •Особенности мфпк
- •Акцепторно-каталитическая (низкотемпературная) пк
- •Трехмерная пк
- •Совместная пк
- •Блок-сополимеры Способы получения
- •Привитые сополимеры
- •Химические превращения полимеров (хпп)
- •Особенности химических реакций полимеров
- •Рассмотрим эти взаимодействия:
- •II Конформационные эффекты
- •III Надмолекулярные эффекты
- •II Полимераналогичные превращения
- •1 Деструкция
- •II хпп приводящие к изменению молекулярной массы
- •1 Сшивание макромолекул (структурировние)
- •2 Отверждение смол
Влияние различных факторов на аП
Влияние природы растворителя и температуры
При одинаковой температуре и природе противоиона kрвозрастает с ростом полярности среды. При высокой полярности растворителя, обладающего высокой сольватирующей способностью, происходит разделение ионных пар на свободные ионы, которые резко увеличивают скорости роста цепи. Однако при этом уменьшается координирующая способность противоиона и снижается стереорегулярность и регулярность полимера.
Растворители, способные легко вступать в реакцию передачи цепи, снижают молекулярную массу полимера. Например: молекулярная масса, получаемая при полимеризации бутадиена и изопрена (катализатор К):
-
растворитель
мономер
бензол
толуол
бутадиен
362000
41700
изопрен
168000
7400
При уменьшении температуры скорость полимеризации уменьшается.
Например: АП стирола (противоион Na+)
-
растворитель
диоксан
тетрагидрофуран
Температура, 0С
25
25
2
ε
2,2
7,6
7,6
kр, м3/(кмоль·с)
5
600
183
Влияние противоиона
С увеличением радиуса катиона в ряду Li<Na<K<Rb<Csуменьшается прочнсть ионной пары, и полимеризация может идти на свободных ионах. Поэтому скорость реакции роста цепи возрастает.
Например: влияние природы щелочного металла на скорость АП бутадиена в ТГФ при 100С
-
Противоион
Li+
Na+
K+
kр, м3/(кмоль·с)
0,85
5,4
70,0
С увеличением размера противоиона снижается регулярность и стереорегулярность полимера, за счет участия свободных ионов в стадии роста цепи. Например, соединение звеньев изопрена при полимеризации возможно 4 способами:
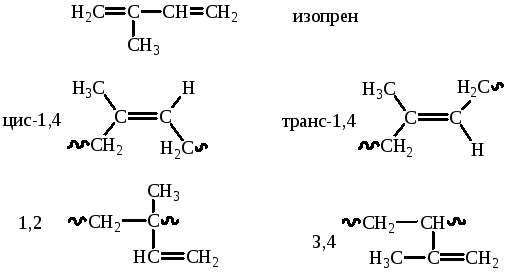
При полимеризации изопрена в присутствии щелочных металлов в растворителе – пентане получены следующие данные:
|
Катализатор |
Содержание звеньев, % | |||
|
Цис-1,4 |
Тран-1,4 |
1,2 |
3,4 | |
|
Li |
94 |
0 |
0 |
6 |
|
Na |
0 |
43 |
6 |
51 |
|
K |
0 |
52 |
8 |
40 |
|
Rb |
5 |
47 |
8 |
40 |
|
Cs |
4 |
51 |
8 |
37 |
Как видно из таблицы наибольшую стереорегулярность полимеру обеспечивают литий органические катализаторы.
В неполярных растворителях в присутствии литиевых катализаторов получены изотактические полимеры метил-, изопропил-, и циклогексилмеакрилатов, а в присутствии полярного растворителя синдиотактический ПММА.
Кинетика АП сложна, т.к. зависит от типа катализатора и исследована лишь для простейших систем.
Особенностью АП как КП является то, что иногда полимеризация протекает без обрыва кинетической цепи с образованием «живущих» полимеров. Если создать условия, когда исключены передача цепи на растворитель, мономер или другие способы обрыва цепи, то макрокатионы, имеющие одинаковые заряды не могут соединится между собой и поэтому вполне устойчивы. Однако если в раствор внести новую порцию мономера то рост цепи возобновится. Поскольку обрыв цепи исключен, при дальнейшем добавлении мономера будет происходить только рост цепей без увеличения их числа. Полученные «живые» полимеры используются для синтеза блок-сополимеров.
Если Ки>>Кр, а также обеспечено идеальное смешение реагирующих веществ, постоянство температуры, то все активные центры начнут расти почти одновременно и период роста будет практически один и тот же для всех макромолекул.
Чем дольше будет продолжатся этот процесс, тем меньше станут первоначальные различия в периоде роста и длина отдельных цепей. Т.о. метод «живых» цепей открывает возможности синтеза монодисперсных мономеров, у которых все молекулы имеют одну и ту же степень полимеризации.
