- •Влияние различных факторов на црп Влияние температуры
- •Влияние концентрации инициатора
- •Влияние концентрации мономера
- •Влияние давления
- •Влияние примесей
- •Роль кислорода при црп
- •Ионная полимеризация (ип)
- •Катионная полимеризация (кп)
- •Механизм кп
- •Кинетика катионной полимеризации
- •Анионная полимеризация
- •Механизм ап
- •I Инициирование ап
- •II Рост цепи
- •III Способы дезактивации активного центра (ограничение роста цепи)
- •Влияние различных факторов на аП
- •Ионно-координационная полимеризация (икп)
- •Оксидно-металлические катализаторы (омк)
- •Сополимеризация
- •Свободнорадикальная сополимеризация
- •Ионная сополимеризация
- •Ступенчатая (миграционная) полимеризация
- •Другие примеры мп
- •Полимеризация циклов
- •Полимеризация циклов в присутствии активаторов
- •Влияние концентрации активатора на скорость полимеризации и молекулярную массу полимера
- •Влияние температуры на скорость полимеризации и молекулярную массу полимера
- •Ионная полимеризация циклов
- •Катионнная полимеризация циклов
- •Полимеризация циклических простых эфиров
- •Анионная полимеризация циклов
- •Поликонденсация (пк)
- •Некотрые важнейшие примеры пк
- •Влияние строения мономеров на способность к пк см. В курсе «СиРсм»
- •Равновесная пк
- •Молекулярно-массовое распределение при пк
- •Поликонденсационное равновесие
- •Влияние различных факторов на скорость пк и молекулярную массу полимера Влияние концентрации и соотношения мономеров
- •Влияние примесей монофункциоанльных соединений
- •Влияние температуры
- •Влияние катализатора
- •Способы проведения равновесной пк
- •Неравновесная пк
- •Способы проведения мфпк
- •Особенности мфпк
- •Акцепторно-каталитическая (низкотемпературная) пк
- •Трехмерная пк
- •Совместная пк
- •Блок-сополимеры Способы получения
- •Привитые сополимеры
- •Химические превращения полимеров (хпп)
- •Особенности химических реакций полимеров
- •Рассмотрим эти взаимодействия:
- •II Конформационные эффекты
- •III Надмолекулярные эффекты
- •II Полимераналогичные превращения
- •1 Деструкция
- •II хпп приводящие к изменению молекулярной массы
- •1 Сшивание макромолекул (структурировние)
- •2 Отверждение смол
Полимеризация циклов в присутствии активаторов
Протекает она по ступенчатому механизму, при этом, как и в случае ЦРП, концевые группы содержат остатки активаторов.
Общая схема полимеризации в присутствии активаторов:
Расщепление цикла активатором:
![]()
X,Y– концевые функциональные группы, образующиеся при раскрытии цикла.
Взаимодействие полученной активной молекулы с циклом, по механизму ступенчатой полимеризации, благодаря миграции подвижных групп от активной молекулы к циклу:
![]()
Z– функциональная группа образующаяся при взаимодействииXиY.
Рассмотрим примеры.
Полимеризация ε-аминокапролактама в присутствии воды (гидролитическая полимеризация):
1.

2.
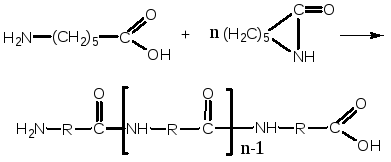
Расщепление продолжается до установления равновесия: амидного и цикл – полимер.
Влияние концентрации активатора на скорость полимеризации и молекулярную массу полимера
Скорость ПЦ возрастает с увеличением количества активатора. Чем выше концентрация активатора, тем большее число циклов распадается в единицу времени, тем выше общая скорость процесса.
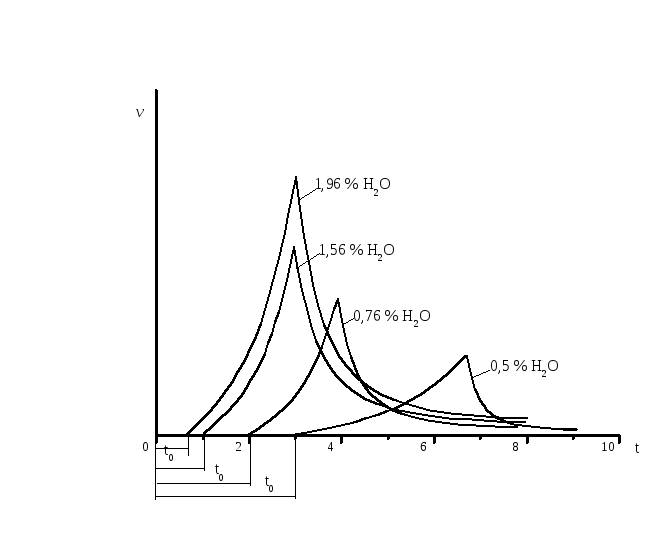
Полимеризация капролактама
Наличие индукционного периода определяется самой медленной стадией реакции – гидролизом цикла водой. Наличие максимума указывает на автокатализ. Образующаяся в результате гидролиза цикла аминокапроновая кислота, содержащая группы NH2и СООН, начинают выполнять двойную роль – активатора, размыкающего цикл, и катализатора ускоряющего размыкание цикла водой.
При полимеризации капролактама устанавливается 2 независимых равновесия:
Равновесие гидролиза амидной связи (амидное):
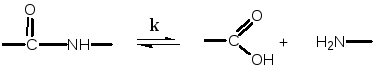
Равновесие цикл – полимерное звено:

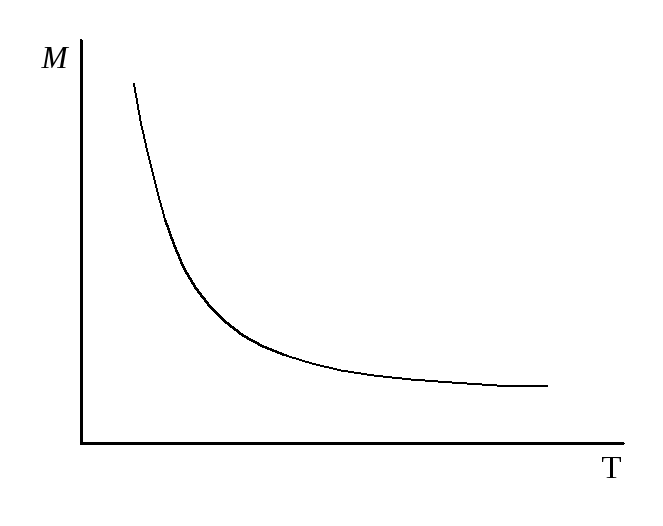
Равновесие цикл – полимер определяет выход полимера и не зависит от концентрации активатора. Амидное равновесие определяет молекулярную массу полимера, которая связана с концентрацией активатора следующим уравнением:
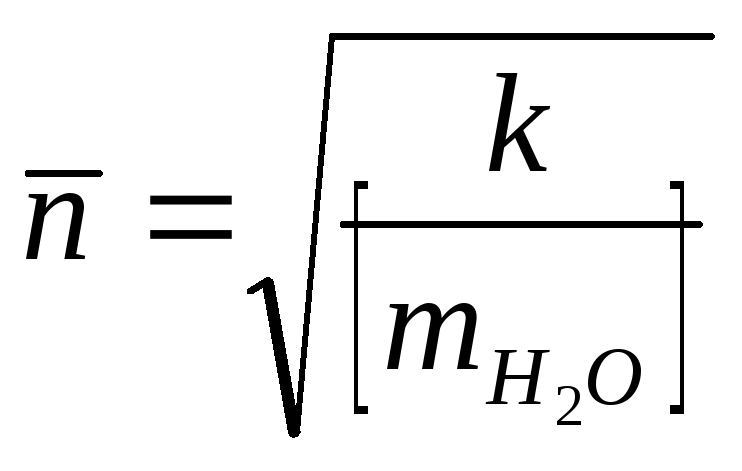 гдеk– константа амидного
равновесия,
гдеk– константа амидного
равновесия,![]() - число моль воды, приходящихся на одно
элементарное звено полимера.
- число моль воды, приходящихся на одно
элементарное звено полимера.
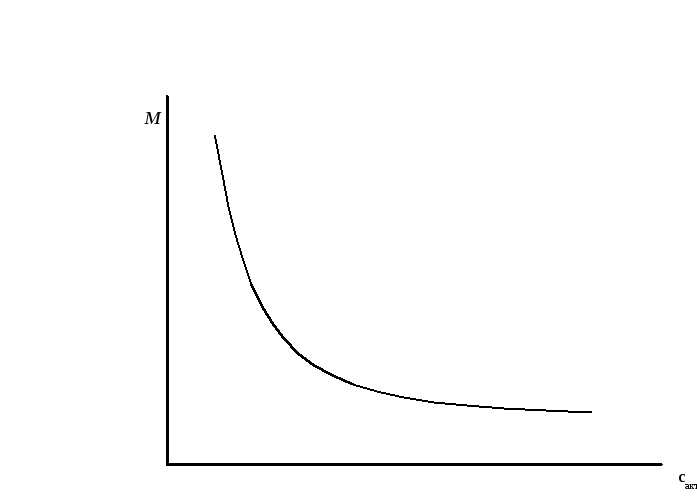
С увеличением концентрации активатора молекулярная масса сначала уменьшается, т.к. увеличивается число активных центров полимеризации и на каждый активный центр приходится меньшее число молекул мономера. Затем образовавшиеся макромолекулы начинаю взаимодействовать друг с другом например по механизму диспропорционирования:
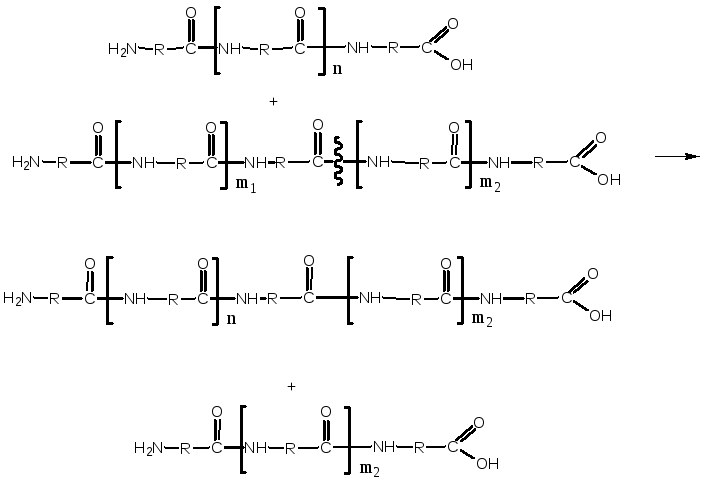
При этом меняется длина и той и другой макромолекулы, но средняя молекулярная масса практически не зависит от концентрации активатора.
Влияние температуры на скорость полимеризации и молекулярную массу полимера
С повышением температуры уменьшается индукционный период, увеличивается скорость реакции. Пример: влияние температуры на полимеризации капролактама при концентрации воды 2%:
|
|
|
С увеличением температуры увеличивается скорость гидролиза амидной связи, что ведет к увеличению скорости реакции, так и в полимере, приводя к деструкции макромолекул и снижению молекулярной массы.
Кроме того, полимеризация капролактама протекает с выделением тепла, поэтому повышение температуры смещает положение равновесия цикл – полимер в сторону образования мономера. Так, при 2200С содержание мономера в продукте 1,8 %, а при 3000С – 8,9 %.
Аналогично ε-аминокапролактаму в реакции
полимеризации под влиянием активаторов
могут участвовать и другие лактамы
(ε-аминоэнантолактам
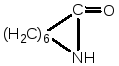 ),
а также эпоксиды (активаторы вторичные
амины).
),
а также эпоксиды (активаторы вторичные
амины).
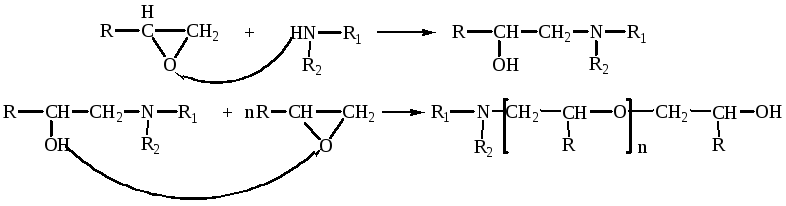
Полимеризация с применением активаторов является очень избирательной. Более универсальной является ионная полимеризация циклов.