- •Влияние различных факторов на црп Влияние температуры
- •Влияние концентрации инициатора
- •Влияние концентрации мономера
- •Влияние давления
- •Влияние примесей
- •Роль кислорода при црп
- •Ионная полимеризация (ип)
- •Катионная полимеризация (кп)
- •Механизм кп
- •Кинетика катионной полимеризации
- •Анионная полимеризация
- •Механизм ап
- •I Инициирование ап
- •II Рост цепи
- •III Способы дезактивации активного центра (ограничение роста цепи)
- •Влияние различных факторов на аП
- •Ионно-координационная полимеризация (икп)
- •Оксидно-металлические катализаторы (омк)
- •Сополимеризация
- •Свободнорадикальная сополимеризация
- •Ионная сополимеризация
- •Ступенчатая (миграционная) полимеризация
- •Другие примеры мп
- •Полимеризация циклов
- •Полимеризация циклов в присутствии активаторов
- •Влияние концентрации активатора на скорость полимеризации и молекулярную массу полимера
- •Влияние температуры на скорость полимеризации и молекулярную массу полимера
- •Ионная полимеризация циклов
- •Катионнная полимеризация циклов
- •Полимеризация циклических простых эфиров
- •Анионная полимеризация циклов
- •Поликонденсация (пк)
- •Некотрые важнейшие примеры пк
- •Влияние строения мономеров на способность к пк см. В курсе «СиРсм»
- •Равновесная пк
- •Молекулярно-массовое распределение при пк
- •Поликонденсационное равновесие
- •Влияние различных факторов на скорость пк и молекулярную массу полимера Влияние концентрации и соотношения мономеров
- •Влияние примесей монофункциоанльных соединений
- •Влияние температуры
- •Влияние катализатора
- •Способы проведения равновесной пк
- •Неравновесная пк
- •Способы проведения мфпк
- •Особенности мфпк
- •Акцепторно-каталитическая (низкотемпературная) пк
- •Трехмерная пк
- •Совместная пк
- •Блок-сополимеры Способы получения
- •Привитые сополимеры
- •Химические превращения полимеров (хпп)
- •Особенности химических реакций полимеров
- •Рассмотрим эти взаимодействия:
- •II Конформационные эффекты
- •III Надмолекулярные эффекты
- •II Полимераналогичные превращения
- •1 Деструкция
- •II хпп приводящие к изменению молекулярной массы
- •1 Сшивание макромолекул (структурировние)
- •2 Отверждение смол
Кинетика катионной полимеризации
Несмотря на большое разнообразие и сложность процессов КП, некоторое общее представление о кинетических особенностях можно получить, если допустить, что скорость процесса образования макромолекулы складывается из скоростей четырех основных стадий: инициирование vин, роста цепиvр, ограничение роста цепи путем обрываvобри передачи цепи на мономерvпер(основной способ обрыва цепи). Упрощенные уравнения скоростей элементарных стадий можно представить в следующем виде:
![]() (1)
(1)
![]() (2)
(2)
![]() (3)
(3)
![]() (4)
основной способ
(4)
основной способ
Допустив установление равновесного
состояния, когда vин=
vобр, можно
вычислить концентрацию![]() :
:
vин= vобр
или![]()
![]() (5)
(5)
Суммарная скорость процесса vобщ, т.е. скорость убывания мономера, иожет быть выражена уравнением скорости роста цепи:
![]() (6)
(6)
Подставив в уравнение (6) значение
![]() из уравнения (5), получим зависимостьvобщот
концентрации мономера, катализатора и
сокатализатора:
из уравнения (5), получим зависимостьvобщот
концентрации мономера, катализатора и
сокатализатора:
![]() (7)
(7)
При
![]()
![]()
Это соотношение не отражает влияние температуры и природы среды, которое распространяется не только на состав активного центра, но и на характер всех реакций.
Средняя степень полимеризации:
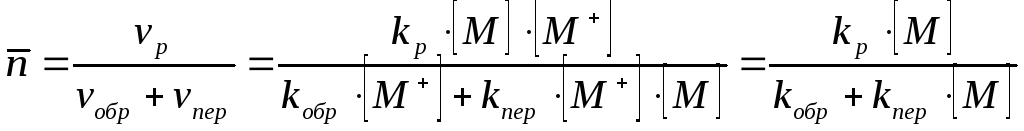
![]() (8)
(8)
Из уравнения (8) следует, что степень
полимеризации не зависит от концентрации
катализатора, в отличии от ЦРП. Если
скорость передачи цепи намного выше
скорости обрыва
![]() ,
то молекулярная масса не зависит от
концентрации мономера, т.к.
,
то молекулярная масса не зависит от
концентрации мономера, т.к.
при
![]()
![]() или
или![]()
Если же
![]() ,
то молекулярная масса пропорциональна
концентрации мономера, т.к.
,
то молекулярная масса пропорциональна
концентрации мономера, т.к.
при
![]()
![]() или
или![]()
Влияние различных факторов на кП
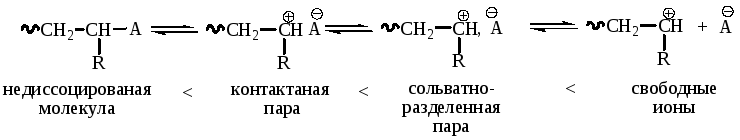
Влияние природы растворителя объясняется тем, что процесс полимеризации связан с образованием и диссоциацией ионных пар:
 активность
растет в этом ряду
активность
растет в этом ряду
Степень участия каждого из указанных состояний определяется не только полярными свойствами растворителя, но также природой мономера, противоиона и другими факторами.
Полярные растворители сольватируют растущие макрокатионы и способствуют смещению равновесия в сторону образования сольватно-разделенных пар, которые более реакционноспособны, чем контактные пары.
Пример: влияние диэлектрической проницаемости растворителя на молекулярную массу и скорость полимеризации α-метилстирола:
|
растворитель |
ε |
v, моль/мин |
М |
|
циклогексан |
1,9 |
1,25 |
2040 |
|
дихлорэтан |
10 |
3,3 |
4200 |
|
нитроэтан |
28 |
20,4 |
4450 |
|
нитробензол |
36 |
150 |
8300 |
Сольватирующая способность растворителя также влияет на кинетику полимеризации, т.к. растворитель может изменить активность реакционного центра. Например, КП стирола в среде нитротолуола протекает с достаточной скоростью, а в среде этанола не идет, хотя диэлектрические проницаемости этих растворителей близки.
Увеличение скорости КП и молекулярной массы под действием некоторых хлорсодержащих растворителей объясняется их участием в КП как сокатализаторов.
Влияние противоиона.
Чем меньше размеры противоиона и чем больше его нуклеофильность, тем более прочна его связь с реагирующим макрокатионом, и тем сложнее внедрение мономера в цепь.
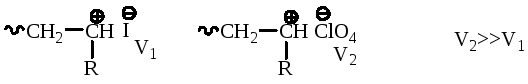
Например: скорость полимеризации стирола в CH2Cl2 в присутствииHClO4выше, чем в присутствииI2, т.к. размерыI-меньше размераClO4-.
Влияние температуры.
С понижением температуры скорость процесса уменьшается. Однако, при этом возрастает диэлектрическая проницаемость среды и уменьшается влияние противоиона на процесс, что может привести к повышению константы реакции роста цепи.
КП обычно проводят при температурах порядка -50÷-70 0С, в некоторых случаях ниже. Например, ПК изобутилена при -1000С в присутствии катализаторовAlCl3илиBF3заканчивается за несколько секунд с образованием полимера с молекулярной массой в несколько миллионов.
Влияние примесей.
При малых концентрациях примеси выполняют роль сокатализаторов и способствуют увеличению скорости полимеризации. При больших количествах они участвуют в реакциях ограничения роста цепи, снижают молекулярную массу и скорость реакции.
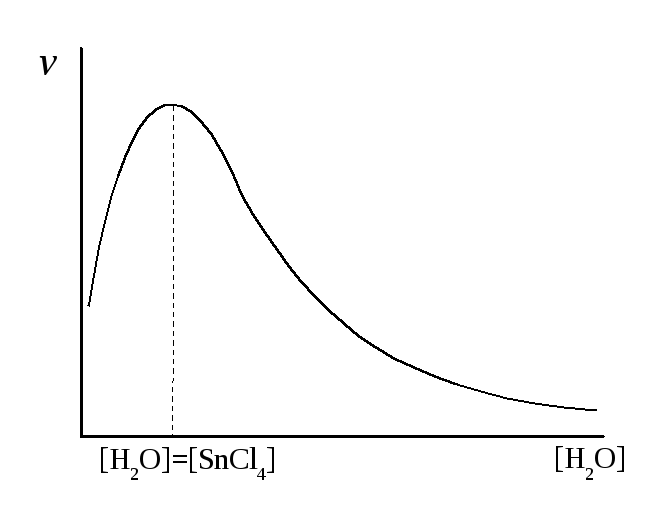
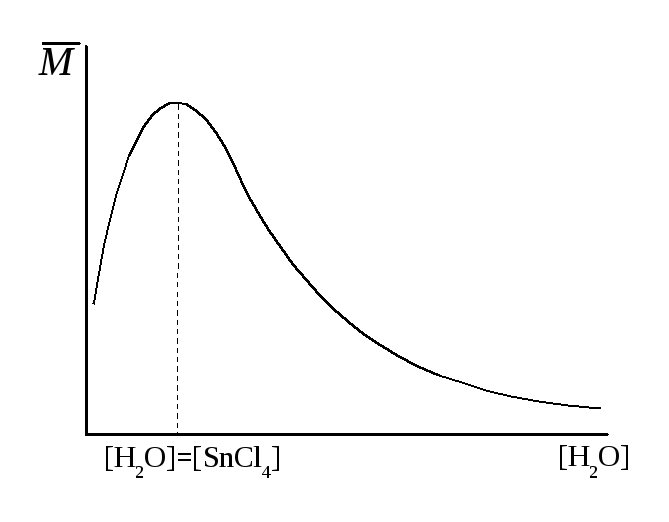
Например: влияние концентрации воды на полимеризацию стирола в присутствии SnCl4.
|
|
|