
- •Глава первая почвенная биота
- •В ельнике (по б.Д. Абатурову и г. В. Кузнецову):
- •Pw 47 Гелиобактерии Heliobacterwm chlorum |к50(ю)
- •Глава вторая участие почвенных микроорганизмов в превращении веществ и энергии в биосфере
- •Характеристика микробного метаболизма
- •Органические вещества
- •Разложение сложных органических безазотных веществ
- •Внутриклеточные аминокислоты
- •Молекула мочевой кислоты
- •Биологические процессы в почвообразовании
- •Разложение растительных остатков и формирование подстилки
- •Участие почвенных микроорганизмов в разрушении и новообразовании минералов
- •Глава третья экологические аспекты биологии почв
- •Распределение микроорганизмов в перегнойно-глеевой и дерново-подзолистой почве по частицам разной величины (число адгезированных клеток)
- •Относительная влажность воздуха, активность воды и потенциал влаги при 20 °с
- •Величины активности воды, лимитирующие рост микробов
- •Примеры летучих органических веществ, образуемых микроорганизмами и их влияние иа другие микроорганизмы
- •Примеры летучих органических веществ, образуемых микроорганизмами в анаэробных условиях
- •Примеры неорганических веществ, превращаемых микроорганизмами в летучие органические вещества
- •Кардинальные значения рН для роста некоторых почвенных микроорганизмов
- •Кардинальные температуры роста различных групп микроорганизмов
- •Строение и функционирование комплекса почвенных микроорганизмов
- •Концепция ненасыщенности комплекса почвенных микроорганизмов
- •Концепция почвы как множества сред обитания микроорганизмов
- •21 28 35 42 49 56 Сутки
- •Типы межвидовых биотических взаимодействий
- •Конкуренция (непосредственное взаимодействие) — прямое взаимное подавление обоих видов. Микробы антагонисты образуют антибиотики, действующие друг против друга.
- •Методологические подходы к изучению структурно-функциональной организации микробных сообществ в наземных экосистемах локусный подход
- •Использование разработанных подходов и методов для экологической оценки микробных сообществ наземных экосистем структура микробоценозов лесных экосистем: вертикально-ярусный подход
- •Численность дрожжей (тыс./г) в лесных подстилках и почвах в разные сезоны года (Московская обл.)
- •Численность представителей разных родов актиномицетов в подстилке и дерново-подзолистой почве (тыс. Кое/г субстрата)
- •Доминирующие роды бактерий в разных ярусах лесного биогеоценоза
- •В почвенных ярусах лесных биогеоценозов наблюдается постепенное снижение численности актиномицетов вниз по профилю, в то время как в степных и пустынных биогеоценозах не
- •Доминирующие виды мицелиальных грибов в разных ярусах ельника волосисто-осокового
- •1. Виды, относящиеся к собственно подстилочным сапроби- онтам, несомненно играющие важную функциональную роль в
- •Доминирующие виды дрожжевых грибов в разных ярусах лесного биогеоценоза
- •Сравнение структурно-функциональной организации микробных сообществ различных природных зон: географический подход одноклеточные бактерии
- •Спектры потенциальных доминант в сообществах бактерий пустынь и болот
- •Время, сут
- •Особенности развития двух груш микроорганизмов, выделенных из чернозема типичного в процессе сукцессии
- •Состав различных групп микроорганизмов в ризосфере злаков
- •Структура комплекса микромицетов (%) в дерново-подзолистой почве в ходе микробной сукцессии
- •Окончание табл. 21
- •Структура комплекса микромицетов (%) в ризоплане гороха в ходе микробной сукцессии
- •Структура комплекса микромицетов (%) в ризосфере гороха в ходе микробной сукцессии
- •Взаимодействие микроорганизмов и почвообитающих животных
- •Основные принципы биологической индикации и диагностики почв
- •Ботаническая и зоологическая биоиндикация и диагностика почв
- •Почвенные микроорганизмы и здоровье человека
- •Положительное влияние
Распределение микроорганизмов в перегнойно-глеевой и дерново-подзолистой почве по частицам разной величины (число адгезированных клеток)
Диаметр частиц, мкм |
Величина поверхности, мкм2 |
Перегнойно- глеевая почва |
Дерново- подзолнстая почва |
1-2 |
13 |
1 |
0,1 |
4-5 |
121 |
4 |
0,3 |
10-12 |
726 |
8 |
1,1 |
20-25 |
2 905 |
29 |
5,0 |
40-50 |
12 150 |
110 |
7,0 |
100-110 |
66 150 |
300 |
14,0 |
400-500 |
1 215 000 |
10 100 |
53,0 |
80-90% клеток в почве обычно находится в адгезированном состоянии. Много свободно плавающих клеток появляется в почвенном растворе только после внесения в почву легкорастворимых питательных веществ (сахара, органические кислоты), хотя каждый микроорганизм, по-видимому, имеет прикрепленную стадию, обычно предназначенную для жизнедеятельности или для сохранения, и свободную стадию, предназначенную для расселения. Адгезия микроорганизмов зависит от 1) особенностей микроорганизма, 2) особенностей адсорбента, 3) состава жидкой среды, в которой она осуществляется: рН, концентрации и природы катионов и других веществ. В первом приближении можно говорить о прямо пропорциональной зависимости количества адгезированных клеток от величины поверхности почвенных частиц (табл. 2), хотя более подробное изучение показывает, что бактерии располагаются на отдельных частицах крайне неравномерно. Некоторые частицы несут очень много клеток, другие частицы того же размера почти лишены их, что обусловлено различиями в химическом составе поверхности частиц.
ПРИРОДА ЯВЛЕНИЯ АДГЕЗИИ МИКРООРГАНИЗМОВ
Адгезия микроорганизмов представляется важной экологической чертой существования микроорганизмов. Она экологически оправдана, и без адгезии микробы не могли бы нормально существовать в почве: во-первых, адгезия помогает микробам удержаться в почвенном профиле и не подвергаться вымыванию в нижележащие горизонты; во-вторых, адгезированные клетки оказываются на границе раздела твердого тела и жидкости, где сосредоточены основные питательные вещества. Адгезия имеет и более целенаправленное значение. Так, бактерии, использующие целлюлозу, преимущественно адгезируются на целлюлозе, использующие крахмал — на крахмале, окисляющие серу — на ее кристаллах или каплях. Микробы, утилизирующие углеводороды, также избирательно адгезируются на них, а клубеньковые бактерии и фитопатогенные микроорганизмы избирательно адгезируются на корнях растений-хозяев. Обычно микроорганизмы по-разному адгезируются на разных стадиях своего развития. Есть стадии, на которых они находятся в свободном состоянии, и есть стадии, на которых они ведут прикрепленный образ жизни. Некоторые микробы переходят в адгезированное состояние в стадиях покоя, другие, наоборот, в активном состоянии адгезируются, а в стадиях покоя могут находиться в свободном состоянии.
С помощью каких же механизмов достигается такая тонкая регулировка процессов прикрепления и отрыва?
В настоящее время существует гипотеза, что микроорганизмы могут очень тонко и точно регулировать свое положение (свободное или адгезированное), для чего у них имеется ряд генетически запрограммированных особенностей. Это возможность синтеза определенных ферментов, изменения заряда и степени гидрофобное™ своей поверхности, синтез поверхностно-активных веществ, образование выростов, деление, хемотаксис и др. Микробы экологически целесообразно могут менять свое положение, располагаясь в свободном или адгезированном положении в зависимости от того, что в данный момент экологически выгодно.
Существовало несколько подходов к изучению природы адгезии микроорганизмов. Многие исследователи, изучавшие это явление до 70-х годов XX в., пытались проводить аналогию между адгезией микроорганизмов и адсорбцией ионов и молекул. Именно тогда широко употреблялся термин «адсорбция микроорганизмов». Пытались установить, в чем сходство и в чем различие в адсорбции микробных клеток и молекул, строили изотермы адсорбции, определяли влияние рН и концентрации катионов, устанавливали емкость поглощения, обменность адсорбции макроорганизмов и др. Обменная адсорбция изучалась с двух разных позиций: с одной стороны, устанавливалась возможность обмена одних микробных клеток на другие, с другой — изучалась возможность замены клеток на ионы. «Адсорбционное» направление продолжает развиваться и в настоящее время, но теперь имеет подчиненное значение. Это направление исследований было плодотворно, так как был установлен ряд пенных закономерностей адсорбции микробных клеток. Однако такой подход не мог разрешить все вопросы.
Некоторые исследователи изучали явление концентрации клеток на твердых поверхностях с позиций адгезионных процессов. Адгезией называется слипание поверхностей двух разнородных твердых тел. Адгезия обусловлена теми же причинами, что и адсорбция, но проявления этого процесса несколько другие, поскольку взаимодействуют не молекулы или ионы, а более крупные частицы. С теоретических позиций такой подход является более правильным, и в последнее время почти все исследователи пользуются термином «адгезия микроорганизмов», а не «адсорбция микроорганизмов». Это направление успешно развивается, что позволит уточнить ряд закономерностей.
В последнее время были введены еше один подход и еще один термин для обозначения того же явления — «иммобилизация клеток» (обездвиживание клеток). Представление об иммобилизованных клетках пришло из биохимии, где усиленно изучают иммобилизованные ферменты. Во многих случаях изучена природа связи ферментов с адсорбентом и специфика их активности. Поскольку было выяснено, что в ряде случаев для проведения определенных биохимических процессов, особенно многоступенчатых, часто выгоднее и удобнее использовать не отдельные ферменты, а их комплексы, локализованные в целых живых или убитых клетках микроорганизмов, то от изучения иммобилизованных ферментов перешли к изучению иммобилизованных клеток. Под иммобилизованными понимают либо клетки, адгезированные на твердых поверхностях самых различных частиц (пористое стекло, полимерные частицы, керамика, полимеры и др.), либо клетки, заключенные в различные гели. Последний случай часто используется и он хорошо изучен. Следует отметить, что оба случая имеют прямое отношение к почвенным микроорганизмам, поскольку в почве микробы также либо адгезированы на почвенных частицах, либо заключены в органоминеральный гель, покрывающий почвенные частицы. Интересно отметить, что часто клетки, заключенные в прочные сети геля, не могут размножаться. При изучении иммобилизованных клеток были использованы методы и достижения биохимии и молекулярной биологии. Однако природа сил, связывающих клетки, изучена гораздо хуже, чем природа сил, связывающих ферменты. Часто биохимики создают условия, которые могут быть аналогичны природным, но в ряде случаев создаются и чисто искусственные условия.
Наконец, четвертый подход, который стал очень популярным в последнее десятилетие и был особенно широко использован в медицинской микробиологии, — это молекулярно-био- логический подход, подобный тому, который используется в иммунохимии.
Внимание к вопросу об адгезии микроорганизмов было привлечено в связи с тем, что адгезия является первым этапом многих инфекционных болезней, и если предотвратить адгезию, то можно предотвратить и возникновение заболевания. Полагают, что адгезия клеток микроорганизмов основывается на специфическом механизме и происходит по принципу взаимодействия антигена с антителом — поверхность клетки подходит к адсорбирующей поверхности, как ключ к замку. Особенные успехи достигнуты в изучении адгезии клеток микроорганизмов на животных и растительных клетках.
Исследуя адгезию микроорганизмов, первые исследователи особенно большое значение придавали электрическому заряду взаимодействующих поверхностей и считали, что происходит взаимодействие противоположно заряженных поверхностей. Считали, что происходит взаимодействие разноименно заряженных поверхностей. Это явление наблюдали при адгезии клеток на оксидах железа и алюминия при низких значениях рН, а также при адгезии на ионообменных смолах (анионитах).
Однако в большинстве случаев при адгезии клеток происходит взаимодействие поверхностей с одноименным отрицательным суммарным зарядом. Прежде всего это взаимодействие с большинством почвенных частиц, с минералами и гумусом. При этом микроорганизмы несут на поверхности преимущественно карбоксильные и аминогруппы, отчасти фосфорные, сульфгид- рильные, спиртовые и др. Минералы в основном имеют ОН-груп- пы, гумус — карбоксильные группы. В ряде случаев адгезия объяснялась мозаичностью зарядов поверхности клеток и поверхности адсорбента. Австралийский ученый К. Маршалл, изучавший адгезию мелких частиц монтмориллонита (0,1 мкм) на клетках клубеньковых бактерий, пришел к выводу, что в опытах имело место электростатическое притяжение положительно заряженных концов пластинчатых частиц глины и отрицательно заряженных карбоксильных групп поверхности клетки. Для некоторых штаммов клубеньковых бактерий происходило взаимодействие положительно заряженных участков клетки, несущих аминогруппы, с отрицательно заряженными боковыми плоскостями частиц монтмориллонита.
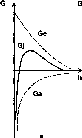
Рис.
92. Зависимость свободной
энергии от удаления от частицы как
функция концентрации электролита при
сближении одноименно заряженных
поверхностей:
а
—
низкая концентрация;
б
— средняя концентрация;
в —
высокая концентрация;
h
—
расстояние
от поверхности;
Gj
—
свободная энергия;
Ga
—
свободная
энергия сил Ван-дер- Ваапьса;
Ge—
энергия,
связанная с присутствием на поверхности
заряженных групп
Взаимодействие рассматриваемых сил приводит к существованию двух областей, в которых преобладают силы притяжения. Одна область расположена от поверхности на расстоянии 5-10 А. Прочность сцепления в этой области большая. На больших расстояниях начинают преобладать силы отталкивания, и затем на расстоянии около 100-150 А от поверхности имеется вторая область притяжения, однако прочность сцепления в этой области невелика.
Для того чтобы поверхности сблизились до расстояния 5-10 А, они должны преодолеть электростатическое отталкивание. Силы отталкивания между поверхностями снижаются при введении катионов, особенно многовалентных, или при подкислении среды. Они пропорциональны радиусу взаимодействующих поверхностей. Видимо, поэтому палочковидные клетки, по крайней мере на первых этапах, прикрепляются полюсом. Большинство микроорганизмов прикрепляется с помощью тонких нитей — фимб- рий, стебельков, выростов капсул и др.
Точные определения расстояния между клетками и поверхностью проводить довольно трудно. Однако есть основания полагать, что клетки могут располагаться на расстоянии первого и второго максимумов притяжения, а также может устанавливаться химическая связь между клеткой и поверхностью. Наблюдения, проведенные под микроскопом, показали, что клетки часто свободно скользят вдоль поверхности, но не могут отойти от нее, т.е. находятся на расстоянии 100-150 А. После высушивания препарата и последующей его регидратации клетки оказываются прочно закрепленными на определенных местах и их не удается смыть даже сильной струей воды. Вероятно, здесь проявилось прикрепление во втором максимуме притяжения или образование химических связей. Отметим, что для прочного прикрепления высушивание необязательно. Иногда клетки очень прочно прикрепляются и из водной среды.
Микроорганизмы по своим размерам (1-10 мкм) относятся к той категории частиц, которые должны быть подвержены наиболее сильной адгезии. У частиц большего размера гравитационные силы превосходят силы прилипания, частицы меньшего размера из-за малого веса не в состоянии выдавить слой жидкости и вступить в непосредственный контакт с поверхностью.
Некоторые исследователи утверждают, что главную роль в адгезии клеток микроорганизмов играют силы Ван-дер-Ваальса. Однако в ряде случаев прочность связи оказывается гораздо больше, чем можно было бы ожидать за счет этих сил.
При адгезии действует сложный комплекс сил. Силы притяжения.
Химические связи между взаимодействующими поверхностями, например, водородные, тиоловые, амидные, эфирные и др.
Образование ионных пар и ионных триплетов, например NH3...-OOC- и -СОО-...Са...-ООС- Этот тип связей включает энергию десольватации.
Силы, вызванные флуктуацией зарядов взаимодействующих тел.
Мозаичный заряд на поверхностях подобного или противоположного общего заряда, специфически возникающий из электростатического притяжения геометрически упорядоченных зарядов.
Силы, обусловленные притягательным взаимодействием противоположно заряженных тел.
Электростатическое притяжение между поверхностями, несущими одинаковый заряд.
Электростатическое притяжение, обусловленное отраженными силами, которые можно рассматривать как обусловленные десольватацией внутримембранных ионов при объединении мембран.
Силы Ван-дер-Ваальса.
Гидрофобные взаимодействия.
Помимо сил притяжения при адгезии клеток могут действовать силы отталкивания.
Силы отталкивания одноименно заряженных поверхностей.
Препятствия притяжению, обусловленные пространственными барьерами, такими как сольватные слои.
Таким образом, комбинация сил, действующих при адгезии, представляется довольно сложной, расчет и предсказание величины этих сил практически невозможны.
Очень долго изучали адгезию клеток на чистых минеральных поверхностях и только в последнее время пришли к выводу, что в подавляющем большинстве случаев взаимодействие происходит между макромолекулами поверхности клеток и макромолекулами или более простыми органическими молекулами, такими как ли- ииды, поверхностно-активные вещества и др., адсорбированными на минеральной поверхности почвенных частиц. Таким образом, вопрос об адгезии сводится к проблеме взаимодействия макромолекул, которое очень разнообразно.
После того как проблема изучалась с физико-химических позиций, она, как видно, в некоторых отношениях зашла в тупик.
В последнее время ее пытаются решить с позиций молекулярной биологии.
Молекулярно-биологические аспекты адгезии микроорганизмов на почвенных частицах представляют интригующую область, которая только начинает развиваться в основном в медицинской микробиологии при установлении взаимодействия бактерий с поверхностью клеток животных тканей. Микробы адгезируются на поверхности различных органов и тканей, причем адгезия идет специфично и избирательно. Микрофлора языка, щек, нёба, зубов, разных отделов кишечного тракта различна, т.е. специфична для каждого органа. Наиболее подробно изучена адгезия холерного вибриона, гонококка, патогенных штаммов кишечной палочки и микробов, вызывающих кариес зубов.
Адгезия бактерий включает в себя несколько этапов. Первый этап состоит в целенаправленном движении бактерий к адсорбирующей поверхности. Он возможен для подвижных микроорганизмов и осуществляется благодаря наличию хемотаксиса. Хемотаксис у бактерий в настоящее время хорошо изучен и осуществляется по градиенту концентрации какого-либо вещества. Подробно исследован хемотаксис в градиенте концентраций Сахаров и аминокислот.
Предполагается, что во всех случаях прикрепление осуществляется за счет специфического субстрат-ферментного взаимодействия. В ряде случаев адгезия проходит за счет специфического химического взаимодействия адгезина и акцептора, причем установлены конкретные химические группировки, ответственные за адгезию. Более подробно это изучено для адгезии патогенных бактерий на эпителии кишечного тракта, но относится также к адгезии фитопатогенов и симбиотических клубеньковых бактерий на корнях бобовых растений.
Для животных и человека установлено, что микробы адгезируются на поверхности различных органов и тканей, причем адгезия идет специфично и избирательно. Подобное явление наблюдается и для растений, и почвенных беспозвоночных животных. Адгезия бактерий включает в себя несколько этапов. Первый этап состоит в целенаправленном движении бактерий к адсорбирующей поверхности. Он возможен для подвижных микроорганизмов и осуществляется благодаря наличию хемотаксиса. У бактерий хемотаксис в настоящее время хорошо изучен и осуществляется по градиенту концентрации какого-либо вещества. Подробно исследован хемотаксис в градиенте концентраций Сахаров и
аминокислот. Приблизившись к поверхности, бактерии взаимодействуют с ней сначала с помощью достаточно слабых водородных и гидрофобных взаимодействий, а также сил Ван-дер- Ваальса согласно теории Дерягина-Ландау-Вервея-Овербика (ДЛВО) (рис.92), которые, однако, не могут обеспечить большой специфичности взаимодействия. При этом молекула адге- зина — полимера, расположенного на поверхности бактерий, взаимодействует с рецептором — полимером, расположенным на поверхности адсорбента (рис. 93). Взаимодействие адгезина с рецептором осуществляется по тому же механизму, что и взаимодействие антигена с антителом (ключ-замок). Затем часто наступает более прочное прикрепление, которое требует времени и осуществляется только через несколько часов или даже суток после начала адгезии и достигается благодаря синтезу бактериями биополимера, обычно полисахаридов, но иногда и полипептидов, с помощью которых клетки прикрепляются иногда так прочно, что легче разрушить клетку, чем отделить ее от адсорбента. Экспериментально показано, что именно так прочно прикреплены многие собственно почвенные бактерии.

♦ • • • •
в
#3
Л

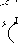
I 4 fl 5
«> V. «у t Ч ч t г 'г' xj
Рис. 93. Взаимодействие бактерий с поверхностью животных клеток по принципу ключ-замок:
1 — молекула специфических адгезинов; 2 — О комплементарные или рецепторные молеку
лы; 3 — протеины: 4 — гидрофобные молекулы; 5— фосфолипиды; а — адгезия осуществилась; 6, в — адгезия не наступила из-за введения избыточною количества рецептора или
адгезина
животных и человека являются почти исключительно углеводы: манноза, галактоза, фукоза, а также сиаловая кислота.
КЛЕТКА
йТйй
гп
Адгезии
ЧАСТИЦА



Рис. 94. Взаимодействие клеток бактерий с гидрофильной (/) и гидрофобной (2) поверхностями
Таким образом, адгезия генетически запрограммирована, имеет важное экологическое значение и во многих случаях определяет выживание вида.
ДЕСОРБЦИЯ МИКРООРГАНИЗМОВ ПРИ ИХ КОЛИЧЕСТВЕННОМ УЧЕТЕ В ПОЧВЕ
Для правильного количественного учета микроорганизмов в почвах необходимо вызвать три процесса: 1) разрушить почвенные агрегаты, 2) десорбировать почвенные микроорганизмы с твердых поверхностей, 3) разделить находящиеся в почве микроколонии на отдельные составляющие их клетки. Все три процесса вызываются одинаковыми воздействиями, хотя очень трудно осуществить их полностью. Типы воздействия могут быть механическими и химическими. Механические воздействия — это растирание, обработка почвенной суспензии на пропеллерной мешалке (миксер, микроизмельчитель тканей, магнитная мешалка),
ультразвуковая (УЗ) обработка. Химические воздействия — это обработка щелочью или раствором пирофосфата натрия, который обладает щелочным действием, воздействие поверхностно- активными веществами (ПАВ), например додецилсульфатом натрия, обработка ферментами.
Наиболее эффективными оказались механические обработки. Для учета бактерий методом посева или прямым микроскопическим методом используют УЗ небольшой частоты и мощности, так как в противном случае будут разрушены сами клетки. Собственно почвенные бактерии гораздо более устойчивы к УЗ, чем их лабораторные культуры. Существует такая закономерность: чем крупнее клетки, тем больше они разрушаются УЗ. Поэтому для грибов, как более крупных организмов УЗ довольно губителен и при учете грибов лучше применять пропеллер-' ную мешалку, добиваясь разрушения почвенных агрегатов и дробления мицелия на однородные части длиной 15-30 мкм при сохранении ими жизнеспособности и целостности конидий и половых спор.
Если количественный учет микроорганизмов в почве проводится без тщательной предварительной подготовки почвенной суспензии, получают совершенно неверные результаты. Предварительная обработка почвенной суспензии повышает определяемое количество микроорганизмов в зависимости от типа и состояния почвы в 3-300 раз. Особенно сильный эффект получается для сухих оструктуренных почв. Малый эффект наблюдается для сильно увлажненных нижних минеральных горизонтов почв. При традиционном способе подготовки почвенной суспензии путем 10-минутного перемешивания почвенной суспензии в колбе можно получить, хотя и не абсолютные, но годные для сравнения результаты, например, для разных делянок одной и той же почвы одинаково увлажненных, но содержащих разные количества удобрений. Такое сравнение невозможно для почв разных типов или почвенных образцов из разных генетических горизонтов, а также для сравнения сухих и увлажненных почв. Часто делают вывод о том, что при высушивании почв клетки погибают, а они по крайней мере частично переходят в адсорбированное состояние и не учитываются.
Если старый метод давал различие в содержании бактерий в разных типах почв в 2-3 раза, то с применением новых методов диспергирования почв и десорбции микроорганизмов оказалось, что эти различия достигают десятков и даже сотен раз.
АКТИВНОСТЬ АДГЕЗИРОВАННЫХ КЛЕТОК
Адгезированные клетки находятся в специфической микрозоне, образующейся на границе раздела жидкости и твердого тела, где адсорбируется большинство полимерных органических веществ в том числе и гумус, происходит адсорбция гидролитических ферментов. Поскольку большинство почвенных частиц заряжены отрицательно, здесь концентрируются положительно заряженные органические мономеры, повышается концентрация адсорбированных катионов (К, NH4 Са, Mg, Н), уменьшается концентрация неорганических и органических анионов (рис. 95). Активность адгезированных клеток по сравнению со свободными часто резко изменяется. Она может быть больше или меньше, чем у свободных в зависимости от того,
Рис.
95.
Концентрирование клеток бактерий
(Г), катионов (2), субстратов (3), экзоферментов
и других биологически активных
веществ (4) на поверхности почвенных
частиц
1
•2 А 3 ■
4
окажутся ли условия в микрозоне на поверхности раздела более или менее благоприятными, чем в почвенном растворе. Обычно эта микрозона более благоприятная, так как адсорбированные гидролазы осуществляют гидролиз полимеров и появляются легкодоступные мономеры (сахара, аминокислоты, органические кислоты, спирты). Микробы лучше обеспечены минеральными питательными веществами в том числе фосфором и железом, которые также осаждаются на поверхности частиц. Автотроф- ные нитрификаторы используют преимущественно адсорбированный аммоний.
Однако на поверхности раздела жидкой и твердой фаз могут концентрироваться и токсичные вещества, такие как тяжелые металлы, антибиотики. Здесь может быть меньше отрицательно заряженных органических кислот или аминокислот и тогда адгезированные микробы будут развиваться хуже. На поверхности раздела отрицательно заряженных частиц в кислых почвах будет
более низкое рН из-за высокой концентрации ионов водорода, что также будет оказывать влияние на развитие микробов. Почвенные биохимики предложили молекулярный рН-метр для
Активность
катаяазы мл
0мии
18
1Б
14
12
8
9 рН раствора
Рис.
96.
Кажущийся сдвиг рН оптимума каталазы
при ее адсорбции на частицах минерала
шиттшттп*
t)
ТГ
1
Рис. 97. Адсорбция фермента (белые круги) и субстрата (черные круги) на поверхности минерала в слое органоминерального геля и в межплоскостном пространстве монтмориллонита
тельно заряженные, гидрофильные и гидрофобные участки. Поэтому на разных почвенных частицах адсорбция проходит разными сторонами. Если закрывается активный центр, фермент
теряет активность. Обычно при адсорбции изменяется конфор- мация (конфигурация) молекулы, что ведет к изменению активности фермента, но он становится более устойчивым к воздействию неблагоприятных факторов (высушивание, хранение, температурные воздействия и др.). Фермент может быть закрыт органоминеральным гелем или может попасть в межплоскостные пространства минералов типа монтмориллонита. Все это будет отражаться на его активности. Молекула субстрата может быть очень маленькой (Н202) или очень крупной, например, белковая молекула для протеазы (на рисунке обозначена черными кружками).
Адсорбированные (иммобилизованные) ферменты в последние 30 лет широко применяются в биотехнологии. Однако, как обнаружилось, природа использует эти механизмы уже миллиарды лет.
В настоящее время хорошо изучено влияние адсорбентов на различные типы брожений, на азотфиксацию, нитрификацию, использование кислых и основных аминокислот, окисление метана, водорода, использование некоторых углеводородов. Наиболее сильно влияние твердых частиц проявляется в разбавленных растворах, каковым, в частности, обычно является почвенный раствор. Здесь микроорганизмы часто не могут развиваться в растворе из-за низкой концентрации питательных веществ, но на поверхности частиц они развиваются, так как здесь концентрация питания оказывается гораздо больше. Это явление было подробно изучено водными микробиологами для олиготрофных водоемов (см. рис. 95). Влияние адсорбента может оказывать различный и даже прямо противоположный эффект в зависимости от взаимного расположения частиц адсорбента и клеток (рис. 98). В случае а на клетки будет оказывать влияние специфика поверхности раздела
Рис.
98.
Различные случаи взаимного расположения
частиц адсорбентов и клеток бактерий
(объяснения
см. в тексте)
а
б
в г
жидкости и твердого тела. В случае 6 адсорбент не будет оказывать непосредственного действия на клетки. В случае в клетки покрываются чехлом из коллоидных частиц гумуса или глинистых
Рис.
100.
Отрыв эпителиальных клеток с
адгезированными микробами от
поверхности растительной ткани
Рис.
99.
Степень удаленности адгезирован-
ных клеток от твердой поверхности
минеральной частицы и покрывающего
ее органоми- нерального геля
жение, влияющее на жизнедеятельность, будет особым. Четвертый случай г представляет собой заключение клеток внутри конгломерата из частиц. Часто активность клеток в таких условиях вообще невозможна.
Активность будет зависеть от плотности контакта с частицами (рис.99). Показано 10случаев более или менее плотного контакта клетки бактерии с почвенной частицей, покрытой пленкой из органического или минерального геля: от полного удаления от частицы до расположения на поверхности геля, внутри геля или на поверхности минеральной частицы. Поверхность минеральной частицы показана на рисунке черной линией, а органоминеральный слой окрашен в серый цвет. Клетки со стебельком, жгутиками, фимбриями, с капсулой или без нее будут располагаться в разных по свойствам микрозонах. Особое положение занимают клетки, погруженные в органоминеральный гель (собственно иммобилизованные клетки). Во многих случаях они вообще не могут делиться. Ясно, что в каждом случае микросреда
для развития клетки будет разной, а клетка всегда развивается в микросреде.
Эффективный способ борьбы с прикрепившимися фитопато- генными микроорганизмами имеется у растительных и животных организмов. Если клетки прикрепились и нет возможности от них избавиться, корень или другой орган растения или животного сбрасывает клетки своего эпителия и таким образом освобождается от вредных микроорганизмов (рис. 100).
Жидкая фаза почвы
'///////////////У///////////,
^7777777^}
7777777777777777777777777777
7777777^77^^
чие. 101. Пространственное расположение клеток бактерий (Г) и различных форм воды (2)
чаться и по потенциалу влаги. Он может быть различным в течение долгого времени в разных почвенных горизонтах.
Жидкая фаза почвы всегда содержит некоторое количество минеральных, органических и органоминеральных веществ в молекулярном или коллоидном состоянии, а также растворенные газы. Однако концентрация питательных веществ в почвенном растворе обычно очень мала, и развитие микроорганизмов в объеме почвенного раствора происходит сравнительно редко. Они
развиваются в адгезированном состоянии. Таким образом, главная функция почвенного раствора заключается в переносе веществ и обеспечении микроорганизмов водой. Снабжение питательными веществами обычно проходит два этапа: 1) перенос питательных веществ с почвенным раствором на твердую поверхность и концентрирование на ней, 2) использование адсорбированных веществ адгезированными микробными клетками.
Почвенный раствор в сотни и тысячи раз менее концентрирован по сравнению с обычно применяемыми микробиологическими питательными средами, например средой Чапека, мясо-пептон- ным бульоном или крахмало-аммиачной средой. Отсюда возникла идея о необходимости применения при культивировании почвенных микроорганизмов очень разбавленных питательных сред, особенно в тех случаях, когда исследователь хочет приблизиться к воссозданию естественной обстановки. В этих условиях удается выделять и изучать олиготрофы. Микроорганизмы успешно развиваются в разбавленных питательных растворах и здесь их вырастает гораздо больше, чем на богатых средах. Так, на разбавленном в 10 раз мясо-пептонном агаре вырастает в 5-10 раз больше колоний, чем на исходном, на агаризованной воде — еще больше, но их уже нужно подсчитывать через месяц, а не через три дня, как на МПА и рассматривать в бинокулярную лупу, так как колонии очень малы. Трудность изучения состоит в том, что они растут очень медленно и экспериментатор должен затратить длительное время. Необходимо также иметь в виду, что в отдельных микрозонах и в естественной почве могут создаваться высокие концентрации растворенных и нерастворенных органических питательных веществ. Примером микрозон первого типа может служить ризоплана с непрерывным поступлением большого количества корневых выделений, а примером микрозон второго типа— отмерший корешок растения или погибший дождевой червь.
ТЕРМОДИНАМИЧЕСКАЯ ХАРАКТЕРИСТИКА СОСТОЯНИЯ ПОЧВЕННОЙ ВЛАГИ (ТЕРМОДИНАМИЧЕСКИЙ ПОТЕНЦИАЛ, АКТИВНОСТЬ ВОДЫ)
Условия увлажнения в почве обычно характеризовали ее влажностью, выраженной в процентах от веса. Однако эта величина недостаточно точно определяет степень доступности воды для организмов. Например, при 20%-й влажности глинистой и песчаной почв степень доступности воды для организмов различная. В глинистой почве она меньше, так как вода будет связана с огромной поверхностью глинистых частиц, а в песчаной — больше. Возможность объективно оценить состояние воды в почве и ее влияние на жизнедеятельность микроорганизмов дает определение потенциала влаги (активности воды), так как в этом случае состояние воды в почве, растениях, микроорганизмах, атмосфере, снегу и во льду характеризуется при помощи единой, физически строго определенной величины — термодинамического потенциала. Этот показатель характеризует степень связанности и термодинамической подвижности воды в системе, причем он не зависит от того, связана ли вода с поверхностью почвенных частиц, ионов солей, макромолекул или кристаллов льда.
В микробиологии наиболее часто используется термин активность воды (aw), который характеризует степень связанности ее молекул и тем самым степень доступности для микроорганизмов. Активность воды соответствует проценту относительной влажности воздуха, о которой ежедневно сообщается в сводках погоды. Только эта величина выражена не в процентах, а в долях единицы. Активность свободной воды равна единице. При взаимодействии воды с твердыми поверхностями, катионами и анионами, молекулами мономеров и полимеров, т.е. любыми гидрофильными группировками, активность воды становится меньше единицы. Активность воды определяется по формуле
^ Р __ ов _ п2
°w PQ 100 /7, - П2 '
где Р— давление водяного пара в исследуемой системе, Р0 — давление пара над чистой водой, ОВ — относительная влажность воздуха в системе, Я, — число молей растворителя, П2 — число молей растворенного вещества.
Состояние воды в системе часто определяется потенциалом влаги. Он характеризуется давлением, которое нужно приложить, чтобы при данных условиях началось удаление молекул воды из системы. Иначе можно сказать, что потенциал влаги измеряется количеством работы, которая должна быть затрачена для извлечения воды:
p=d± dV'
где А — работа, V— объем.
Потенциал чистой воды равен нулю. По отношению к чистой воде все растворы имеют отрицательные потенциалы, которые выражаются в отрицательных атмосферах или мегапаскалях (МПа) (1 атм = О,I МПа).
Сопоставление различных величин, выражающих термодинамическое состояние воды, представлено в табл. 3.
Водный потенциал часто выражается в барах (1 бар= 106дин/см2 = = 0,987 атм). Его также можно выразить через активность воды (табл. 3).
Таблица 3
