
- •Лабораторне заняття №1
- •1. Загальна частина
- •1.1. Правила техніки безпеки під час роботи в агрохімічній лабораторії
- •1.2 Основні положення техніки безпеки на робочому місці
- •2. Теоретична частина
- •3. Практична частина
- •Хід роботи
- •Хід роботи
- •Контрольні питання.
- •Лабораторне заняття №2
- •1. Теоретична частина
- •Оптимальний валовий вміст азоту, фосфору і калію в рослинах, % на абсолютно суху речовину.
- •Вміст азоту у вегетативній масі зернових культур по фазам розвитку, % на повітряно-суху речовину.
- •Вміст білка та азоту в насінні різних культур, %.
- •Коефіцієнти для перерахунку вмісту азоту на вміст білка.
- •Дсту 3768:2009 Пшениця. Технічні умови
- •2. Практична частина
- •Хід роботи.
- •Хід роботи
- •Хід роботи
- •Контрольні питання
- •Лабораторне заняття №3
- •1. Теоретична частина
- •2. Практична частина.
- •Хід роботи.
- •Шкала стандартних розчинів порівняння для побудови калібрувального графіку при визначенні вмісту калію в рослинному матеріалі
- •Контрольні питання.
- •Лабораторне заняття №4
- •1. Теоретична частина.
- •Групування ґрунтів за ступенем кислотності та лужності (згідно з Методикою агрохімічної паспортизації земель сільськогосподарського призначення. – к.: 2003. – 64с.)
- •Групування ґрунтів за гідролітичною кислотністю
- •Класифікація ґрунтів за вмістом обмінних основ
- •2. Практична частина
- •Хід роботи
- •Хід роботи
- •Контрольні питання.
- •Лабораторне заняття №5
- •1. Теоретична частина
- •1.1 Визначення потреби ґрунту у вапнуванні
- •Потреба ґрунтів у вапнуванні за результатами аналізів (за м.Ф.Корніловим)
- •Потреба та черговість проведення вапнування ґрунтів (за г.А.Мазуром та г.К.Медвідь)
- •1.2 Методи встановлення норм вапна
- •Орієнтовні норми СаС03 залежно від рНксі і гранулометричного складу ґрунтів Полісся та західних районів України з дуже низьким вмістом гумусу, т/га (за п.О.Дмитренко та б.С.Носко)
- •Орієнтовні норми СаС03 залежно від рНксі і гранулометричного складу ґрунтів Лісостепу з низьким та середнім вмістом гумусу, т/га (за а.Н.Небольсіним)
- •Розрахунки норм вапняних добрив для опідзолених і чорноземних ґрунтів з вмістом гумусу понад 3% (за м.В.Козловим і а.А.Плішко)
- •Нормативні витрати СаСо3 для зміщення реакції ґрунту на 0,1рН, т/га (Бука і.Я., Дуда г.Г.)
- •Класифікація ґрунтів за ступенем засолення та солонцюватості
- •Орієнтовні норми внесення гіпсу залежно від типу ґрунтів, т/га
- •2. Практична частина
- •Хід роботи
- •Шкала стандартних розчинів порівняння для побудови калібрувального графіка при визначенні натрію в ґрунті
- •Хід роботи
- •Хід роботи
- •Контрольні питання
- •Лабораторне заняття №6
- •1. Теоретична частина
- •Вміст азоту в орному шарі різних ґрунтів
- •Групування ґрунтів за вмістом легкогідролізованого азоту (по Корнфілду)
- •2. Практична частина
- •Хід роботи
- •Контрольні питання
- •Лабораторне заняття №7
- •1. Теоретична частина
- •1.1 Фосфор у ґрунті.
- •Вміст органічних і мінеральних форм фосфатів в різних ґрунтах
- •1.2 Калій в ґрунті
- •Вміст к20 в орному шарі різних ґрунтів, %
- •1.3 Визначення вмісту рухомих форм фосфору і калію в ґрунті за методом а.Т. Кірсанова.
- •1.4 Визначення вмісту рухомого фосфору і обмінного калію в ґрунті за методом ф.В. Чирикова.
- •1.5 Визначення рухомих форм фосфору і калію за методом б.Т. Мачигіна.
- •1.6 Визначення вмісту обмінного калію за методом а.А. Маслової.
- •Групування ґрунтів за вмістом рухомого фосфору
- •Групування ґрунтів за вмістом обмінного калію
- •1.7 Складання і використання агрохімічних картограм та паспортизація полів.
- •Групування ґрунтів за вмістом гумусу (по Тюріну)
- •2. Практична частина
- •1.1 Екстрагування сполук фосфору і калію з однієї наважки. Хід роботи
- •1.2 Визначення вмісту рухомого фосфору в ґрунті за ф.В. Чириковим. Хід роботи
- •Шкала для визначення вмісту рухомого фосфору в ґрунті за методом ф.В.Чирикова в модифікації цінао
- •1.3 Визначення вмісту обмінного калію в ґрунті.
- •Хід роботи
- •Шкала для визначення вмісту обмінного калію в ґрунті за методом ф.В.Чирикова
- •Контрольні питання
- •Лабораторне заняття №8
- •1. Теоретична частина
- •1.1 Класифікація добрив
- •1.2 Розпізнавання добрив
- •На розпеченому вугіллі
- •Властивості найпоширеніших азотних добрив
- •2. Практична частина
- •Хід роботи
- •Хід роботи
- •Контрольні питання
- •Лабораторне заняття №9
- •1. Теоретична частина
- •Властивості найпоширеніших фосфорних добрив
- •Властивості найпоширеніших калійних добрив
- •2. Практична частина
- •Хід роботи
- •Хід роботи
- •Контрольні питання
- •Лабораторне заняття №10
- •1. Теоретична частина
- •1.1 Мікроелементи та мікродобрива
- •Особливості використання мікроелементів
- •1.2 Комплексні добрива
- •Основні види комплексних добрив
- •Допустимість змішування різних форм добрив
- •2. Практична частина
- •Контрольні питання
- •Лабораторне заняття №11
- •1. Теоретична частина
- •1.1 Гумус ґрунту і потреба в органічних добривах
- •1.2 Види органічних добрив
- •Склад свіжого гною в залежності від виду тварин (солом’яна підстилка), %
- •Норми підстилки на голову худоби за добу, кг
- •Кількість підстилкового гною, яка отримується від 1 голови тварин за стійловий період, т
- •Річний вихід і склад пташиного посліду
- •2. Практична частина.
- •Хід роботи
- •Хід роботи
- •Контрольні питання
- •Лабораторне заняття №12
- •1. Теоретична частина.
- •1.1 Бактеріальні препарати.
- •Ефективність симбіотичної азотфіксації у різних бобових культур (л.А. Тихонович, 2007)
- •Основні бактеріальні препарати, дозволені для використання в Україні
- •1.2 Регулятори росту рослин.
- •Основні ррр дозволені до використання в Україні.
- •Контрольні питання
- •Лабораторне заняття №13
- •1. Теоретична частина.
- •Орієнтовні оптимальні норми мінеральних добрив (кг/га) під основні сільськогосподарські культури (узагальнені дані)
- •Орієнтовні норми удобрення сільськогосподарських культур з урахуванням забезпеченості ґрунту рухомими формами азоту, фосфору і калію (а.О. Мельничук та ін.)
- •Середній вміст рухомих сполук елементів живлення в ґрунті (Дмитренко п.О., Носко б.С.), мг/кг
- •Поправкові коефіцієнти для рекомендованих норм мінеральних добрив на ґрунтах з різним ступенем забезпеченості рослин елементами живлення
- •Приблизні витрати основних елементів живлення (кг) на одиницю (т) товарної продукції з урахуванням нетоварної для деяких культур
- •Витрати основних елементів живлення (кг) на одиницю (т) товарної продукції деяких сільськогосподарських культур
- •Коефіцієнти використання сільськогосподарськими культурами елементів живлення з ґрунту за різного вмісту їх рухомих сполук, %
- •Коефіцієнти використання елементів живлення сільськогосподарськими культурами з гною і мінеральних добрив, %
- •Розрахунок норм добрив під пшеницю озиму для отримання приросту врожайності 2,0т/га (за врожаю без внесення добрив 3,0т/га)
- •Нормативи витрат елементів живлення добрив на формування врожаю і приросту врожаю
- •Ціна бала ґрунту та окупність добрив
- •Рекомендоване співвідношення між елементами живлення в мінеральних добривах для внесення під сільськогосподарські культури в Лісостепу України
- •2. Практична частина.
- •Контрольні питання.
- •Лабораторне заняття №14.
- •1. Теоретична частина.
- •1.1 Удобрення пшениці озимої.
- •1.2 Удобрення ярих зернових культур.
- •1.3 Удобрення зернобобових культур.
- •1.4 Удобрення кукурудзи.
- •1.5 Удобрення буряку цукрового.
- •1.6 Удобрення соняшнику.
- •2. Практична частина.
- •Контрольні питання.
- •Лабораторне заняття №15.
- •1. Теоретична частина.
- •1.1 Сучасні системи удобрення культур у сівозмінах з різною ротацією в зоні Лісостепу.
- •Поправочні коефіцієнти для ґрунтів із різним ступенем забезпеченості поживними речовинами (е.Г. Дегодюк, 1988, 1993)
- •Система розподілу добрив у 10-пільній польовій сівозміні на чорноземах типових і вилугуваних у підзоні достатнього зволоження Лісостепу
- •Система розподілу добрив у 10-пільній польовій сівозміні на чорноземах типових, вилугуваних і сірих лісових ґрунтах у підзоні нестійкого зволоження Лісостепу (Центральний Лісостеп)
- •Система розподілу добрив у 10-пільній польовій сівозміні на чорноземах типових, опідзолених і сірих лісових ґрунтах у підзоні недостатнього зволоження Лісостепу
- •Система удобрення в короткоротаційній польовій сівозміні в підзоні достатнього зволоження Лісостепу з насиченням 50% зернових і по 25% цукрових буряків та кормових культур
- •Система удобрення в короткоротаційній польовій сівозміні на чорноземах і сірих лісових ґрунтах в підзоні нестійкого зволоження Лісостепу з насиченням 80% зернових і по 20% соняшнику
- •1.2 Система удобрення культур у сівозмінах Степової зони.
- •Система удобрення культур у короткоротаційних сівозмінах для господарств площею до 100га
- •Система удобрення культур у сівозмінах для господарств площею до 250-1000га
- •Система удобрення культур у сівозмінах для господарств площею понад 1000га
- •Система удобрення культур у сівозмінах із внесенням гною для господарств площею до 250-1000га
- •Система удобрення культур у сівозмінах із внесенням гною для господарств площею понад 1000га
- •1.3 Система удобрення культур у сівозмінах на зрошуваних землях Південного Степу.
- •Система удобрення культур у короткоротаційній зрошуваній сівозміні
- •Система удобрення культур у польові зрошуваній сівозміні з використанням післяжнивних решток як органічних добрив
- •2. Практична частина.
- •Контрольні питання.
- •Рекомендована література
Хід роботи
1. Відважити 1-2г тонко розмеленого повітряно-сухого рослинного матеріалу, перенести в хімічний стакан на 150-200мл, прилити 50мл дистильованої води, нагріти до кипіння. Якщо рослинний матеріал містить багато крохмалю, його нагрівають не більше 10 хвилин на водяній бані при температурі 60°С, помішуючи скляною паличкою.
2. Провести осадження білків. Для цього в стакан долити 25мл 6%-го розчину CuS04 перемішати і додати 1,25% розчину NaOH для утворення основної солі сульфату міді — CuS04•Cu(OH)2, яка осаджує білки. При цьому випадає комплексний осад молекул білка і міді.
3. Дати можливість відстоятися осаду 30—40хв. і потім профільтрувати через беззольний фільтр (пронумерований простим олівцем). Для цього розчин обережно злити по паличці на фільтр, а осад відмивати шляхом декантації гарячою дистильованою водою, поки промивні води перестануть утворювати з розчином ВаСІ2, осад, що засвідчує відсутність S042-.
4. Висушити відмитий осад із фільтром при температурі 50—60°С, перенести в колбу К'єльдаля, долити 20мл концентрованої H2S04 (густина 1,84г/см3) та додати 0,5г мідного купоросу (як каталізатора) і грудочку парафіну для зменшення піноутворення у відгінній колбі.
5. Спалити фільтр з осадом в H2S04 до повного знебарвлення вмісту колби К'єльдаля.
6. Підготувати колбу-приймач. Для цього відміряти 40—60мл 0,1М розчину H2S04, додати 3—4 краплі метилоранжу і кінець трубки холодильника занурити в кислоту колби-приймача.
7. Озолений осад кількісно перенести в дистиляційну колбу, додати 2г цинку, 1—2 краплі фенолфталеїну та обережно по стінці прилити 70-80мл 30-40%-го лугу і швидко сполучити з холодильником.
8. Провести відгонку аміаку. Дистиляцію закінчити при відсутності реакції на іони NН4+, пробуючи реактивом Неслера.
9. Відтитрувати лишок 0,1М розчину H2S04 0,1М розчином NaOH.
10. Обчислити вміст білкового азоту за формулою:
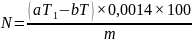
де N — вміст білкового азоту в рослинному матеріалі, %;
а — кількість 0,1М розчину H2S04, влитого в колбу приймач, мл;
Т1 – поправка до титру кислоти;
b – кількість 0,1М розчину NaOH, витраченого на титрування лишку кислоти, мл;
T — поправка до титру лугу;
0,0014 - кількість грамів азоту, що зв'язується 1мл 0,01М розчину Н2SO4;
100 — коефіцієнт для вираження результатів у відсотках;
m — наважка повітряно-сухого рослинного матеріалу, взятого для озолення, г;
Обчислення результатів. Для визначення вмісту білка в зерні гороху наважка тонко розмеленого повітряно-сухого борошна становила 1,5г. Після її обробки, спалювання і відгонки аміаку в колбу-приймач взято 60мл 0,1М розчину Н2SO4, на титрування лишку якої витрачено 16мл 0,1М NaOH. Поправки до титру кислоти 0,96, лугу — 1,02. Тоді вміст білкового азоту:

Обчисливши вміст білкового азоту в рослинному матеріалі, досить легко можна визначити вміст білка, користуючись коефіцієнтами (табл.4). Так, при аналізі зерна гороху вміст білкового азоту склав 3,85%, помноживши його на коефіцієнт 5,7 знаходимо, що вміст білка в зерні становить 3,85×5,7 = 21,9%.
Дослід 3. Визначення вмісту клейковини в зерні пшениці.
Принцип методу кількісного визначення клейковини в зерні базується на властивостях ряду його білків (гліадинів і глютелінів) утворювати з водою в'язку масу, яку в процесі промивання водою відмивають від крохмалю та інших розчинних сполук, потім віджимають і зважують з точністю до ± 0,1г, обчислюють її вміст у відсотках.
