
- •Дс. 04 технохимический контроль ликероводочного производства лабораторный практикум
- •260200 Производство продуктов питания из растительного сырья Специальность 260204 Технология бродильных производств и виноделие
- •Введение
- •Оглавление
- •Лабораторная работа №1 анализ растительного сырья
- •3.1 Определение массовой доли влаги в плодово-ягодном сырье
- •3.2 Определение массовой доли влаги в эфирно-масличном сырье
- •Лабораторная работа №2 анализ воды
- •3.1 Определение запаха
- •3.2 Определение вкуса и привкуса
- •3.3 Определение мутности
- •3.4 Определение цветности
- •4.1 Определение реакции воды
- •4.2 Определение сухого остатка
- •4.3 Определение щелочности
- •4.4 Определение содержания органических веществ (перманганатная окисляемость)
- •4.5 Определение общей жесткости воды
- •4.6 Определение остаточного активного хлора
- •Лабораторная работа №3 анализ ингредиентов
- •1 Определение качества сахара-песка и сахара-рафинада
- •2 Определение качесва натурального меда
- •Лабораторная работа №4 анализ красителей
- •3.1 Определение растворимости колера
- •3.2 Определение относительной плотности колера
- •3.3 Расчет расхода колера с относительной плотностью 1,30-1,40 для подкраски ликероводочных изделий
- •3.4 Определение массовой доли видимых сухих веществ колера
- •3.5 Определение цвета колера
- •Лабораторная работа №5 анализ полуфабрикатов ликероводочного производства
- •2.1 Определение вкуса и аромата
- •2.2 Определение цвета и прозрачности
- •3.1 Определение объемной доли этилового спирта
- •3.2 Определение массовой доли общего экстракта
- •3.2.1 Пикнометрический метод
- •3.2.2 Рефрактометрический метод
- •3.3 Определение массовой концентрации титруемых кислот
- •Лабораторная работа №6 анализ цветных ликероводочных изделий
- •2.1 Определение наличия посторонних примесей
- •2.2 Определение прозрачности
- •2.3 Определение цвета
- •2.4 Определение запаха и аромата
- •2.5 Определение вкуса
- •3.1 Определение объемной доли этилового спирта
- •3.2 Определение массовой концентрации общего экстракта рефрактометрическим методом
- •3.3 Определение массовой концентрации титруемых кислот
- •3.4 Определение массовой концентрации сахара
- •Лабораторная работа №7 анализ водок
- •4.1 Определение объемной доли этилового спирта
- •4.2 Определение щелочности
- •Лабораторная работа №8 анализ эмульсионных ликеров
- •3.1 Определение объемной доли этилового спирта
- •3.2 Определение массовой концентрации общего экстракта
4.4 Определение содержания органических веществ (перманганатная окисляемость)
Показатель окисляемости воды характеризует содержание в ней органических веществ, способных к окислению. Окисляемость выражается в расходе перманганата калия или молекулярного кислорода в миллиграммах на 1 дм3 воды. При этом 4 мг перманганата калия примерно соответствует 1 мг кислорода.
Метод определения окисляемости воды основан на окислении веществ, присутствующих в пробе воды, раствором перманганата калия концентрацией 0,01 моль/дм3 в кислой среде при кипячении.
Без разбавления можно определять окисляемость до 10 мг 02/дм3 воды. Наивысшее допустимое разбавление проб - десятикратное, т. е. метод можно использовать только для проб, окисляемость которых ниже 100 мг 02/дм3 воды.
При определении окисляемости, дающей представление о содержании в пробе окисляемых органических веществ, необходимо устранить влияние неорганических соединений, которые могут быть окисленными при определении. К таким соединениям относятся хлориды, сульфаты, нитраты, железо (II). Когда концентрация хлоридов даже после разбавления пробы превышает 300 мг/дм3, прибавляют 0,4 г сульфата ртути (II).
Железо (II), сероводород, сульфаты и нитраты следует определять отдельно, а результат, пересчитанный на окисляемость (мг 02/дм3), необходимо вычесть из найденной величины окисляемости пробы:
- 1 мг H2S соответствует 0,47 мг 02;
- 1 мг N02 соответствует 0,35 мг 02;
- 1 мг Fе2+соответствует 0,14 мг 02.
Для разбавления проб применяют дистиллированную воду, не содержащую окисляющих веществ.
Проведение анализа
В колбу вносят 100 см3 пробы (после двухчасового отстаивания) или меньшее ее количество, доведенное до 100 см3 дистиллированной водой для разбавления, приливают 5 см3 разбавленной серной кислоты и 10 см3 раствора перманганата калия концентрации 0,01 моль/дм3.
Смесь нагревают так, чтобы она закипела через 5 мин, и кипятят точно 10 мин. К горячему раствору прибавляют 10 см3 раствора щавелевой кислоты концентрации 0,01 моль/дм3. Обесцвеченную смесь титруют горячим (лучше при 80-90 °С) раствором перманганата калия до розового окрашивания. Температура смеси при титровании не должна падать ниже 80 °С. Израсходованный объем раствора КМп04 измеряют с точностью до 0,05 см3.
Одновременно готовят контрольный опыт с водой для разбавления.
Если раствор при кипячении обесцветится или побуреет, определение повторяют с разбавленной пробой. Определение повторяют и тогда, когда раствора КМп04 расходуется более 60% добавленного в пробу количества, т. е. расход на титрование превышает 6 см3. При титровании разбавленных проб не должно быть израсходовано меньше 20% добавленного в пробу количества перманганата калия, т. е. меньше 2 см3.
Для контрольной пробы отмеривают 100 см3 воды для разбавления и обрабатывают ее так же, как и анализируемую пробу. Расход раствора перманганата калия концентрацией 0,01 моль/дм3 не должен превышать 0,2 см3.
Окисляемость (мг/дм3) вычисляют по формуле (2.3):
 =
=
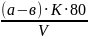 ,
(2.3)
,
(2.3)
где а - объем раствора перманганата калия, израсходованного на титрование основной пробы, см3;
в- объем раствора перманганата калия, израсходованного на титрование контрольной пробы, см3;
К - поправочный коэффициент к раствору;
8 - эквивалент кислорода;
V- объем пробы, взятой для анализа, см3.
Результаты округляют с точностью до 0,1 при значениях окисляемости от 0 до 10 мг 02/дм3 и до 1 при значениях от 10 до 100 мг 02/дм3.
