- •Методичні розробки
- •Частина 1
- •Ужгород – 2002
- •Передмова
- •Техніка експерименту в хімічній лабораторії
- •Загальні правила роботи в хімічній лабораторії
- •Предмет
- •Атомно-молекулярна теорія
- •Основні
- •Поняття
- •Прості та складні речовини
- •Хімічна символіка
- •Фізичні величини
- •Закон збереження маси
- •Закон еквівалентів
- •Закон сталості складу речовини
- •Закон кратних відношень
- •Газові закони
- •Закон Авогадро
- •Рівняння Менделєєва-Клапейрона
- •Хімічна термодинаміка
- •Термодинамічна система
- •Внутрішня енергія системи
- •Перший закон термодинаміки
- •Ентальпія системи
- •Тепловий ефект реакції
- •Закони термохімії
- •Термохімічні рівняння реакцій
- •Стандартний стан речовини
- •Термохімічні розрахунки
- •Поняття про ентропію
- •Другий закон термодинаміки
- •Хімічна кінетика
- •Поняття про швидкість хімічної реакції
- •Швидкість гомогенних реакцій
- •Швидкість гетерогенних реакцій
- •Залежність швидкості хімічної реакції від температури
- •Енергія активації хімічної реакції
- •Фотохімічні реакції
- •Ланцюгові реакції
- •З розгалуженими ланцюгами
- •Оборотні та необоротні реакції
- •Хімічна рівновага
- •Зміщення хімічної рівноваги
- •Фазові рівноваги
- •Каталіз
- •Розчини
- •Дисперсні системи
- •Розчини
- •Теорії розчинів
- •Розчинність речовин
- •Розчини
- •Розчини
- •Розчини твердих речовин
- •Способи вираження концентрації розчинів
- •Розчини неелетролітів
- •Тиск пари розчинів
- •Температура кипіння і температура замерзання розчинів
- •Розчини електролітів
- •Теорія електролітичної дисоціації
- •Ступінь електролітичної дисоціації
- •Ізотонічний коефіцієнт
- •Константа електролітичної дисоціації
- •Закон розведення
- •Властивості розчинів сильних електролітів
- •Добуток розчинності
- •Іонний добуток води
- •Водневий показник
- •Буферні розчини
- •Індикатори
- •Реакції у розчинах електролітів
- •Гідроліз солей
- •Ступінь гідролізу солі
- •Колоїдні розчини
- •Будова колоїдних часток
- •Окисно-відновні процеси електрохімічні процеси корозія
- •Ступінь окиснення елементу
- •Поняття про окисно-відновні реакції
- •Окисно-відновні властивості речовин
- •Класифікація окисно-відновних реакцій
- •Методи складання рівнянь окисно-відновних реакцій
- •У кислому середовищі:
- •У нейтральному середовищі:
- •В лужному середовищі:
- •Окисно–відновний потенціал
- •Еквівалент окисника і відновника
- •Електродний потенціал
- •Електричного шару
- •Гальванічний елемент
- •Стандартний електродний потенціал
- •Водневий електрод
- •Ряд стандартних електродних потенціалів металів
- •Електроди першого роду
- •Електроди другого роду
- •Окисно-відновні електроди
- •Іонселективні електроди
- •Електроліз
- •Закони електролізу (м.Фарадей)
- •2. Рівні кількості електрики виділяють при електролізі з різних хімічних сполук еквівалентні кількості речовин.
- •Масу речовини, що виділилася при електролізі, розраховують за формулою
- •Корозія
- •Електрохімічна корозія
- •Захист металів від корозії
- •Загальні властивості полімерів
- •Полімери як високомолекулярні речовини
- •Структура полімерів
- •Реакція полімеризації
- •Механізми полімеризації
- •Властивості полімерів
- •Каучуки
- •Структура каучуків
- •Синтетичні каучуки
- •Вулканізація каучуків
- •Реакція поліконденсації
- •Пластмаси
- •Література для самостійної роботи студентів
φ
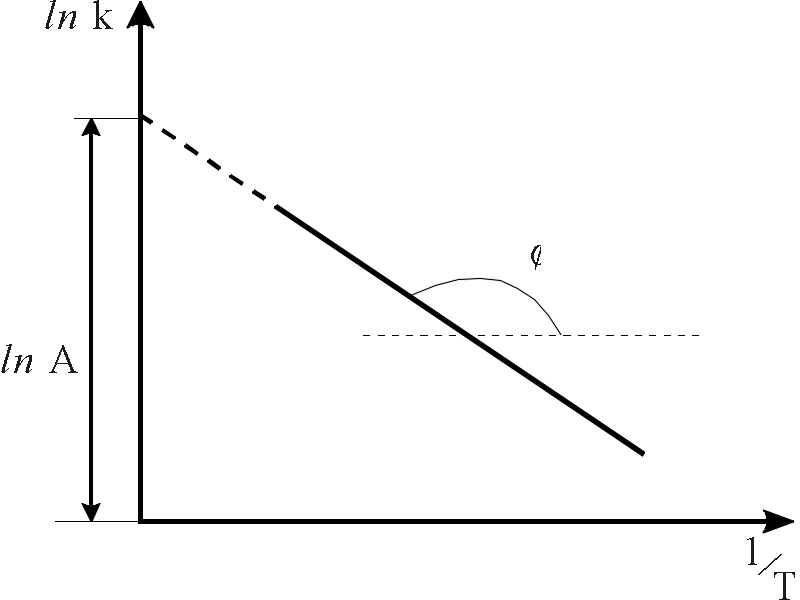
Рис.3. Графічна
залежність
lnk
= –
Еа/RT
+ lnAЗалежність швидкості хімічної реакції від температури
![]() = v
= v![]()
![]() ,
де v
і v
,
де v
і v![]() – швидкості реакції при температурах
t2
і t1,
– температурний коефіцієнт швидкості.
=
– швидкості реакції при температурах
t2
і t1,
– температурний коефіцієнт швидкості.
= ![]() ,
коли різниця температур t2–t1 = 10,
тобто коефіцієнт
показує, у скільки разів збільшиться
швидкість реакції при підвищенні
температури на 10 градусів. При концентраціях
реагуючих речовин 1 моль/л швидкість
реакції чисельно рівна константі
швидкості k,
тоді k
= k
·
.
,
коли різниця температур t2–t1 = 10,
тобто коефіцієнт
показує, у скільки разів збільшиться
швидкість реакції при підвищенні
температури на 10 градусів. При концентраціях
реагуючих речовин 1 моль/л швидкість
реакції чисельно рівна константі
швидкості k,
тоді k
= k
·
.
Функціональну
залежність константи швидкості
хімічної реакції k
від температури встановив шведський
вчений Ареніус (1889 р.); рівняння
Ареніуса:
k = А·е![]() ,
де А
– передекспоненціальний множник; Еа–
енергія активації, Т
–
температура. Графічно виразити залежність
можна так: ln k = –Еа/RT
+
lnA,
тобто
tg = –
,
де А
– передекспоненціальний множник; Еа–
енергія активації, Т
–
температура. Графічно виразити залежність
можна так: ln k = –Еа/RT
+
lnA,
тобто
tg = –![]() (рис.3).
(рис.3).
Енергія активації хімічної реакції
Хімічна
взаємодія між молекулами, що стикаються,
відбувається лише в тому випадку, коли
енергія, якою вони володіють, вище певної
енергії, характерної для даної
реакції, тобто вище її так званого
енергетичного
бар’єру.
Всі молекули, запас енергії яких нижче
енергетичного бар’єру реакції,
знаходяться в особливому стані,
який прийнято називати перехідним
або станом
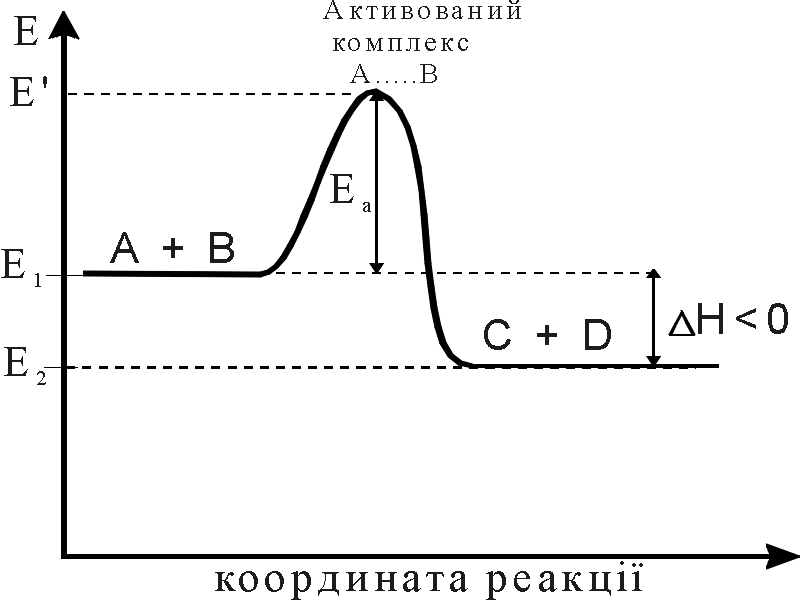
активованого комплексу.
Система, що складається з активованого
комплексу, характеризується тим, що
в ній уже немає вихідних речовин, але
ще немає і продуктів реакції. Схематично
перехід вихідних речовин А і В в продукти
реакції С і D через стан активованого
комплексу А…...В представлений на
рис.4,5.
Рис.4. Енергетична діаграма для екзотермічної реакції
|
Рис.5. Енергетична діаграма для ендотермічної реакції
|
Для того, щоб молекули вступили у взаємодію, необхідно не тільки щоб вони мали надлишок енергії, рівний Еа, але і певну взаємну орієнтацію. Вплив просторової орієнтації молекул на швидкість реакції (або на константу швидкості) можна врахувати з допомогою так званого стеричного (імовірнісного) фактора Р: А = Р·z, А – множник в рівнянні Ареніуса; z – загальне число молекул реагуючих речовин, що стикаються.
Фотохімічні реакції
Реакції,
що проходять під дією світла, називають
фотохімічними.
Молекули
реагуючих речовин поглинають енергію
випромінювання квантами h
(h
– cтала Планка;
– частота) і переходять в активний стан.
Кожен квант поглинутого світла викликає
елементарну хімічну реакцію. Закон
фотохімічної еквівалентності:
n = E/h,
де Е – кількість енергії, поглинутої
речовиною; n
– число молекул, що прореагували.
Відношення E/h
називають квантовим
виходом хімічної реакції.
Радіаційно-хімічні реакції проходять під дією іонізуючого випромінювання (-випромінювання, потік нейтронів). Ці реакції вивчає радіаційна хімія. Механохімія вивчає хімічні перетворення, що ініціюються або прискорюються механічними діями (ультразвукова обробка, надвисокі тиски, ударні хвилі твердих тіл і рідин).