
- •2. Освобождение его от нерастворимых примесей и стандартизация,
- •3. Фасовка в аэрозольные баллоны,
- •4. Герметизация,
- •5. Заполнение баллонов пропеллентом,
- •Вопрос 2. Препараты являются производными амида сульфаниловой кислоты.
- •Вопрос 4. Рецепт должен быть выписан на бланке ф.№107/у. Заверенным личной печатью и подписью врача. Проверка доз:
- •Вопрос 1. Приемку лек. Сырья производят партиями.
- •Вопрос 2. На рисунке представлена формула рутина.
- •Вопрос 3. Настойки сложные
- •Вопрос 4. Рецепт выписан правильно.
- •Вопрос 1. На рисунке представлена формула атропина сульфата. —Atropine Sulfate —атропина сульфат
- •Вопрос 2. Folia Hyoscyami (Folia Hyoscyami nigri) — листья белены (Hyoscyami folia —
- •Вопрос 4. Рецепт выписан не правильно. На рецепте должна быть печать лечебно-профилактического учреждения "Для рецептов"
- •Вопрос 2. Технология таблеток.
- •Вопрос 4. Рецепт выписан правильно. Нео для гамк не регламентированы.
- •Вопрос 1. Свойства лекарственных веществ группы пурина
- •Вопрос 2. Измельчение порошков приводит к увеличению биодоступности.
- •Вопрос 3. Radices Taraxaci — корни одуванчика
- •Вопрос 2.
- •Вопрос 2.
- •Вопрос 3.
- •Вопрос 2. Rp.: Sodium Chloride 0?9
- •Вопрос 4. Требование выписано не верно. Не указано назначение лек. Форы (для инфузий). На требовании нет круглой печати лпу. Требование выписывается в 3 экз.
- •Вопрос 4. Порядок назначения лекарственных средств
- •1.2. Лекарственные средства могут быть назначены специалистом со средним медицинским образованием (зубным врачом, фельдшером, акушеркой) в соответствии со статьей 54 Основ законодательства
- •Вопрос 3. Herba Convallariae — трава ландыша (Convallariae herba — ландыша трава)
- •Вопрос 4. Рецепт выписан не правильно. Должен быть выписан на бланке №148-1у-88, заверенным личной печатью и подписью врача, печатью лпу»Для рецептов»
- •Вопрос 3.
- •Вопрос 4. Рецепт выписан не правильно. Должен быть выписан на бланке №148-1у-88, заверенным личной печатью и подписью врача, печатью лпу»Для рецептов»
- •Вопрос 3.
- •Вопрос 2. Качество глазных капель, изготовляемых в аптеке регламентированы приказом №214, изготовляемых в промыш. Уел - правила gmp.
- •Вопрос 3. Folia Salviae (Folia Salviae qfflcinalis) — листья шалфея {Salviae folium (Salviae qfficinalis folium) — шалфея лист)
- •Вопрос 4. Рецепт выписан верно. Срок действия рецепта - 2 мес. Рецепт отдается
- •Вопрос 2. Bismuthi subnitras — висмута нитрат основной
- •Вопрос 3. Rhizomata Calami (Rhizomata Acori calami) — корневища аира, ирный
- •Вопрос 4. Рецепт выписан верно, веществ списков а. Б, пккн нет, дозы не проверяем. Нео не регламентированы.
- •Вопрос 2. Rp.: Resorcini 1,5
- •Вопрос 3. Folia Uvae ursi (Folia Arctoslaphyli uvae ursi) — листья толокнянки
- •Вопрос 4. Рецепт выписан верно. Нео не регламентированы. Лек. Форму хранят в прох. Защищ. От света месте при т не выше 25с. Оплата наличными через ккм.
- •Вопрос 2. Таблетки гмта получают прямым прессованием.
- •Вопрос 3. Radices Althaeae корни алтея (Althaeae radix — алтея корень)
- •Вопрос 4. Рецепт выписан не верно. Рецепт должен быть выписан на бланке ф.№107/у, заверенный личной печатью и подписью врача. Нео не регламентированы. Нео установлены пр.№328.
- •Вопрос 2. Получение воды для инъекций в промышленных условиях.
- •Вопрос 3. Cortex Frangulae (Cortex Frangulae aini) — кора крушины {Frangulae cortex — рутины кора)
- •Вопрос 4. Рецепт выписан не верно. Рецепт д.Б. Выписан на бланке ф. №148-1у-88, заверенный личной печатью и подписью врача, печатью лпу»Для рецептов»
- •Вопрос 2. ) —-3. Вспомогательные вещества.
- •Вопрос 3. Fructus Rosae — плоды шиповника (Rosae fructus — шиповника плод)
- •Вопрос 2. Пролонгаторы.
- •Вопрос 3.
- •Вопрос 3. Fructus Sorbi (Fructus Sorbi aucupariae) - плоды рябины (Sorbi fructus — рябины плод)
- •Вопрос 2. При изготовлении лекарственных форм из порошкового материала, помимо смешения и прессования, проводятся операции измельчения, грануляции и таблетирования.
- •2. Подготовительные мероприятия.
- •Вопрос 3. (Flores Stoechados citrinae) — цветки бессмертника песчаного {Helichrysi
- •Вопрос 2.
- •Вопрос 2. Acidum sulfocam-phoratum — кислота сульфокамфорная
- •Вопрос 2. Настойка перца стручкового (Tinetura Capsici). Настойка (1:10) на 90% спирте.
- •Вопрос 3. Fructus Capsici - плоды стручкового перца (Capsici fructus — стручкового перца плод)
- •1.2. Гидрогенизированные жиры
- •1.3. Растительные жиры (масла)
- •Вопрос 2. Требования, предъявляемые к инъекционным лекарственным формам.
- •Вопрос 4. Рецепт выписан не верно. Рецепт должен быть выписан на бланке ф. №107/у, заверенный личной печатью и подписью врача.
- •Вопрос 3.
- •Вопрос 4. Рецепт выписан верно. Дигитоксин - Список а. В условиях аптеки хранят в металлическом, запирающемся на ключ шкафу в прохладном месте.
- •Вопрос 2. Fructus Ammi majoris — плоды амми большой (Ammi majoris fructus — аммибольшой плод)
- •Глава XI. Информация о лекарственных средствах. Реклама лекарственных средств
- •Вопрос 2. Carbutamide — карбутамид (Букарбан)
- •Вопрос 3. Rhizomata et radices Inulae (Rhizomata et radices Inulae
- •Вопрос 2. Radices Glycyrrhizae (Radices Liquiritiae) — корни солодки (лакричный корень) (Glycyrrhizae radix (Liquiritiae radix) — солодки корень)
- •Вопрос 4. Рецепт выписан не верно. Рецепт должен быть выписан на бланке ф.№107/у, заверенным личной печатью и подписью врача.
- •Вопрос 4. Рецепт выписан не верно. Рецепт должен быть выписан на бланке ф.№г07/у, заверенным личной печатью и подписью врача.
- •Вопрос 3. Механизм извлечения действующих веществ.
- •Вопрос 2.
- •Вопрос 3.
- •Вопрос 4. Рецепт выписан верно.
- •Вопрос 2. Соки растений (Succi plantarum)
- •Вопрос 3.
- •Вопрос 4. Рецепт выписан верно. Нео не регламентированы, нео регламентируются Приказом мз рф №785 от 14.12.05 «о порядке отпуска лс».
- •Вопрос 2. Экстракты (от лат. Extractum — вытяжка, извлекать, вытягивать) — это :онцентрированные вытяжки из лекарственного растительного сырья, известны за несколько ъюячелетий до нашей эры.
- •Вопрос 4. Рецепт выписан верно.
- •Вопрос 3. Metamizole Sodium — метамизол-натрий (Анальгин)
- •Вопрос 2. Folia Sennae (Folia Cassiae) — листья сенны (кассии) (Sennae folium -сениы лист) Fructus Sennae — плоды сены (кассии) (Sennae fructus — сены плод)
- •Вопрос 3.
- •Вопрос 2.
- •Вопрос 3. Машины для измельчения твердых тел
- •1. Конвективные (воздушные)
- •Вопрос 2. Fructus Hippophaes rhamnoidis recentes — плоды облепихи крушиновидной свежие
- •Вопрос 3. Масляные экстракты. Масляные экстракты (медицинские масла) — это извлечения из лекарственного растительного сырья, приготовленные с использованием растительных или минеральных масел.
- •Вопрос 2.
Вопрос 3.
В ряде случаев препараты индивидуальных веществ имеют значительные преимущества перед синтетическими средствами. Природные биологически активные соединения менее токсичны и реже вызывают нежелательные побочные явления, особенно аллергические реакции по сравнению с их синтетическими аналогами. Применяя препараты индивидуальных веществ, можно точно определить дозу, регулировать всасываемость и, следовательно, оказывать влияние на их терапевтическую эффективность.
КЛАССИФИКАЦИЯ
Индивидуальные вещества в зависимости от их химической структуры и характера биологического действия на организм делят на гликозиды циклопентапергидрофенантрена (сердечные гликозиды), алкалоиды и другие соединения.
ТЕХНОЛОГИЯ ПРЕПАРАТОВ ИНДИВИДУАЛЬНЫХ ВЕЩЕСТВ
Процесс получения препаратов индивидуальных веществ многостадийный и может быть представлен следующей схемой: подготовка сырья и экстрагента, экстрагирование лекарственного сырья, очистка полученного извлечения, выделение суммы индивидуальных веществ (или вещества), стандартизация.
При получении извлечения большое внимание уделяется выбору экстрагента, как и в технологии других экстракционных препаратов. Его подбирают в зависимости от физико-химических свойств выделяемых индивидуальных веществ. Для экстрагирования лабильных сердечных гликозидов используют 90—95 % этанол, метанол (при получении целанида), которые обладают селективной способность в отношении этих биологически активныхсоединений, и в тоже время инактивируют ферменты, содержащиеся наряду с сердечными гликозидами в растительном материале и тем самым исключают гидролитическое расщепление гликозидов; ацетон; смесь метилена хлористого и этанола (в технологии дигитоксина); другие растворители. С целью сохранения нативности биологически активных веществ экстракция комплекса сердечных гликозидов, чувствительных к повышенной температуре, проводится на холоду, при строго регламентированном значении рН среды.
Для экстрагирования алкалоидов применяют различные растворители, строго соблюдая определенный режим экстрагирования, обращая особое внимание на значение рН среды, так как от этого зависит степень экстракции алкалоидов. Положение, согласно которому алкалоиды экстрагируются органическим растворителем только из щелочной среды, справедливо лишь для отдельных представителей этого класса соединений. Большинство алкалоидов экстрагируется из растворов как кислой, так и щелочной среды, но для каждого имеется определенная, довольно узкая область значений рН, при которых он извлекается в максимальных количествах. В качестве органических растворителей используют хлороформ, дихлорэтан, бензол, спирт изоамиловый, спирт изопропиловый, предпочитая последний, как менее ядовитый и дешевый. Для экстрагирования флавоноидов чаще применяют этанол, для кумаринов — метанол.
Экстрагирование проводят дробной мацерацией по принципу противотока, мацерацией с циркуляцией экстрагента.
Ускоренная дробная мацерация по принципу противотока (по ЦАНИИ) Противоточное экстрагирование в модификации ЦАНИИ дает возможность значительно сократить время на выпуск готовой продукции.
Растительный материал в сухом виде загружают поровну в три экстрактора. Экстрагент подают в первый экстрактор «до зеркала» и настаивают в течение 2 ч. Полученную вытяжку переносят на сырье во второй экстрактор, одновременно в первый снова заливают чистый экстрагент «до зеркала». Сырье в обоих экстракторах настаивают 2 ч, после этого вытяжку из второго экстрактора переносят на сырье в третий, а из первого — на сырье во второй экстрактор. В первый экстрактор заливают весь оставшийся экстрагент. Загруженные экстракторы оставляют для настаивания сырья на 24 ч. Затем из третьего экстрактора получают первый слив готового продукта. Вытяжку из второго экстрактора переносят на сырье в третий, сливом из первого — заливают сырье во втором экстракторе. Оба экстрактора оставляют на 2 ч для настаивания сырья. В это время первый экстрактор отключают, сырье выгружают и отжимают. Через 2 ч из третьего экстрактора получают второй слив готового продукта. Вытяжкой из второго экстрактора заливают сырье в третьем, второй экстрактор разгружают, сырье отжимают. После двухчасового настаивания из третьего экстрактора получают третью порцию готового продукта, сырье выгружают и отжимают. Все сливы и отжимы объединяют.
Циркуляционное экстрагирование
Сущность метода заключается в многократном экстрагировании растительного сырья одной и той же порцией летучего экстрагента (эфир, хлороформ, метилен хлористый и т. д.).Экстрагирование осуществляется в замкнутом цикле в аппарате типа «Сокслет» (рис. 5) Лучшие условия экстрагирования сырья создаются в нижней части экстрактора (4), так как оно находится там в контакте с экстрагентом более длительное время, чем в верхней. В связи с этим конструируются экстракторы, снабженные специальными приспособлениями для перемещения сырья внутри аппарата.
Рис. 5. Устройство циркуляционного аппарата Сокслета. 1 — куб; 2 —
конденсатор; 3 — сборник; 4 экстрактор.
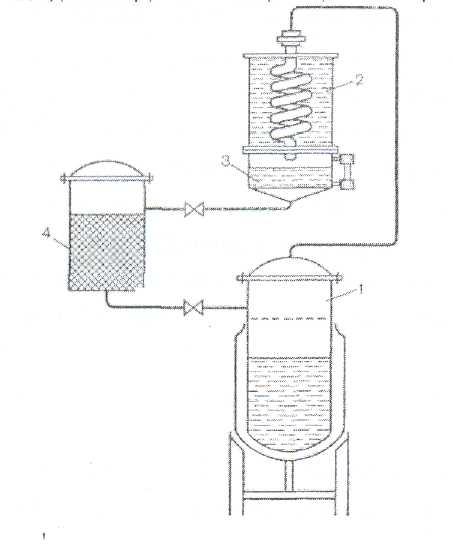
Основными узлами установки для проведения циркуляционного экстрагирования являются: испаритель (1), снабженный паровой рубашкой, экстрактор (4), конденсатор (2) и сборник (3). Все узлы коммунифицированы между собой.
Во избежание засорения трубопровода растительный материал загружают в полотняном мешке, заливают экстрагентом и оставляют для настаивания на несколько часов. После этого вытяжку переводят в испаритель (1) и доводят до кипения. Образующиеся пары поступают в конденсатор и в виде дистиллята возвращаются на сырье в экстрактор. Циркуляция экстрагента повторяется 10—15 раз до истощения растительного материала. Полученную вытяжку концентрируют отгонкой экстрагента в приемник. В испарителе остается концентрированный раствор экстрактивных веществ.
Иногда перед экстрагированием сырье специально обрабатывают (ферментация при производстве дигитоксина).
Из полученного извлечения экстрагент удаляют упариванием (отгонкой) в роторных испарителях, в которых вытяжка подвергается кратковременному контакту с поверхностью теплоносителя при сравнительно большой площади испарения и глубоком вакууме (остаточное давление 1333,22—1999,83 Н/м2). Для уменьшения потерь органического растворителя на всех стадиях упаривания охлаждение паров осуществляют рассолом.
Очистка вытяжек проводится щадящими методами. На первых стадиях очисткиизвлечения применяют фракционное избирательное осаждение действующих или сопутствующих веществ (часто путем смены растворителей), жидкостную очистку — экстракцию жидкость — жидкостью (в перфораторах), абсорбционную хроматографию (для очистки и разделения сердечных гликозидов), ионообменную хроматографию на смолах КАУ-1, КАУ-2 (для очистки водных вытяжек, содержащих алкалоиды)
Очищенные вытяжки, (элюаты) упаривают под вакуумом и получают, как правило, суммарный препарат, представляющий собой смесь нескольких индивидуальных веществ.
Для разделения суммы индивидуальных веществ проводят многократную перекристаллизацию до выделения из суммы одного вещества.
Стандартизуют готовый продукт по содержанию действующих веществ или активности в ЕД.
Дигитоксин (Digitoxinum) получают при ферментации листьев, экстрагировании из них действующих веществ, очистке вытяжки, выделении суммы гликозидов, получении дигитоксина, стандартизации.
Предварительная ферментация листьев увеличивает выход дигитоксина в 4 раза. С- этой целью измельченные листья наперстянки замачивают водой (37— 40 °С) и оставляют при этой температуре на 40—48 ч Листья после ферментации помещают в реактор с мешалкой и трижды экстрагируют смесью метилена хлористого и этанола. Полученную вытяжку упаривают под вакуумом при температуре 50 °С. Концентрированный экстракт обрабатывают формамидом и проводят очистку (жидкостную экстракцию), обрабатывая вытяжку бензолом 5 раз, смесью бензола и хлороформа (3:2) до 10 раз. Вытяжку упаривают под вакуумом, остаток растворяют в хлороформе. Хлороформный раствор сердечных гликозидов переносят на колонку с алюминия оксидом для их распределения: в верхнем участке — гитоксин, в нижнем—дигитоксин.
Дигитоксин элюируют с алюминия оксида метанолом под контролем Уф-лампы. Дигитоксин имеет голубое свечение, гитоксин — коричневое. Элюат, содержащий дигитоксин, упаривают под вакуумом досуха. Остаток растворяют в ацетоне, упаривают под вакуумом, добавляют бензол и оставляют для кристаллизации дигитоксина. Перекристаллизацию повторяют несколько раз при комнатной температуре. Кристаллы промывают этанолом и высушивают на воздухе.
В условиях аптеки можно приготовить из листьев наперстянкт настой в соотношении 1:400.
Биотрансформация дигитоксина в дигоксин происходит в результате реакции 12-гидроксилирования, катализируемой ферментом клеток Digitalis lanata.
