
Шевченко Ю.Л. - Актуальные вопросы грудной хирургии
.pdf
32 *
позволяла выполнять несколько сочетанных операций. Следует привести публикацию В.Д. Федорова, благополучно выполнившего 7 вмешательств из одного лапаротомного доступа [3].
3.1. Продолжительность оперативного вмешательства и общего обезболивания. Существует прямая зависимость между продолжительностью общей анестезии, а вместе с ней и продолжительностью вмешательства и частотой возникновения послеоперационных осложнений. Доказано, что у лиц, перенесших операцию под наркозом продолжительностью менее 2 ч, число возникших послеоперационных осложнений гораздо меньше, чем у пациентов, оперированных в течение 120 мин и более. Следует указать и на другую интересную особенность, связанную с прямым влиянием продолжительности общего обезболивания на число послеоперационных осложнений. Доказано, что число респираторных осложнений одинаково после операций продолжительностью как 2 ч, так и 5 ч, а степень выраженности гипоксии не зависит от сроков нахождения больного под наркозом. В связи с этим хирургами и анестезиологами выделен такой значимый фактор операционного риска легочных и других послеоперационных осложнений, как «пребывание пациента под наркозом 2 ч и более».
Что касается времени операции, то мы исходим из опыта ФХК, свидетельствующего о том, что лобэктомия длится менее 2 ч, а расширенная пневмонэктомия – более 2 ч.
Нам представилось возможным изучить характер течения наркозного периода в зависимости от продолжительности операции. С этой целью мы проанализировали наркозные карты у больных разных возрастных групп в зависимости от продолжительности общего обезболивания (см. табл. 3).
Осложнения (экстрасистолия, артериальная гипертензия и гипотензия) во время общего обезболивания отмечаются в два раза чаще при более продолжительной операции. Как представляется, отмечаемое у больных старшей возрастной группы достоверное увеличение осложнений в течение наркозного периода следует объяснить наличием у этих пациентов большего числа конкурирующих заболеваний.
Характер (продолжительность оперативного вмешательства), а также наличие конкурирующих заболеваний определяют послеоперационный прогноз у больных раком легкого. Вид операций, характер конкурирующих заболеваний и осложнений представлены в табл. 4–6.
Таким образом, наличие у больных обширного рака легкого в сочетании с рядом конкурирующих заболеваний – распространен-

* 33
ный атеросклероз (например, поражение коронарных и/или сонных артерий и сосудов ног) с ДН 2–3-й степеней позволяют обоснованно отказаться от оперативного лечения этих пациентов в связи с тем, что летальность у этой тяжелой категории больных может дости-
Таблица 4. Характер конкурирующих заболеваний у оперированных больных разных возрастных групп
|
|
|
|
|
|
|
|
|
|
|
|
|
Сочетание |
|
|
|
Группы |
|
|
|
|
||
|
конкурирующих заболеваний |
|
|
|
|
|
|
|
|
|
|
|
1-я |
|
|
|
2-я |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
абс. |
|
|
% |
|
абс. |
|
|
% |
|
|
|
|
|
|
|
|
|
|
|
||
|
ИБС II,III ФК+НРиФПС |
3 |
|
|
2,8 |
|
2 |
|
|
3,1 |
|
|
|
|
|
|
|
|
|
|
|
||
|
ИБС I,II ФК +НРиФПС+ДН 1–3 ст. |
27 |
|
|
25,5 |
|
19 |
|
|
29,2 |
|
|
|
|
|
|
|
|
|
|
|||
|
ИБС I,II ФК +коронаросклероз+ДН 1,2 ст. |
66 |
|
|
62,3 |
|
41 |
|
|
63,1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ИБС I–III ФК+ДН 1 ст.+атеросклероз |
3 |
|
|
2,8 |
|
2 |
|
|
3,1 |
|
|
брахиоцефальных артерий |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
ИБС I,II ФК +ДН 1–3 ст.+ОААНК |
3 |
|
|
2,8 |
|
1 |
|
|
1,5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ДН 3 ст.+ИБС IIФК |
4 |
|
|
3,8 |
|
– |
|
|
– |
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 5. Послеоперационная летальность у больных раком легкого в зависимости от характера конкурирующих заболеваний и травматичности вмешательства
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Сочетание кон- |
|
Лоб/ билобэк- |
|
Пневмонэкто- |
|
Всего |
|
Число |
|
||||||
|
курирующих |
|
томия |
|
|
|
мии |
|
опериро- |
|
умерших |
|
||||
|
заболеваний |
|
|
|
|
|
|
|
|
|
|
|
ванных |
|
|
|
|
|
абс. |
|
|
% |
|
абс. |
|
|
%. |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ИБС I–II ФК + |
|
3 |
|
|
6,5 |
|
3 |
|
|
6,5 |
|
46 |
|
13 |
|
|
НРиФПС + ДН |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2–3 ст. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
ИБС I,II ФК + |
|
4 |
|
|
3,7 |
|
10 |
|
|
9,3 |
|
107 |
|
13 |
|
|
коронароскле- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
роз + |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ ДН 1,2 ст. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
ИБС II–III ФК + |
|
1 |
|
|
20 |
|
2 |
|
|
40 |
|
5 |
|
60 |
|
|
ДН 2 ст. + ате- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
росклероз бра- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
хио-цефальных |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
артерий |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
ИБС II ФК + ДН |
|
2 |
|
|
50 |
|
– |
|
|
– |
|
4 |
|
50 |
|
|
3 ст. +ОААНК |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

34 *
Таблица 6. Характер фатальных осложнений в зависимости от объема оперативного вмешательства у больных разных возрастных групп
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ГРУППЫ |
|
|
|
||
|
ОСЛОЖНЕНИЕ |
|
|
|
|
|
|
|
|
|
|
|
|
1-я |
|
2-я |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
лобэктомия |
|
пневмонэк- |
|
лобэктомия |
|
пневмонэк- |
|
|
|
|
|
|
томия |
|
|
|
томия |
|
|
|
|
|
|
|
|
|
|
||
|
Летальный исход |
|
4,6% |
|
8,3% |
|
2,8% |
|
5,6% |
|
|
|
|
(5 больных) |
|
(9 больных) |
|
(3 больных) |
|
(6 больных) |
|
|
|
|
|
|
|
|
|
|
|
|
|
Острое нарушение |
|
– |
|
3 |
|
2 |
|
– |
|
|
сердечного ритма |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
ИМ |
|
1 |
|
4 |
|
– |
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
ТЭЛА |
|
2 |
|
3 |
|
– |
|
– |
|
|
|
|
|
|
|
|
|
|||
|
Пневмония |
|
2 |
|
4 |
|
3 |
|
3 |
|
|
|
|
|
|
|
|
|
|
||
|
Несостоятельность |
|
1 |
|
4 |
|
– |
|
4 |
|
|
швов культи бронха |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
гать 60%. Подчеркнем, что вопрос о возможности операций у этих пациентов может быть рассмотрен лишь после выполненных в качестве первого этапа лечения реваскуляризации миокарда или мозга. Отметим, что следующее сочетание конкурирующих заболеваний у больных раком легкого: ИБС I–II ФК (ИМ в анамнезе) + ДН 1–3-й ст. – позволяет предполагать послеоперационную летальность у оперированных около 15%. Целесообразным при принятии решения о возможности вмешательства у пациентов, имеющих значительное количество конкурирующих заболеваний, следует считать выбор менее радикальной операции (лобэктомии, например), что ведет соответственно к более низким показателям летальности. При планировании травматичной (пневмонэктомия) операции у больных, имеющих четыре и более конкурирующих заболевания, следует предполагать послеоперационную летальность не менее 20%. Паспортный возраст не является значимым фактором послеоперационного прогноза.
Литература
1. Борисов И.А. Факторы риска хирургического лечения ИБС и их влияние на ближайшие и отдаленные результаты // Автореф. дисс… д-ра мед. наук. М., 1994.

* 35
2.Кузнецов Н.А., Голубева-Монаткина Н.И. Операционный риск: некоторые проблемы и методы анализа. // Хирургия. 1990; 8: 106– 109.
3.Федоров В.Д., Будаев К.Д., Назаренко Н.А. и др. Одномоментная резекция 7 органов при раке восходящей ободочной кишки. // Хирургия. 1998; 11: 55–58.
4.Шевченко Ю.Л., Шихвердиев Н.Н., Оточкин А.В. Прогнозирование в кардиохирургии. М.: Питер, 1998, 36–38.
МЕДИКАМЕНТОЗНОЕ ЛЕЧЕНИЕ БОЛЬНЫХ ГИПЕРТРОФИЧЕСКОЙ КАРДИОМИОПАТИЕЙ
Н.В. Аверкина
В настоящее время ишемия миокарда считается одним из факторов риска развития внезапной смерти больных гипертрофической кардиомиопатией (ГКМП) [1]. Наиболее информативным неинвазивным методом диагностики недостаточности кровоснабжения миокарда является перфузионная сцинтиграфия, проводимая в сочетании с нагрузочными тестами. Во многих исследованиях было доказано наличие ишемии миокарда у больных ГКМП, а также необходимость уменьшения нарушений перфузии миокарда с помощью медикаментозной терапии у данной категории больных [2].
β-Блокаторы и антагонисты кальция являются препаратами первого ряда в медикаментозной терапии больных ГКМП. В ранее проведенных исследованиях было выявлено положительное влияние этих препаратов на клиническое состояние и «качество жизни» пациентов с ГКМП, однако в отношении гемодинамических показателей и перфузии миокарда имеются неоднозначные результаты [3]. В связи с этим данная проблема представляет особый интерес и требует дальнейшего изучения.
Цель исследования: изучить влияние длительной терапии атенололом, изоптином и соталолом на клинико-гемодинамические показатели и перфузию миокарда у больных ГКМП.
Материал и методы
В исследование включали пациентов с диагнозом ГКМП (ВОЗ, 1995 г.). Не включали больных ГКМП с IV ФК хронической сердечной недостаточности (NYHA), нарушением атриовентрикулярной про-

36 *
водимости сердца, брадикардией (ЧСС<50 уд/мин), артериальной гипотонией (АД<90/60 мм рт. ст.), обструктивными заболеваниями легких. Обследованы 62 пациента: 22 женщины и 40 мужчин (средний возраст – 44,7±12,0 лет, длительность заболевания – 13,1±10,2 лет).
Больным во время стационарного наблюдения проведены опрос, физикальное обследование, оценка «качества жизни», ЭКГ в 12 отведениях, суточное мониторирование ЭКГ, ЭхоКГ, однофотонная эмиссионная компьютерная томография (ОЭКТ) миокарда с 99mТс–МИБИ покое и в сочетании с велоэргометрией (ВЭМ).
Эхокардиографическое исследование проводили на аппаратах «Sonos 2000» (Hewlett Packard, США). Измеряли следующие параметры: размеры ЛП, ПЖ, КДР ЛЖ и КСР ЛЖ, ТМЖП и ТЗСЛЖ. Признаком асимметричной гипертрофии миокарда считали соотношение ТМЖП/ТЗСЛЖ >1,3, КДО и КСО ЛЖ рассчитывали по формуле Teichholz и Gorlin (1972 г.): КДО (мл) = [7/(2,4+КДР)] × КДР3; КСО (мл) = [7/(2,4+КСР)] × КСР3. Фракцию выброса (ФВ) ЛЖ вычисляли по формуле: ФВ (%) = [(КДО-КСО)/КДО]×100%. Массу миокарда (ММЛЖ) определяли по формуле Troy (1970 г.) в модификации Ю.Н. Беленкова (1975 г.):
ММЛЖ(г)=1,05×[(7/(2,4+КДР+ ТМЖП+ТЗСЛЖ))× (КДР+ТМЖП+ТЗСЛЖ)3-КДО],
где 1,05 – относительная плотность миокарда. Величину градиента давления в выходном тракте ЛЖ и степень митральной регургитации определяли методом допплерЭхоКГ.
При проведении ВЭМ использовали комплекс «Astrocard Polysystem-4FS» (Россия). Нагрузку начинали с 20 Вт и непрерыв- но-ступенчато увеличивали каждые 2 минуты на 20 Вт при скорости выкручивания педалей 60 оборотов в минуту.
ОЭКТ с 99mТс–МИБИ проводили дважды: в покое и после нагрузочной пробы по стандартному протоколу. Использовали цифровую ротационную гаммакамеру «Sophy camera DSX» («Sopha Medical», Франция). Преходящие дефекты перфузии (ДП) отсутствовали на томосцинтиграммах (ТСЦ) покоя и появлялись на постнагрузочных ТСЦ, стабильные ДП отмечались на ТСЦ, зарегистрированных в покое и после ВЭМ. Преходящие ДП считали характерными для ишемии миокарда, стабильные ДП – для стойкого повреждения миокарда. Обработку данных проводили на компьютере «Sophy» («Sopha Medical», Франция) по визуальным и количественным показателям. Для визуальной оценки использовали срезы миокарда ЛЖ в трех плоскостях. Одним из методов количественного анализа было пост-
* 37
роение карты полярных координат («бычий глаз»). Локализацию участков включения радиофармпрепарата (РФП) определяли соответственно 5 областям: перегородочная, передняя, боковая, нижне-зад- няя, верхушечная. Степень нарушений перфузии оценивали по 5-балльной шкале, где 0 – нормальное распределение РФП, 1 – слабое, 2 – умеренное, 3 – выраженное, 4 – глубокое снижение концентрации или практически отсутствующее включение РФП. Стабильные ДП классифицировали как умеренные (< 3 баллов) и выраженные (> 3 баллов).
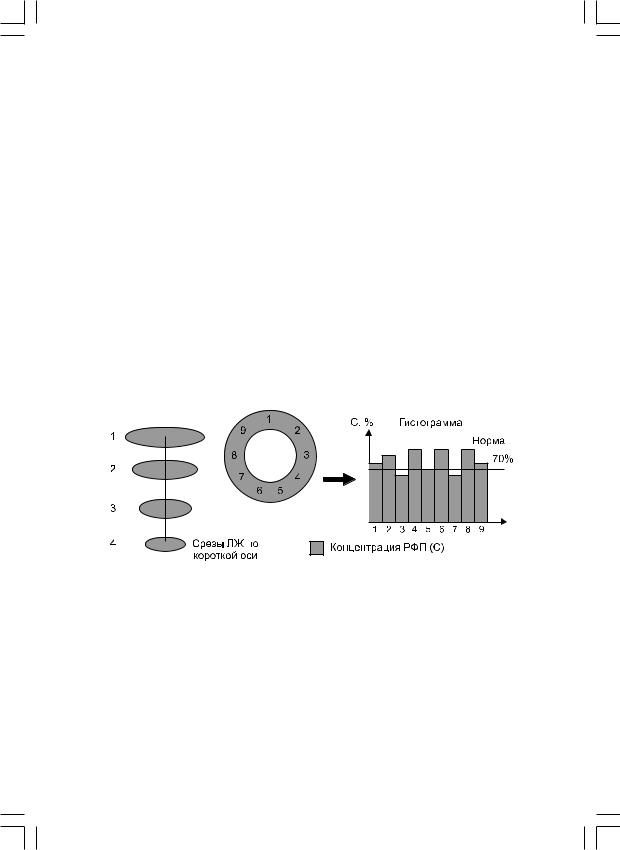
Другим методом количественного анализа была обработка данных с помощью программы CO CSMS FRANKFURT с построением гистограмм распределения РФП в 4 срезах ЛЖ по короткой оси, разделенных на 9 сегментов. Достоверным считали снижение накопления РФП более 15% в средних и базальных срезах, более 20% в верхушечных срезах ЛЖ относительно максимума, не выходящего за пределы условной границы нормального распределения (70%) (рис. 1).
Рис. 1. Программа количественной обработки данных (FRANKFURT).
Рассчитывали индексы гипоперфузии, ишемии и стабильного повреждения, отражающие одновременно площадь и глубину нарушений перфузии миокарда.
Для оценки «качества жизни» (КЖ) больных использовали опросник Миннесотского Университета (MLHFQ, Rector T., 1989) для больных ХСН.
Статистическую обработку данных проводили с помощью программы «STATISTICA 5.0». Использовали непараметрические методы.

38 *
Этапы проведения исследования
На первом этапе обследованы 62 пациента до назначения терапии. После обследования больным была назначена терапия одним из препаратов: атенолол, изоптин, соталол. Атенолол и изоптин назначали методом случайной выборки, а соталол – строго по показаниям (желудочковые нарушения ритма): 24 больных получали атенолол, 24 больных – изоптин, 14 больных – соталол.
На втором этапе проведено повторное обследование 40 больных через год медикаментозной терапии: 17 больных получали атенолол, 12 больных – изоптин, 11 больных – соталол.
Результаты и обсуждение
Оценка клинического состояния и «качества жизни» больных ГКМП на фоне медикаментозной терапии.
Группы больных, обследованных на фоне длительной терапии атенололом, изоптином и соталолом, были сопоставимы по возрасту, полу и длительности заболевания (табл. 1). На фоне лечения атенололом, изоптином и соталолом выявлено улучшение клинического состояния у большинства больных ГКМП (76,4%, 75% и 81,8% больных соответственно) в виде уменьшения основных симптомов заболевания и ФК ХСН, у остальных – стабильное состояние. Терапия атенололом, изоптином и соталолом привела к достоверному
Таблица 1. Характеристика больных, обследованных на фоне терапии (n=40).
|
|
|
|
|
|
|
|
|
|
Препарат |
|
Атенолол |
|
Изоптин |
|
Соталол |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Суточная доза, мг |
|
67,6±28,9 |
|
310±95,1 |
|
189,1±53,9 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Количество больных |
|
17 |
|
12 |
|
11 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
Пол, (мужчины/женщины) |
|
10:7 |
|
9:3 |
|
4:7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Возраст, лет |
|
44,2±11,9 |
|
44,3±13,1 |
|
39,1±12,6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
Длительность заболевания, лет |
|
13,9±8,3 |
|
10,8±8,3 |
|
11,8±9,8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

* 39
уменьшению систолического АД (на 4,4%, 5,5% и 16,2%, соответственно), диастолического АД (на 7,5%, 9,6% и 15,7%, соответственно) и ЧСС (на 14,6%, 13,1% и 27,8%, соответственно). Указанные препараты повышали КЖ больных ГКМП, что сопровождалось достоверным уменьшением среднего балла КЖ (на 25,4%, 34% и 33,9%, соответственно).
При межгрупповом сравнении влияния препаратов на клинические симптомы и КЖ у больных ГКМП достоверных отличий не выявлено. Терапия соталолом приводила к достоверно большему снижению уровня АД и ЧСС по сравнению с изоптином и атенололом. Следует отметить, что длительное лечение изучаемыми препаратами было безопасным (не отмечено снижения ЧСС ниже 55 уд/мин., систолического АД ниже 90 мм рт. ст., диастолического АД ниже 60 мм рт. ст., отрицательной динамики ЭКГ, развития побочных эффектов) и отличалось хорошей переносимостью. Полученные в настоящей работе результаты согласуются с данными ранее проведенных исследований [5].
Влияние медикаментозной терапии на показатели толерантности к физическим нагрузкам у больных ГКМП.
На фоне лечения атенололом, изоптином и соталолом выявлено достоверное увеличение мощности (на 38,8%, 28,5% и 39,2%, соответственно) и времени (на 48,9%, 27,4% и 31,7%, соответственно) выполненной работы у больных ГКМП. Межгрупповой анализ показал, что изучаемые препараты в равной степени увеличивали толерантность к физическим нагрузкам у больных ГКМП. При анализе ЧСС, зарегистрированной на высоте ВЭМ, у обследованных больных выявлено, что препараты достоверно снижали этот показатель, при этом соталол – в достоверно большей степени, чем изоптин. Отличий в действии изучаемых препаратов на показатели АД во время нагрузочной пробы не получено. Изучаемые препараты, сдерживая прирост ЧСС во время нагрузок за счет отрицательного хронотропного действия, снижают потребность миокарда в кислороде, а также удлиняют время диастолического наполнения ЛЖ, улучшают микроциркуляцию в миокарде у больных ГКМП.
Динамика эхокардиографических показателей у больных ГКМП на фоне медикаментозной терапии.
У обследованных пациентов с ГКМП лечение атенололом, изоптином и соталолом не оказывало существенного влияния на основные эхокардиографические параметры, не приводило к ухудшению сократительной функции ЛЖ, отмечена лишь тенденция к снижению градиента давления в выходном тракте ЛЖ (на 14%, 27,7% и 4,5% соответственно) и степени митральной регургитации (на 16%,
40 *
22,8% и 18% соответственно). Данные настоящей работы согласуются с результатами большинства современных исследований [4].
Влияние медикаментозной терапии на перфузию миокарда у больных ГКМП.
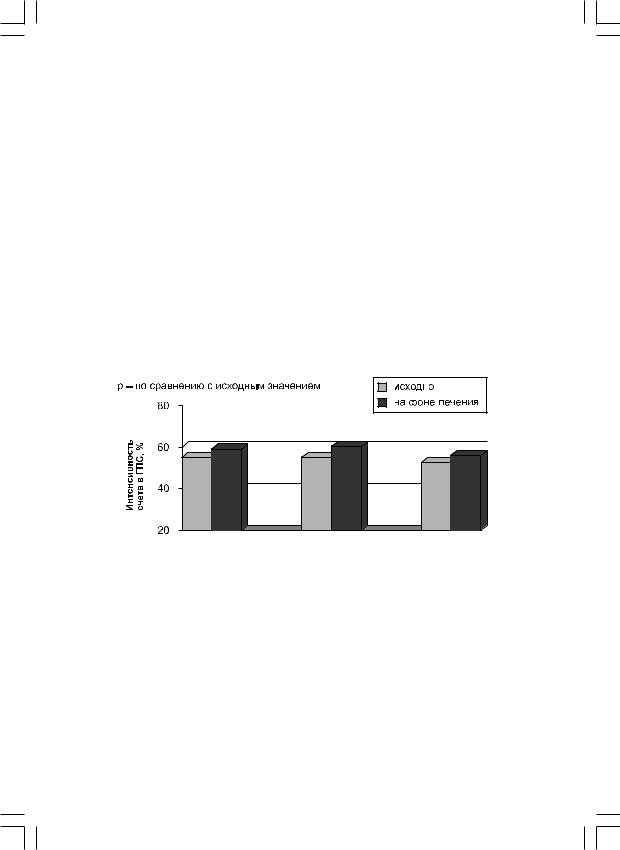
При визуальном анализе данных ОЭКТ миокарда с 99mТс-МИБИ на фоне лечения атенололом, изоптином и соталолом выявлено улучшение перфузии миокарда у большинства обследованных больных ГКМП (88,2%, 91,7% и 81,8% соответственно), у остальных пациентов наблюдались стабильные показатели. Улучшение происходило за счет уменьшения площади и/или глубины или исчезновения преходящих ДП и стабильных ДП умеренной степени. Терапия не влияла на стабильные ДП выраженной степени. Отмечено достоверное уменьшение индексов ишемии и стабильного повреждения. Обнаружено достоверное увеличение интенсивности счета включения РФП в сегменты миокарда со сниженной перфузией на фоне проводимого лечения (рис. 2).
Рис. 2. Интенсивность счета включения РФП в миокард левого желудочка у больных ГКМП на фоне терапии.
Анализ динамики стабильных ДП показал, что на фоне лечения атенололом, изоптином и соталолом происходит достоверное уменьшение площади и глубины только стабильных ДП умеренной степени (<3 баллов). Важно, что достоверных отличий в действии изучаемых препаратов на перфузию миокарда у обследованных больных ГКМП не выявлено.
Улучшение перфузии миокарда у больных ГКМП на фоне медикаментозного лечения можно объяснить улучшением микроциркуляции в гипертрофированном миокарде, увеличением коронарного

* 41
резерва за счет вазодилатирующего действия (в том числе воздействие на измененные мелкие интрамуральные артерии и артериолы), снижением потребности миокарда в кислороде, влиянием на диастолическую функцию ЛЖ [5].
Влияние соталола на перфузию миокарда у больных ГКМП в настоящей работе оценено впервые.
Выводы
1.Длительная терапия атенололом, изоптином и соталолом в равной степени приводит к уменьшению клинических симптомов, достоверному улучшению «качества жизни» и повышению толерантности к физическим нагрузкам у большинства больных ГКМП.
2.Длительная терапия атенололом, изоптином и соталолом не оказывает существенного влияния на размеры левого желудочка и левого предсердия, степень гипертрофии миокарда левого желудочка, величину градиента давления в выходном тракте левого желудочка, выраженность митральной регургитации и не приводит к ухудшению систолической функции левого желудочка у больных ГКМП.
3.На фоне длительной терапии атенололом, изоптином и соталолом выявлено достоверное уменьшение площади и глубины нарушений перфузии миокарда левого желудочка у большинства больных ГКМП, при этом действие изучаемых препаратов на перфузию миокарда сопоставимо.
Литература
1.Мухарлямов Н. М. Кардиомиопатии. // М, Медицина, 1990,
288 с.
2.Haley J.H., Miller T.D. Myocardial ishemia on thallium scintigraphy in hypertrophic cardiomyopathy: predictor of sudden cardiac death.// Circulation 2001; 104(13):E71-1.
3.Goodwin J., Olsen E. Cardiomyopathies:realisations and expectations.
//Springer-Verlag, 1993.
4.Maron B. J., Roberts R. Hypertrophic cardiomyopathy. Lancet. 1997; 350(9071):127-33.
5.Dimitrov P.P., Krzanowski M., Nizanowski R., et al. Comparison of the effect of verapamil and propranolol of coronary vasomotion to cold pressor test in symptomatic patients hypertrophic cardiomyopathy.
//Cardiovasc. Drugs Ther. 2000; 14(6):643-50.
