
3 курс / Общая хирургия и оперативная хирургия / Хирургия_пищеварительного_тракта_Шалимов_А_А_,_Саенко_В_Ф_
.pdf
Рис. 26. Варианты тонкокишечной эзофагопластики:
I — по Ру; 2 — по Герцену; 3 — по Юдину
середины шеи и в него проводят мобилизо ванную кишку. Во второй этап выделяют и пересекают мобилизованную кишку. Дистальный конец образованного транспланта та вшивают в желудок. В третий этап раз резом на шее выделяют и пересекают пище вод, аборальный конец которого зашивают наглухо и погружают, а оральный сшивают с подведенной кишкой.
Применив способ Ру—Герцена, многие хирурги не получили обнадеживающих ре зультатов. Кишку или невозможно было довести до нужного уровня, или наступало частичное или полное нарушение ее крово снабжения. Трудность мобилизации доста точно длинных отрезков тонкой кишки и частый их некроз побуждали разработать другие, более безопасные методы пластики пищевода. Так, в 1911 г. Lexer предложил комбинированный способ пластики пищево да, объединив способы Ру и Вулльштейна (рис. 27). Операцию Lexer начал в 1908 г. и закончил в 1910 г. При этом способе меньше риск омертвения кишки, реже случаи медиастинита от погружения аборального конца пищевода в средостение, исключается обра зование ретенционной кисты средостения.
Недостатками операции являются ее дли тельность и многоэтапность. Как правило, образуются свищи, которые требуют повтор ных, подчас многочисленных оперативных вмешательств.
^Большие успехи в тонкокишечной эзофагопластике были достигнуты С. С. Юди
ным, который за 20 лет (1928—1948) выпол нил 318 операций; летальность состави ла 9 %. К 1950 г. операция Ру—Герце на—Юдина стала наиболее распростра ненной.
Методика операции Юдина заключается в следующем.
1. Накладывают предварительную гастростому из левого параректального разреза для выведения больного из тяжелого состояния.
2. Мобилизуют петли тощей кишки, от ступя 8—10 см от позадиподжелудочной фасции путем дугообразного разреза бры жейки на 1,5—2 см ниже сосудистой аркады. Кишечные сосуды выделяют и перевязыва ют изолированно, кишку пересекают (рис. 28). Проксимальный конец кишки вши вают в бок трансплантата. Специальным ко пьевидным расширителем образуют тоннель под кожей груди до угла нижней челюсти, в который проводят мобилизованную петлю тощей кишки, располагающуюся в боль шинстве случаев впереди поперечной обо дочной кишки.
3. Через 6—15 дней после первого этапа операции накладывают анастомоз между мобилизованной кишкой и пищеводом (рис. 29). В тех случаях, когда невозможно вывести кишку на нужное расстояние для непосредственного соединения с пищеводом, на кишку и пищевод накладывают стомы (на пищевод накладывают боковую стому). В последующем с помощью кожи восстанав-
79

Рис. 27. Варианты тонкокишечной ээофагопластики:
1 — по Лексеру; 2 — по Юдину: 3 — по Вулльштейну; 4 — по Еремееву
80

Рис, 28. Мобилизация тонкой кишки:
1—4 — выделение и пересечение радиаоных сосудов тонкой кишки; 5 — радиарные -сосуды пере вязаны; 6 — формирование тонкокишечного трансплантата закончено
81

Рис. 29. Наложение пищеводно-кишечного 
ливают непрерывность искусственного пи щевода, причем вначале включают в кож ный тоннель и закрывают нижнюю стому, а потом — верхнюю. Если расстояние между свищами небольшое, операцию включения свищей в кожную трубку выполняют одно моментно.
Благодаря хорошо разработанной мето дике операции в Институте скорой помощи им. Н. В. Склифосовского непосредственное соединение пищевода с кишкой выполнено у 43,5 % больных. У остальных больных удалось закончить пластику с кожной над ставкой.
Для удлинения тонкокишечного транс плантата предложен ряд приемов. Van Ргоhaska и Sloan (1947) удаляли серозно-мы- шечный слой верхней части трансплантата, оставляя лишь слизистую оболочку, что де лало верхнюю часть трансплантата более растяжимой. Однако такой прием приводил к ухудшению кровоснабжения остающейся слизистой оболочки и рубцеванию шейного анастомоза.
В 1950 г. Г. А. Петров и Г. Р. Хундадзе предложили новый способ мобилизации тон кой кишки для создания искусственного пищевода: разрезом париетальной брюшины в области слепой кишки корень брыжейки вместе со всеми петлями кишечника смеща ют кверху до уровня двенадцатиперстной кишки, что позволяет удлинить брыжейку мобилизованной кишки на 8—10 см. Не достатком этой методики является оставле ние задней части брюшной стенки непокры той брюшиной. Это, безусловно, ведет к образованию спаек, а также сопровождает ся болью в послеоперационный период, которая держится в течение 3—4 сут. Пре
имуществом данного способа является то, что авторы благодаря добавочной мобилиза ции кишки добились непосредственного соединения ее с пищеводом у большего числа больных (60 % ) , чем до применения этой методики.
Jezioro и K.us (1957) при мобилизации корня брыжейки пересекают затрудняющие мобилизацию подвздошно-ободочные сосу ды, что позволяет не смещать илеоцекальный отдел кишечника.
С. С. Юдин (1954) предложил для увели чения длины брыжейки отдельно обрабаты вать сосуды, листки брюшины и жировую клетчатку. При натяжении между оральным концом трансплантата и пищеводом можно воспользоваться приемом, разработанным 3. Т. Сенчилло-Явербаум (1957). Автор установила, что при циркулярном рассече нии серозной оболочки кишка удлиняется почти на 5 см. А. А. Русанов (1964) фикси ровал корень брыжейки к апоневрозу по белой линии живота и расправлял оральный конец трансплантата путем пересечения 2— 3 прямых сосудов и первичной аркады. Это увеличивало длину выкраиваемой кишки на 8—10 см. Но даже при смещении корня брыжейки тонкую кишку не всегда удается вывести до угла нижней челюсти (Ю. Т. Коморовский, 1953; Б. А. Петров, А. П. Сытник, 1962, 1972; И. М. Бородин, 1967).
М. И. Коломийченко (1967) предложил использовать интервал между первой и вто рой операцией (если из-за риска расстрой ства кровообращения трансплантат нельзя довести до нужного уровня) для массажа антеторакально перемещенной кишки. Для улучшения кровоснабжения тонкокишечно го трансплантата Е. Ю. Крамаренко (1921)
82
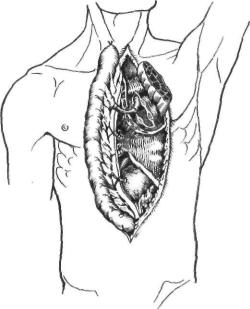
разработал на трупах методику сосудистого анастомоза между брыжеечной артерией мобилизованной кишки и внутренней груд ной артерией или одной из шейных артерий. Longmire (1946) впервые выполнил эту операцию в клинике.
П. И. Андросов (1952) с помощью аппарата для сшивания сосудов также на кладывал анастомоз между вторым радиарным стволом мобилизованной кишки и пра вой желудочно-сальниковой артерией (рис. 30). У 15 больных достигнуто хорошее кровоснабжение мобилизованной кишки.
В 1951 г. А. А. Шалимов предложил способ предварительной тренировки сосу дистой сети трансплантата. Он предвари тельно перевязывал радиарные сосуды то щей кишки, намеченной для мобилизации, а через 3 мес пересекал их между ранее наложенными лигатурами и выполнял эзофагопластику. К 1962 г. автор выполнил 22 операции. Предварительную тренировку кишки применяли Shumacker, Battersby (1951), Н. М. Амосов (1958), А. Г. Савиных (1962) и другие авторы. Предварительной тренировкой достигается увеличение калиб ра питающей артерии краевого сосуда
трансплантата (А. А. |
Шалимов, 1954; |
И. М. Стельмашонок, |
В. Я- Бондалевич, |
1961; Г. М. Мусагалиев, 1963; Э. Л. Фрайфельд, 1966).
Кишечную пластику шейной части пище вода трансплантатами на длинной сосуди стой ножке разработали и успешно выпол нили В. И. Попов и В. И. Филин в 1962 г. При этом используют участок подвздошной кишки с сосудистой ножкой из средней ободочной артерии и вены, мобилизуют илеоцекальный угол и терминальный отдел подвздошной кишки. Перевязывают и пере секают правую ободочную артерию и вену. Авторы чаще выполняли сегментарную пластику шейной части пищевода в два этапа. Кишечный трансплантат проводят через предгрудинный подкожный тоннель на шею до угла нижней челюсти; верхний конец трансплантата вшивают в глотку. Нижний конец кишечного трансплантата соединяют с культей шейной части пищевода анасто мозом по типу конец в конец. Избыточную часть кишечного трансплантата удаляют через 12—15 дней.
Оригинальную методику внутригрудинной эзофагопластики тонкокишечным трансплан татом на двух сосудистых ножках разрабо тали Г. Е. Островерхое и Р. А. Тощаков (1962), а впервые успешно осуществили в клинике Т. А. Суворова и Р. А. Тощаков в 1963 г. Отступя 20—25 см от двенадцати перстной кишки, намечают участок длиной 8—12 см, подлежащий перемещению В грудную клетку. В питающую ножку входят 2-я и 7-я кишечные артерии. Перевязывают и пересекают 3—6 сосудов. Резецируют участки тощей кишки дистальнее и проксимальнее трансплантата.
Т. А. Суворова произвела сегментарную пластику пищевода при раке после резекции средней трети грудной части и при рубцовой стриктуре, выполнив шунтирование пищевода.
Дальнейшее совершенствование сегмен тарной эзофагопластики шло по пути ис пользования свободной трансплантации кишечника. При такой методике отрезок кишки отделяют от брыжейки и после реваскуляризации сосудистым анастомозом с ближайшими артерией и веной вшивают отрезок кишки между участком резециро ванного пищевода или в обход стриктуры.
Рис. 30. Тонкокишечная эзофагопластика |
Впервые использовали участок кишки для |
свободной пересадки Seidenberg и соавторы |
|
с анастомозом внутренней грудной артерии |
(1959). В. И. Попов и В. И. Филин (1961, 1962) |
и радиарной артерии трансплантата |
производили свободную пересадку кишечника и |
83
при реконструктивных операциях для соединения верхнего конца трансплантата с шейной частью пищевода в тех случаях, когда при первой опера ции трансплантат был выведен недостаточно высоко.
Частые ишемические некрозы в большин стве случаев связаны с большой протяжен ностью мобилизованной тонкой кишки. Для повышения ее жизнеспособности можно применить два способа: уменьшить размеры трансплантата или обеспечить его допол нительным источником кровоснабжения за счет наложения сосудистых анастомозов. Последний способ распространения не по лучил. Мобилизованная тонкая кишка в не сколько раз превосходит длину питающей ее сосудистой ножки и в связи с этим образу ет множество изгибов (петель). Это позво ляет осуществлять сегментарную резекцию кишки, которая заключается в удалении избыточных петель без уменьшения длины сосудистой ножки.
Еще в 1950 г. Ballivet рекомендовал резецировать нижнюю треть или даже поло вину тонкокишечного трансплантата, что улучшает кровоснабжение остающейся час ти трансплантата.
Е. И. Кухаренко (1970) разработал в эксперименте, а А. А. Шалимов (1970) вы полнил в клинике тотальную тонкокишеч ную эзофагопластику с резекцией несколь ких сегментов трансплантата.
Данные литературы свидетельствуют о том, что с уменьшением массы питаемого органа при сохранении источника крово снабжения жизнеспособность его повышает ся. При стриктурах пищевода на ограни ченном протяжении ряд хирургов считают целесообразной сегментарную эзофагопла стику. При такой методике сохраняется лишь проксимальная часть мобилизованной кишки, достаточная для пластики в обход стриктуры или для вставки между концами резецированного пищевода. Неиспользован ную дистальную часть трансплантата резе цируют, тщательно сохраняя первичные сосудистые аркады. Выкроенный таким образом небольшой сегмент кишки, как правило, получает адекватное кровоснабже ние.
Эзофагопластика желудком (рис. 31). Первым шагом в осуществлении пластики пищевода желудком была трубчатая гастростомия, разработанная Depage (1901), кото рый создавал трубку из передней стенки
желудка. Beck и Carrell (1905) исполь зовали большую кривизну желудка.
В 1911 г. Hirsch предложил выкраивать длин ный прямоугольный лоскут из передней стенки желудка, формировать трубку и выводить ее под кожу передней стенки грудной клетки, чтобы в последующем соединить желудочную трубку с пищеводом посредством кожной надставки. Та ким образом Hirsch оперировал 6 больных, но ни у одного ему не удалось довести операцию до конца.
Операция Гирша не получила распростране ния, поскольку при этом способе создается корот кая желудочная трубка с недостаточным крово снабжением.
В 1912 г. независимо друг от друга Я- О. Гальперн и A. Jianu предложили создавать искус ственный пищевод посредством выкраивания трубки из большой кривизны желудка с питани ем за счет левой желудочно-сальниковой артерии. Желудочную трубку выводили под кожу перед ней стенки грудной клетки и затем, как правило, соединяли посредством кожной надставки с пище водом, так как довести желудочную трубку до пищевода не удавалось. Впервые осуществить прямое соединение желудочной трубки с пище водом удалось Lotheissen (1922).
Следует заметить, что операция Гальперна — Жиану не всегда выполнима, так как желудок при Рубцовых сужениях пищевода часто бывает также рубцово суженным и это препятствует созданию желудочной трубки достаточной длины. Для увеличения длины и улучшения кровоснабже ния желудочной трубки Кау (1943), Swenson, Magruder (1944) удаляли селезенку, перевязывая селезеночную артерию в воротах селезенки.
Впоследующем эзофагопластика желудочной трубкой из большой кривизны получила распро странение благодаря работам Gavriliu.
В1951 г. Gavriliu предложил методику вы краивания желудочной трубки для пластики пищевода. Операция заключается в следующем. Рассекают листок париетальной брюшины слева и сзади селезенки. Селезенку и поджелудочную железу мобилизуют до уровня аорты и отводят кпереди. Рассекают передний листок желудочноселезеночной связки и у ворот селезенки пере вязывают сосуды, стараясь не повредить желудоч ных ветвей селезеночной артерии. Удаляют селезенку, но желудочно-поджелудочную связку при этом сохраняют. Большой сальник отделяют от желудка, сохраняя желудочно-сальниковые артерии. Затем с помощью специальных зажимов или сшивающих аппаратов из большой кривиз ны выкраивают трубку диаметром 2—2,5 см, ста раясь не повредить ветви левой желудочно-саль никовой артерии. Сформированную из стенки желудка трубку проводят подкожно, загрудинно или внутриплеврально на шею, где ее соединяют
спищеводом. В тех случаях, когда длина желу дочной трубки недостаточна, Gavriliu (1964) включает в трансплантат препилорический отдел желудка, привратник и начальный отдел двенадцатиперстной кишки. Непрерывность пищеварительного тракта восстанавливают с помощью гастродуоденоанастомоза.
В1923 г. Rutkowski в эксперименте разрабо тал методику выделения трансплантата из боль-
84

Рис. 31. Варианты пластики пищевода желудком:
I — по Папа; 2 — по Gavritiu; 3 — по Fink; 4 — по Rulkowski
шой кривизны желудка с изонеристальтическим расположением желудочной трубки. Основание ее располагают у антральной части желудка. Крово снабжение желудочной трубки при этом осущест вляется за счет правой желудочно-сальниковой артерии. В клинике эта методика была впервые успешно применена Lortat-Jacob (1949), который указывал на недостаточное кровоснабжение верх него конца созданной таким образом трубки вследствие пересечения коротких желудочных
артерий и левой желудочно-сальниковой артерии. В связи с этим А. А. Шалимов (1961) рекомен довал сохранять короткие желудочные артерии и левую желудочно-сальниковую артерию, пере вязывая селезеночную артерию в воротах селезенки.
Ogilvie (1938) и Mes (1948) предложили для создания изоперистальтической трубки из боль шой кривизны включать в трансплантат и дно желудка. При этом линия отсечения идет па-
85

раллельно большой кривизне, дну желудка вплоть до угла Гиса. При выпрямлении созданной таким образом трубки длина ее увеличивается.
Для улучшения кровоснабжения верхнего отде ла трансплантата из большой кривизны желудка Nakayama (1962) накладывал дополнительный сосудистый анастомоз между культей селезеноч ной артерии и одной из артерий шеи.
Наряду с пластикой пищевода с помощью желудочной трубки разрабатывались методики замещения пищевода целым желудком. В 1913 г. Fink предложил перемещать под кожу грудной клетки расположенный антиперистальтически желудок.
Н. Н. Ковальский успешно выполнил операцию Финка у 3 больных. Р. Т. Панченков применил аналогичную операцию после удаления кожного пищевода (цит. по Н. С. Королевой, 1961).
В 1920 г. Kirschner использовал для пластики пищевода желудок, расположенный изоперигтальтически. При этом способе желудок мобили зуют с сохранением правой желудочной и желу- дочно-сальниковой артерий, отсекают у кардии и проводят подкожно на переднюю стенку грудной клетки. Культю пищевода соединяют с выклю ченной по Ру петлей тонкой кишки. Во второй этап пересекают пищевод на шее, аборальный его конец ушивают, а оральный соединяют с подкожно расположенным желудком. Kirschner предложил выполнять эту операцию одномомент но двумя бригадами хирургов. Он оперировал 2 больных, одна операция закончилась успешно.
Оригинальную модификацию эзофагопластики целым желудком успешно выполнил А. Н. Бакулев (1930). Чтобы избежать наложения эзофагоеюноанастомоза и удлинить трансплантат, он сформи ровал из малой кривизны желудочную трубку небольших размеров и соединил ее с двенадцати перстной кишкой. Остальная часть желудка была мобилизована, проведена подкожно на шею, где был наложен эзофагогастроанастомоз (рис. 32). В последующем этот принцип удлинения желу дочного трансплантата (резекция малой кривизны или кардиальной части желудка) разработали В. И. Попов и В. И. Филин (1965).
Применительно к эзофагопластике нужно учитывать, что у некоторых больных желу док можно поднять до уровня мочки уха, а у большинства его с трудом можно довести до яремной вырезки грудины. Так, В. И. Фи лин (1965), исследовавший 25 трупов, толь ко в 10 случаях свободно довел целый желу док после мобилизации до уровня нижнего края гортани, в 15 случаях его удалось довести лишь до яремной вырезки грудины или ниже.
При тотальной эзофагопластике для нало жения анастомоза с глоткой длина транс плантата должна быть больше расстояния от мечевидного отростка до угла нижней челюсти, которое у взрослых равно 35— 40 см (Н. И. Еремеев, 1951; И. С. Мгалоблишвили, 1960).
Рис 32. Варианты пластики пищевода же лудком:
I — по Бакулеву; 2 — по Киршнеру
Наряду с недостаточной длиной желудка трудности эзофагопластики нередко связа ны с вариабельностью его кровоснабжения. При отсутствии или недостаточной выра женности внеорганных анастомозов между правыми и левыми сосудами желудка при мобилизации его нарушается кровоснабже ние проксимального отдела желудка и осо бенно дна, используемого для наложения анастомоза с пищеводом.
В зависимости от уровня сужения, состоя-
86
ния желудка, его сосудов и аркад мы применяем следующие операции. При лока лизации сужения в нижней трети грудной части пищевода резецируем суженный учас ток пищевода и дно желудка с наложением пищеводно-желудочного анастомоза в левой плевральной полости. При сужении в сред ней трети пищевода производим одномо ментную пластику желудком по Льюису. Эта операция выполнима в тех случаях, когда сосудистые аркады желудка хорошо развиты и нет перерыва между правой и левой желудочно-сальниковыми артериями. При отсутствии хороших сосудистых анастомозов выполняем резекцию дна желудка с последующей пластикой.
Внутригрудная пластика пищевода же лудком. Резекция средней трети грудной
• части пищевода по поводу рубцового суже ния с последующей пластикой ее желудком является большой по объему и технически сложной операцией. До настоящего времени отмечается высокая летальность, связанная с возникновением в послеоперационный период недостаточности швов пищеводножелудочного анастомоза. Причиной не достаточности швов анастомоза большин ство авторов считают нарушение крово обращения в сопоставляемых после резек ции органах, вплоть до их некроза.
Мы применяем усовершенствованную А. А. Шалимовым (1963) одномоментную резекцию средней трети грудной части пище вода при рубцовом изменении вместе с кардиальиой частью и дном желудка с по следующей пластикой пищевода остальной частью желудка, расположенной в заднем средостении, на месте удаленного пищевода.
Е. Л. Березов (1951) и Б. А. Королев (1959) производят резекцию пищевода с участком дна и кардиалыюй частью желуд ка и перемещают оставшийся желудок в левую (Е. Л. Березов) или правую (Б. А. Ко ролев) плевральную полость. А. А. Шалимов вместе со средней третью грудной части пищевода в одном блоке удаляет кардиальную часть и дно желудка как наиболее подверженные расстройству кровообраще ния. Линия отсечения желудка проходит на 5 см выше последней сосудистой ветви, отходящей от правой желудочно-сальнико- вой артерии.
При выполнении этого этапа операции мы пользуемся аппаратом УКЛ-60. Перемеща емая вначале в правую плевральную полость
часть желудка в конце операции располага ется в заднем средостении. В парамедиастинальное пространство она выступает лишь частично и поэтому (в отличие от других способов) не нарушает респиратор ной функции легких.
Расположение желудочной трубки в заднем средостении — ложе резецирован ного пищевода — предотвращает травму со судистой аркады желудка вследствие дыха тельных экскурсий легкого. Благодаря рас сечению правой ножки диафрагмы путь прохождения желудочной трубки из брюш ной полости до культи пищевода в ложе резецированного пищевода является самым коротким по сравнению с другими. Пере мещению желудка в плевральную полость и наложению супрааортального пищеводножелудочного анастомоза способствует моби лизация двенадцатиперстной кишки с обязательным освобождением ее нисходя щего колена, включая нижнюю кривизну. Широкая мобилизация двенадцатиперстной кишки способствует тому, что привратник с двенадцатиперстной кишкой и головкой поджелудочной железы значительно подни мается вверх до уровня пересеченной пра вой ножки диафрагмы, а иногда и выше.
Операция выполняется без нарушения целости диафрагмы. Сохранение функции диафрагмы имеет большое значение для последующего восстановления функцио нальной способности легких.
Методика операции. Разрезом от мече видного отростка до пупка по средней ли нии послойно вскрывают брюшную полость. Желудок мобилизуют по большой кривизне рассечением желудочно-ободочной связки, отступя 3—4 см от стенки желудка, с сохра нением сосудистой аркады правой желудоч- но-сальниковой артерии. Затем рассекают желудочно-селезеночную связку, левую треугольную связку печени и выделяют дно желудка. Рассекают малый сальник с сохра нением правой желудочной артерии и сосу дистой аркады по малой кривизне желудка. Затем рассекают желудочно-поджелудоч- ную связку, и ствол левой желудочной артерии пересекают как можно ближе к месту отхождения от чревной артерии.
Рассекают пищеводно-диафрагмальную связку и брюшину над пищеводом. Мобили зуют кардиальную часть желудка и брюш ную часть пищевода. Оба блуждающих нерва пересекают, отсепаровывают и пере-
87
секают правую ножку диафрагмы. Две надцатиперстную кишку мобилизуют путем рассечения брюшины латерально от нее с обязательным освобождением нисходящего ее колена и нижней кривизны. На этом брюшной этап операции заканчивают. Брюшную рану зашивают послойно.
Из переднебокового доступа справа в четвертом межреберье послойно вскрывают плевральную полость. Широко рассекают медиастинальную плевру, пересекают не парную вену. Пораженную среднюю треть грудной части пищевода выделяют до диафрагмы. Через пищеводное отверстие диафрагмы в плевральную полость выводят мобилизованный желудок. Пищевод пересе кают над стриктурой. С помощью аппарата УКЛ-60 кардиальную часть и дно желудка прошивают по намеченной линии, которая на 5 см выше последней сосудистой ветви, отходящей от правой желудочно-сальнико- вой артерии. Мобилизованный отдел пище вода удаляют одним блоком с кардиальной частью и дном желудка. Линию танталового шва погружают узловыми серозно-мы- шечными швами, начиная от малой кривиз ны желудка и не доходя 4,5 см до большой кривизны. Оставленный непогруженным участок танталового шва вблизи большой кривизны желудка используют для наложе ния анастомоза с культей пищевода. Между оставшейся после резекции частью желудка, сформированной в виде трубки, и оральной культей пищевода свободно на кладывают супрааортальный пищеводножелудочный анастомоз двухрядными узло выми шелковыми швами с завязыванием узлов первого ряда швов внутрь просвета сопоставляемых органов. После этого желудок помещают в заднее средостение, в ложе удаленного пищевода, и в таком положении его стенку подшивают узловыми швами к краям медиастинальной плевры на всем протяжении от области анастомоза до отверстия диафрагмы.
Эзофагопластика желудком с наложением внутриплеврального сосудистого анасто м о з а — технически сложная операция. Она связана с наложением анастомоза между сосудами, имеющими разный диаметр. В связи с этим не исключена возможность их тромбирования и нарушения кровоснаб жения стенки дна желудка (что и имело место у 1 наблюдаемой нами больной), так как в создавшихся условиях правые сосуды
не обеспечивают адекватного кровоснабже ния проксимального отдела желудка и области пищеводно-желудочного анастомо за. Поэтому при эзофагопластике желудком и малейшем сомнении в жизнеспособности дна его целесообразно, наряду с резекцией пищевода, шире резецировать и дно же лудка.
Создание искусственного пищевода из ободочной кишки. Достаточная длина, хоро шее кровоснабжение, возможность получить прямой, без лишних петель трансплантат без существенных функциональных наруше ний — вот основные факторы, которые спо собствовали широкому распространению толстокишечной эзофагопластики.
Особенности строения и васкуляризации ободочной кишки. Общая длина ободочной кишки у взрослого человека не превышает 1,5—2 м. Для формирования искусственного пищевода обычно используют участок кишки длиной 40—60 см (И. С. Мгалоблишвили, 1961).
Кровоснабжение правой половины обо дочной кишки осуществляется из ветвей верхней брыжеечной артерии. Самая круп ная из них — подвздошно-ободочная арте рия отходит на расстоянии около 7 см от устья верхней брыжеечной артерии, имеет длину 15—20 см, направлена к илеоцекальному отделу кишечника; ее диаметр 3— 3,5 мм. Она делится на 3—6 ветвей: под вздошную, ободочную, переднюю и заднюю артерии слепой кишки, артерию червеобраз ного отростка и непостоянную добавочную ободочную артерию.
Подвздошно-ободочная артерия является главным источником кровоснабжения илеоцекальной области. Ободочная ветвь отхо дит от основного ствола высоко, и к прокси мальным отделам кишки от нее направляют ся 1—4 сосуда, которые отходят после довательно один от другого. Правая ободочная артерия отходит на расстоянии 2—9 см от устья верхней брыжеечной ар терии и имеет длину от 8 до 20 см. Она часто имеет общий ствол со средней ободочной или подвздошно-ободочной артерией.
Диаметр средней ободочной артерии око ло 2,5—3 мм (П. А. Куприянов, 1924; А. А. Травин, 1958; В. И. Филин, 1963). Эта артерия отходит от верхней брыжеечной у нижнего края поджелудочной железы на расстоянии 1—5 см от устья верхней бры жеечной артерии, имеет длину 7—17 см.
88
