
- •Введение
- •Лекция 1. Нулевое начало термодинамики
- •1.1. Основные определения химической термодинамики. 1.2. Нулевое начало термодинамики.
- •1.1. Основные определения химической термодинамики
- •1.2. Нулевое начало термодинамики
- •Лекция 2. Первое начало термодинамики. Термохимия.
- •2.1. Внутренняя энергия, теплота и работа
- •2.2. Первое начало термодинамики
- •2.3. Применение первого начала термодинамики к химическим реакциям
- •2.4. Термохимия. Закон Гесса
- •2.5. Теплоемкость. Зависимость теплового эффекта от температуры. Уравнение Кирхгофа
- •Лекция 3. Второе начало термодинамики. Энтропия.
- •3.1. Второе начало термодинамики. 3.2. Необратимые процессы. Изменение энтропии в разных процессах. 3.3. Энергии Гиббса и Гельмгольца.
- •3.1. Второе начало термодинамики
- •3.2. Необратимые процессы. Изменение энтропии в разных процессах
- •3.3. Энергии Гиббса и Гельмгольца
- •Лекция 4. Третье начало термодинамики.
- •4.1. Третье начало термодинамики. Абсолютные энтропии химических соединений. 4.2. Энтропия и термодинамическая вероятность.
- •4.1. Третье начало термодинамики. Абсолютные энтропии химических соединений
- •4.2. Энтропия и термодинамическая вероятность
- •Лекция 5. Дисперсность и классификация коллоидных систем
- •5.1. Предмет коллоидной химии. Общие свойства коллоидных растворов. 5.2. Дисперсность коллоидных систем. 5.3. Классификация коллоидных систем.
- •5.1. Предмет коллоидной химии. Общие свойства коллоидных растворов
- •5.2. Дисперсность коллоидных систем
- •5.3. Классификация коллоидных систем
- •Лекция 6. Адсорбция
- •6.1. Основные определения. Изотерма адсорбции. 6.2. Уравнение Гиббса. 6.3. Поверхностно-активные вещества. 6.4. Правило Дюкло-Траубе. Уравнение Шишковского.
- •6.1. Основные определения. Изотерма адсорбции
- •6.2. Уравнение Гиббса
- •6.3. Поверхностно-активные вещества
- •6.4. Правило Дюкло-Траубе. Уравнение Шишковского.
- •Лекция 7. Электрокинетические свойства коллоидных систем
- •7.1. Виды электрокинетических явлений. 7.2. Двойной электрический слой и ζ-потенциал.
- •7.1. Виды электрокинетических явлений
- •7.2. Двойной электрический слой и ζ-потенциал
- •Литература
- •Содержание
5.2. Дисперсность коллоидных систем
Мерой раздробленности всякой дисперсной системы может служить либо поперечный размер частиц (а) (для сферических частиц - диаметр d, а частиц кубической формы - ребро куба ℓ), либо обратная ему величина D = 1/а, называемая дисперсностью, либо удельная поверхность Sуд., т, е. межфазная поверхность, приходящаяся на единицу объема дисперсной фазы. Все эти величины взаимосвязаны:
![]() (5.1)
(5.1)
где S1,2 - поверхность между фазами 1 и 2 (межфазная поверхность); V - суммарный объем дисперсной фазы.
Для системы, содержащей кубические частицы с ребром ℓ, имеем, учитывая, что удельная поверхность численно равна отношению поверхности частицы S1,2 к ее объему V1:
![]() (5.2)
(5.2)
Для системы, содержащей сферические частицы радиусом r, получим:
 (5.3)
(5.3)
В общем случае:
![]() (5.4)
(5.4)
где k - коэффициент, зависящий от формы частицы.
Удельная поверхность прямо пропорциональна дисперсности D и обратно пропорциональна размеру частиц (а). С повышением дисперсности коллоидной системы ее удельная поверхность резко возрастает. Зависимость удельной поверхности системы от размера частиц представлена на рис. 5.1. К коллоидным системам относятся системы, у которых значение (а) лежит в пределах 1- 100 нм (10-7- 10-5 см), а дисперсность - в пределах 1- 100 нм -1 (107- 105 см-1).
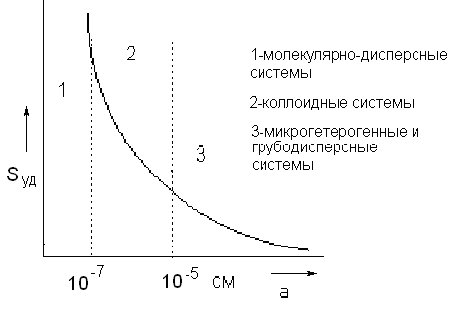
Рис. 5.1
Верхний предел дисперсности коллоидных систем обусловлен тем, что при дальнейшем дроблении вещества в растворе уже будут находиться отдельные молекулы, имеющие размер порядка 0,1 нм. Нижний предел дисперсности определяется резким снижением интенсивности теплового движения частиц поперечным размером больше 100 нм.
Многие свойства дисперсных систем весьма сильно зависят от их дисперсности. Ряд из них проявляются при дисперсности, характерной для коллоидных систем. При объяснении свойств коллоидных систем необходимо учитывать не только размер частиц, но и наличие межфазной поверхности, обусловливающей возможность разнообразных адсорбционных явлений, а также различные химические реакции, которые могут протекать на поверхности частиц.
5.3. Классификация коллоидных систем
В коллоидной химии, как во всякой науке, имеющей дело со множеством объектов, необходима классификация коллоидных систем, чтобы разобраться во всем их многообразии. Однако единая классификация этих систем до сих пор отсутствует. Рассмотрим кратко те классификации, которые получили наибольшее распространение.
Классификация по дисперсности неполно и односторонне учитывает характеристику коллоидных систем. К полидисперсным, т.е. содержащим частицы различных размеров, системам прилагать эту классификацию невозможно.
Классификация по агрегатному состоянию дисперсной фазы и дисперсионной среды была предложена Оствальдом. Возможны девять комбинаций дисперсной фазы и дисперсионной среды в различных их состояниях (табл. 5.1). Однако, практически можно реализовать только восемь комбинаций, так как газы в обычных условиях растворимы друг в друге и образуют гомогенную систему.
В коллоидной химии все системы, отвечающие коллоидной дисперсности, принято называть золями. Поэтому системы Ж/Г и Т/Г имеют общее название аэрозолей. Это название условно, т. к. дисперсионной средой может быть не только воздух, но и любой другой газ.
Системы с жидкой дисперсионной средой (Г/Ж, Ж/Ж, Т/Ж) называются лиозолями (от греч. лиос - жидкость). В зависимости от природы дисперсионной среды лиозоли делятся на гидрозоли, алкозоли, этерозоли, бензозоли (дисперсионной средой соответственно являются, вода, спирт, эфир, бензол). Однако с уменьшением размера частиц разница в агрегатном состоянии дисперсной фазы в различных коллоидных системах постепенно сглаживается. Поэтому Зигмонд упростил классификацию, приняв в качестве классификационного признака лишь агрегатное состояние дисперсионной среды. Тогда остаются три возможных класса: системы с газовой, жидкой и твердой дисперсионной средой.
Таблица 5.1
Классификация дисперсных систем по агрегатному состоянию дисперсной фазы и дисперсионной среды
Дисперсная фаза |
Дисперсиион-ная среда |
Условное обозначение системы |
Название системы |
Газ |
Газ |
Г/Г |
Коллоидная система невозможна |
Жидкость |
Газ |
Ж/Г |
Туманы |
Твердое тело |
Газ |
Т/Г |
Дымы, пыль |
Газ |
Жидкость |
Г/Ж |
Пены |
Жидкость |
Жидкость |
Ж/Ж |
Эмульсии |
Твердое тело |
Жидкость |
Т/Ж |
Коллоидные растворы, суспензии |
Газ |
Твердое тело |
Г/Т
|
Твердые пены, пористые тела |
Жидкость |
Твердое тело |
Ж/Т |
Твердые эмульсии |
Твердое тело |
Твердое тело |
Т/Т |
Твердые золи, сплавы |
Классификация по взаимодействию дисперсной фазы и дисперсионной среды пригодна только для систем с жидкой дисперсионной средой. Она сводится к классификации по способности сухого остатка, полученного в результате осторожного выпаривания жидкости, растворяться в чистой дисперсионной среде. Системы, сухой остаток которых не способен самопроизвольно диспергироваться в дисперсионной среде, называют необратимыми. Сюда относятся типичные коллоидные растворы - лиозоли металлов. Обратимыми коллоидными системами названы системы, сухой остаток которых при соприкосновении со средой обычно сначала набухает, а затем самопроизвольно растворяется и снова образует коллоидную систему. К таким системам относятся, например, раствор желатина в воде или каучука в бензоле. Необратимые коллоидные системы имеют признаки коллоидных растворов: их трудно получить с высоким содержанием дисперсной фазы; они легко коагулируют при введении в них электролитов, образуя при этом компактные, содержащие малое количество дисперсионной среды осадки. Обратимые, наоборот, можно получать достаточно высокой концентрации; они гораздо менее чувствительны к электролитам, а осадки их весьма объемисты, вязки и содержат много дисперсионной среды. Фрейндлих высказал мнение, что обратимость и необратимость связаны с взаимодействием дисперсной фазы с дисперсионной средой. Дисперсная фаза обратимых коллоидных систем взаимодействует молекулярно с дисперсионной средой и поэтому способна в ней растворяться. И такие системы назвали лиофильными (от греч. лиос -жидкостъ, фило - люблю). Обратимые (лиофильные) системы представляют собой растворы высокомолекулярных соединений, а эти растворы являются истинными. Таким образом, классификация Зигмонда и Фрейндлиха по существу представляет собой классификацию не коллоидных систем, а дисперсных систем, содержащих частицы, отвечающие коллоидным размерам, причем в эту классификацию входят как типичные коллоидные системы, так и растворы полимеров.
Согласно классификации по взаимодействию между частицами дисперсные системы разделяются на свободнодисперсные и связнодисперсные. К свободнодисперсным системам относятся бесструктурные системы, в которых частицы дисперсной фазы не связаны друг с другом в одну сплошную сетку и способны независимо перемещаться в дисперсионной среде под влиянием броуновского движения или силы тяжести. К подобным системам относятся лиозоли, достаточно разбавленные суспензии и эмульсии, а также аэрозоли. Среди пищевых масс в качестве примера свободнодисперсной системы можно привести майонез.
В связнодисперсных системах частицы связаны друг с другом за счет межмолекулярных сил, образуя в дисперсионной среде своеобразные пространственные сетки или каркасы (структуры). Частицы, образовавшие структуру, очевидно, не способны к взаимному перемещению и могут совершать лишь колебательные движения, К таким системам относятся гели, концентрированные суспензии (пасты) и концентрированные эмульсии и пены, а также порошки. Гели могут образоваться как в результате коагуляции коллоидных систем и объединения в одно целое выпавшего осадка (коагели), так и вследствие молекулярного сцепления в отдельных местах частиц золя, образующего сравнительно рыхлые сетки или каркасы (лиогели). Переход золя в состояние геля называется гелеобразованием. В пищевой промышленности связнодисперсные системы – это мусс, пена пива.
В табл. 5.2 приведена классификация некоторых пищевых масс как дисперсных систем.
Таблица 5.2
Классификация некоторых пищевых масс как дисперсных систем
Система |
Представители пищевых масс |
Отрасли пищевой промышленности |
Т/Ж |
Фруктовые соки, овощные пасты, расплавленные шоколадные и конфетные массы |
Консервная, сахарная, безалкогольных напитков |
Ж/Ж |
Соус, молоко, маргарин, майонез, пищевые кремы |
Молочная, масложировая, маргариновая, парфюмерная |
Г/Ж |
Полупродукты бродильных производств, шипучие напитки, шампанские и игристые вина |
Пивоварение, безалкогольных напитков |
Т/Т |
Мясо, рыба, колбаса, шоколадные массы |
Мясная, рыбная, кондитерская |
Ж/Т |
Жировые включения в тесто и кондитерские массы |
Кондитерская, хлебопекарная |
Г/Т |
Хлеб, сыр, пастила, зефир |
Хлебопекарная, кондитерская, производство сыра |
Т/Г |
Мука, крупа, крахмал, сухое молоко, молотый кофе |
Хлебопекарная, мукомольная, комбикормовая, сахарная, кондитерская |
Ж/Г |
Промежуточные и сопутствующие вещества |
Практически во всех |
