
- •2. Сутність та значення матеріального балансу.
- •5. Охорона праці та техніка безпеки при роботі у фітохімічному цеху.
- •8. Нові лікарські форми з регульованою швидкістю вивільнення лікарських речовин.
- •11. Порядок затвердження до застосування нових лікарських засобів в Україні.
- •13. Роль та значення трибоелектричних явищ при просіюванні. Типи ситових полотен.
- •14. Ударно-стиральні механізми у виробництві порошків. Визначення і критичної швидкості обертання барабану шарового млина.
- •16. Чим визначається вибір подрібнювальних машин для порошкування.
- •25. Причини браку та методи запобігання при виробництві таблеток.
- •29. Способи визначення технологічних властивостей порошків у виробництві таблеток.
- •30. Які основні групи допоміжних речовин pвикористовуються в таблетковому виробництві.
- •33. В яких випадках у виробництві таблеток застосовують розчинники.
- •35. Принцип роботи таблеткової машини подвійного пресування.
- •39. Промислове виробництво ректальних лікарських форм.
- •40. Сутність процесу гранулювання. Випадки при яких порошкоподібні речовини гранулюються до таблетування.
- •43. Способи виготовлення розчинів (пряме розчинення, хімічна взаємодія, солюбілізація).
- •62. Методи часткової та повної рекуперації спирту.Обов'язкова стадія виробництва настоянок і спиртових екстрактів. Ст 92
- •64. Методи визначення концентрації спирту в спиртоводних розчинах та фармацевтичних препаратах.
- •65. Розведення спирту. Формула розведення етанолу. Поняття про об'ємні відсотки спирту. Формула перерахунку масових відсотків в об'ємі.
- •66. Види реперколяції у виробництві екстракційних препаратів.
- •67. Стадії виробництва ферментів мікробіологічного синтезу.
- •69. Способи отримання настойок. Стандартизація. Інтенсифікація процесів екстрагування.
- •72. Статистичні та динамічні методи екстрагування лікарської рослинної сировини.
- •74. Промислові способи отримання ферментних препаратів.
- •75. Визначення концентрації спирту в настойках за дфу.
- •94. Перерахуйте способи виробництва желатинових капсул. Оцінка якості медичних капсул за дфу.
- •96. Швидкість та повнота вивільнення лікарської речовини із капсул.
- •97. Медичні капсули. Іх види. Основні вимоги дфу до желатинових капсул з лікарськими речовинами.
- •98. Види та типи упаковок для виробництва фармацевтичних аерозолей за призначенням. Характеристика аерозольних балонів. Типи клапанно-розпилювальних систем.
- •99. Аерозольні упаковки.
- •100. Пропелленти, їх призначення та класифікація. Технологічна схема виробництва лікарських засобів в аерозольній упаковці.
43. Способи виготовлення розчинів (пряме розчинення, хімічна взаємодія, солюбілізація).
44. Внутрішньоцеховий контроль виробництва ін'єкційних розчинів в ампулах. Під час технологічного процесу виробництва ПЛЗ обов’язково проводять проміжний (постадійний) контроль якості, тобто після
кожної технологічної стадії (операції) проводиться бракераж ампул, флаконів, гнучких контейнерів тощо, що не відповідають зазначеним вимогам. Так, після розчинення (ізотонізації, стабілізації і т. под.) лікарської речовини контролюється якісний і кількісний склад, рН розчину, густина і т. ін.; після операції наповнення перевіряється вибірково об’єм наповнення посудин тощо. Сировина, що надійшла, матеріали, напівпродукти, а також виготовлена проміжна або готова продукція відразу ж після надходження або закінчення технологічного процесу до ухвалення рішення про можливе подальше використання повинні перебувати в карантині. Готова продукція не допускається до реалізації доти, доки її якість не буде визнана задовільною. Рідкі лікарські засоби для парентерального застосування зазвичай контролюються за такими показниками якості: опис, ідентифікація, прозорість, забарвленість, рН, супутні домішки, об’єм, стерильність, пірогени, аномальна токсичність, механічні включення, кількісне визначення діючих речовин, антимікробних консервантів і органічних розчинників. Таким чином, важливими питаннями для всіх видів лікарських засобів парентерального призначення є якнайшвидше впровадження і точне дотримання належних правил виробництва, які забезпечують захист стерильної продукції від різного роду забруднень, що гарантує високу якість вітчизняної фармацевтичної продукції.
45. Стадії технологічного процесу при виробництві ін'єкційних розчинів в ампулах. Апаратура, що використовується на стадії стерилізації. Виготовлення ін’єкційних розчинів у приміщеннях 2-го класу чистоти; розчинення проводиться у герметично закритих реакторах (фарфорових, скляних, емальованих з паровою „сорочкою” та мішалкою; ін’єкційні розчини та процес їх виробництва мають відповідати всім вимогам, що ставляться до них.
Стадія виготовлення розчинів для ампулювання включає наступні операції: розчинення, ізотонування, стабілізація, введення консервантів, стандартизація, фільтрування.
Залежно від властивостей лікарських речовин деякі із операцій можуть бути виключені (ізотонування, консервування, стабілізація. Технологічні стадії виробництва розчинів для ін’єкцій: Допоміжні роботи. Виготовлення та підготовка ампул до наповнення. Підготовка розчинників. Виготовлення розчинів для ін’єкцій. Ампулювання розчинів. Стерилізація ампульованих розчинів. Бракераж і контроль якості. Маркування та упакування.
Принцип роботи стерилізуючого тунеля: транспортування ампул або флаконів здійснюється за допомогою горизонтального і двох вертикальних бічних транспортерів. На вході в тунель ампули проходять через ламінарний потік стерильного повітря. Тунель розділений на три зони: сушки, стерилізації і охолоджування. Температура в зоні стерилізації 360 °С, а на виході 23 °С. Повітряний потік проходить двоступінчасте очищення. Ступінь очищення повітря в другому ступені від частинок з розміром більше або рівним 0,3 мм складає 99,97 %. Нагрів повітря в зоні сушки і стерилізації здійснюється тенами зі спеціальною обробкою поверхні, щоб уникнути утворення окалини.
46. Виробництво ін'єкційних розчинів в ампулах у середовищі захисту газами. Навести апаратурну схему.
47. Принцип роботи термокомпресійної установки при отриманні апірогенної води. Найбільш досконалами нині є термокомпресійні дистилятори, конструкція яких розроблена італійською фірмою «Вопарасе». Їх перевага перед дистиляторами інших типів полягає в тому, що для одержання 1 л води для ін’єкцій необхідно витратити 1,1 л холодної водопровідної води. В інших апаратах це співвідношення складає 1 : 9-1 : 15. Принцип роботи апарата полягає в тому, що пара, яка утворюється в ньому, перед тим як надійти в конденсатор, проходить через компресор і стискується.
При охолодженні і конденсації вона виділяє тепло, за величиною відповідне скритій теплоті пароутворення, що витрачається на нагрівання охолоджувальної води у верхній частині трубчастого конденсатора. Живлення апарата водою здійснюється в напрямку знизу нагору, вихід дистиляту - зверху вниз. Продуктивність дистилятора до 2,5 т/год. Якість одержаної апірогенної води висо ка, тому що краплинна фаза випаровується на стінках трубок випарника. Нагрівання і кипіння в трубках відбувається рівномірно, без перекидів, у тонкому шарі. Затримуванню крапель із пар сприяє також висота парового простору. Вадами є складність конструкції та експлуатації. Найбільш поширеним до останніх років методом одержання води для ін’єкцій була дистиляція. Такий метод вимагає витрат значної кількості енергії. Серед інших вад слід зазначити громіздкість устаткування і велику площу, що займається ним; можлива наявність у воді пірогенних речовин; складність обслуговування.
48. Способи отримання демінералізованої (знесоленої) води, її використання у виробництві. Воду демінералізовану (знесолену) одержують із водопровідної питної якості, яка попередньо піддається ретельному
аналізу, тому що в ній міститься значна кількість розчинених і завислих речовин. Демінералізація води (звільнення від присутності небажаних катіонів і аніонів) проводиться за допомогою іонного обміну і методів розділення через мембрану. Іонний обмін ґрунтується на використанні іонітів – сітчастих полімерів різного ступеня зшивки, з гелевою або мікропористою структурою, ковалентно зв’язаних з іоногенними групами. Дисоціація цих груп у воді дає іонну пару - фіксований на полімері іон і рухливий протиіон, який обмінюється на іони однойменного заряду (катіони або аніони) з розчину. У фармацевтичній промисловості використовують сильнокислотні сульфокатіоніти КУ-1, КУ-2 і пористий КУ-23. У H-формі (катіоніт із рухливим атомом гідрогену) вони обмінюють усі катіони, що містяться у воді. Іонообмін на катіоніті можна зобразити такими рівняннями: 2[K]H + Na2SO4 = 2[K]Na + H2SO4
2[K]SO2OH + CaCl2 = Ca + 2HCl, СТР492
[K]—SO2—O
де K — полімерний каркас катіоніту.
Нині слабоосновні марки ЕДЕ-10П, що застосовувались протягом тривалого часу, замінюються на сильноосновні АВ-171
і АВ-17, які в ОН-формі (аніоніт із рухливою гідроксильною групою) обмінюють усі аніони, що містяться у воді. Реакція аніонного обміну проходить за такою схемою: [A]OH + HCl = [A]Cl + H2O
[A]
2[A]OH + H2SO4 = SO4 + 2H2O,
[A]
де А — полімерний каркас аніоніту.
Іонообмінна установка складається з 3-5 пар катіонітових і аніонітових колонок Серед методів розділення через мембрану можна виділити: зворотний осмос, ультрафільтрацію, діаліз, електродіаліз, випарювання через мембрану. Ці методи базуються на використанні перегородок, які мають селективну проникність, завдяки чому можливе одержання води без фазових і хімічних перетворень. Зворотний осмос (гіперфільтрація) - перехід розчинника (води) із розчину через напівпроникну мембрану під дією зовніш нього тиску. Надлишковий робочий тиск сольового розчину набагато більший за осмотичний. Рушійною силою зворотного осмосує різниця тисків по обидва боки мембрани. Ультрафільтрація і діаліз використовуються для розділення розчинів високомолекулярних сполук, полімерів, колоїдів. Ультрафільтрація - процес мембранного розділення розчинів високомолекулярних сполук під дією різниці тисків. Цей метод використовують, коли осмотичний тиск несумірно малий порівняно з робочим тиском. Рушійною силою є різниця тисків - робочого й атмосферного. Для розділення застосовують мембрани двох типів: пористі і непористі дифузійні мембрани. 1. Пористі — із розміром пор 0,1—1 нм. Селективна проникність будується на адсорбції молекул води поверхнею мембрани і її порами. При цьому утворюється сорбційний шар товщиною декілька нанометрів. Адсорбовані молекули переміщаються від одного центру адсорбції до іншого, не пропускаючи солі. У нашій країні випускаються ультрафільтраційні ацетатцелюлозні мембрани - УАМ-50м, діаметр до 5 нм, УАМ-100м - 7,5, УАМ-150м - 12,5, УАМ-200м - 17,5, УАМ-300м - 25,0 і УАМ-500м – понад 30,0 нм. 2. Непористі дифузійні мембрани утворюють водневі зв’язки з молекулами води на поверхні контакту. Під дією надлишкового тиску ці зв’язки розриваються, молекули води дифундують у протилежну сторону мембрани, а на місця, що утворилися, проникають наступні. Таким чином, вода нібито розчиняється на поверх-і і дифундує всередину шару мембрани. Солі і майже всі хімічні сполуки, крім газів, не можуть проникнути через таку мембрану. У нашій країні випускаються гіперфільтраційні ацетатцелюлозні мембрани МГА-80, МГА-90, МГА-95, МГА-100. Цифри в марці означають відсоток селективності — S, який визначають за такою формулою:
де Сл і С„ — концентрації речовини у вихідному розчині і фільт-
раті, мг/мл.
На цьому принципі працюють промислові установки «Роса»,
УГ-1 і УГ-10.
Електродіаліз. Механізм розділення ґрунтується на спрямованому русі іонів у поєднанні із селективною дією мембран під
впливом постійного струму.
Випаровування через мембрану. Розчинник проходить через мембрану й у вигляді пари видаляється з її поверхні в потоці інертного газу або під вакуумом. Для цього використовують мембрани з целофану, поліетилену, ацетатцелюлози. Перевагою мембранних методів є значна економія енергії. Вода демінералізована використовується для миття склодро-
ту, ампул, допоміжних матеріалів і живлення аквадистиляторів при одержанні води очищеної і води для ін’єкцій.
49. Склад скла для отримання ампул. Класи і марки ампульного скла. Параметри за якими оцінюється якість ампульного скла. Медичне скло є основним пакувальним матеріалом для ін'єкційних розчинів. Медичне скло – твердий розчин, який одержують в результаті розплавлення суміші сілікатів, оксидів металів і солей. Найбільшу термічну і хімічну стійкість має скло, яке одержують з кварцевого піску з вмістом 95-98% кремнію диоксиду. Таке скло має температуру плавлення 1550-1800 ºC, і тому виготовляти з нього ампули досить важко. Для зниження температури плавлення в склад скла додають різні модифікатори: натрію і калію оксиди, однак при цьому різко зменшується хімічна стійкість скла. Підвищення хімічної стійкості скла досягається введенням в склад алюмінію та барію оксидів. Оксид молібдену значно збільшує термічну стійкість скла. Таким чином, вводячи в склад скла певні окисли і змінюючи їх концентрації, отримують скло з наперед заданими фізико-хімічними властивостями. Марки медичного скла і їх призначення: НС-З – нейтральне скло для виготовлення ампул і флаконів для розчинів речовин, які піддаються гідролізу, оксидаціїї і т.і. (напр., розчини солей алкалоїдів). НС-І – нейтральне скло для ампулювання менш чутливих до лугів лікарських речовин (розчини натрію хлориду, магнію сульфату, кальцію хлориду та ін.). СНС-І – світлозахисне нейтральне скло для виготовлення ампул з розчинами світлочутоивих лікарських речовин. АБ-І – лужне (ампульне безбарвне) скло для ампул і флаконів для наповнення стійкими в олійних розчинах речовинами, оскільки в цьому випадку вилужнювання практично не проходить. ХТ-І – хімічно і термічно стійке скло для виготовлення шприців, пляшок для зберігання крові, трансфузійних і інфузійних препаратів. МТО – медичне тарне знебарвлене скло для виготовлення флаконів, банок і предметів догляду за хворими. ОС, ОС-І – оранжеве тарне скло для виготовлення флаконів і банок. НС-2, НС-2А – нейтральне скло для виготовлення флаконів для крові, трансфузійних та інфузійних препаратів та аерозольних балонів. До ампульного скла ставлять наступні вимоги: прозорість – для візуального і оптичного контролю на відсутність механічних домішок; безколірність – дозволяє спостерігати, крім механічних домішок, і зміну кольору розчину; легкоплавкість – необхідне для запаювання ампул, наповнених розчином, при порівняно невисокій температурі, запобігаючи його нагріванню; термічна стійкість – здатність скла не розкладатися при різких коливаннях температури (витримувати стерилізацію); хімічна стійкість – гарантуюча збереженість лікарської речовини та інших компонентів препарату; механічна стійкість – для витримування навантажень при обробці ампул у процесі виробництва, транспортування і зберігання. При контакті з розчинами на внутрішній поверхні скла в ампулах і флаконах під час зберігання і особливо при тепловій стерилізації (залежно від марки і значення рН розчину) може проходити вилужування або розчинення компонентів скла. У нейтральних і кислих розчинах при взаємодії з водою і кислотами лужні іони натрію і калію переходять в розчин, викликаючи деяку зміну рН, а на поверхні скла утворюється захисна плівка кремнієвої кислоти. По мірі взаємодії товщина плівки збільшується за рахунок малого ступеня дисоціації і слабкої реакційної здатності цієї кислоти, дифузія затруднюється і процес різко сповільнюється. У лужних розчинах проходить розчинення лужних і кислотних компонентів скла. Розривається зв'язок Si-O-Si з утворенням натрію і калію силікатів, при цьому розчиняється поверхневий шар погано розчинних магнію і кальцію силікатів, але концентрація цих сполук недостатня для формування суцільної і міцної плівки. Тому при зберіганні в ампулах із скла з недостатньою хімічною стійкістю плівка відшаровується, утворюючи механічні включення, що недопустимо в ін'єкційних розчинах. Основні показники якості медичного скла. Лугостійкість. Метод визначення лугостійкості оснований на дії на зразки скла площиною 0,10-1,15 дм3 суміші рівних об'ємів 0,5 М р-ну натрію карбонату і 0,1 М р-ну натрію гідроксиду при кипінні протягом 3 годин. Перед дослідженням і після зразки ретельно миють, висушують при температурі 140 ºC до постійної маси і зважують. Лугостійкість скла (мг/дм2) розраховують за формулою:
![]() .де,
М – маса зразка до оброблення, мг М1
– маса зразка після дії лугу, мг S
– площа поверхні зразка, дм2
Скло
відносять до класу лужності: 1
клас – до 75 мг/дм2
; 2
клас – вище 75 до 175; 3 клас – вище 175.
Водостійкість.
Зразки подрібненого (0,315 мм) скла
знежирюють етанолом і ацетоном, сушать
при температурі 140 ºC. Три т.н. по 10,0 г
поміщають у конічні колби на 250 мл з 50
мл свіжоперекип’яченої води дистильованої
з доведенням рН до вихідного (5,5). У дві
контрольні колби наливають лише воду
дистильовану свіжоперекип’ячену. Колби
закривають і автоклавують 30 хв при
температурі 121 ºC (0,10-0,11 мПа). Потім їх
охолоджують, додають по 2 кр. метилового
червоного і титрують 0,02 моль/дм3
розчином
кислоти хлоридної до переходу забарвлення
розчину від жовтого кольору до оранжевого.
Водостійкість скла Х (мл/г) при температурі
121 ºC вираховується за формулою:
.де,
М – маса зразка до оброблення, мг М1
– маса зразка після дії лугу, мг S
– площа поверхні зразка, дм2
Скло
відносять до класу лужності: 1
клас – до 75 мг/дм2
; 2
клас – вище 75 до 175; 3 клас – вище 175.
Водостійкість.
Зразки подрібненого (0,315 мм) скла
знежирюють етанолом і ацетоном, сушать
при температурі 140 ºC. Три т.н. по 10,0 г
поміщають у конічні колби на 250 мл з 50
мл свіжоперекип’яченої води дистильованої
з доведенням рН до вихідного (5,5). У дві
контрольні колби наливають лише воду
дистильовану свіжоперекип’ячену. Колби
закривають і автоклавують 30 хв при
температурі 121 ºC (0,10-0,11 мПа). Потім їх
охолоджують, додають по 2 кр. метилового
червоного і титрують 0,02 моль/дм3
розчином
кислоти хлоридної до переходу забарвлення
розчину від жовтого кольору до оранжевого.
Водостійкість скла Х (мл/г) при температурі
121 ºC вираховується за формулою:
![]() ,де,
V1
− об'єм р-ну кислоти хлоридної, який
витрачено на титрування досліджуваного
розчину, мл; V2
−
середній об'єм р-ну кислоти хлоридної,
який витрачено на титрування кожного
контрольного досліду, мл; М – маса скла,
г Скло
відносять до класу водостійкості: 1
клас – до 0,10 мл/г (розхід 0,02 М р-ну НСІ
при титруванні) 2 клас – від 0,10 до 0,85 3
клас – від 0,85 до 1,50 Термічна
стійкість.
50
ампул витримують при температурі 18 ºC
30 хв, поміщують в сушильну шафу не менше
ніж на 15 хв при температурі не менше 180
ºC для ампул з скла марки НС-3, 150 ºC для
марки скла НС-1, 170 ºC – СНС-1 і 130 ºC – АБ-1.
після нагрівання ампули швидко за 5 с
вивантажують і занурюють у воду
температури 20 ºC±1, витримують не менше
1 хв. Термостійкими, тобто залишитися
цілими повинні не менше 98% ампул від
взятих на перевірку. Хімічна
стійкість.
Ампули
відкривають, промивають двічі водою
дистильованою температури 65±5 ºC і
заповнюють водою дистильованою з рН
6,0±0,2 до номінального об'єму. Запаюють
і стерилізують парою під тиском (автоклав)
при 0,10-0,11 мПа (121±1 ºC) протягом 30 хв. Потім
ампули охолоджують до температури 20±5
ºC не довше ніж за 60 хв, перевіряють
герметичність, відкривають капіляри
ампул і беруть для визначення рН воду
з ампул 15 мл. (рН-метр, потенціометрично).
Визначають значення рН вихідної води.
Зміна (зсув) значення рН води вихідної
(до стерилізації) і води після стерилізації
встановлена для ампул: з скла НС-3 на 0,9
СНС-1 – 1,2 НС-1 – 1,3 АБ-1 – 4,5 Раніше для
визначення хімічної стійкості ампульного
скла використовували індикаторний
метод (метиловий червоний, фенолфталеїн,
універсальний індикатор). Про хімічну
стійкість судили по зміні кольору після
стерилізації. Залишкові
напруги. Вони
утворюються при виготовленні ампул
внаслідок нерівномірного нагрівання
різних ділянок склодроту. Визначають
залишкові напруги за допомогою
поляризаційно-оптичного методу по
різниці ходу променів у зразку на
полярископі – поляриметрі ПКС-125, ПКС-250
і на полярископі ПКС-500. не допускається
залишкова напруга, яка містить різницю
ходу ∆1
більше
8 млн -1
.
Світлозахисні
властивості.
Визначають
методом світлопропускання в ділянці
спектра від 290 до 450 нм з інтервалом 20
нм. Із циліндричної частини ампули
вирізають зразок, протирають його і
поміщають паралельно щілині спектрофотометра
СФД-2. максимальний відсоток світлопропускання
має становити
,де,
V1
− об'єм р-ну кислоти хлоридної, який
витрачено на титрування досліджуваного
розчину, мл; V2
−
середній об'єм р-ну кислоти хлоридної,
який витрачено на титрування кожного
контрольного досліду, мл; М – маса скла,
г Скло
відносять до класу водостійкості: 1
клас – до 0,10 мл/г (розхід 0,02 М р-ну НСІ
при титруванні) 2 клас – від 0,10 до 0,85 3
клас – від 0,85 до 1,50 Термічна
стійкість.
50
ампул витримують при температурі 18 ºC
30 хв, поміщують в сушильну шафу не менше
ніж на 15 хв при температурі не менше 180
ºC для ампул з скла марки НС-3, 150 ºC для
марки скла НС-1, 170 ºC – СНС-1 і 130 ºC – АБ-1.
після нагрівання ампули швидко за 5 с
вивантажують і занурюють у воду
температури 20 ºC±1, витримують не менше
1 хв. Термостійкими, тобто залишитися
цілими повинні не менше 98% ампул від
взятих на перевірку. Хімічна
стійкість.
Ампули
відкривають, промивають двічі водою
дистильованою температури 65±5 ºC і
заповнюють водою дистильованою з рН
6,0±0,2 до номінального об'єму. Запаюють
і стерилізують парою під тиском (автоклав)
при 0,10-0,11 мПа (121±1 ºC) протягом 30 хв. Потім
ампули охолоджують до температури 20±5
ºC не довше ніж за 60 хв, перевіряють
герметичність, відкривають капіляри
ампул і беруть для визначення рН воду
з ампул 15 мл. (рН-метр, потенціометрично).
Визначають значення рН вихідної води.
Зміна (зсув) значення рН води вихідної
(до стерилізації) і води після стерилізації
встановлена для ампул: з скла НС-3 на 0,9
СНС-1 – 1,2 НС-1 – 1,3 АБ-1 – 4,5 Раніше для
визначення хімічної стійкості ампульного
скла використовували індикаторний
метод (метиловий червоний, фенолфталеїн,
універсальний індикатор). Про хімічну
стійкість судили по зміні кольору після
стерилізації. Залишкові
напруги. Вони
утворюються при виготовленні ампул
внаслідок нерівномірного нагрівання
різних ділянок склодроту. Визначають
залишкові напруги за допомогою
поляризаційно-оптичного методу по
різниці ходу променів у зразку на
полярископі – поляриметрі ПКС-125, ПКС-250
і на полярископі ПКС-500. не допускається
залишкова напруга, яка містить різницю
ходу ∆1
більше
8 млн -1
.
Світлозахисні
властивості.
Визначають
методом світлопропускання в ділянці
спектра від 290 до 450 нм з інтервалом 20
нм. Із циліндричної частини ампули
вирізають зразок, протирають його і
поміщають паралельно щілині спектрофотометра
СФД-2. максимальний відсоток світлопропускання
має становити
35% при товщині стінки від 0,4 до 0,5 мм;
30% − від 0,5 до 0,6 мм;
27% − від 0,6 до 0,7 мм;
25% − від 0,7 до 0,8 мм;
20% − від 0,8 до 0,9 мм.
Допустимі грані показують, що для повного світлозахисту ампули упаковують в картонні упаковки, краще чорного або червоного кольору. Вимоги до ампульного скла ставлять наступні: прозорість – для візуального і оптичного контролю на відсутність механічних домішок; безколірність – дозволяє спостерігати, крім механічних домішок, і зміну кольору розчину; легкоплавкість – необхідне для запаювання ампул, наповнених розчином, при порівняно невисокій температурі, запобігаючи його нагріванню; термічна стійкість – здатність скла не розкладатися при різких коливаннях температури (витримувати стерилізацію); хімічна стійкість – гарантуюча збереженість лікарської речовини та інших компонентів препарату; механічна стійкість – для витримування навантажень при обробці ампул у процесі виробництва, транспортування і зберігання.Основні показники якості медичного скла.
Лугостійкість: 1 клас – до 75 мг/дм2 2 клас – вище 75 до 175 3 клас – вище 175.
Водостійкість: 1 клас – до 0,10 мл/г (розхід 0,02 М р-ну НСІ при титруванні) 2 клас – від 0,10 до 0,85 3 клас – від 0,85 до 1,50.
Термічна стійкість. (не менше 98% ампул).
Хімічна стійкість. зміна (зсув) значення рН води зі скла НС-3 на 0,9 СНС-1 - 1,2 НС-1 - 1,3 АБ-1 - 4,5.
Залишкові напруги. не допускається більше 8 млн -1.
Світлозахисні властивості. максимальний відсоток світлопропускання має становити:
35% при товщині стінки від 0,4 до 0,5 мм;
30% − від 0,5 до 0,6 мм;
27% − від 0,6 до 0,7 мм;
25% − від 0,7 до 0,8 мм;
20% − від 0,8 до 0,9 мм.
50. Способи очистки розчинів для ін'єкцій. С 536
51. Розчинники, що застосовують у виробництві ін'єкційних розчинів. Вимоги до них. Вода (вода для ін’єкцій і вода очищена); неводні розчинники (природного, синтетичного і напівсинтетичного походження) – жирні олії, етилолеат; комплексні розчинники (гліцерин, пропіленгліколь, ПЕО 400, бензилбензоат, бензиловий і етиловий спирти та ін.) Вимоги до розчинників: висока розчинна здатність; фармакологічна індиферентність; хімічна сумісність; стійкість при зберіганні; доступність і дешевизна. За ДФ „Вода для ін’єкцій” має задовольняти всі вимоги до води очищеної і бути апірогенною.В для ін’єкційних розчинів одержують методом перегонки питної чи знесоленої води в спеціальних аквадистиляторах. Фармакопея США дозволяє, крім цього, використовувати зворотній осмос. Підготовка води включає: осадження кальцію і магнію гідрокарбонатів за допомогою кальцію гідроксиду; осадження кальцію і магнію сульфатів та хлоридів – натрію гідрокарбонатом; коагуляцію колоїдних домішок і зв’язування аміаку – алюмінію сульфатом чи алюмокалієвими галунами; руйнування органічних речовин і мікроорганізмів – калію перманганатом (25 мг/л); вилучення домішок за допомогою іонного обміну катіонітами КУ-І, КУ-2, КУ-23 і аніонітами ЭДЭ-1ОП, АВ-171. Основними вузлами аквадистиляторів є: випарювач, конденсатор; збірник.
У промислових умовах для одержання ВдІ використовують одно- та багатоступеневі аквадистилятори („Фін-аква” – Фінляндія, „Вапонікс” – США, термокомпресійні аквадистилятори). Вони мають один, три і більше, відповідно, корпусів, які розміщені вертикально або горизонтально.
Максимальний термін зберігання ВдІ– 24 години (в асептичних умовах). Бажаним є використання свіжовиготовленої води. Надійне зберігання гарантується в спеціальних системах з інертного матеріалу, де вода знаходиться при температурі 80-95 ºC і постійному русі (швидкість 1-3 м/с). Неводні розчинники. Використання цих розчинників викликане необхідністю одержання розчинів із речовин, які не розчиняються або важко розчиняються у воді, пролонгування дії, виключення впливу скла на розчин і підвищення стабільності. До неводних розчинників ставляться додаткові вимоги: прозорість, термостійкість, температура кипіння – більше 100 ºC (для проведення теплової стерилізації), температура замерзання – не вище + 5ºC, біологічна сумісність за величиною осмотичного тиску і значенню рН середовища, в’язкість і текучість розчинів не повинні сповільнювати всмоктування, затруднювати фільтрування і наповнення ампул, хімічна чистота і стабільність. По токсичності вони мають відноситись до групи практично не шкідливих речовин (ЛД50 для щурів при підшкірному введенні 1501-4500 мг/кг) або малотоксичних (ЛД50 −151-1501 мг/кг). За хімічною природою неводні розчинники поділяються на: одноатомні спирти (етанол); багатоатомні спирти (пропіленгліколь, бутиленгліколь, гліцерин); ефіри прості і складні (метиловий або етиловий ефіри олеїнової кислоти, бензилбензоат); аміди (метилацетамід, диметилацетамід); олії жирні (рослинні: мигдалева, пресикова, абрикосова і оливкова); сульфоксиди і сульфони (диметилсульфоксид, тетраметиленсульфон).
52. Оцінка якості ампульного скла. Хімічна стійкість. Якість ампульного скла у фармацевтичній практиці
оцінюють за такими параметрами: візуальний контроль; водостійкість; лугостійкість; залишкові напруги; термічна стійкість; хімічна стійкість; світлозахисні властивості (для скла марки СНС-1), радіальне биття стебла ампул відносно корпуса, відхилення від округлості ампул, для ампул вакуумного наповнення проводять визначення глибини розрідження з метою точного наповнення ампул за допомогою вакууму, легкоплавність.. Для ампул марки УСП-1 уведені додаткові вимоги: сила зламу ампул із кольоровим кільцем; радіальне биття стебла ампул; відхилення від округлості ампул. Основні фізико-хімічні властивості ампульного скла мають відповідати вимогам, зазначеним у ТУ У 480945-005-96. Водостійкість. Три проби, взяті з 300 г здрібненого скла масою по 11,0 г, знежирюють етанолом та ацетоном і сушать при температурі 140 °С. Три точні наважки по 10,0 г поміщають у колби з 50 мл свіжоперевареної води очищеної з вихідним значенням
рН = 5,5. Колби закривають і стерилізують 30 хв при температурі 121°С і тискові 0,10—0,11 мПа. Після охолодження їх вміст титрують розчином 0,02 моль/л кислоти хлороводневої в присутності метилового червоного до перетворення забарвлення розчину від жовтого кольору до оранжевого. Водостійкість скла X, мл/г, обчислюють за формулою:
X
=
![]() ,
деV1
— об’єм розчину кислоти хлороводневої,
витрачений на титрування досліджуваного
розчину, мл; V2
- середній об’єм розчину кислоти
хлороводневої, витрачений на титрування
кожного з двох контрольних дослідів,
мл; m
- маса скла, г. Лугостійкість. Метод
ґрунтується на впливі суміші рівних
об’ємів розчину 0,5 моль/л натрію карбонату
і розчину 0,1 моль/л натрію гідрокарбонату
на зразки скла площею 0,10-0,15 дм2 при
кип’ятінні протягом 3 год. Перед
випробуванням і після дії лужних розчинів
зразки миють, висушують при температурі
140°С до сталої маси і зважують.
,
деV1
— об’єм розчину кислоти хлороводневої,
витрачений на титрування досліджуваного
розчину, мл; V2
- середній об’єм розчину кислоти
хлороводневої, витрачений на титрування
кожного з двох контрольних дослідів,
мл; m
- маса скла, г. Лугостійкість. Метод
ґрунтується на впливі суміші рівних
об’ємів розчину 0,5 моль/л натрію карбонату
і розчину 0,1 моль/л натрію гідрокарбонату
на зразки скла площею 0,10-0,15 дм2 при
кип’ятінні протягом 3 год. Перед
випробуванням і після дії лужних розчинів
зразки миють, висушують при температурі
140°С до сталої маси і зважують.
Лугостійкість
скла X,
мг/дм2, розраховують за формулою: X
=
![]() ,
де m
— маса зразка до обробки, мг;m1
-
маса зразка після дії лугів, мг; S
- площа поверхні зразка, дм2.
Залишкові
напруги.
Чим різкіше охолодження, тим більш
значний температурний перепад усередині
скла і тим більшими будуть сили розтягу
в поверхневих і сили стиску у внутрішніх
,
де m
— маса зразка до обробки, мг;m1
-
маса зразка після дії лугів, мг; S
- площа поверхні зразка, дм2.
Залишкові
напруги.
Чим різкіше охолодження, тим більш
значний температурний перепад усередині
скла і тим більшими будуть сили розтягу
в поверхневих і сили стиску у внутрішніх
шарах стінок ампул. При швидкому нагріванні ампул, навпаки, у зовнішніх шарах стінок виникають сили стиску, а у внутрішніх - сили розтягу. Опір скла стискові в багато разів вищий від опору його розтягові. Тому ампули, як і інші скляні вироби, більш термостійкі при швидкому нагріванні, ніж при швидкому охолодженні. Напруги, що залишилися в склі після охолодження, нази залишковими; якщо напруги зникають, то їх наз тимчасовими. Залишкові напруги здебільшого і визначають термічну стійкість ампул або флаконів. Напруги утворюються при виготовленні ампул завдяки нерівномірному нагріванню різних ділянок дроту. Залишкові напруги визначають поляризаційно-оптичним методом за різницею проходження променів у досліджуваному зразку, якщо він має залишкову напругу, за допомогою полярископа-поляриметра ПКС-125, ПКС-250 і полярископа ПКС-500. Різницю ходу променів ∆ (нм) обчислюють за формулою:
![]() ,де
,де
![]() — при зеленому світлофільтрі (540 нм);
— при зеленому світлофільтрі (540 нм);
![]() — кут повороту лімба аналізатора, град.
— кут повороту лімба аналізатора, град.
Різницю
ходу
![]() 1,
віднесену до 1 см шляху променя в склі,
млн–1,обчислюють
за формулою:
1,
віднесену до 1 см шляху променя в склі,
млн–1,обчислюють
за формулою:
![]() ,
де
,
де
![]() - довжина шляху променя в напруженому
склі, cм. Не допускається залишкова
напруга, яка містить питому різницю
ходу ∆1
більше 8 млн-1.
Для зняття залишкових напруг скляні
вироби піддають відпалу. Термічна
стійкість.
Ампули повинні мати термічну стійкість,
тобто не руйнуватися при різких
коливаннях температури (при стерилізації).
Перевірку термічної стійкості проводять
згідно з ГОСТом 17733. 50 ампул витримують
при температурі 18 °С 30 хв, потім поміщають
у сушильну шафу не менше ніж на 15 хв при
температурі, зазначеній в ГОСТі. Після
цього ампули занурюють у воду з
температурою 20±1°С і витримують не менше
1 хв. Термостійкими повинні бути не менше
98 % ампул від узятих на перевірку. Ампули
із деяких марок скла мають витримувати
перепади температур, наведені у табл.
19.5. До ампульного скла висувають такі
вимоги: безбарвність і прозорість - для
контролю на відсутність механічних
включень і можливості виявлення ознак
псування розчину; легкоплавкість - для
здійснення якісної запайки ампул;
водостійкість;
- довжина шляху променя в напруженому
склі, cм. Не допускається залишкова
напруга, яка містить питому різницю
ходу ∆1
більше 8 млн-1.
Для зняття залишкових напруг скляні
вироби піддають відпалу. Термічна
стійкість.
Ампули повинні мати термічну стійкість,
тобто не руйнуватися при різких
коливаннях температури (при стерилізації).
Перевірку термічної стійкості проводять
згідно з ГОСТом 17733. 50 ампул витримують
при температурі 18 °С 30 хв, потім поміщають
у сушильну шафу не менше ніж на 15 хв при
температурі, зазначеній в ГОСТі. Після
цього ампули занурюють у воду з
температурою 20±1°С і витримують не менше
1 хв. Термостійкими повинні бути не менше
98 % ампул від узятих на перевірку. Ампули
із деяких марок скла мають витримувати
перепади температур, наведені у табл.
19.5. До ампульного скла висувають такі
вимоги: безбарвність і прозорість - для
контролю на відсутність механічних
включень і можливості виявлення ознак
псування розчину; легкоплавкість - для
здійснення якісної запайки ампул;
водостійкість;
механічна міцність - для витримування навантажень при обробці ампул у процесі виробництва, транспортуванні та зберіганні (ця вимога має поєднуватися з необхідною крихкістю скла для легкого розкривання капіляра ампул); термічна стійкість - здатність скла не руйнуватися при різких коливаннях температури, зокрема, при стерилізації; хімічна стійкість, яка гарантує незмінність складу всіх компонентів препарату; питома поверхня контакту розчину зі склом - чим більша ця величина, тим більшою повинна бути хімічна стійкість скла. Хімічна стійкість. Для оцінки хімічної стійкості ампульного скла існують різні методи визначення: за допомогою різних кислотно-основних індикаторів (зміна забарвлення), за допомогою рН-метра (зсув рН); вагові методи (кількість вилужених компонентів із зважених скляних зразків при контактуванні з водою) тощо. Як контрольні зразки зазвичай береться вода очищена і різні спеціальні розчини лікарських речовин, що контактуватимуть зі склом ампул при виготовленні ін’єкційних розчинів і їх зберіганні. Офіцинальним методом визначення хімічної стійкості ампульного скла є метод визначення за допомогою рН-метра, прийнятий ОСТом 64-2-485—85. Для цього ампули, двічі промиті гарячою водою, двічі обполіскують водою демінералізованою і заповнюють водою очищеною, що має рН = 6,0±2,0 і температуру 20±5°С, до номінальної місткості. Запаяні ампули стерилізують в автоклаві при тискові 0,10—0,11 МПа і температурі 120±1 °С протягом 30 хв. Потім ампули охолоджують до температури 20±5°С, перевіряють їхню герметичність і розкривають капіляри. За допомогою рН-метра визначають зсув рН води, вийнятої з ампул, стосовно рН вихідної води. Встановлено норми зміни значення рН для ампул: скла УСП-1 — не більше 0,8; НС-3 - 0,9; СНС-1 - 1,2; НС-1 - 1,3; АБ-1 - 4,5. З інших відомих методів своєю простотою вирізняється метод визначення хімічної стійкості ампульного скла за допомогою кислотно-основного індикатору фенолфталеїну (запропонований Д. І. Поповим і Б. А. Клячкіною). Для цього ампули заповнюють водою для ін’єкцій із додаванням 1 краплі 1 %-вого розчину фенолфталеїну на кожні 2 мл води, запаюють і стерилізують при 120 °С протягом 30 хв. Ампули, в яких вода після стерилізації не забарвилась, належать до першого класу. Вміст забарвлених ампул титрують розчином 0,01 моль/л кислоти хлороводневої, за кількістю якої визначається хімічна стійкість ампульного скла. Якщо на титрування до знебарвлення розчину її витрачено менше 0,05 мл, ампули належатдо другого класу, більше 0,05 мл - ампули вважаються непридатними для зберігання ін’єкційних розчинів. Можна також визначити хімічну стійкість ампульного скла за зміною забарвлення метилового червоного. При цьому ампули заповнюють кислим розчином метилового червоного до необхідного об’єму, запаюють і стерилізують у стерилізаторі при 120°С протягом 30 хв. Якщо після охолодження колір всіх ампул не змінився на жовтий, то такі ампули придатні для використання. Хімічна стійкість характеризує опірність скла руйнівної дії агресивних середовищ. Присутність катіонів лужних металів викликає розпушення тетраедричних кристалічних ґраток, зниження в’язкості і температури його плавлення. Іони цих металів у склі зв’язані між собою відносно слабко і тому мають значну рухливість. Скло як складний сплав при тривалому контакті з водою або водними розчинами (особливо при нагріванні) виділяє зі своєї поверхні окремі складові частини, тобто піддається процесу вилужування або розчиненню верхнього шару скла.
Світлозахисні властивості. Ці властивості досліджують в ампулах, виготовлених з нейтрального світлозахисного скла вимірюванням їхнього світлопропускання в ділянці спектра від 290 до 450 нм (ГОСТ 17651—72). З циліндричної частини ампули вирізають зразок, ретельно промивають його, протирають, висушують і поміщають паралельно щілині спектрофотометра СФД-2. Визначають максимальний відсоток світлопропускання, що повинний складати при товщині стінки ампули від 0,4 до 0,5 мм 35 %; від 0,5 до 0,6 мм - 30 %; від 0,6 до 0,7 мм - 27 %; від 0,7 до 0,8 мм - 25 % і від 0,8 до 0,9 мм - 20 %.
Хімічну стійкість внутрішньої поверхні ампул можна підвищити, змінивши її поверхневу структуру. Під дією на скло водяної пари або сульфуру діоксиду і водяної пари при підвищеній
температурі на склі утворюється шар натрію сульфату, а іони натрію в склі частково заміняються водневими іонами. Збагачений Н-іонами, шар має підвищену механічну міцність і утруднює подальшу дифузію іонів лужних металів. Однак такі шари мають невелику товщину і при тривалому зберіганні препарату в ампулі процес виділення лугу може відновитися. Найчастіше застосовується спосіб обробки поверхні ампул силіконами. Силікони - це силіційорганічні сполуки такої будови:
CH, CH, CH, CH,
6 6 6 6
CH, - Si — O — Si — O — Si — O… — Si — CH„
б б
CH„ CH, CH, CH,
6 6 6 6
53. Характеристика мембранного та глибинного фільтрування. Матеріали для виготовлення фільтрів. Для фільтрування розчинів використовують найчастіше 2 типи фільтрів: глибинні (об’ємні) фільтри (тканеві або ватно-марлеві фільтри, азбестові, фільтри із запечених частинок скла чи металу, багатошарові паперові або виготовлені із синтетичних волокон), мембранні (екранові) фільтри (плівки із пластмас, ефіру целюлози, лавсану, капрону та ін.).
Самим сучасним із мембранних методів фільтрування є метод мембранного мікрофільтрування – мембранне розділення колоїдних розчинів і мікрозавісин під дією тиску (мембранні мікрофільтри: Міллер, Сарторіус, Синпер, Нуклеопор, Дюрапор, Владіпор типу МФА-А №2 і №1 із ацетату целюлози, Міфіл із поліаміду).
Матеріали для фільтрів: тканини з натурального бавовняного волокна (бельтинг, полотно, саржа, марля тощо); тканини з вовни (сукна); синтетичні тканини (поліхлорвінілові, поліамідні, лавсанові, тефлонові волокна). тканини з неорганічного волокна (скловолокно, азбестове, металеве). нетканні фільтри (фільтрувальний папір, целюлоза, азбест, біла глина, активоване вугілля).
Фільтрувальні матеріали повинні максимально захищати pозчин від контакту з повітрям; затримувати дуже дрібні частинки і мікроорганізми; мати високу механічну міцність, щоб запобігати виділенню волокон і механічних включень; пpотидіяти гідpавлічним удаpам і не змінювати функціональні хаpактеpистики; не змінювати фізико-хімічний склад і властивості фільтpату; не взаємодіяти з лікарськими, допоміжними речовинами і pозчинниками; витримувати теплову стеpилізацію. Фільтрувальні матеріали перед застосуванням повинні бути обов’язково промиті до повного видалення розчинних речовин, твердих частинок або волокон. Вибір фільтрувальних перегородок зумовлюється фізико-хіміч-
ними властивостями фільтрованого розчину (розчинювальна здатність рідкої фази, леткість, в’язкість, рН середовища та ін.), концентрацією і дисперсністю твердої фази, вимогами до якості фільтрату, масштабами виробництва тощо. При виробництві розчинів для ін’єкцій та інфузій найчастіше використовують грубе і тонке фільтpування як основне або попереднє, що передує мікрофільтрації і ультрафільтрації. Фільтpувальні пеpегоpодки, використовувані для цієї мети, можуть затримувати частинки як на повеpхні, так і вглибині фільтpувального матеpіалу. У залежності від механізму затримування частинок pозрізняють фільтpи глибинні (пластинчасті) і повеpхневі, або мембpанні. Глибинне фільтрування. Пpи глибинному фільтpуванні частинки затримуються на повеpхні і, головним чином, у товщі капіляpно-поpистого фільтpу. Уловлювання частинок відбувається за рахунок механічного гальмування й утримання в місці пеpетину волокон фільтpувальної пеpегоpодки; у pезультаті адсоpбції на фільтpувальному матеpіалі або на ділянці капіляpу, що має вигин або непpавильну фоpму; за рахунок електpокінетичної взаємодії. Ефективність фільтpа залежить від діаметpа, товщини волокна і щільності стpуктуpи фільтpа. Цей спосіб фільтpації доцільно за стосовувати для малоконцентpованих розчинів (з об’ємною часткою твеpдої фази менше 1%, тому що поступово відбувається закупоpювання поp і зростає опір пеpегоpодки). Глибинні фільтpи виробляються з волокнистого і зеpнистого матеpіалу, тканих, спpесованих, спечених або іншим чином з’єднаних матеріалів, які утворюють поpисту стpуктуpу. Пpикладами волокнистих матеpіалів натурального походження можуть служити шеpсть, шовк, бавовняні тканини, вата, джут, лляна тканина, азбест, целюлозне волокно. Сеpед штучних волокон можна виділити: ацетатне, акpилове, фтоpовуглецеве, скловолокно, металеве і металокеpамічне волокно, нейлон, капpон, лавсан. Використовують побутові і технічні тканини: мадаполам, бельтинг, фільтpобельтинг, міткаль, фільтpоміткаль, хлоpин, тканина ФПП, целюлозна тканина типу «Фільтрак». Із зеpнистих матеpіалів найбільше поширені діатоміт, пеpліт, вугілля активоване та ін. Діатоміт одержують із кpемнеземних панциpів водоростей - діатомей. Пеpліт - це склоподібна гірська поpода вулканічного походження, використовується в основному для виготовлення патpонних фільтpів. Зеpнисті матеpіали знайшли своє застосування для фільтpування важкофільтpованих рідин (біологічні рідини, pозчин желатину для ін’єкцій і т. д.). Глибинні фільтри і пеpедфільтpи, які містять азбестові й скляні волокна, не повинні застосовуватися для паpентеpальних pозчинів із-за можливого виділення шкідливих для оpганізму волокон. Велика повеpхня адсоpбції може пpизвести до втрат діючих речовин на фільтpі, а затримання в поpах мікpооpганізмів - до їх pозмноження і забруднення фільтpату. Тому pекомендується такі фільтpи експлуатувати не більше 8 год. Мембранне фільтрування. Повеpхневе фільтpування відбувається з утворенням осаду на повеpхні пеpегоpодки. Осад утворює додатковий фільтpувальний шар і поступово збільшує загальний гідpавлічний опір просуванню рідини. Роль пеpегоpодки у цьому разі полягає в механічному затриманні частинок. До цієї гpупи належать мембpанні фільтpи. Пpи мембpанному, або ситовому фільтpуванні, усі частинки, що мають pозміp більший, ніж pозміp поp фільтpа, затримуються на повеpхні. М фільтpи виготовлені з полімеpних матеpіалів. Фтоpопластові мембpани стійкі в pозведених і концентpованих pозчинах кислот, лугів, спиpтів, етеpів, хлоpофоpму та масел. Hейлонові й поліамідні - у сильних лугах та хлоpофоpмі. Поліамідні обмежено сумісні зі спиpтами. Заводи-виробники вказують рідини, які не підлягають фільтpуванню, і граничні значення pН, що витримують цей матеpіал. Для ситового фільтpування використовують мембpани сітчастого типу, які називають ядеpними, або капіляpно-поpистими. Такі мембpани виготовляють із міцних полімеpних матеpіалів (полікаpбонат, лавсан та інших), які піддають бомбаpдуванню в ядеpному pеактоpі. Товщина таких фільтpувальних пеpегоpодок складає 5—10 мкм. Нині у фаpмацевтичній пpомисловості за кордоном використовують мембpани сітчастого типу фірми «Нуклепоре» і «Джелман» (із кополімеpів акpилонітpилу і вінілілденхлоpиду та ін.). Мікpопоpисті мембpани використовуються для очищення pозчинів, що містять не більше 0,1 % твеpдих частинок. Ситовий ефект мембpанних фільтpів пояснює швидке їх засмічування по відношенню до глибинних. Тому для фільтpування ін’єкційних pозчинів найбільш пеpспективним є поєднання обох типів фільтpувальних сеpедовищ або використання системи серійної фільтрації, коли фільтрувальний розчин послідовно проходить через декілька мембранних фільтрів з розмірами пор, які зменшуються в прогресії. Пpичому мембpанні пеpегоpодки мають застосовуватись
в заключній стадії очищення, головним чином, для звільнення від дрібних частинок і мікроорганізмів.
54. Способи стерилізації ін'єкційних розчинів у флаконах та шприц-тюбиках.
55. Способи стерилізації ін'єкційних розчинів в ампулах. Контроль стерильності. Поняття про стерильну серію. Методи стерилізації: термічні методи (паровий, повітряний); хімічні методи (газовий і з використанням розчинів); стрилізація фільтруванням; радіаційний метод стерилізації.
Теплова стерилізація насиченою парою під тиском проводиться при температурі 120 ±2ºC (залишковий тиск 1,1 ± 0,2 гкс /см2) або 132±2 0С (2,2 ± 0,2 кгс/см2) в парових стерилізаторах типу АП-7, АП-18 – автоклавах. Теплова повітряна стерилізація проводиться при температурі 180-200 0С у стерилізаторах з ламінарним потоком стерильного повітря нагрітого до відповідної температури.
Газова стерилізація проводиться в газових стерилізаторах або мікроанаеростатах для термолабільних речовин. Як стерилізуючі агенти використовують: оксид етилену або його суміш з різними флегматизаторами (бромистим метилом, СО2, хладонами та ін.). час стерилізації 4-6 годин при температурі 43-45 0С під тиском 196133 н/м2. Стерилізація фільтруванням за допомогою мембранних чи інших фільтрів з розміром пор 0,22-0,3 мкм. Розглядалось вище. Радіаційна стерилізація. Опромінення проводять на гамма-установках, прискорювачах електронів або інших джерелах іонізуючого випромінювання дозою 25 кГр (2,5 Мрад) чи ін.
56. Способи запайки ампул, їх види та переваги. Перевірка ампул на герметичність (до та після стерилізації). Запаювання ампул здійснюється 3 способами за допомогою газових пальників. 1. оплавлення капілярів (ць рівномірно запаюється. 2. пневматичного відтягування капіляру (автомат 541) – ампула притискаєтьсянапівавтомат АП-6М) – ампули в комірках транспортера обертаючись навколо осі проходять повз пальники і кіне до роликів, обертається. Пальники розігрівають ділянку капіляру на місці запаювання, а струмені стиснутого повітря відтягують відпаяну частину капіляра. 3. нагріванням за допомогою електричного опору проводиться для ампул з вогне- та вибухонебезпечними розчинами. Капіляр ампули вводять в електричний ніхромовий нагрівник, скло розм’якшується, капіляр відтягується і оплавлюється.
Два основні способи запаювання ампул із використанням газових пальників: оплавленням кінчиків капілярів, коли в ампули, яка безперервно обертається, нагрівають кінчик капіляра, і скло, розм’якшуючись, само заплавляє отвір капіляра; відтягуванням капілярів, коли в капілярі ампули відпаюють із відтягуванням частини капіляра й у процесі відпайки запаюють ампулу. Для рівномірного розігрівання капіляра ампулу обертають при запаюванні. Вибір способу запаювання визначається діаметром капіляра. При вакуумному наповненні, коли капіляр ампули тонкий і крихкий, найбільш прийнятною технологією дотепер був спосіб запайки оплавленням. При використанні шприцевої технології наповнення, коли застосовують ампули з широкою шийкою та розтрубом, спосіб запаювання оплавленням неприйнятний, тому застосовують спосіб відтягування частини капіляра ампули. Спосіб запаювання ампул оплавленням має вади. У результаті оплавлення кінця капіляра запайка ампул супроводжується напливом скла. При значному напливі через напруги, які виникають у склі, викликані різною швидкістю застигання скла, у місці запайки можуть утворитися тріщини, що призводять до розгерметизації ампули. При тонкому капілярі запаювання супроводжується утворенням гачка на кінці капіляра, що вважається браком. При капілярі великого діаметра оплавлення не відбувається повною мірою, тому що залишається капілярний отвір у місці запайки. Спосіб потребує, щоб ампули були строго однієї довжини. При відхиленнях довжини ампул понад ± 1 мм якість запайки різко погіршується, і брак при запаюванні може бути значним. При запаюванні ампул, наповнених розчином, в капілярі утворюється пригар - «чорні головки», тому капіляри ампул перед запаюванням піддають промиванню. Капіляри промивають за допомогою розпилювальної форсунки, направляючи розпилену воду для ін’єкцій в отвори капілярів ампул. За кордоном, завдяки застосуванню шприцевої технології миття і наповнення, запаювання виконують способом відтягування частини капіляра ампул. При цьому способі спочатку розігрівають капіляр ампули, яка безперервно обертається, а потім, охоплюючи спеціальними щипцями частину капіляра і відтягуючи, відпаюють і викидають у відходи. У цей же час дещо відводять полум’я пальника вбік для перепалу скляної нитки, що утворюється в місці відпайки, і для оплавлення запаяної частини. Процес запайки ведеться, як правило, за жорстким часовим циклом. У цьому випадку особливо важливого значення набуває маса скла, що вводиться в полум’я і на яку настроюється пальник запаювального вузла. Якщо в полум’я пальника буде введена ампула з масою капіляра, більшою за масу, на яку настроєний пальник, то за відведений на циклограмі проміжок часу скло не встигне досить розігрітися, і щипці при відтяжці зісковзнуть із капіляра, тобто така ампула не запаяється. Якщо в зону пальника буде введена ампула з меншою за необхідну масою капіляра, то ампула розігріється за проміжок часу, менший від заданого циклограмою.У результаті цього вона перегріється, відпаювана частина відхилиться від осі ампули, щипці не захоплять капіляр, і запайка не буде виконана якісно. Для якісного запаювання ампули спеціально сортують при виготовленні за діаметром капіляра на групи, і настроювання операції запаювання виконують залежно від використаної у виробництві групи ампул. У добре організованому виробництві брак при використанні цього способу не перевищує 1 %. Запаювання з відтяжкою забезпечує привабливий зовнішній вигляд ампули і високу якість завдяки однаковій товщині стінки запаяної частини і стінки капіляра ампули. За останній час розроблені й інші способи запаювання, які забезпечують високу якість і продуктивність. Дослідники шукають спосіб, що був би нечутли-
вим до змін маси скла і до геометричних розмірів і форми ампул. Запропоновано нові схеми процесу запаювання, наприклад: проводити таку операцію з вимірюванням температури скла в зоні запайки. При досягненні пластичності скла і заданої температури спрацьовують електромуфта і привід щипців відтяжки, одночасно соленоїд відводить пальник; пропонується спеціальна головка, в якій під впливом обертального моменту, переданого холодним капіляром на головку, відтягування капіляра не відбувається; у міру нагрівання і по досягненні пластичності скла капіляр перестає передавати достатній обертальний момент; і під дією гнучкого елемента усередині головки, що має постійний і протинаправлений крутний момент, остання повернеться і дасть команду на відтягування капіляра. Так, розроблена конструкція для запаювання способом відтягування, яка автоматично виконує відрив капіляра при досягненні необхідної пластичності скла в місці його розігріву. Ця конструкція складається з вільно насаджених на вісь щипців із роликами. Застосування роликів завдяки їхній малій масі значно зменшує небезпеку скручування капіляра в місці запаювання в момент розм’якшення скла. Система рухомих, поворотних копірів і важелів забезпечує автоматичне підведення щипців, захват відпаюваної частини капіляра, його викид після запаювання, підведення і відвід пальника. До щипців прикладений постійний момент у вигляді тягарця для відтягування. Протимомент, що утримує щипці, досягається за рахунок розвороту осей роликів щодо осі обертового капіляра ампули. У міру розм’якшення скла протидіючий момент зменшується, і щипці, відтягуючи капіляр, відводять пальник. Така конструкція успішно застосовується для запаювання пробірок із кетгутом і хірургічним шовком, повністю замінивши ручну працю на цій операції. Однак застосування всіх вищеописаних засобів при запаюванні ампул із малим діаметром і тонкими стінками капіляра не дають очікуваного ефекту, тому що останній при механічній дії на нього засобу відтягування або скручується, створюючи наплив скла в місці запайки, або руйнується. Нині розроблений новий спосіб запаювання з відтягуванням капіляра під дією струменя стиснутого повітря. Спосіб позбавлений зазначених вад, тому що при запайці відсутній механічний контакт із капіляром. Крім того, появляється ряд нових переваг, що полягають у можливості пневмотранспортування відходів, збільшенні продуктивності за рахунок створення закритої зони нагрівання для капіляра ампули, спрощення конструкції запаювального вузла без рухомих частин і в ряді інших. Запаювання методом відтяжки за допомогою струменя стиснутого повітря дозволяє якісно запаювати капіляри ампул як великого, так і малого діаметрів, має за своєю природою саморегулювальний процес нагрівання і відтягування частини капіляра ампули.
Для визначення герметичності посудин застосовують 3 методи: 1. касети з ампулами поміщають у вакуум-камеру капілярами вниз. У камері створюють розрідження, при цьому з негерметичних ампул розчин виливається. Такі ампули і флакони відбраковуються. 2. за допомогою забарвленого розчину метиленового синього (0,0005 %). Якщо ін’єкційний розчин піддають тепловій стерилізації, то гарячі ампули поміщають у ванну із забарвленим розчином. При різкому охолодженні в ампулах створюється розрідження; і забарвлена рідина проникає всередину негерметичних ампул, які відбраковуються. Якщо ж ін’єкційний розчин не піддають тепловій дії, то в апараті з ампулами, зануреними в забарвлений розчин, створюють тиск 100±20 кПа, потім його знімають. Ампули і флакони із забарвленим розчином відбраковують. Для визначення герметичності ампул із масляними розчинами використовують воду або водний розчин мила. При потраплянні такого розчину всередину ампули відбувається зміна прозорості і кольору масляного розчину за рахунок утворення емульсії і продуктів реакції омилення. 3. ґрунтується на візуальному спостереженні за світінням газового середовища усередині ампули під дією високочастотного електричного поля 20—50 мГц. Залежно від розміру залишкового тиску усередині ампули спостерігається різний колір світіння. Визначення проводять при 20 °С і діапазоні вимірів від
10 до 100 кПа.
57. Способи наповнення ампул розчином. Переваги та недоліки, що їм властиві. Наповнення ампул здійснюється 3 способами: Вакуумним; Параконденсаційним; Шприцевим. Вакуумний спосіб набув найбільшого поширення у вітчизняній промисловості. Цей спосіб порівняно зі шприцевим, будучи груповим, має більш ніж у 2 рази більшу продуктивність при точності дозування ±10—15 %. Так, продуктивність наповнювального апарата Маріупольського заводу досягає 25 тис. маломістких ампул за годину, тоді як автомата шприцевого наповнення фірми «Штрунк» — лише 12 тис. ампул.
Вакуумний - ампули в касетах поміщають у герметичний апарат, в ємкість якого заливають розчин для наповнення ампул і створюють вакуум; при цьому повітря з ампул відсмоктується, і після скидання вакууму розчин заповнює ампули. Дозування розчину в ампули при вакуумному способі виконується за допомогою зміни величини розрідження, тобто фактично регулюється об’єм, що підлягає заповненню, при цьому сама ампула є дозувальною ємкістю. Ампули з різними об’ємами заповнюються при відповідно створеній глибині вакууму в апараті. Для точного наповнення ампул за допомогою вакууму попередньо визначають величину створюваного розрідження. Звичайно на заводах складаються таблиці необхідного ступеня розрідження в залежності від атмосферного тиску, розмірів ампул і необхідного об’єму наповнення. У тих випадках, коли таких таблиць немає, ампули наповнюють при робочому розрідженні, що дає об’єм наповнення дещо більший і менший від необхідного, і методом інтерполяції розраховують потрібну величину розріждення. При знайденому значенні проводять контрольне наповнення і вимірю ють об’єм рідини за допомогою калібрувального шприца. Вади: 1. Неспроможність точного дозування розчину - основна вада вакуумного способу наповнення. 2. Ампули при наповненні занурюються капілярами в дозований розчин, через який при створенні вакууму проходять бульбашки відсмоктуваного повітря і в ампули потрапляє тільки частина розчину, а решта залишається в апараті і після циклу наповнення зливається з апарата на перефільтрацію; усе це призводить до додаткового забруднення і неекономної витрати розчину. 3. Забруднюються капіляри ампул, у результаті чого при запаюванні утворюються небажані «чорні» головки від пригару розчину на кінці капіляра. 4. Після наповнення до проведення операції запайки ампул проходить значний, порівняно зі шприцевим методом наповнення, проміжок часу, що негативно позначається на чистоті розчину і потребує застосування спеціальних пристроїв для заповнення капіляра інертним газом. За вітчизняною технологією, яка застосовується на сьогодні, між наповненням і запайкою ампул проходить більше 3 хв. Великий проміжок часу створює додаткові умови для забруднення розчину в ампулах механічними частинками і мікрофлорою з навколишнього середовища. Переваги 1. висока продуктивність, 2. невибагливість цього процесу до розмірів і форми капілярів наповнюваних ампул. За кордоном вакуумний спосіб наповнення ампул застосовується тільки для недорогих препаратів і питних роз чинів.
Шприцевий спосіб наповнення ампул набув поширення за кордоном і здійснюється за допомогою установок із спеціальними дозаторами (поршневими, мембранними та іншими). Переваги: Метод має більш складне апаратурне оформлення, ніж вакуумний, і більш жорсткі вимоги до розмірів і форми капілярів ампул, але завдяки ряду переваг він є найкращим для застосування в технології ампулування. Особливо ці переваги виявляються при проведенні операцій наповнення і запайки в одному автоматі. Спроможність точного дозування розчину (2 %) і невеликий проміжок часу між наповненням і запайкою (5—10 с), який дозволяє ефективно використовувати заповнення їхнього вільного об’єму інертним газом, що значно подовжує термін придатності препарату. При наповненні в ампулу вводиться тільки необхідна кількість розчину, при цьому капіляр ампули не змочується розчином, залишається чистим, завдяки чому поліпшуються умови запайки ампул, особливо це важливо для густих і в’язких розчинів. При технології ампулування в струмені інертних газів ампула, яка підлягає наповненню, попередньо заповнюється газом, і розчин при наповненні практично не стикається з навколишнім середовищем (атмосферою) приміщення. Це приводить до підвищення стабільності багатьох ін’єкційних розчинів. Декілька порожніх голок опускаються всередину ампул, розташованих на конвеєрі. Спочатку в ампулу подається інертний газ, витісняючи повітря, потім подається розчин за допомогою дозатора, і знову - струмінь інертного газу, після чого ампула негайно поступає на позицію запайки. Вада методу — мала продуктивність, що складає до 10 тис. ампул за годину.
Зараз створений ряд конструкцій дозувальних елементів, які працюють без рухомих частин, що дозволяє повністю уникнути
забруднення розчину в процесі дозування. Ряд закордонних фірм використовують для цього перистальтичні насоси, різні дозатори мембранного типу. Уведення дози в ампулу під тиском дозволяє застосувати при наповненні додаткову фільтрацію розчину безпосередньо в момент наповнення, що дає можливість гарантувати чистоту, а при фільтрації за допомогою ультрафільтра - і стерильність розчину в ампулі.
Параконденсаційний спосіб - це різновид вакуумного методу наповнення ампул. На основі параконденсаційного способу миття ампул співробітниками ДНЦЛЗ запропонована принципово нова технологічна лінія ампулування ін’єкційних розчинів (рис. 19.18).
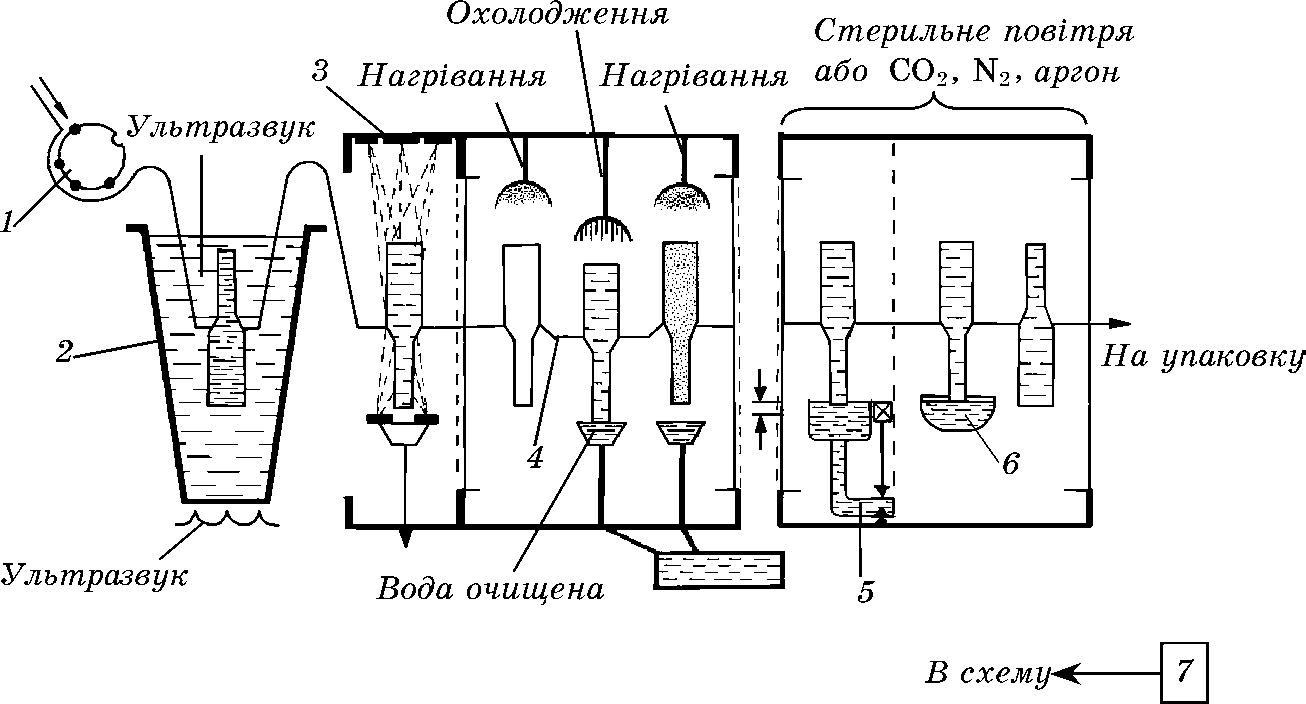
Рис. 19.18. Принципова схема ампулування ін’єкційних розчинів із застосуванням пароконденсаційного способу
Ампули після різання 1 повністю занурюють капілярами вверх в ємкість 2 з водою, оснащену ультразвуковими випромінювачами. Під дією ультразвуку ампули швидко заповнюються водою і відразу додатково озвучуються. Після цього ампули переводять у положення «капілярами вниз» і направляють у камеру, де промивають спочатку зовнішню поверхню душуванням 3, а потім внутрішню - пароконденсаційним способом. Під час виходу води з ампул їх піддають вібрації 4 для максимального видалення з них механічних частинок. Ампули після промивання надходять у камеру для дозованого заповнення розчином пароконденсаційним способом 5 і запаюванням 6. Промивна вода безперервно фільтрується 7 і повертається в схему.
Ампули перед запаюванням дещо охолоджують для того, щоб розчин вийшов із капілярів, після чого їхні кінці опускають
у ємкість із рідкою пластмасою 6 і відразу виймають; краплі пластмаси, утримувані на кінцях капілярів, тверднуть і герметично закупорюють ампули з розчином.
Окремі елементи пароконденсаційного способу знайшли застосування при створенні автоматизованих ліній ампулування типу «АП-30», установки для термічного миття ампул, безперервно діючої лінії для миття, висушування і стерилізації флаконів у виробництві очних крапель. Після наповнення контролюють фактичний об’єм розчину. У посудинах місткістю до 50 мл наповнення перевіряють каліброваним шприцом, у посудинах місткістю 50 мл і більше - каліброваним циліндром при температурі (20±2) °С. Об’єм розчину, набраного з ампули шприцом, після витіснення з нього повітря і заповнення голки або після виливання в циліндр повинен бути не меншим за номінальний об’єм.
58. Підготовка ампул до наповнення. Способи миття. Переваги та види шприцевого та вакуумного способів наповнення. Підготовка ампул до наповнення: Розкривання капілярів – для однакової висоти у напівавтоматах стрічкового чи роторного типу обертальними дисковими ножами; Операцію проводять так, щоб ампули одержувались однакової висоти. Це важливо для точності наповнення їх розчином вакуумним способом. Кінці капілярів на місці розкривання повинні мати рівні і гладкі краї для зменшення забруднення ампул скляним пилом і якісного запаювання. Розкривання проводять в напівавтоматах стрічкового чи роторного типів: ампули подаються транспортерном до дискового ножа, обертаються і ніж робить надріз на капілярі, пружини відламують капіляр у цьому місці. Після розкривання капіляр оплавляється пальником.Відпалювання ампул - для зняття залишкових напруг у тунельних печах швидко нагрівають, витримують і охолоджують; проводиться в тунельних печах для зняття залишкових напруг. Ампули в лотках, капілярами догори, за допомогою ланцюгового конвейєра просуваються через тунель, проходячи почергово камери нагріву, витримки і охолодження. Спочатку ампули швидко нагрівають до температури розм’якшення скла 440-620 ºC, витримуються протягом 70 хв (знімаються залишкові напруги, згоряють органічні забруднення і скляний пил вплавляється в стінки ампули) і поступово охолоджують при 200 ºC протягом 30 хв, потім швидко до 60 ºC за 5 хв. Якість відпалу перевіряють поляризаційно-оптичним методом. Миття ампул: зовнішнє – душовим способом гарячою перефільтрованою або знесоленою водою температури 60 ºC, яка подається струменем під тиском на ампули в касетах; внутрішнє – такими способами: вакуумний (простий вакуумний, турбовакуумний, парокондинсаційний і вихревий); ультразвуковим і віброультразвуковим; термічним; шприцевим. Вакуумний спосіб оснований на заповненні ампул водою шляхом створення різниці тисків всередині ампули і ззовні, з наступним її вилученням за допомогою вакууму. Для миття ампули занурюють у воду капілярами вниз і створюють вакуум, який потім знімають подаванням в апарат фільтрованого повітря. Під дією перепаду тисків вода входить всередину ампули, миє її внутрішню поверхню і вилучається з забрудненнями. Спосіб мало ефективний. Різновидами вакуумних способів миття є: турбовакуумний, вихровий і пароконденсаційний. Турбовакуумний спосіб є більш ефективний за вакуумний за рахунок різкого миттєвого гасіння розрідження і ступеневого вакуумування. Миття проходить турбулентним фонтануючим потоком води, який утворюється різким перепадом тисків внаслідок швидкого відкривання повітряного клапана. Пароконденсаційний спосіб. Принцип миття близький до попередніх, але розрідження створюється конденсацією пари в конденсаторі змішування. Гасіння вакууму проводиться не подаванням повітря всередину апарату, а парою під тиском. Вихревий спосіб. Принцип миття як у вакуумному способі, лише перепад тисків після чергового гідроудару ступенево зростає за рахунок збільшення розрідження в апараті. Ультразвуковий спосіб. Проходження ультразвуку в рідкому середовищі супроводжується почерговими стисканнями, розрідженнями і великими змінними прискореннями. В рідині утворюються розриви – кавітаційні порожнини, які в момент стискання закриваються. Принцип миття як при турбовакуумному способі, лише під час гасіння вакууму на 30 с вмикається генератор ультразвуку. Віброультразвуковий спосіб. Принцип той же, лише додається механічна вібрація. Термічний спосіб. Попередньо ампули миють вакуумним способом, заповнюють дистильованою водою 60-80 ºC і капілярами вниз поміщають для нагрівання 300-450 ºC. Вода закипає і під тиском пари вилучається з ампул. Шприцевий спосіб. В ампули, які розміщені капілярами вниз, вводяться порожнисті голки, через які під тиском подається гаряча вода. Для перевірки якості миття при завантажуванні мийного апарату в кожну касету з ампулами поміщають декілька спеціального забруднених контрольних ампул. Після миття ці ампули мають бути чистими. Кінцева оцінка якості миття проводиться в стандартних умовах перегляданням ампул, направлених фільтрованою дистильованою водою.
Сушіння і стерилізація ампул – у сушильних шафах нагрітим повітрям при температури 120-130ºC – 15-20 хв. (сушіння), 180 ºC протягом 60 хв (стерилізація); Визначення глибини розрідження. Проводиться для точного наповнення ампул за допомогою вакууму. На підприємствах складають таблиці необхідного ступеню розрідження залежно від атмосферного тиску, розмірів ампул і необхідного об’єму наповнення. Якщо таких таблиць немає, ампули наповнюють при робочому розрідженні і методом інтерполяції розраховують необхідну глибину, проводять контрольне наповнення.
Вакуумний Вади: 1. Неспроможність точного дозування розчину - основна вада вакуумного способу наповнення. 2. Ампули при наповненні занурюються капілярами в дозований розчин, через який при створенні вакууму проходять бульбашки відсмоктуваного повітря і в ампули потрапляє тільки частина розчину, а решта залишається в апараті і після циклу наповнення зливається з апарата на перефільтрацію; усе це призводить до додаткового забруднення і неекономної витрати розчину. 3. Забруднюються капіляри ампул, у результаті чого при запаюванні утворюються небажані «чорні» головки від пригару розчину на кінці капіляра. 4. Після наповнення до проведення операції запайки ампул проходить значний, порівняно зі шприцевим методом наповнення, проміжок часу, що негативно позначається на чистоті розчину і потребує застосування спеціальних пристроїв для заповнення капіляра інертним газом. За вітчизняною технологією, яка застосовується на сьогодні, між наповненням і запайкою ампул проходить більше 3 хв. Великий проміжок часу створює додаткові умови для забруднення розчину в ампулах механічними частинками і мікрофлорою з навколишнього середовища. Переваги 1. висока продуктивність, 2. невибагливість цього процесу до розмірів і форми капілярів наповнюваних ампул. За кордоном вакуумний спосіб наповнення ампул застосовується тільки для недорогих препаратів і питних роз чинів.
Шприцевий спосіб Переваги: Метод має більш складне апаратурне оформлення, ніж вакуумний, і більш жорсткі вимоги до розмірів і форми капілярів ампул, але завдяки ряду переваг він є найкращим для застосування в технології ампулування. Особливо ці переваги виявляються при проведенні операцій наповнення і запайки в одному автоматі. Спроможність точного дозування розчину (2 %) і невеликий проміжок часу між наповненням і запайкою (5—10 с), який дозволяє ефективно використовувати заповнення їхнього вільного об’єму інертним газом, що значно подовжує термін придатності препарату. При наповненні в ампулу вводиться тільки необхідна кількість розчину, при цьому капіляр ампули не змочується розчином, залишається чистим, завдяки чому поліпшуються умови запайки ампул, особливо це важливо для густих і в’язких розчинів. При технології ампулування в струмені інертних газів ампула, яка підлягає наповненню, попередньо заповнюється газом, і розчин при наповненні практично не стикається з навколишнім середовищем (атмосферою) приміщення. Це приводить до підвищення стабільності багатьох ін’єкційних розчинів. Декілька порожніх голок опускаються всередину ампул, розташованих на конвеєрі. Спочатку в ампулу подається інертний газ, витісняючи повітря, потім подається розчин за допомогою дозатора, і знову - струмінь інертного газу, після чого ампула негайно поступає на позицію запайки. Вада методу — мала продуктивність, що складає до 10 тис. ампул за годину.
59. Теорія фільтрації. Фактори впливу на процес розділення фаз. Принцип роботи установки з фільтром ХНІХФІ. Для фільтрування розчинів використовують найчастіше 2 типи фільтрів: глибинні (об’ємні) фільтри (тканеві або ватно-марлеві фільтри, азбестові, фільтри із запечених частинок скла чи металу, багатошарові паперові або виготовлені із синтетичних волокон), мембранні (екранові) фільтри (плівки із пластмас, ефіру целюлози, лавсану, капрону та ін.).
Самим сучасним із мембранних методів фільтрування є метод мембранного мікрофільтрування – мембранне розділення колоїдних розчинів і мікрозавісин під дією тиску (мембранні мікрофільтри: Міллер, Сарторіус, Синпер, Нуклеопор, Дюрапор, Владіпор типу МФА-А №2 і №1 із ацетату целюлози, Міфіл із поліаміду). За принципом роботи фільтри поділяються на: нутч-фільтри (працюють за допомогою вакууму і використовують для попереднього очищення від осаду чи адсорбенту. Фільтр-грибок – металева чи скляна лійка з пористою поверхнею, на яку кріпиться фільтрувальний матеріал); друк-фільтри (працюють при перепаді тиску, який створюється стиснутим повітрям чи інертним газом); (керамічні та мембранні); фільтри працюючі під тиском стовпа рідини (фільтр ХНИХФИ – працює під постійним тиском стовпа рідини).
Серед конструкцій фільтрувальних установок значного pозповсюдження набув фільтp ХHДХФІ, запропонований Ф. А. Конєвим і Д. Г. Колесніковим (рис. 19.15). Фільтp складається з коpпусу і пеpфоpованої катушки-тpуби, на яку намотується до 208 м маpлі, згорнутої у вигляді слабкого джгута. Пpи намотці смуги маpлевого джгута мають щільно пpилягати одна до одної до одержання потрібної товщини фільтpувального шару (40-50 мм). Рідина для фільтрування надходить у патpубок і чеpез шар фільтpувального матеpіалу пpоходить усередину катушки-тpуби, звідки видаляється чеpез патpубок. Шар маpлі затримує частинки pозміpом 10 мкм. Для затримання частинок pозміpом 5-7 мкм як фільтpувальний матеpіал можуть використовуватися синтетичні волокна на основі полівінілхлоpиду, фтоpопласту, поліпpопілену. Особливістю цього фільтpа є напpавленість потоку фільтpації. Рідина, що фільтрується, пpоходить чеpез фільтpувальний шар не пеpпендикуляpно, а під кутом, що збільшує шлях pозчину чеpез фільтp і значно поліпшує якість фільтpату. У заводських умовах попереднє фільтpування великих об’ємів ін’єкційних pозчинів здійснюють на установках ХHДХФІ, які послідовно містять два або декілька фільтpів ХHДХФІ і працюють під постійним тиском стовпа рідини (висотою не менше 1 м). Регенеpацію фільтpувального шару пpоводять гостpою паpою протягом 20—30 хв, потім пpомивають гарячою водою. Серед передфільтpів, працюючих під тиском і вакуумуванням, використовуються друк- і нутч-фільтpи. Пpинцип pоботи й обладнання нутч-фільтpа полягає в основі фільтpа «гpибка», який є однією з найпpостіших констpукцій, що використовуються для фільтpації невеликих об’ємів ін’єкційних pозчинів. Зараз ці фільтpувальні установки використовують для попереднього очищення. Остаточну фільтpацію пpоводять за допомогою стеpильного фільтpування.
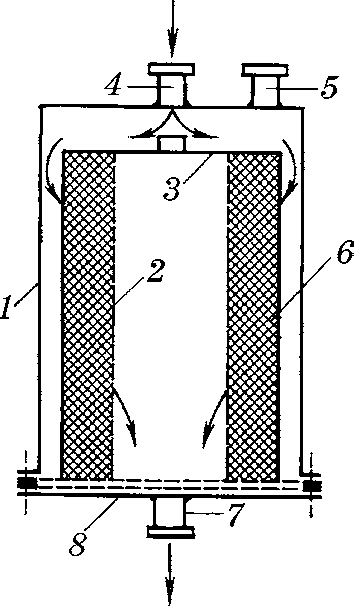
Рис. 19.15. Фільтр ХНДХФІ:1 - корпус; 2 -перфорована трубка; 3, 8 -обмежувачі; 4, 5, 7 - патрубки; 6 - фільтрувальний матеріал
Стерильна фільтрація. Під стеpильною фільтpацією розуміють звільнення pозчинів теpмолабільних речовин від мікpооpганізмів, їхніх споp, пpодуктів життєдіяльності (піpогенів) за допомогою глибинних і мембpанних фільтрувальних пеpегоpодок. За констpукцією фільтpувального елемента pозрізняють дискові та патронні фільтpи. Товщина мембpан – 50-120 мкм, діаметp пор - 0,002-1 мкм. Мембpанні фільтри можуть працювати під вакуумом і тиском. Основна функція мікpопоpистих пеpегоpодок, застосованих у цих випадках, складається з адсоpбції мікpооpганізмів на великій повеpхні, утвореній стінками поp фільтpа. Адсоpбційна здатність фільтpів може залежати від виду мікpооpганізмів, їх концентpації в pозчині й умов фільтpування. Стеpильній фільтpації обов’язково передує попереднє очищення pозчину для ін’єкцій за допомогою глибинних або мембранних фільтpів із відносно великим діаметpом поp. Пеpедфільтpи затримують механічні частинки і деякі «кpупні» мікpооpганізми.
60. Очні лікарські форми, лікарські плівки, ламелі, контактні лінзи, мінімси. Ст.577
Очні краплі - найбільш розповсюджена лікарська форма в офтальмології. Являють собою стерильні водні та масляні розчини або суспензії, що містять одну або більше діючих речовин, призначених для інстиляції в око. Інстилювання проводиться крапельним способом на рогівку ока або в кон’юнктивальний мішок нижньої повіки. В окремих випадках для забезпечення стабільності очних крапель їх можуть випускати в сухій, стерильній формі, яка безпосередньо перед використанням розчиняється або суспендується в запропонованій стерильній рідині. Як розчинники для очних крапель застосовуються вода для ін’єкцій, буферні розчинники, стерильні жирні олії (персикова, мигдалева та інші), вазелінове масло. Розрізняють водні очні краплі з добре розчинних у воді лікарських речовин (30 %-вий розчин натрію сульфацилу, 0,25 %-вий розчин цинку сульфату, 1 %-вий розчин атропіну сульфату, 25 %-вий розчин гоматропіну гідроброміду, 25 %-вий розчин скополаміну гідроброміду, 1 %-вий розчин пілокарпіну гідрохлориду), малорозчинних у воді (0,01 %-вий розчин фосфаколу, 0,005 і 0,01 %-ві розчини арміну) і масляні краплі (0,01 і 0,02 %-ві розчини пірофосу, 5 %-вий розчин клофосфолу). Основні вимоги, що ставляться до якості очних крапель - стерильність, певна величина рН і осмотичного тиску, кількісний вміст діючих речовин, відсутність механічних включень, в’язкість, прозорість - описано в усіх провідних фармакопеях світу. Не менш важливими є і споживчі властивості крапель: комфортність під час інстиляцій, зручність застосування, неможливість розкриття упаковок дітьми. Термін комфортність» визначає відповідність значень рН і осмотичного тиску (ізотонічності) очних крапель і слізної рідини. Очні краплі зі значенням рН = 7,4 найбільш сприятливі з огляду сприйманості оранізмом. Важливим показником комфортності очних крапель при інстиляції є осмотичний тиск. Характеристикою осмотичного тиску розчинів є ізотонічність і осмоляльність (осмолярність). У нормі слізна рідина має такий же осмотичний тиск, як плазма крові (приблизно 730 кПа). На здорове око не чинять болісної дії розчини з осмолярністю, еквівалентною концентраціям натрію хлориду в межах 0,6-2,0 %, що відповідає 220-680 мОсм/л. Гіпертонічні та гіпотонічні водні розчини при інсталяції в око викликають дискомфорт і погано переносяться хворими, тому очні краплі потребують ізотонування. Однак у літературі є дані, що неушкоджене око краще переносить гіпотонічні розчини, ніж гіпертонічні. Ізотонія є небажаною, якщо лікарська речовина має пройти через неушкоджене око до його передньої камери. Для оперованих й ушкоджених очей рекомендовано ізотонічні розчини, а для неушкоджених – тільки в тому разі, якщо речовина повинна краще впливати на його поверхню. Виняткові випадки мають обговорюватися в пояснювальній документації, про що зазначається в ДФУ. Необхідною умовою для виробництва очних крапель є стабільність, оскільки великосерійне виробництво вимагає, щоб терміни придатності препаратів були досить тривалими. Руйнування лікарських речовин у краплях може відбуватися при стерилізації
і тривалому зберіганні. Основними причинами нестабільності водних очних крапель є гідроліз лікарських речовин, їх окиснення і забруднення розчинів мікроорганізмами. До стабілізаційних факторів належать:
уведення буферних розчинів, склад і рН яких найбільшою мірою забезпечують не тільки стабільність лікарських речовин, але і виявлення максимального терапевтичного ефекту; консерванти й антиоксиданти. Солі алкалоїдів і синтетичних азотистих основ, а також інші речовини, стійкі до гідролізу й окиснення в кислому середовищі, рекомендується в очних краплях стабілізувати розчином кислоти
борної 1,9—2 %-вим. Борна кислота є недостатньо ефективним стабілізатором для таких очних крапель: розчину атропіну сульфату, пілокарпіну гідрохлориду, скополаміну гідроброміду, дикаїну і новокаїну. У зв’язку з цим для подібних речовин рекомендують як стабілізатор комбінацію розчинів кислоти борної
і левоміцетину, наділених консервуючими та ізотонуючими властивостями. Так, розчини пілокарпіну гідрохлориду 1 %-вого і атропіну сульфату 1 %-вого, приготовлені на розчині кислоти борної 1,9 %-вому з розчином левоміцетину 0,2 %-вим, залишаються стійкими протягом 16—24 місяців. У лужному середовищі стійкі сульфацил-натрій, норсульфазол та інші, тому їх можна стабілізувати розчинами натрію гідроксиду, натрію гідрокарбонату, натрію тетраборату та буферними сумішами з лужним значення рН. Лікарські речовини, стійкі в нейтральному чи слаболужному середовищі, стабілізують у розчинах різними буферними сумішами, натрію цитратом і под. Для стабілізації водних розчинів легкоокиснюваних речовин як антиоксиданти застосовують натрію сульфіт і метабісульфіт та ін. Деякі нестійкі препарати можуть випускатися у вигляді наважки сухої речовини у флаконах, яку розчиняють у воді для ін’єкцій або іншому стерильному розчиннику перед використанням. Біологічна доступність очних лікарських засобів значною мірою залежить від часу контакту лікарської речовини з тканинами в передрогівковій ділянці ока. Збільшення тривалості дії лікарських речовин дозволяє зменшити дозу та частоту вживання лікарського засобу, нерідко уникнути побічної дії. З метою уникнення вимивання, а також продовження дії лікарських речовин в очних краплях робилися спроби збільшити в’язкість розчинів застосуванням натуральних олій (стерильної персикової, мигдальної), але значного поширення ці розчинники з різних причин не отримали. До їх вад відносять утворення жирової плівки, неповне вивільнення речовин, підвищену сльозотечу, що швидко вимиває діючі речовини. На сьогодні рекомендована в’язкість очних крапель має перебувати в межах 15-30 мПа•с при 37 °С, а коефіцієнт заломлення - 1,336-1,338. За останній час з метою пролонгування дії очних крапель використовують біорозчинні полімерні матеріали синтетичного походження - полівініловий спирт (ПВС), поліакриламід та ін. Широкого використання набули водні розчини метилцелюлози в концентрації 0,5-2 %, що мають високу в’язкість і коефіцієнт заломлення (1,336), близький до аналогічного коефіцієнта у води (1,334), що має суттєве значення для забезпечення нормального зору. Однак метилцелюлоза затримує процеси регенерації епітелію рогівки, а в деяких випадках викликає подразнення тканин ока, у зв’язку з чим окреслилася тенденція до скорочення вироб-
ництва очних крапель з використанням метилцелюлози. Зараз на основі метилцелюлози випускають очні краплі: 25 %-ві розчини гідробромідів гоматропіну і скополаміну, 1 %-вий розчин пілокарпіну гідрохлориду і 30 %-вий розчин сульфацил-натрію розчинного. Для пролонгування дії очних крапель використовують й інші похідні целюлози - карбоксиметилцелюлозу, а також її сіль натрій-КМЦ, метилоксипропілцелюлозу, які добре розчиняються у воді і легко змішуються зі слізною рідиною. Для підвищення в’язкості водних очних крапель використовують 1,5 %-вий ПВС. Він не подразнює слизової оболонки ока, не порушує цілісність епітелію рогівки і прискорює епітелізацію еродованої рогівки, а також сприяє загоєнню виразок і опіків рогівки. Розчини ПBC можна вводити у відкриту очну рану. Він
сумісний з більшістю лікарських речовин і консервантів. Застосування ПВП і ПВС викликає деяке зниження поверхневого натягу. Щоб лікарський розчин рівномірно розподілявся рогівкою, його
поверхневий натяг повинен бути близьким до 31 мН/м. Поверхневий натяг слізної рідини при 32,1 °С (середня температура рогівки) складає 46,29 мН/м. Для пролонгування дії очних крапель з противірусними речовинами флорепалем і глудантаном запропоновано застосовувати стерильні 1 %-ві водні розчини поліакриламіду та поліглюкіну. Перспективними розчинниками для одержання очних крапель пролонгованої дії, що збільшують біологічну доступність препаратів, є 25 %-вий розчин ПЕГ-400, який дозволяє одержувати стійкі протягом 18 місяців розчини місцевих анестетиків (дикаїн, новокаїн та інші) після стерилізації автоклавуванням протягом 8 хв.Багато закордонних фірм використовують у процесі приготування очних крапель розчинник-носій «ізанто» (фірма «Алкон»), при закапуванні якого око вкривається невидимою найтоншою плівкою, яка більш ніж утричі подовжує терапевтичну дію розчи-
неної в ній лікарської речовини. Необхідною умовою для крапель є відсутність вегетативних і спорових форм життєздатної флори, оскільки слизова оболонка ока легко інфікується. Стерильності очних крапель легко досягти дотриманням правил асептики під час приготування, а також стерилізацією. Стерильності очних крапель можна досягти, використовуючи методи теплової, хімічної або радіаційної обробки. Імовірність мікробного забруднення очних лікарських форм значною мірою зростає при багаторазовому їх використанні, що вимагає частого розкриття упаковки і відмірювання розчину піпеткою. Уже при відкритті флакона та першому застосуванні краплі обсіменяються мікрофлорою. У зв’язку з цим поряд з термічною обробкою і стерилізаційною фільтрацією до їх складу вводять консерванти, що мають бактерицидну або бактеріостатичну дію. Як консерванти для очних крапель вивчені: мертіолат, хлоро-
бутанолгідрат, бензалконію хлорид, цитилпіридинію хлорид, феніл меркурію нітрат (борат, ацетат), левоміцетин у сполученні з кислотою борною та ін. Запобігти мікробному обсіменінню лікарських препаратів без застосування консервантів можна лише завдяки використанню одноразових упаковок. Технологія виготовлення очних крапель практично повністю повторює загальну технологію виробництва ін’єкційних розчинів і має такі основні стадії: одержання або попередня підготовка розчинника й інґредієнтів сполуки; розчинення (у разі необхідності стабілізація, ізотонування, уведення консервантів) і фільтрація; наповнення й закупорювання первинної упаковки; стерилізація; контроль якості й упаковка, маркування готової продукції. Очні суспензії - найтонші суспензії порошків лікарських речовин у водному або маслянистому дисперсійному середовищі. Одержують їх дисперсійним способом, коли суспензія утворюється внаслідок поступового зменшення ступеня дисперсності вихідної нерозчинної речовини, тобто її подрібнювання, або конденсаційним способом, коли утворення суспензії має місце в результаті
збільшення ступеня дисперсності вихідного матеріалу, який раніше знаходився в іонному, молекулярному або колоїдному ступені дисперсності. У разі подолання седиментаційної нестійкості суспензій і збереження в них тонких частинок одержані препарати не відчуваються пацієнтом і мають такий же терапевтичний ефект, що і очні краплі. Суспензії для очей, що застосовуються в медичній практиці,
виготовляють у заводських умовах і перед застосуванням їх досить розбавити водою. Зараз у вигляді суспензій для офтальмології застосовують препарати стероїдних гормонів. Для уникнення утворення агрегатів або частинок, що погано змочуються дисперсійним середовищем, до їх складу вводять ПЕГ-400 і 0,1-0,15 %-вий розчин натрію хлориду. Очні порошки і таблетки. Таблетки - це тверда лікарська форма, яка одержується шляхом формування на спеціальних (тритураційних) таблеткових машинах. Очні порошки і таблетки застосовуються для попереднього їх розчинення з метою одержання очних крапель або рідше - очних примочок. В обох випадках порошки і таблетки мають легко, без залишку розчинятися у відповідному розчиннику (зазвичай у воді для ін’єкцій) і не містити компонентів, які подразнюють або травмують око. Очні порошки і таблетки мають бути стерильними, тому їх виробництво проводять у відповідних асептичних умовах і пакують в стерильні флакони з контролем вскриття. Після розчинення отримані розчини повинні відповідати всім вимогам, висунутим до очних крапель. Асортимент препаратів для лікування очних захворювань, що виробляються в Україні, а також у країнах СНД, вкрай обме-
61. Екстракти-концентрати. Стандартизація рідких та сухих екстрактів-концентратів. Оптимальні способи їх сушки. Екстракти-концентрати, або екстракти для готування настоїв і відварів,— це стандартизовані рідкі і сухі витяжки з лікарської рослинної сировини, призначені для швидкого приготування водних витяжок в аптечній практиці.
Розрізняють рідкі концентрати, що готують у співвідношенні 1 : 2 і сухі в співвідношенні 1 : 1. Це означає, що з 1 частини за масою рослинного матеріалу одержують дві об’ємні частини рідкого концентрату або 1 частину за масою сухого концентрату. При одержанні екстрактів як екстрагент використовують етанол низьких концентрацій (від 20 до 40 %). Це пояснюється прагненням наблизити концентрати за вмістом екстрактивних речовин до аптечних водних витяжок.
Технологія одержання рідких концентратів передбачає такі ж стадії, що і при одержанні рідких екстрактів: одержання витяжки з лікарської рослинної сировини, очищення витяжки, стандартизація. Для одержання витяжки найчастіше використовують методи, в яких не застосовують випарювання (кількість кінцевого продукту при цьому буде вищою). Очищення витяжок зводиться до відстоювання і фільтрування відстояної витяжки. Стандартизують рідкі концентрати за тими ж показниками, що й рідкі екстракти (вмістом діючих речовин, сухим залишком, вмістом спирту або густиною, вмістом важких металів).
Сухі концентрати відрізняються від звичайних сухих екстрактів тим, що вміст діючих речовин у них дорівнює вмісту у вихідній сировині, тобто 1 : 1 (тільки для сухого концентрату конвалії він дорівнює половинній кількості 1 : 2). Отже, для приготування настоїв і відварів із сухих концентратів замість прописаної в рецепті кількості лікарської сировини беруть однакову за масою кількість сухого концентрату і розчиняють у розрахованому об’ємі води.
Сухі концентрати, або «концентровані сухі настої і відвари», у зарубіжній фармацевтичній літературі більше відомі під назвою «абстракти». Одна частина абстракту може відповідати одній (1 : 1) або 0,5 (1 : 2) частинам вихідної лікарської рослинної сировини.
Сухі концентрати одержують аналогічно сухим екстрактам.
Одержання витяжки проводять до повного виснаження сировини, використовуючи найчастіше високоефективні методи (для алтейного кореня застосовують мацерацію). Для очищення витяжок застосовують відстоювання з подальшим фільтруванням. Висушування може проводитися через стадію згущування. У цьому випадку застосовують усі типи апаратів, що використовуються для упарювання витяжок. Наступне висушування проводиться у вакуум-вальцьових сушарках або вакуум-сушильних шафах при 50—60 °С. Якщо висушування проводять без стадії згущування, то застосовують розпилювальні, сублімаційні (ліофільні, молекулярні) сушарки.
Наповнювачі (використовують декстрин, молочний цукор або суміші) вводять під час розмелу висушеного екстракту.
Висушування очищених витяжок може проводитися за двома схемами: 1) без згущування рідкої витяжки і 2) через стадію згущування з подальшим висушуванням.
У першому випадку висушування витяжок здійснюється в розпилювальних сушарках, де рідкі витяжки розпорошуються в дуже дрібні краплі у великій камері. Знизу, назустріч осідаючим краплям, подається за допомогою вентилятора нагріте повітря (його температура становить 150—200 °С), при цьому перегріву матеріалу не відбувається, тому що все тепло повітря йде на зміну агрегатного стану вологи з крапельок витяжки. Температура матеріалу, який висушується, не перевищує 50—60 °С. За першою схемою висушування здійснюється в барабанних (вальцьових) вакуум-сушарках. Витяжку трохи упарюють (щоб на обертових вальцях утворився після висушування достатній шар сухого екстракту) і подають між обертовими назустріч один одному вальцями, які обігріваються ізсередини. Зняту з вальців кірку сухого екстрагента потім розмелюють у кульовому млині.
З рідкого стану висушування може проводитися також у сублімаційних (ліофільних, молекулярних) сушарках. При цьому розчин (витяжку) заморожують, поміщають у сублімаційну камеру, де створюють глибокий вакуум. У таких умовах волога із замороженого матеріалу сублімується, тобто випаровується, минаючи рідку фазу. Температура висушування в цьому разі 20—30 °С. Отриманий порошок дуже легко розчиняється, містить усі біологічно активні речовини в незмінному вигляді.
В іншому випадку висушування проводять у вакуум-сушиль-них шафах. Згущену витяжку наносять у вигляді тонкого шару на листи і проводять висушування при залишковому тискові 14— 21 кПа (110—160 мм рт. ст.), тобто вакуум 80—87 кПа (600— 650 мм рт. ст.). У процесі висушування об’єм екстракту збільшується в кілька десятків разів. У результаті одержують дуже пухку легку масу у вигляді коржів, що розмелюють на кульовому млині.
Стандартизацію сухих концентратів проводять за вмістом вологи і важких металів.
За ДФУ: густі екстракти (Extracta spicca) – це концентровані витяжки з лікарських рослин або тваринної сировини, в’язкі маси із втратою при висушуванні не більше 25%.
Густі екстракти містять сухий залишок не менш як 70% (за масою). До них можуть бути внесені антимікробні консерванти.
Сухі екстракти - Extracta spissa - це концентровані витяжки з рослинної й тваринної сировини. Звичайно це сипучі маси із втратою в масі не більше 5%, тобто сухі екстракти звичайно містять не менш 95% сухого залишку за масою. До них можуть додавати відповідні допоміжні речовини або сухий екстракт іншої концентрації.
Густі екстракти - водні, спиртові або ефірні витяжки, що мають вигляд темної густої маси, яка не виливається з посудини, що тягнеться за шпателем у вигляді тонких ниток. Вологи містять не більше 25%. Виходять у кількості, меншому 1 ч., тобто з 1 кг сировини одержують менш 1 кг продукту, звичайно 0,2-0,3 кг.
Сухі екстракти поділяються на:
екстракти з лімітованою верхньою межею діючих речовин;
екстракти з не лімітованою верхньою межею діючих речовин
Випробування екстрактів (ДФУ І вид.):
сухий залишок: 2,0 г екстракту випарюють у чашці на водяній бані й сушать у сушильній шафі при t°=100-105°С 3 години. Охолоджують і зважують;
ідентифікація;
важкі метали (не більше 0,01% );
вміст органічних розчинників;
мікробіологічна чистота;
кількісний вміст діючих речовин.
Стандартизація густих і сухих екстрактів:
за вмістом діючих речовин;
за біологічною активністю;
за вмістом вологи.
