
- •Химическая Кинетика, равновесия, термодинамика
- •1. Основные понятия кинетики [1, § 57; 2, § 6.2, 6.2.1]
- •1.1. Химическая кинетика
- •1.2. Понятие скорости реакции
- •2. Зависимость скорости гомогенной реакции
- •2.3. Лабораторная работа: определение порядка реакции тиосульфата натрия с кислотой в растворе
- •2.3.1. Постановка задачи
- •2.3.2. Зависимость скорости реакции от концентрации ионов водорода
- •2.3.3. Зависимость скорости реакции от концентрации ионов тиосульфата
- •3. Зависимость скорости реакции от температуры
- •3.3. Лабораторная работа: влияние температуры на скорость реакции
- •4. Катализ [1, § 60; 2, § 6.2.6]
- •5. Особенности кинетики гетерогенных реакций [1, § 61; 2, § 6.2.4]
- •5.1. Общие сведения
- •5.3. Реакции, лимитируемые химическим взаимодействием
- •5.4. Реакции, лимитируемые диффузией в растворе реагента
- •5.5. Реакции, лимитируемые образованием зародышей новой фазы
- •5.6. Демонстрационные опыты
- •6. Обзор факторов, влияющих на скорость
- •7. Общие сведения о Химическом равновесии [1, § 63; 2, § 6.2.8]
- •7.1. Истинное и ложное равновесия
- •7.2. Закон действующих масс (здм) для равновесия
- •7.3. Стандартные состояния веществ и стандартное представление
- •8. Частные случаи констант равновесия
- •8.1. Гомогенные равновесия в растворах электролитов
- •8.2. Гетерогенные равновесия
- •8.3. Квазихимические равновесия в кристаллах
- •9. Факторы, влияющие на смещение равновесия.
- •9.2. Влияние концентрации
- •9.3. Влияние разбавления раствора
- •9.4. Влияние давления
- •9.5. Влияние температуры
- •9.6. Факторы, влияющие на кинетику, но не на равновесие
- •9.7. Выбор оптимальных условий проведения реакций
- •10. Задачи и упражнения по химическому равновесию
- •11. Лабораторная работа по химическому равновесию
- •11.1. Прогноз направления реакций и его экспериментальная проверка
- •11.2. Влияние температуры и концентраций на химическое равновесие
- •12. Введение в химическую термодинамику.
- •12.1. Общие сведения
- •12.2. Первое начало термодинамики. Энтальпия
- •12.3. Закон Гесса и стандартные теплоты образования веществ
- •12.4. Ещё три следствия из закона Гесса
- •13. Направление процессов.
- •13.1. Второе начало термодинамики. Энтропия.
- •13.2. Критерии самопроизвольного протекания процессов
- •13.3. Связь между стандартным изменением энергии Гиббса и константой равновесия
- •13.4. Задачи и упражнения по термодинамике
13.2. Критерии самопроизвольного протекания процессов
а) В изолированной системе самопроизвольно идут только процессы с увеличением энтропии. S > 0 – процесс возможен, S < 0 – невозможен. Когда S достигает максимума, наступает равновесие, макроскопические изменения прекращаются. Типичный пример – диффузия, которая происходит без теплового эффекта: система самопроизвольно переходит в состояние с максимальной вероятностью – молекулы, атомы, ионы перемешиваются.
б) Там, где возможен теплообмен с окружающей средой, это уже не совсем верно. Возможны экзотермические процессы с уменьшением S, например, кристаллизация жидкости, конденсация пара. Поэтому первоначально был введен критерий Бертло: самопроизвольно идут только экзотермические процессы, то есть процессы с уменьшением U или H. Этот критерий при низких температурах оправдывается часто. Действительно, потерять энергию проще, чем приобрести. Простая механическая аналогия: предмет на столе имеет большую потенциальную энергию, чем на полу, скатиться и упасть на пол он может самопроизвольно, но не может сам заскочить с пола на стол. Но все же и этот критерий не совсем верен. Возможны и эндотермические процессы, например, испарение жидкости.
Одновременно действуют обе тенденции – и стремление к минимуму энергии (U или H), и стремление к максимуму беспорядка (S). Нужны критерии, учитывающие сразу обе тенденции. Такими критериями являются:
энергия Гельмгольца F = U – TS для изохорно-изотермических процессов
и энергия Гиббса G = H – TS = U + pV – TS = F + pV – для изобарно-изотермических.
В старой литературе их еще называют термодинамическими потенциалами (изохорно-изотермическим и изобарно-изотермическим), а также свободными энергиями Гельмгольца и Гиббса.
Тут более прямая аналогия с механической потенциальной энергией: макротела самопроизвольно скатываются в яму, к минимуму потенциальной энергии, а физико-химические системы – к минимуму термодинамического потенциала.
В изохорно-изотермических условиях самопроизвольно идут только процессы с уменьшением F: F < 0 – процесс возможен, F > 0 – процесс невозможен. Когда F достигает минимума – наступает равновесие.
Аналогично, в изобарно-изотермических условиях самопроизвольно идут только процессы с уменьшением G.
G = H – TS < 0 – условие самопроизвольного протекания процесса в изобарно-изотермических условиях. Возможны четыре варианта (рис. 5):
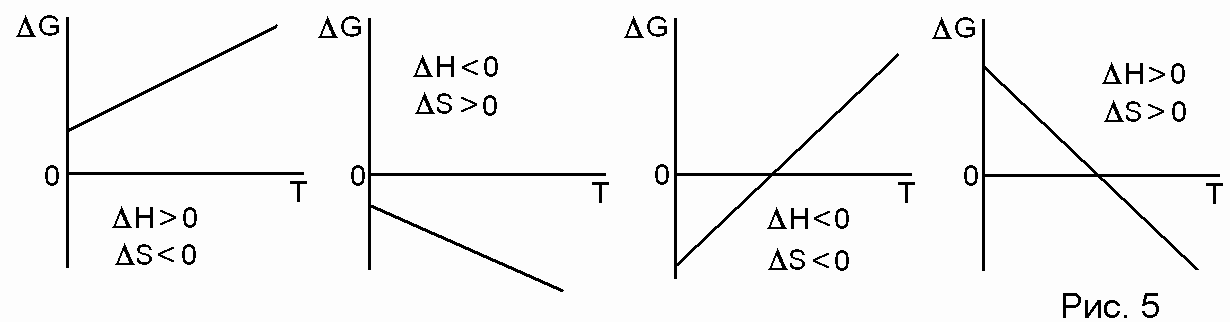
1) Н > 0, S < 0. При любых температурах G > 0, значит, прямой процесс невозможен.
2) Н < 0, S > 0. При любых температурах G < 0, значит, прямой процесс возможен.
3) Н < 0, S < 0. Возможны разные знаки G в зависимости от Т.
Если Т 0, то G Н и справедлив принцип Бертло. В данном случае прямой процесс может идти, обратный – нет.
Если Т , то G –TS, и направление процесса определяется ростом энтропии. В данном случае может идти только обратный процесс.
4) Н < 0, S < 0. Случай, обратный предыдущему. Процесс идёт самопроизвольно лишь при высоких температурах
Но где граница между “низкими” и “высокими” температурами ? Это зависит от соотношения H и S. Температура, при которой равновероятны прямой и обратный процессы (G = 0): Т0 = Н/S. Ниже этой температуры равновесие смещается в сторону протекания экзотермической реакции, выше – в сторону эндотермической. В качественной форме это известно как частный вариант принципа Ле Шателье. Очевидно, что при разных знаках Н и S такой температуры не может быть.
Демонстрация: обратимое разложение NH4Cl ←→ NH3 + HCl и необратимое (NH4)2Сr2O7 N2 + Cr2O3 + 2H2O. Знак S очевиден по выделению газов, знак H во втором случае также очевиден – саморазогрев.
Вопрос. Как изменяются H, S и G при реакции BaCl2(p-p) + H2SO4(p-p) → BaSO4(тв.) + 2HCl(p-p) в изобарно-изотермических условиях? в изолированной системе? Процесс идет самопроизвольно, значит в изобарно-изотермических условиях G < 0. Но образование кристаллов позволяет утверждать, что S < 0. Тогда однозначно Н < 0. Будет ли Н < 0 в изолированной системе? Нет, Н = 0, т.к. нет теплообмена. Система не может отдать тепло в окружающую среду, поэтому температура повышается. Но если процесс идет самопроизвольно, значит S > 0. Но может ли кристаллизация идти с ростом энтропии? Кристаллизация – вряд ли, но раствор-то нагрелся, и рост его энтропии перевесил убыль энтропии от кристаллизации. Здесь G = – ТS < 0.
Для F, G и S, как и для U, H, справедлив закон Гесса.
