
onch_posobie
.pdf
Производной серной кислоты является тиосерная кислота. Тиосерная кислота в свободном виде не получена, но широко используются её соли – тиосульфаты. В молекуле тиосульфата центральный атом серы находится в степени окисления +6, внешний – минус 2. За счёт наличия сульфидной серы тиосульфаты – сильные восстановители и могут окисляться с образованием свободной серы и сульфат-иона:
Na2S2O3 + Cl2 + H2O = Na2SO4 + S + 2HCl (в технике Na2S2O3
называют «антихлор»),
Na2S2O3 + H2SO4 = Na2SO4 + S + SO2 + H2O.
Окисление менее сильными окислителями:
I2 + 2Na2S2O3 = 2NaI + Na2S4O6.
Эта реакция используется в аналитической химии – иодометрический метод анализа.
Получение тиосульфатов:
Na2SO3 + S = Na2S2O3.
Кроме рассмотренных кислородсодержащих кислот, сера образует и другие кислородсодержащие кислоты, отвечающие общим формулам H2SOn (n = 2…5) и H2S2On (n = 4…6). Названия некоторых кислот этих двух рядов и их анионов представлены в табл. 16.3.
Таблица 16.3 Химические формулы и названия соответствующих
кислот и анионов
Формула |
Название кислоты |
Название анионов |
|
|
|
H2SO2 |
Сульфоксиловая |
Сульфоксилаты |
|
|
|
H2SO5 |
Пероксосерная |
Пероксосульфаты |
|
|
|
H2S2O2 |
Тиосернистая |
Тиосульфиты |
|
|
|
H2S2O4 |
Гиподисернистая |
Гиподисульфиты |
|
|
|
H2S2O5 |
Пиросернистая |
Пиросульфиты |
|
|
|
H2S2O6 |
Дитионовая |
Дитионаты |
|
|
|
H2S2O8 |
Надсерная |
Персульфаты |
Применения p-элементов VI группы представлены в табл. 16.4.
251

|
|
|
|
|
|
Таблица 16.4 |
||
|
Способы получения и применения p-элементов VI группы |
|
||||||
|
|
|
|
|
|
|
|
|
|
Мировое произ- |
|
|
|
|
|
|
|
Э |
водство в 1990 г, |
Способ получения |
|
Применение |
||||
|
т. |
|
|
|
|
|
|
|
O |
1 108 |
Сжижение воздуха с по- |
При сварке и резке метал- |
|||||
|
|
следующей ректификацией |
лов, для интенсификации |
|||||
|
|
(дробной перегонкой). При |
технологических |
(метал- |
||||
|
|
этом N2 испаряется, оста- |
лургических) |
процессов; |
||||
|
|
ётся O2 с примесью Ar. Бо- |
топливо на основе жидко- |
|||||
|
|
лее чистый |
O2 |
получают |
го О2 отличается высокими |
|||
|
|
электролизом воды. |
энергетическими |
показа- |
||||
|
|
К(-): 2НОН + 2е = Н2 + |
телями |
– окислитель для |
||||
|
|
+ 2ОН- |
ракет |
дальнего |
действия. |
|||
|
|
А(+): 2НОН – 4е = О2 + |
Медицина – при затрудне- |
|||||
|
|
+ 2Н+ |
|
нии дыхания |
|
|
||
|
|
: 2НОН = 2Н2 + О2. |
|
|
|
|
||
|
|
В лаборатории: |
|
|
|
|
|
|
|
|
2KMnO4 = K2MnO4 + |
|
|
|
|
||
|
|
+ MnO2 + O2 |
|
|
|
|
||
S |
64 106 |
Выплавка самородной S |
В резиновой |
промышлен- |
||||
|
|
|
|
|
ности, в с/х, производство |
|||
|
|
|
|
|
спичек, ультрамарина (си- |
|||
|
|
|
|
|
няя краска), CS2 |
|
||
Se |
1650 |
Получают |
из |
анодного |
В фотоэлементах, фотоко- |
|||
|
|
шлама при электролитиче- |
пирующих |
устройствах, |
||||
|
|
ском рафинировании Cu |
солнечных батареях и по- |
|||||
|
|
|
|
|
лупроводниках |
|
||
Te |
215 |
-//- |
|
В сплавах для улучшения |
||||
|
|
|
|
|
их механических |
свойств, |
||
|
|
|
|
|
для получения катализато- |
|||
|
|
|
|
|
ров, в электронике |
|||
Po |
В количестве |
Нейтронная |
|
бомбарди- |
Источник тепла в косми- |
|||
|
нескольких |
ровка Bi |
|
|
ческом оборудовании; ис- |
|||
|
грамм |
|
|
|
точник |
-частиц для науч- |
||
|
|
|
|
|
ных исследований |
|||
Задачи
Задачи по теме «Нахождение в природе.
Получение и применение простых веществ»
1277. Нахождение кислорода в природе. Дайте описание методов и приведите уравнения реакций, лежащих в основе получения кислорода в свободном состоянии. Укажите основные области его применения.
252

1278. Нахождение озона в природе. Дайте описание методов, лежащих в основе его получения. Строение молекулы озона. Является ли озон термодинамически устойчивым веществом? Укажите основные области его применения.
1279. Нахождение серы в природе. Приведите химические формулы соединений, в виде которых сера входит в состав минерального сырья. Формы существования серы (ее модификации). Способы получения серы. Укажите основные области ее применения.
1280. Нахождение селена в природе, его полиморфные модификации. Приведите реакции, лежащие в основе получения селена в свободном состоянии. Укажите основные области его применения.
1281. Нахождение теллура в природе, его полиморфные модификации. Приведите реакции, лежащие в основе получения теллура в свободном состоянии. Укажите основные области его применения.
Задачи по теме «Физико-химические свойства простых веществ»
Для 1282-1284. На основании электронного строения атомов p- элементов VI группы объясните …
1282. изменение радиусов и энергии ионизации атомов и ионов соответствующих элементов. Данные представьте графиком в координатах: свойство – порядковый номер элемента. Укажите число атомов в молекуле и аллотропные модификации простых веществ.
1283. изменение неметаллических и окислительно-восстанови- тельных свойств простых веществ в группе; их температуры плавления и кипения. Как изменяется устойчивая степень их окисления, чем это объясняется? Укажите возможные степени окисления кислорода.
1284. изменение степеней окисления, электродных потенциалов и таких свойств, как плотность, температуры плавления и кипения кислорода, серы, селена и теллура.
Для 1285-1288. Закончите реакции, характеризующие отношение р- элементов VI группы к некоторым простым веществам. Дайте характеристику образующихся продуктов; их отношение к воде. Укажите их области применения.
1285. |
а) O2(г) + H2(г) |
… |
в) S(т) |
+ O2(г) |
… |
|
б) Se(т) + H2(г) |
… |
г) S(т) |
+ H2(г) |
… |
1286. |
а) Se(т) + O2(г) |
… |
в) S(т) |
+ Cl2(г) |
… |
|
б) S(т) + F2(г) |
… |
г) Se(т) + F2(г) |
… |
|
1287. |
а) Te(т) + O2(г) |
… |
в) Te(т) + Cl2(г) |
… |
|
|
б) Se(т) + Cl2(г) |
… |
г) S(т) |
+ Br2(г) |
… |
1288. |
a) O3(г) + К(т) |
… |
в) S(т) |
+ Hg(т) |
… |
|
б) Te(т) + F2(г) |
… |
г) S(т) |
+ Zn(т) |
… |
253

Для 1289-1291. Отношение простых веществ к сложным окислителям: воде, кислотам (разбавленным и концентрированным) и щелочам. Напишите уравнения реакций (полуреакции, ионные и молекулярные уравне-
ния) для … |
|
1289. |
серы и селена. |
1290. |
серы и теллура. |
1291. |
селена и теллура. |
1292. По данным |
Hпл и |
Sпл . (см. ч. 3, табл. 14) вычислите темпера- |
туры плавления серы, селена и теллура. |
||
1293. По данным |
Hисп и |
Sисп (см. ч. 3, табл. 14) вычислите темпе- |
ратуры кипения серы, селена и теллура.
1294. Вычислите теплоту полиморфного превращения моноклиннической серы в ромбическую, если теплоты сгорания моноклиннической и ромбической серы равны 296,83 и 297,21 кДж/моль, соответственно.
1295. Как изменяется окислительная активность элемента при переходе от кислорода к теллуру и как это сказывается на возможности образования Н2Э непосредственным взаимодействием простых веществ? Ответ обоснуйте данными по Gо образования Н2Э (см. ч. 3, табл. 15). Каким способом получают Н2Se и H2Te?
Для 1296-1300. Двумя способами (с использованием а) Gо образования участников процесса (см. ч. 3, табл. 15) и б) стандартных потенциалов окислительно-восстановительных пар (см. ч. 3, табл. 21)) рассчитайте, возможно ли в стандартных условиях протекание реакции получения серы взаимодействием сероводорода с …
1296. перманганатом калия в кислой среде.
1297. сернистой кислотой.
1298. раствором серной кислоты.
1299. кислородом.
1300. сернистым газом.
Для 1301-1305. Двумя способами (С использованием: а) Gо образования участников процесса (см. ч. 3, табл. 15), б) стандартных потенциалов окислительно-восстановительных пар (см. ч. 3, табл. 15)) рассчитайте, возможно ли в стандартных условиях протекание реакции получения …
1301. селена взаимодействием SeO2 c SO2.
1302. селена взаимодействием селенистой кислоты с KBr.
1303. теллура взаимодействием TeO2 и SO2.
1304. кислорода взаимодействием пероксида водорода с перманганатом калия в кислой среде.
1305. кислорода взаимодействием озона с KI в водном растворе.
254

Задачи по теме «Важнейшие соединения: свойства, получение и применение»
Для 1306-1309. Используя основные положения метода ВС, рассмотрите образование химических связей в предложенных соединениях. Укажите их возможное строение и тип гибридизации орбиталей центрального атома. Укажите степени окисления атомов в соединениях …
1306. SO2, SO32- и H2SO5. |
|
|
|||
1307. SF4, SO2F2 и SO3. |
|
|
|||
1308. H2O, H2S, H2Se и H2Te. |
|
|
|||
1309. |
SeF6, TeO66- и TeO2. |
|
|
||
|
|
|
о |
о |
образования (см. ч. 3, табл. 15) и |
Для 1310-1312. Сравните H и G |
|
||||
сделайте вывод об изменении прочности связи в соединениях: |
|||||
1310. оксидов ЭО2 |
в ряду S – Se – Te. |
||||
1311. |
оксидов ЭО3 |
в ряду S – Se – Te. |
|||
1312. |
гидридов ЭН2 |
в ряду O – S – Se – Te. |
|||
1313. |
Представьте |
графическую |
|
формулу соединений Na2SO4, |
|
Na2S2O3, Na2SO3; укажите механизм образования и - и -связи между атомами. Предскажите предполагаемую структуру аниона при диссоциации соединения в воде.
1314. Используя основные положения метода МО, дайте схему образования (энергетическую диаграмму) химических связей в O2, O2+, O2-; оцените энергию, длину и порядок связи.
1315. Сколько литров сероводорода при температуре 18 оС и давлении 99 кПа потребуется для полного восстановления йода, содержащегося в 1,65 л 0,15 н. водного раствора KI3?
(Отв. 3,023 л)
1316. Вычислите массовую долю пероксида водорода в растворе, если 24 г его выделили 9 г йода из подкисленного раствора йодида калия.
(Отв 5 %)
1317. Какова молярность раствора пероксида водорода, если для количественного взаимодействия с 25 мл 0,02 М раствора перманганата калия в кислой среде израсходован такой же его объем
(Отв. 0,05 моль/л)
1318. Вычислите объем H2S (20 оС, 100 кПа), необходимый для полного восстановления 150 мл его 6 %-го раствора ( = 1,040 г/см3) перманганатом калия в кислой среде.
(Отв. 3,6 л)
1319. Вычислите массовую долю сернистой кислоты в растворе, если 100 г его потребовалось для количественного выделения серы из 0,44 л 0,25 М раствора сероводородной кислоты.
(Отв. 4,51%)
255

1320. На взаимодействие с 125 мл 0,125 М раствора йода при проведении реакции был израсходован такой же объем водного раствора Na2S2O3. Какова масса пятиводного кристаллогидрата этой соли в растворе?
(Отв. 3,88 г)
1321. Какой объем 25 %-го раствора H2SO4 ( = 1,178 г/см3) можно приготовить из 3 кг пиросерной кислоты?
(Отв. 11,2 л)
1322. Каково общее содержание SO3 (мас.%) в 20 %-м олеуме? Какой объем моногидрата ( = 1,8305 г/см3) можно получить из 1 т олеума?
= 1,8305 г/см3) можно получить из 1 т олеума?
(Отв. 85,3 %)
1323. Напишите выражение закона действующих масс и укажите направление смещения равновесия реакций при увеличении давления:
SO2(г) + O2(г) 2SO3(г) ; |
2SO3(г) 2SO2(г) + O2(г) . |
|||
Для 1324-1327. Напишите в молекулярной и ионной формах реакции, |
||||
лежащие в основе следующих превращений: |
||||
1324. Na2S |
H2S SO2 |
Na2SO3 Na2SO4. |
||
1325. S H2S |
FeS Fe2O3 |
NaFeO2. |
||
1326. H2S |
S |
SO2 |
Na2SO3 |
Na2SO4. |
1327. FeS2 |
SO2 |
SO3 |
H2SO4 |
BaSO4. |
Для 1328-1329. Если реакция возможна, составьте ее электронно- |
||||
ионные и молекулярное уравнения: |
|
|||
1328. Na2S2O3 + NaClO + NaOH |
SO42- + Cl- + …; |
|||
1329. Se + KBrO3 + H2O |
SeO42- + Br - + …. |
|||
17. р-ЭЛЕМЕНТЫ VII ГРУППЫ, s- И p-ЭЛЕМЕНТЫ VIII ГРУППЫ*
p-элементы VII группы
К р-элементам VII группы (галогенам) относятся: 9F [He]2s22p5, 17Cl
[Ne]3s23p5, 35Br [Ar]4s24p5, 53I [Kr]5s25p5, 85At [Xe]6s26p5. Согласно элек-
тронной конфигурации атомов (одинаковая структура внешнего и предвнешнего электронных слоев), 35Br, 53I и 85At объединяют в подгруппу брома; фтор и хлор относят к типическим элементам.
Некоторые свойства галогенов и их соединений приведены в табл. 17.1. Как видно из табл. 17.1, радиусы атомов в группе возрастают, а энергия ионизации уменьшается. Это свидетельствует об ослаблении неметал-
лических свойств: фтор – наиболее ярко выраженный элемент-неметалл, а астат проявляет уже некоторые признаки элемента-металла. При стандарт-
* Материал по s- и р-элементами VIII группы представлен только зада-
чами.
256
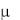
ных условиях фтор и хлор – ядовитые газы, бром – токсичная летучая жидкость, иод – кристаллы фиолетового цвета. Между молекулами галогенов действуют силы Ван-дер-Ваальса, которые усиливаются по мере увеличения размеров молекул. Поэтому бром и иод находятся в конденсированном состоянии. Благодаря высокой реакционной способности в свободном состоянии в природе галогены не встречаются.
Таблица 17.1
Характеристика галогенов и их соединений
Элемент |
9F |
17Cl |
35Br |
53I |
85At |
|
|
|
|
|
|
|
|
Молекулярная |
F2 |
Cl2 |
Br2 |
I2 |
At2 |
|
формула |
|
|
|
|
|
|
Агрегатное со- |
Газ |
Газ |
Жидкость |
Твердый |
Твердый |
|
стояние |
|
|
|
|
|
|
Цвет |
|
Светло- |
Желто- |
Красно- |
Черно- |
- |
|
|
зеленый |
зеленый |
коричневый |
фиолетовый |
|
Радиус атома, нм |
0,071 |
0,099 |
0,114 |
0,133 |
- |
|
Радиус иона Э-, |
0,133 |
0,181 |
0,196 |
0,220 |
0,23 |
|
нм |
|
|
|
|
|
|
Энергия сродства |
3,45 |
3,61 |
3,37 |
3,08 |
2,81 |
|
к электрону, эВ |
|
|
|
|
|
|
Энергия иониза- |
17,42 |
12,97 |
11,86 |
10,45 |
9,2 |
|
ции Еи1, эВ |
|
|
|
|
|
|
Содержание в |
2,8·10-2 |
2,6·10-2 |
8,5·10-5 |
4·10-5 |
Следы |
|
земной коре, |
|
|
|
|
|
|
моль. доли, % |
|
|
|
|
|
|
Tкип, 0С |
-187 |
-35 |
59 |
183 |
299 |
|
Е02Э-/Э |
, В |
+2,87 |
+1,36 |
+1,07 |
+0,54 |
- |
2 |
|
|
|
|
|
|
Длина связи НЭ, |
0,092 |
0,128 |
0,141 |
0,161 |
- |
|
нм |
|
|
|
|
|
|
НЭ, D |
|
1,92 |
1,04 |
0,79 |
0,38 |
- |
Е св НЭ, кДж/моль |
565,7 |
431,6 |
366,1 |
298 |
- |
|
Степени окисле- |
-1 |
-1, +1, |
-1, +1, 3, |
-1, +1, |
- |
|
ния |
|
|
3, 5, 7 |
5, 7 |
3, 5, 7 |
|
Свойства простых веществ
Галогены реагируют с большинством металлов. В атмосфере фтора металлы сгорают с образованием высших фторидов. С другими галогенами большинство металлов реагируют при нагревании.
Продукты взаимодействия галогенов с неметаллами приведены в табл. 17.2.
Галогениды неметаллов – ковалентные соединения, гидролизуются под действием воды, например:
PCl3 + 3H2O = H3PO4 + 3HCl.
257

Таблица 17.2 Продукты взаимодействия галогенов с неметаллами
Галоген |
|
|
|
Реагент |
|
|
|
||
|
|
|
|
|
|
|
|
||
H2 |
O2 |
S |
P |
C |
Si |
F2 |
Cl2 |
||
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
HF |
OF2 |
SF6, |
PF5 |
CF4 |
SiF4 |
- |
ClF, |
|
Фтор |
|
|
SF4 |
|
|
|
|
ClF3, |
|
|
|
|
|
|
|
|
|
ClF5 |
|
|
HCl |
Cl2O, |
S2Cl2, |
PCl5, |
CCl4 |
SiCl4 |
ClO2F3, |
- |
|
|
|
ClO2, |
SCl2, |
PCl3 |
|
|
ClO3F, |
|
|
Хлор |
|
Cl2O6, |
SCl4, |
|
|
|
ClOF3, |
|
|
|
|
Cl2O7 |
SOCl2 |
|
|
|
ClO2F, |
|
|
|
|
|
|
|
|
|
ClOF5 |
|
|
|
HBr |
- |
S2Br2 |
PBr3, |
- |
SiBr4 |
BrF, |
BrCl |
|
Бром |
|
|
|
PBr5 |
|
|
BrF5, |
|
|
|
|
|
|
|
|
|
BrF3 |
|
|
Иод |
HI |
- |
- |
PI3 |
- |
SiI4 |
IF7, |
ICl3, |
|
|
|
|
|
|
|
|
IF5, |
ICl |
|
Взаимодействие с водой
Благодаря высокому электродному потенциалу фтор разлагает воду: 2F2 + 2H2O = 4HF + O2.
Другие галогены при взаимодействии с водой диспропорционируют, например:
Cl2 + H2O HCl + HСlO.
Ослабление окислительной активности сказывается на уменьшении склонности брома и иода к реакциям диспропорционирования. Так, константа гидролиза реакции
Э2 + Н2О НЭ + НЭО
в ряду Cl2 – Br2 – I2 заметно уменьшается: 3·10-4, 4·10-9 и 5·10-23. Следовательно, равновесие реакции взаимодействия галогенов с водой при переходе от хлора к иоду все более смещается влево.
Взаимодействие с растворами щелочей
При взаимодействии фтора с разбавленным раствором щелочи образуется дифторид кислорода:
2F2 + 2KOH = OF2 + 2KF + H2O.
Хлор при взаимодействии со щелочами при комнатной температуре диспропорционирует по схеме:
Cl2 + 2KOH = KCl + KClO + H2O.
258

Если вместо KOH взять Ca(OH)2, то в результате реакции получается двойная соль CaCl(OCl), называемая хлорной или белильной известью. При нагревании образуются хлорид и хлорат калия:
3Cl2 + 6KOH = 5KCl + KClO3 + 3H2O.
Аналогичным образом ведут себя бром и иод.
Степень окисления фтора, как самого электроотрицательного элемента (см. ч. 3, табл. 23) принимается равной минус 1. Максимальная валентность фтора, согласно теории ВС, как и у других элементов 2-го периода, равна 4.
Из минералов фтора наибольшее значение имеют: CaF2 – плавиковый шпат (флюорит), Na3AlF6 – криолит и Ca5(PO4)3F – фторапатит.
Фтор исключительно химически активен. В атмосфере фтора горят такие стойкие вещества, как стекло (в виде ваты), вода:
SiO2 + 2F2 = SiF4 + O2; 2H2O + 2F2 = 4HF + O2.
Фтор окисляет некоторые так называемые инертные газы: Xe + 2F2 = XeF4; H = -252 кДж/моль.
Непосредственно фтор не взаимодействует лишь с гелием, неоном и аргоном. В качестве материала аппаратуры для получения фтора, его хранения и перевозки используется никель (и некоторые его сплавы), который устойчив к воздействию фтора за счет образования защитной пленки NiF2.
Фтор получают электролизом его расплавленных соединений. Для этих целей обычно используют эвтектическую смесь HF – KF или фторогидрогенаты калия. Фтор широко применяется для синтеза различных хладагентов и полимерных материалов-фторопластов, отличающихся высокой химической стойкостью. Жидкий фтор и ряд его соединений применяются
вкачестве окислителя ракетного топлива.
Всоответствии с закономерным изменением характера элементов по периодам и группам периодической системы изменяются и свойства фторидов, например:
|
NaF MgF2 |
AlF3 |
SiF4 PF5 SF6 |
Химическая природа – |
основная |
амфотерная |
кислотная |
Анионные комплексы – |
|
AlF63- |
SiF62- PF6- SF6 |
Ионные фториды (проявляют основные свойства) – кристаллические вещества с высокой температурой плавления. Ковалентные фториды (проявляют кислотные свойства) – газы или жидкости.
В реакции 2NaF + SiF4 = Na2[SiF6] ионный NaF выступает в качестве донора, а ковалентный SiF4 – в качестве акцептора электронных пар, носителем которых является F--ион. Основные фториды при гидролизе создают щелочную среду, а кислотные фториды – кислотную:
NaF + H2O NaOH + HF; |
SiF4 + 3H2O H2SiO3 + 4HF. |
259
Соединения с водородом типа HBF4, HPF6, H2SiF6 в свободном состоянии неустойчивы. Их водные растворы – очень сильные кислоты.
HF обычно получают действием серной кислоты на флюорит:
CaF2 + H2SO4 = CaSO4 + 2HF.
Характерной особенностью плавиковой кислоты (водного раствора HF) является ее способность взаимодействовать с SiO2:
SiO2 + 4HF(раствор) = SiF4 + 2H2O(жидкая),
поэтому ее не хранят в стеклянной посуде, а обычно в сосудах из полиэтилена, каучука или парафина. Плавиковая кислота применяется для травления стекла, удаления песка с металлического литья, получения фторидов, в органическом синтезе и т.д.
Хлор – типичный неметаллический элемент. Встречается главным образом в виде хлоридов. Из них наиболее важными минералами являются
NaCl – каменная соль, NaCl·KCl – сильвинит, KCl·MgCl2·6H2O – карнал-
лит. В огромном количестве хлориды содержатся в морской воде, входят составной частью во все живые организмы.
Молекула хлора подобно молекулам фтора и других галогенов двухатомна. Энергия ее диссоциации существенно выше (см. ч. 3, табл.10), чем у остальных двухатомных молекул галагенов. Полагают, что в молекуле Cl2 существует дополнительное связывание по донорно-акцепторному механизму за счет неподеленной электронной пары одного атома хлора и свободной d-орбитали другого. Считается, что порядок связи в молекуле Cl2 составляет 1,12.
Хлор – активный окислитель. Он энергично реагирует с металлами и большинством неметаллов (за исключением O2, N2 и инертных газов), легко окисляет многие сложные соединения. Восстановительные свойства хлор проявляет лишь при взаимодействии с фтором. Получают свободный хлор окислением хлоридов: в лаборатории – химическим окислением концентрированной соляной кислоты, например:
MnO2 + 4HCl = MnCl2 + Cl2 + 2H2O,
в технике – электролизом водного раствора NaCl и как побочный продукт – при получении натрия электролизом расплава NaCl. Хлор применяют для стерилизации питьевой воды, широко используют в качестве окислителя в самых разнообразных отраслях химической промышленности.
Основные хлориды, бромиды и иодиды (см. выше основные и кислотные фториды) гидролизу практически не подвергаются, а кислотные гидролизуются полностью и необратимо с образованием кислот:
SiCl4 + 3H2O = H2SiO3 + 4HCl;
BBr3 + 3H2O = H3BrO3 + 3HBr; PI3 + 3H2O = H3PO3 + 3HI.
260
