
- •Руководство к выполнению
- •Настоящее практическое пособие составлено согласно учебной программе курсов. Термохимия
- •Калориметр и методика калориметрических измерений
- •Контрольные вопросы
- •Лабораторная работа № 1. Определение теплоты гидратации соли.
- •Методика выполнения работы Определение постоянной калориметра
- •Форма отчета
- •Навески солей, взятые для растворения
- •Результаты калориметрических опытов при определении теплоты гидратации соли
- •Лабораторная работа № 2. Определение теплоты нейтрализации сильной кислоты сильным основанием.
- •Методика выполнения работы
- •Форма отчета
- •Результаты калориметрических опытов при определении теплоты нейтрализации сильных кислот сильным основанием
- •Химическое равновесие контрольные вопросы
- •Лабораторная работа № 3. Изучение равновесия гомогенной реакции в растворе.
- •Методика выполнения работы
- •Форма отчета
- •Фазовое равновесие контрольные вопросы
- •Лабораторная работа № 4. Растворение фенола в воде.
- •Методика выполнения работы
- •Форма отчета
- •Экспериментальные данные для построения диаграммы «состав — температура растворения» двойной жидкой системы вода — фенол.
- •Лабораторная работа № 5. Изучение кристаллизации вещества из растворов при низких температурах.
- •Методика выполнения работы
- •Форма отчета
- •Температура при охлаждении смеси
- •Результаты определения температуры кристаллизации
- •Лабораторная работа № 6. Определение коэффициента распределения.
- •Методика выполнения работы
- •Форма отчета
- •Определение коэффициента распределения органической кислоты между двумя несмешивающимися жидкостями: водой и эфиром
- •Молекулярные растворы Термометр Бекмана
- •Криоскоп
- •Контрольные вопросы
- •Лабораторная работа № 7.
- •Форма отчета
- •Криоскопические константы некоторых растворителей
- •Лабораторная работа № 8. Криоскопический метод определения молекулярной массы вещества по Расту (микрометод).
- •Методика выполнения работы
- •Форма отчета
- •Определение молекулярной массы исследуемого вещества по методу Раста
- •Лабораторная работа № 9. Изучение равновесия жидкость — пар в двойных жидких системах.
- •Методика выполнения работы
- •Форма отчета
- •Химическая кинетика контрольные вопросы
- •Лабораторная работа № 10. Определение порядка реакции окисления йодид-ионов ионами трехвалентного железа.
- •Методика выполнения работы
- •Определение частного порядка по отношению к I-.
- •Форма отчета
- •Лабораторная работа № 11. Изучение скорости реакции разложения комплексного оксалата марганца.
- •Фотоэлектрокалориметр фэк-м
- •Методика выполнения работы
- •Сосуд для
- •Форма отчета
- •Лабораторная работа № 12. Изучение скорости реакции разложения мурексида в кислой среде.
- •Методика выполнения работы
- •Форма отчета
- •Лабораторная работа № 13. Определение константы скорости омыления уксусноэтилового эфира в присутствии гидроксид- ионов.
- •Омыление этилацетата протекает по уравнению
- •Методика выполнения работы
- •Форма отчета
- •Результаты обратного титрования при определении константы скорости омыления сложного эфира в присутствии щелочи
- •Лабораторная работа № 14. Определение скорости разложения пероксида водорода в присутствии катализатора.
- •Методика выполнения работы
- •Форма отчета
- •Свойства электролитов контрольные вопросы
- •Методы и аппаратура, применяемые для измерения электропроводности растворов электролитов
- •Определение константы электролитического сосуда и измерение удельной электропроводности растворов электролита.
- •Удельная электропроводность водных растворов кСl при концентрации 1/50 и 1/100 моль/л
- •Константа сосуда рассчитывается по уравнению
- •Лабораторная работа № 15. Определение коэффициента электропроводности сильного электролита.
- •Методика выполнения работы
- •Измерение удельной электропроводности воды
- •Форма отчета
- •Лабораторная работа № 16. Определение растворимости и произведения растворимости труднорастворимой соли.
- •Тогда из уравнения следует
- •Методика выполнения работы
- •Форма отчета
- •Определение константы электролитического сосуда и удельной электропроводности дистиллированной воды и исследуемой соли
- •Лабораторная работа № 17. Определение буферной емкости потенцометрическим методом.
- •Измерение рН с помощью стеклянного электрода
- •Методика выполнения работы
- •Форма отчета
- •Лабораторная работа № 18. Потенциометрическое титрование кислот щелочью.
- •Кривая потенциометрического Дифференциальная кривая
- •Методика выполнения работы
- •1. Потенциометрическое титрование сильной кислоты щелочью.
- •2. Потенциометрическое титрование слабой кислоты щелочью.
- •3. Потенциометрическое титрование смеси кислот (сильная плюс слабая).
- •4. Потенциометрическое определение концентрации кислот во фруктах и овощах.
- •Форма отчета
- •Результаты потенциометрического титрования
- •Электрохимия лабораторная работа № 19. Приготовление медного кулонометра.
- •Методика выполнения работы
- •Медный кулонометр
- •Проверка калибровки амперметра
- •Форма отчета
- •Лабораторная работа № 20. Выход по току.
- •Методика выполнения работы
- •Форма отчета
- •Адсорбция
- •Лабораторная работа № 21. Адсорбция на границе жидкость – газ. Влияние жирных кислот на поверхностное натяжение воды.
- •Влияние жирных кислот на поверхностное натяжение воды
- •Методика выполнения работы
- •Форма отчета
- •Лабораторная работа № 22.
- •Методика выполнения работы
- •Форма отчета
- •Свойства коллоидных растворов контрольные вопросы
- •Лабораторная работа № 23. Получение золей и их коагуляция.
- •Методика выполнения работы Получение золей при химических реакциях
- •Определение знака заряда золей методом капиллярного анализа
- •Определение порога коагуляции золей
- •Форма отчета
- •Коагуляция золя гидрата оксида железа (III) под влиянием электролитов
- •Коагуляция золя берлинской лазури под влиянием электролитов
- •Рекомендуемая литература
О Рис.
15.
Рис. 16.
титрования
сильной кислоты щелочью
потенциометрического титрования
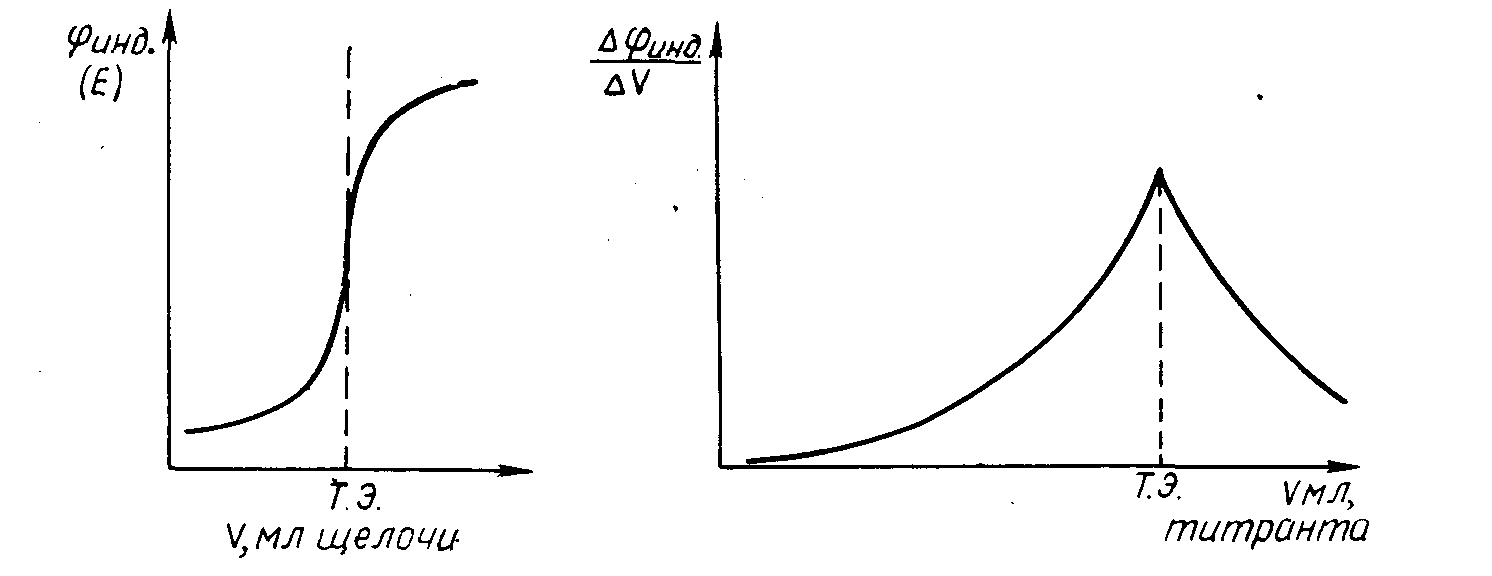
Кривая потенциометрического Дифференциальная кривая
ΔE/ΔV = f(V мл, титранта) или Δφинд./ΔV = f(V мл, титранта).
На основании полученных данных строят дифференциальную кривую потенциометрического титрования (рис. 16). Эквивалентную точку определяют по точке возврата.
При потенциометрическом титровании для измерения ЭДС неудобно применять компенсационный метод, так как измеряемая ЭДС постоянно меняется. Компенсация, требующая сравнительно много времени, становится затруднительной.
Для измерения ЭДС в этом случае рекомендуется прибор рН-340 или аналогичный, перед работой необходимо ознакомиться с методикой измерения ЭДС на приборе (изложена ниже).
Методика выполнения работы
1. Потенциометрическое титрование сильной кислоты щелочью.
В качестве индикаторного электрода можно брать стеклянный или хингидронный электрод, а в качестве электрода сравнения — хлорсеребряный или каломельный.
Потенциометрическое титрование щелочью удобнее проводить с применением в качестве рН-индикаторного стеклянного электрода, а в качестве электрода сравнения брать промышленный хлорсеребряный электрод ЭВЛ-1МЗ. Собирают гальванический элемент, электроды подключают к соответствующим клеммам датчика прибора рН-340.
В стаканчик (емкостью 50 мл) наливают 10 мл примерно 0,1 н. раствора НСl и в раствор погружают электроды. Измеряют ЭДС, данные записывают в табл. I (см. форму отчета). Закрепив бюретку (объемом 25 мл), заполненную 0,1 н. раствором NаОН (раствор щелочи должен быть титрован), в лапке штатива над стаканчиком, приливают в кислоту 1 мл щелочи, перемешивая раствор механической или магнитной мешалкой. Измеряют ЭДС. Продолжают прибавлять таким же образом по 1 мл щелочи и определяют ЭДС.
Когда общий объем прилитой щелочи достигнет 7 мл, прибавление проводят меньшими объемами (по 0,5 мл). Объемы добавляемой щелочи заносят в табл. I.
При приближении к эквивалентной точке, когда суммарный объем прибавленной щелочи достигнет 8 мл, дальнейшее титрование проводят, добавляя по 0,2 мл щелочи.
О конце титрования можно судить по значительному увеличению ЭДС при прибавлении небольшого количества щелочи (0,2 мл).
После точки эквивалентности продолжают титрование, прибавляя по 0,5 мл щелочи. В процессе титрования возможно изменение знака потенциала стеклянного электрода, поэтому изменяется направление тока в цепи и знак ЭДС. В этом случае при работе на приборе рН-340 необходимо переключатель «род работы» перевести в положение «—тV», при работе на приборе ЛПУ-01 переключатель «вид работы» перевести на диапазон измерений «+200 ÷ —1400 тV».
2. Потенциометрическое титрование слабой кислоты щелочью.
Для опыта берут слабую одноосновную кислоту (например, уксусную) примерно 0,1 н. и титруют щелочью. Методика работы и форма отчета те же, что и в предыдущем опыте. Кривые потенциометрического титрования слабой кислоты сравнивают с таковыми для сильной кислоты.
3. Потенциометрическое титрование смеси кислот (сильная плюс слабая).
Смешать по 5 мл 0,1 н. растворов соляной и уксусной кислот. Титровать смесь кислот потенциометрически в том же элементе, что и в опыте 1. Обработка материала та же.
