
- •Руководство к выполнению
- •Настоящее практическое пособие составлено согласно учебной программе курсов. Термохимия
- •Калориметр и методика калориметрических измерений
- •Контрольные вопросы
- •Лабораторная работа № 1. Определение теплоты гидратации соли.
- •Методика выполнения работы Определение постоянной калориметра
- •Форма отчета
- •Навески солей, взятые для растворения
- •Результаты калориметрических опытов при определении теплоты гидратации соли
- •Лабораторная работа № 2. Определение теплоты нейтрализации сильной кислоты сильным основанием.
- •Методика выполнения работы
- •Форма отчета
- •Результаты калориметрических опытов при определении теплоты нейтрализации сильных кислот сильным основанием
- •Химическое равновесие контрольные вопросы
- •Лабораторная работа № 3. Изучение равновесия гомогенной реакции в растворе.
- •Методика выполнения работы
- •Форма отчета
- •Фазовое равновесие контрольные вопросы
- •Лабораторная работа № 4. Растворение фенола в воде.
- •Методика выполнения работы
- •Форма отчета
- •Экспериментальные данные для построения диаграммы «состав — температура растворения» двойной жидкой системы вода — фенол.
- •Лабораторная работа № 5. Изучение кристаллизации вещества из растворов при низких температурах.
- •Методика выполнения работы
- •Форма отчета
- •Температура при охлаждении смеси
- •Результаты определения температуры кристаллизации
- •Лабораторная работа № 6. Определение коэффициента распределения.
- •Методика выполнения работы
- •Форма отчета
- •Определение коэффициента распределения органической кислоты между двумя несмешивающимися жидкостями: водой и эфиром
- •Молекулярные растворы Термометр Бекмана
- •Криоскоп
- •Контрольные вопросы
- •Лабораторная работа № 7.
- •Форма отчета
- •Криоскопические константы некоторых растворителей
- •Лабораторная работа № 8. Криоскопический метод определения молекулярной массы вещества по Расту (микрометод).
- •Методика выполнения работы
- •Форма отчета
- •Определение молекулярной массы исследуемого вещества по методу Раста
- •Лабораторная работа № 9. Изучение равновесия жидкость — пар в двойных жидких системах.
- •Методика выполнения работы
- •Форма отчета
- •Химическая кинетика контрольные вопросы
- •Лабораторная работа № 10. Определение порядка реакции окисления йодид-ионов ионами трехвалентного железа.
- •Методика выполнения работы
- •Определение частного порядка по отношению к I-.
- •Форма отчета
- •Лабораторная работа № 11. Изучение скорости реакции разложения комплексного оксалата марганца.
- •Фотоэлектрокалориметр фэк-м
- •Методика выполнения работы
- •Сосуд для
- •Форма отчета
- •Лабораторная работа № 12. Изучение скорости реакции разложения мурексида в кислой среде.
- •Методика выполнения работы
- •Форма отчета
- •Лабораторная работа № 13. Определение константы скорости омыления уксусноэтилового эфира в присутствии гидроксид- ионов.
- •Омыление этилацетата протекает по уравнению
- •Методика выполнения работы
- •Форма отчета
- •Результаты обратного титрования при определении константы скорости омыления сложного эфира в присутствии щелочи
- •Лабораторная работа № 14. Определение скорости разложения пероксида водорода в присутствии катализатора.
- •Методика выполнения работы
- •Форма отчета
- •Свойства электролитов контрольные вопросы
- •Методы и аппаратура, применяемые для измерения электропроводности растворов электролитов
- •Определение константы электролитического сосуда и измерение удельной электропроводности растворов электролита.
- •Удельная электропроводность водных растворов кСl при концентрации 1/50 и 1/100 моль/л
- •Константа сосуда рассчитывается по уравнению
- •Лабораторная работа № 15. Определение коэффициента электропроводности сильного электролита.
- •Методика выполнения работы
- •Измерение удельной электропроводности воды
- •Форма отчета
- •Лабораторная работа № 16. Определение растворимости и произведения растворимости труднорастворимой соли.
- •Тогда из уравнения следует
- •Методика выполнения работы
- •Форма отчета
- •Определение константы электролитического сосуда и удельной электропроводности дистиллированной воды и исследуемой соли
- •Лабораторная работа № 17. Определение буферной емкости потенцометрическим методом.
- •Измерение рН с помощью стеклянного электрода
- •Методика выполнения работы
- •Форма отчета
- •Лабораторная работа № 18. Потенциометрическое титрование кислот щелочью.
- •Кривая потенциометрического Дифференциальная кривая
- •Методика выполнения работы
- •1. Потенциометрическое титрование сильной кислоты щелочью.
- •2. Потенциометрическое титрование слабой кислоты щелочью.
- •3. Потенциометрическое титрование смеси кислот (сильная плюс слабая).
- •4. Потенциометрическое определение концентрации кислот во фруктах и овощах.
- •Форма отчета
- •Результаты потенциометрического титрования
- •Электрохимия лабораторная работа № 19. Приготовление медного кулонометра.
- •Методика выполнения работы
- •Медный кулонометр
- •Проверка калибровки амперметра
- •Форма отчета
- •Лабораторная работа № 20. Выход по току.
- •Методика выполнения работы
- •Форма отчета
- •Адсорбция
- •Лабораторная работа № 21. Адсорбция на границе жидкость – газ. Влияние жирных кислот на поверхностное натяжение воды.
- •Влияние жирных кислот на поверхностное натяжение воды
- •Методика выполнения работы
- •Форма отчета
- •Лабораторная работа № 22.
- •Методика выполнения работы
- •Форма отчета
- •Свойства коллоидных растворов контрольные вопросы
- •Лабораторная работа № 23. Получение золей и их коагуляция.
- •Методика выполнения работы Получение золей при химических реакциях
- •Определение знака заряда золей методом капиллярного анализа
- •Определение порога коагуляции золей
- •Форма отчета
- •Коагуляция золя гидрата оксида железа (III) под влиянием электролитов
- •Коагуляция золя берлинской лазури под влиянием электролитов
- •Рекомендуемая литература
Методы и аппаратура, применяемые для измерения электропроводности растворов электролитов
Электропроводность объема ионопроводящих систем рассчитывают по электрическому сопротивлению, диэлектрической и магнитной проницаемости и другим физико-химическим характеристикам. Для этого используют измерительные приборы, питаемые током в широком диапазоне частот.
Для определения сопротивления растворов собирают из отдельных стандартных конструктивных элементов мост Уитстона, работающий на переменном токе, который называют мостом Кольрауша.
Измерительное устройство (рис. 13) состоит из замкнутых четырех ветвей сопротивлений R1, R2, R3 и Rx. Источник питания переменного тока (на схеме обозначен знаком ∞) подключен к клеммам l и f. В каждой из ветвей моста возникает ток, величина которого зависит от сопротивления. Подбирая сопротивления R1, R2 и R3 при постоянном сопротивлении объема испытуемого раствора электролита Rx, помещенного в кондуктометрическую ячейку, добиваются такого распределения токов в ветвях моста, при котором ток в измерительной вертикали bd упадет до нуля. Отсутствие тока в вертикали bd. возможно при равенстве потенциалов в точках b и d. Это означает, что должны быть равными падения потенциала в ветвях аb и аd. и соответственно bс и dс. Такое состояние моста называется балансом. Следовательно, баланс возможен, если соблюдается равенство соотношений сопротивлений ветвей моста:
R2/R3 = R1/Rx (1)
Р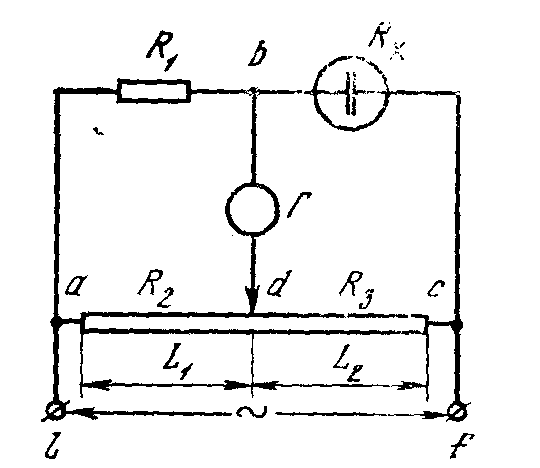 азрешая
уравнение (1) относительноRx
– искомого сопротивления раствора
электролита, получим
азрешая
уравнение (1) относительноRx
– искомого сопротивления раствора
электролита, получим
Rx = (R2/ R3) R1
г
Рис. 13.
Принципиальная схема измерительного моста
Кольрауша.
R2, R3 – постоянные сопротивления.
Клеммы ad и соединяют одинаковыми проводами (R2 = R3). К клеммам ab подключают магазин сопротивлений (R1).
Магазин сопротивлений представляет набор сопротивлений, которые подключают последовательно, чтобы ветвь моста имела необходимую величину сопротивления. Используют магазины сопротивлений со штепсельными или рычажными переключателями. Каждый рычажный переключатель обеспечивает подключение электрических сопротивлений в пределах одной декады, т. е. набора из десяти сопротивлений. Максимальное сопротивление каждой последующей декады относится к максимальному сопротивлению предыдущей, как 10:1..
Сопротивление раствора электролита Rx измеряют непосредственным отсчетом величины ветви, равной набору в магазине сопротивлений R1. При измерении подбирая сопротивление R1, добиваясь баланса моста. Так как по условию опыта R2 = R3 то в соответствии с уравнением (1) R1= Rx.
Источником питания моста служит индукционная катушка или ламповый звуковой генератор ГЗ-33, ЗГ-10 и др. с рабочей звуковой частотой от 300 до 5000 Гц. Обычно используют для работы ток частотой 1000 Гц. Выходное напряжение регулируют от 8 при малой до 30 В при большой концентрации раствора. Выход звукового генератора подключен к клеммам l и f (см. рис. 13). Нуль-инструментом Г является прибор, при помощи которого отмечают момент баланса моста. Для этого используют стрелочный гальванометр переменного тока (или постоянного тока с выпрямителем), низкоомный телефон или осциллографический индикатор и др. Полному балансу моста при работе с осциллографом должна соответствовать прямая линия на экране электроннолучевой трубки, которая сливается с линией горизонтальной развертки. Когда мост разбалансирован, на экране вычерчивается светящаяся синусоида (эллипс). При уравновешивании моста ось эллипса поворачивается и стягивается в прямую линию, сливающуюся с горизонтальной осью трубки. Полной балансировки моста, чтобы ток в вертикали bd равнялся нулю, добиться невозможно. Дело в том, что балансирующие элементы компенсируют только омическую — активную составляющую полного сопротивления, в то время как токи в ветвях реального моста, питаемого переменным током, зависят и от реактивных составляющих: емкостных и индуктивных. Реактивные составляющие сопротивления по возможности следует устранять заземлением ветвей моста и индикатора нуля, включением в плечо моста параллельно сопротивлению магазина емкости.
Поэтому момент баланса определяют по минимальному отклонению стрелки гальванометра, минимуму звука в телефоне, фиксирующем минимальный ток, или по минимальной амплитуде синусоиды на экране электроннолучевой трубки. К «равновесной» точке подходят уменьшением и увеличением сопротивления в магазине сопротивления.
Провода, соединяющие все ветви схемы, для уменьшения реактивного сопротивления должны быть по возможности прямыми, относительно большого сечения и короткими. Перед соединением окислившиеся концы проводов и зажимы тщательно зачищают наждачной бумагой, где возможно, припаивают. До подключения собранного моста к источнику питания проверяют правильность соединений ветвей схемы и контакты проводов с зажимами.
Электролитическая ячейка представляет собой сосуд, изготовленный из малорастворимого стекла типа «пирекс», в который с помощью платиновых стержней впаяны электроды из листовой платины. Расстояние между электродами жестко фиксировано и не изменяется во время эксплуатации. Для предотвращения насыщения измеряемого раствора углекислым газом из воздуха сосуд снабжен притертой пробкой. Конструкция электролитической ячейки позволяет помещать ее в термостат, при этом шарообразная форма сосуда для раствора электролита создает наилучшие условия для теплообмена с окружающей средой.
Точность определения электропроводности зависит от состояния поверхности электродов. Для получения хороших результатов электроды платинируются. Платинирование электродов осуществляется лаборантом.
