
- •Руководство к выполнению
- •Настоящее практическое пособие составлено согласно учебной программе курсов. Термохимия
- •Калориметр и методика калориметрических измерений
- •Контрольные вопросы
- •Лабораторная работа № 1. Определение теплоты гидратации соли.
- •Методика выполнения работы Определение постоянной калориметра
- •Форма отчета
- •Навески солей, взятые для растворения
- •Результаты калориметрических опытов при определении теплоты гидратации соли
- •Лабораторная работа № 2. Определение теплоты нейтрализации сильной кислоты сильным основанием.
- •Методика выполнения работы
- •Форма отчета
- •Результаты калориметрических опытов при определении теплоты нейтрализации сильных кислот сильным основанием
- •Химическое равновесие контрольные вопросы
- •Лабораторная работа № 3. Изучение равновесия гомогенной реакции в растворе.
- •Методика выполнения работы
- •Форма отчета
- •Фазовое равновесие контрольные вопросы
- •Лабораторная работа № 4. Растворение фенола в воде.
- •Методика выполнения работы
- •Форма отчета
- •Экспериментальные данные для построения диаграммы «состав — температура растворения» двойной жидкой системы вода — фенол.
- •Лабораторная работа № 5. Изучение кристаллизации вещества из растворов при низких температурах.
- •Методика выполнения работы
- •Форма отчета
- •Температура при охлаждении смеси
- •Результаты определения температуры кристаллизации
- •Лабораторная работа № 6. Определение коэффициента распределения.
- •Методика выполнения работы
- •Форма отчета
- •Определение коэффициента распределения органической кислоты между двумя несмешивающимися жидкостями: водой и эфиром
- •Молекулярные растворы Термометр Бекмана
- •Криоскоп
- •Контрольные вопросы
- •Лабораторная работа № 7.
- •Форма отчета
- •Криоскопические константы некоторых растворителей
- •Лабораторная работа № 8. Криоскопический метод определения молекулярной массы вещества по Расту (микрометод).
- •Методика выполнения работы
- •Форма отчета
- •Определение молекулярной массы исследуемого вещества по методу Раста
- •Лабораторная работа № 9. Изучение равновесия жидкость — пар в двойных жидких системах.
- •Методика выполнения работы
- •Форма отчета
- •Химическая кинетика контрольные вопросы
- •Лабораторная работа № 10. Определение порядка реакции окисления йодид-ионов ионами трехвалентного железа.
- •Методика выполнения работы
- •Определение частного порядка по отношению к I-.
- •Форма отчета
- •Лабораторная работа № 11. Изучение скорости реакции разложения комплексного оксалата марганца.
- •Фотоэлектрокалориметр фэк-м
- •Методика выполнения работы
- •Сосуд для
- •Форма отчета
- •Лабораторная работа № 12. Изучение скорости реакции разложения мурексида в кислой среде.
- •Методика выполнения работы
- •Форма отчета
- •Лабораторная работа № 13. Определение константы скорости омыления уксусноэтилового эфира в присутствии гидроксид- ионов.
- •Омыление этилацетата протекает по уравнению
- •Методика выполнения работы
- •Форма отчета
- •Результаты обратного титрования при определении константы скорости омыления сложного эфира в присутствии щелочи
- •Лабораторная работа № 14. Определение скорости разложения пероксида водорода в присутствии катализатора.
- •Методика выполнения работы
- •Форма отчета
- •Свойства электролитов контрольные вопросы
- •Методы и аппаратура, применяемые для измерения электропроводности растворов электролитов
- •Определение константы электролитического сосуда и измерение удельной электропроводности растворов электролита.
- •Удельная электропроводность водных растворов кСl при концентрации 1/50 и 1/100 моль/л
- •Константа сосуда рассчитывается по уравнению
- •Лабораторная работа № 15. Определение коэффициента электропроводности сильного электролита.
- •Методика выполнения работы
- •Измерение удельной электропроводности воды
- •Форма отчета
- •Лабораторная работа № 16. Определение растворимости и произведения растворимости труднорастворимой соли.
- •Тогда из уравнения следует
- •Методика выполнения работы
- •Форма отчета
- •Определение константы электролитического сосуда и удельной электропроводности дистиллированной воды и исследуемой соли
- •Лабораторная работа № 17. Определение буферной емкости потенцометрическим методом.
- •Измерение рН с помощью стеклянного электрода
- •Методика выполнения работы
- •Форма отчета
- •Лабораторная работа № 18. Потенциометрическое титрование кислот щелочью.
- •Кривая потенциометрического Дифференциальная кривая
- •Методика выполнения работы
- •1. Потенциометрическое титрование сильной кислоты щелочью.
- •2. Потенциометрическое титрование слабой кислоты щелочью.
- •3. Потенциометрическое титрование смеси кислот (сильная плюс слабая).
- •4. Потенциометрическое определение концентрации кислот во фруктах и овощах.
- •Форма отчета
- •Результаты потенциометрического титрования
- •Электрохимия лабораторная работа № 19. Приготовление медного кулонометра.
- •Методика выполнения работы
- •Медный кулонометр
- •Проверка калибровки амперметра
- •Форма отчета
- •Лабораторная работа № 20. Выход по току.
- •Методика выполнения работы
- •Форма отчета
- •Адсорбция
- •Лабораторная работа № 21. Адсорбция на границе жидкость – газ. Влияние жирных кислот на поверхностное натяжение воды.
- •Влияние жирных кислот на поверхностное натяжение воды
- •Методика выполнения работы
- •Форма отчета
- •Лабораторная работа № 22.
- •Методика выполнения работы
- •Форма отчета
- •Свойства коллоидных растворов контрольные вопросы
- •Лабораторная работа № 23. Получение золей и их коагуляция.
- •Методика выполнения работы Получение золей при химических реакциях
- •Определение знака заряда золей методом капиллярного анализа
- •Определение порога коагуляции золей
- •Форма отчета
- •Коагуляция золя гидрата оксида железа (III) под влиянием электролитов
- •Коагуляция золя берлинской лазури под влиянием электролитов
- •Рекомендуемая литература
Форма отчета
Указать цель работы.
Составить блок схему исследования.
3. Привести схему прибора для определения молекулярной массы по методу Раста.
4. Таблица I.
Таблица I
Определение молекулярной массы исследуемого вещества по методу Раста
Растворитель А — камфора, растворенное вещество В — ...
Вес пустой пробирки = ...
Вес пробирки + вещество В = ...
Вес пробирки + вещество В + камфора = ...
Навеска камфоры m1 = ... г; навеска вещества В m2 = ... г.
Криоскопическая константа камфоры К = ...
|
Номер капилляра |
Вещество |
Температура, °С |
Депрессия Δtºзам | ||||||
|
плавления |
кристаллизации |
средняя | |||||||
|
1 |
2 |
3 |
1 |
2 |
3 | ||||
|
1 |
Камфора |
|
|
|
|
|
|
|
|
|
2 |
Камфора+10% С10Н8 |
|
|
|
|
|
|
|
|
|
3 |
Камфора+20% С10Н8 |
|
|
|
|
|
|
|
|
|
4 |
Камфора + В |
|
|
|
|
|
|
|
|
5. Рассчитать криоскопическую константу камфоры и молекулярную массу исследуемого вещества, исходя из второго закона Рауля, по уравнению
Δ tзам.=![]() ,
,
где К– криоскопическая константа, град/моль;m(в-ва) – масса вещества, г;M– молярная масса вещества, г/моль;m(р-ля) – масса растворителя, г.
6. Вывод.
Лабораторная работа № 9. Изучение равновесия жидкость — пар в двойных жидких системах.
Цель работы:
Изучить равновесие между жидкостью и паром.
Построить равновесную диаграмму состав — температура кипения двойной жидкой системы.
Приборы и посуда:
Конические колбы объемом 20 мл;
Прибор для определения показателя преломления;
Установка для изучения равновесия жидкость-пар в двойных системах;
Кристаллизатор.
Реактивы и материалы:
1. Исследуемая система из двух органических веществ.
Методика выполнения работы
Для построения диаграммы состав — температура кипения в двойных жидких системах необходимо приготовить из двух органических жидкостей десять смесей различного процентного состава (объемные проценты). Эти смеси приготовляются в сухих конических колбочках на 20 мл с притертыми пробками.
Каждая колба должна содержать по 10 мл смеси, кроме первой и последней (100 и 0%), куда наливают 10 мл одного компонента. В таблице дано содержание высококипящей жидкости (С6Н5СН3, С6Н6, С6Н5Сl и др.) Если второй составляющей смеси является жидкость (СНз)2СО, СНСlз, ССl4 или С4Н9ОН, то смеси составляют по составу А, если вторая жидкость СНзОН — смесь составляют по составу М
|
Номер колбы |
Содержание более высококипящей жидкости, об. % | |
|
|
А |
М |
|
1 |
100 |
100 |
|
2 |
95 |
95 |
|
3 |
90 |
90 |
|
4 |
85 |
75 |
|
5 |
80 |
60 |
|
6 |
70 |
50 |
|
7 |
60 |
35 |
|
8 |
45 |
20 |
|
9 |
30 |
10 |
|
10 |
0 |
0 |
Измерив показатели преломления чистых жидкостей и растворов известного состава, вычертить кривую зависимости показателя преломления от состава (калибровочная кривая). Зная плотности чистых жидкостей, можно перейти от объемных процентов к весовым или молярным и построить график зависимости показателя преломления от состава, выраженного в весовых или молярных процентах. Пользуясь калибровочной кривой, можно по показателю преломления раствора неизвестной концентрации определить его состав. Затем определяют температуры кипения смесей.
Точное определение температур кипения представляет значительные трудности, так как жидкость может перегреваться, а пар может охлаждаться (особенно в верхних частях прибора). Для определения температур кипения служат аппараты разной конструкции, называемые эбуллиоскопами. В данной работе используется прибор (рис. 10), состоящий из сосуда 1 для кипячения, термометра 2 и холодильника 3. Внутренняя трубка холодильника вставлена в пробку так, чтобы холодильник можно было перевести в положение, необходимое для отбора пара. Укрепить в штативе сосуд для кипячения с 10 мл смеси известного состава. Во избежание перегрева жидкости для обеспечения равномерного кипения в сосуд помещают мелкие кусочки неглазурованного фарфора. После этого сосуд закрывают пробкой с термометром так, чтобы шарик термометра был погружен в жидкость. Затем соединяют сосуд с холодильником, в холодильник пускают воду и сосуд начинают медленно нагревать. После того, как температура нагреваемой жидкости установится, записывают температуру кипения, затем холодильник поворачивают в положение для отбора конденсата, т. е. открытым концом вниз. В заранее приготовленную пробирку отбирают пять-десять капель конденсата, пробирку немедленно закрывают пришлифованной пробкой. Чтобы состав пробы не изменился, пробирку следует погрузить в тающий лед или холодную воду (ни в коем случае не держать ее в руках). После этого холодильник вновь ставят в вертикальное положение и продолжают кипячение 2—3 мин и вновь записывают температуру кипения, при этом температура не должна отличаться от температуры до отбора пробы более чем на 1°. Затем нагревание прекращают, сосуд после охлаждения вынимают из прибора и содержимое выливают в колбу.
Т Рис.
10. Схема установки для изучения равновесия
жидкость – пар в двойных системах.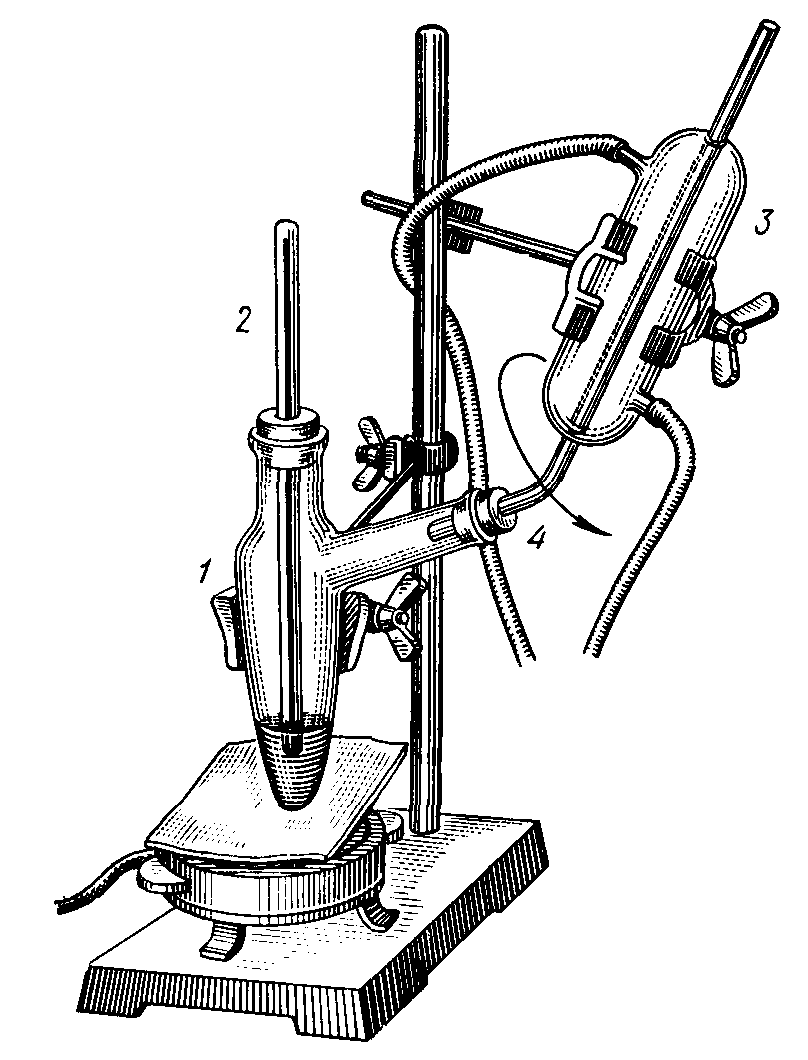
Первый график — калибровочная кривая. Второй график строят в координатах температура кипения — состав, причем нижняя кривая строится по температурам кипения до отбора пробы и по процентному составу смесей. Верхняя кривая строится по средним температурам кипения и процентному составу пара. Этот состав не может быть измерен непосредственно. Его находят интерполяцией из калибровочной кривой, беря на ней вместо коэффициента преломления жидкой смеси коэффициент преломления конденсированного пара, и определяют соответствующий процентный состав конденсата. Третий график строят в координатах состав пара — состав жидкости. Все три графика целесообразно чертить на одном листе миллиметровой бумаги, одни под другим, сохраняя абсциссу (состав) в одном и том же масштабе.
