
s5_atomfiz_exam_nah_book
.pdf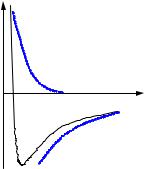
Глава 8. Уявлення про будову атомів в квантовій механіці
U ( r ) |
e 2 Z |
|
L2 |
|
U (r ) |
L2 |
|
|
|
|
r |
2 m0 r 2 |
2 m0 r 2 . |
(8.49) |
|||||||
|
|
|
||||||||
Його можна розглядати як ефективний потенціал U (r), до складу якого, крім електростатичного потенціалу, входить ще й енергія кутового руху. Залежність цього потенціалу від відстані між електроном і ядром наведена на схематичному рис.8.4.
Для Е > 0 ефективний потенціал має форму потенціального бар’єра, тому енергетичний спектр власних значень Е буде неперервним, як у вільного електрона.
Для Е < 0 ефективний потенціал має форму потенціальної ями, тому електрон в цій ямі матиме дискретний спектр власних енергій.
Розв’язок рівняння (8.48) знаходять у вигляді спеціальних по-
ліномів Лягера:
U(r) |
|
|
E > 0 |
|
2 |
0 |
r |
|
E < 0 |
|
3 |
|
1 |
Рис.8.4. Залежність потенціалу U(r) від відстані r:
1 - U1 (r) = - |
e 2 Z |
; 2 - U 2 (r) = |
|
L2 |
|
|
|
|
|
= U 2 . |
|
||||||||||
|
r |
2m0 r 2 |
; |
3 - U (r) = U1 |
|
||||||||||||||||
R |
|
|
|
|
r 2 Z |
|
C |
|
|
e |
0 ,5 |
|
|
Q |
2 1 |
( ) , |
(8.50) |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
n , |
|
a |
|
n |
n , |
|
|
|
n 1 |
||||||||||||
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
де окремі члени у (8.50) зв’язані співвідношенням
Q 2 1 |
( ) |
d ( 2 1) |
Q |
|
( ) |
d ( 2 1) |
|
||||
n 1 |
|
|
n l |
|
Находкін М.Г., Харченко Н.П., Атомна фізика |
203 |
Глава 8. Уявлення про будову атомів в квантовій механіці
|
|
|
n 1 |
|
2Z |
|
(n 1)(n 2) |
|
2Z |
2 |
|
|
|||
|
|
|
|
|
|
|
|
|
|||||||
2 1 |
1 |
1 1!(2 2) |
n |
2!(2 2)(2 3) n |
|
... |
|
||||||||
Qn 1 ( ) a0 |
|
|
|
|
|
(n 1)(n 2)...1 |
|
|
n 1 |
||||||
|
|
|
n 1 |
2Z |
|
||||||||||
|
|
( 1) |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
2!(2 2)(2 3)...(2 n 1 1) |
n |
||||||||||
|
|
|
|
|
|
|
|||||||||
Проаналізуємо власні значення Е рівняння (8.48). Введемо позначен-
ня: 2 |
2m E |
|
|
a |
|
2 |
|
|
|
|
|
|
|
|
|||||||||
0 |
|
|
|
; |
|
|
|
|
. Тоді рівняння (8.48) стає наступним: |
||||||||||||||
2 |
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
0 |
|
e2m |
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
1 |
|
|
|
|
d |
2 |
R |
|
2 dR |
|
|
|
|
2 |
|
2Z |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
2 |
(8.51) |
|||||
|
|
dr |
r dr |
|
|
a0r |
R 0 . |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
r |
|
|
|
||||||||
Розглянемо асимптотичні розв’язки (8.51). При r |
|
|||
|
d2R |
2R 0; |
R exp r , де α > 0, бо при α < 0 |
R . |
|
dr2 |
|||
|
|
|
|
|
У випадку, коли r 0 , в (8.51) повинні залишитися члени з максимальним показником степені
d 2R |
|
2 dR |
|
1 |
R 0 . |
(8.52) |
||||||||||
dr2 |
r dr |
|
|
|
|
|
|
|
||||||||
|
|
|
r2 |
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||
Розв’язок (8.52) будемо шукати у вигляді R r . Це дає наступне: |
||||||||||||||||
|
|
|
2 |
|
1 |
|
0 |
(8.53) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
1 |
|
|
|
|
|
|
1 |
|
|
|
1 |
|
|
|
|
|
|
|
|
|
(8.53*) |
||||||||
|
|
|
||||||||||||||
|
1,2 |
|
2 |
|
|
|
|
2 |
|
|
|
|
||||
Залишаємо лише перший корінь 1 |
1, бо при |
2 |
і r 0 |
|||||||||||
R . Тому залишається тільки R r 1 . |
|
|
||||||||||||
Будемо шукати розв’язок (8.51) |
у вигляді |
|
|
|||||||||||
|
|
|
R |
W r |
e r |
|
(8.54) |
|||||||
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
r |
|
|
|
|
|
|||
Після підстановки (8.54) у (851) |
отримаємо рівняння відносно W r : |
|||||||||||||
|
d2W |
2 |
dW |
|
|
2Z |
W |
1 |
W 0 |
(8.55) |
||||
|
dr2 |
dr |
|
|
||||||||||
|
|
|
a r |
|
r2 |
|
|
|||||||
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
Нехай
Находкін М.Г., Харченко Н.П., Атомна фізика |
204 |
Глава 8. Уявлення про будову атомів в квантовій механіці
|
|
W r r ak rk . |
(8.56) |
k 0 |
|
Для того щоб ряд (8.56) при r 0 та при k=0 прямував до нуля, він повинен починатись членом r +1
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
W r a r 1 |
|
|
|
|
|
|
|
|
(8.57) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Підстановкою (8.57) у (8.51) одержимо тотожність |
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
2Z |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
r |
|
0 (8.58) |
|||||||||||||||
|
|
|
|
a |
|||||||||||||||||||||||||||
|
a |
|
|
|
|
|
|
1 r |
|
|
|
2 1 |
|
|
|
||||||||||||||||
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Прирівняємо коефіцієнти при однакових показниках степенів |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|||
|
|
|
|
|
|
a 1 1 1 1 1 |
r |
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2Z |
|
|
|
|
|
|
|
|
|
|
(8.59) |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
a |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
a |
|
2 |
1 |
|
0 |
|
r |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Із (8.59) отримаємо рекурентне співвідношення: |
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
a |
|
|
|
|
|
|
|
|
2 1 |
|
2Z |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
a |
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
. |
|
|
|
|
|
(8.60) |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
a |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
1 1 1 1 |
|
|
|
|
|
|
||||||||||||||||
Для того щоб ряд (8.56) був скінченним, потрібно, щоб з певного номера його коефіцієнти дорівнювали нулю, тобто виконувалась умова
|
|
|
a |
|
|
2 1 |
|
2Z |
0 . |
(8.61) |
|
|
|||||
|
|
0 |
|
|
|
Скориставшись позначеннями використаними в (8.51), маємо:
2 |
|
2 Ea 0 |
|
E |
|
|
|
e 2 |
E 1 . |
(8.61*) |
|||||
|
|
|
|||||
Комбінуючи (8.60) і (8.61), остаточно запишемо вираз для власного значення енергії електрона
|
|
|
|
|
E |
|
E1Z 2 |
|
|
|
|
|
|
|
|
, |
(8.62) |
||
|
|
|
|
(nr 1)2 |
|||||
|
E 1 |
|
|
e 2 |
|
|
|
|
|
|
|
|
|
|
|
||||
де |
|
|
. Позначимо n = nr + + 1, тоді |
|
|||||
|
|
|
|||||||
|
|
|
|
2 a 0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Находкін М.Г., Харченко Н.П., Атомна фізика |
205 |
Глава 8. Уявлення про будову атомів в квантовій механіці
E = - |
e 2 Z 2 |
, |
(8.63) |
||
2 a |
0 n 2 |
||||
|
|
|
|||
де n = nr+ +1 - головне квантове число. Його фізичний зміст полягає в тому, що воно визначає власні енергії (енергії стаціонар-
них станів) електрона в атомі водню. Головне квантове число n
набуває всі значення від нуля до |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
n = 1, 2, 3, 4, 5,....... |
|
|
|
|
|
|
||||||
|
Розглянемо найпростіший випадок стану 1s, коли = 0, nr = 0 а |
|||||||||||||||
n = 0 + 0+ 1 = 1. Для нього із (8.51) та (8.56) можна записати |
|
|||||||||||||||
|
|
W (r) |
|
r |
|
e r |
|
1 |
|
e r |
0 0 1 |
|
r |
|
||
R |
|
|
e |
|
|
|
a r |
|
|
|
a 0r |
|
Ce |
|
. (8.64) |
|
r |
|
r |
|
|
|
|
||||||||||
|
|
|
|
|
0 |
|
|
|
r |
|
|
|
|
|||
Перевіримо, чи (8.64) є розв’язком рівняння (8.46). Для цього підста-
вимо (8.64) в (8.48)
|
d 2R |
|
2dR |
|
2m0 |
|
|
e2 Z |
|
|
2 |
( 1) |
|
(8.65) |
||||||
|
dr |
2 |
rdr |
|
|
2 |
E |
r |
|
2m0r |
2 |
|
R 0 |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
2 R |
2 |
R |
|
2 m 0 |
E R |
|
2 m 0 e 2 Z |
R 0 |
(8.66) |
|||||||||||
r |
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
2 |
|
|
|
|
2 r |
|
|
|
|
|||
Воно стає тотожністю, коли коефіцієнти при членах з однаковими степенями від 1/r стають рівними нулеві
|
2 |
|
2 m |
0 |
|
E |
0 ; |
|
|
|
|
2 Z |
|
||||
|
|
|
|
2 |
|
|
0 |
(8.67) |
|||||||||
|
|
2 |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
a 0 |
|
|||
або =Z/а0. Тоді |
E |
2Z 2 |
Z2 |
e2 |
, де а0 – радіус Бора. Таким |
||||||||||||
2m e2 |
2a |
||||||||||||||||
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
0 |
0 |
|
|
|
|
|
|||
чином, ми отримали вираз для енергії основного стану електрона в атомі водню, коли n = 1.
8.8. Радіальний розподіл електронної хмари атома водню
Проаналізуємо радіальний розподіл електронної хмари
|R*(r)R(r)|4 r2dr або ймовірність того, що електрон знаходиться в інтервалі значень r від r до r+dr. Вона є добутком густини ймовірності |R*(r)R(r)| і елементу об’єму 4 r2dr. Знайдемо її для стану 1s, в якому
Z = 1, n = 1, = 0
Находкін М.Г., Харченко Н.П., Атомна фізика |
206 |

Глава 8. Уявлення про будову атомів в квантовій механіці
|
2r |
4 r2dr C 2 |
|
2r |
|
|
w(r)dr R0R0e |
a0 |
4 r2 exp |
dr |
(8.68) |
||
1 1 |
|
|
|
a0 |
|
|
|
|
|
|
|
|
|
Ймовірність w(r) має екстремум. Знайдемо його положення
dw |
|
2 |
|
|
|
|
|
|
2 |
|
|
2 |
|
2 |
|
|
|
|
|
|
|
|
|
2r |
|
|
|
|
|
|
2r |
0 . |
|||||||||
|
C |
|
8 r exp |
|
|
|
|
C |
|
4 |
|
|
r |
|
exp |
|
|
|
|
|
dr |
|
a |
|
|
a |
|
a |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
||||
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
0 |
|
|||||
|
|
|
2 r |
2 r 2 |
0 . |
|
|
|
|
|
|
|
|
|||||||
|
|
|
a 0 |
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Екстремум знаходиться за умовою rmax = a0, тобто найбільша ймовірність знайти електрон у стані 1s атома водню має місце на відстані першої борівської орбіти а0.
Наведемо в таблиці 8.2 радіальний розподіл електронної хмари
Таблиця 8.2. Радіальна частина хвильових функцій та радіальний розподіл електронної хмари атома H для n = 1, 2, 3 = r/a0.
|
n |
|
R( ) |
R2( ) |
2R2( ) |
1s |
1 |
0 |
e- |
e-2 |
2 e-2 |
2s |
2 |
0 |
0,177(2- )e- /2 |
0,031(2- )2e- |
20,031(2- )2e- |
2p |
2 |
1 |
0,102 e- /2 |
0,010 2e- |
20,010 2e- |
3s |
3 |
0 |
0,007(27-18 +2 2)e- |
0,000005(27- |
20,000005(27- |
|
|
|
/3 |
-18 +2 2)e- |
-18 +2 2)e- |
3p |
3 |
1 |
0,01 (6- )e- /3 |
0,0001(6- )2e- /3 |
20,0001(6- )2e-2 /3 |
3d |
3 |
2 |
0,004e- /3 |
0,0000016e-2 /3 |
20,0000016e-2 /3 |
або радіальну частину атомних орбіталей в атомі водню. Він зале-
жить від квантових чисел n і .
Находкін М.Г., Харченко Н.П., Атомна фізика |
207 |
Глава 8. Уявлення про будову атомів в квантовій механіці
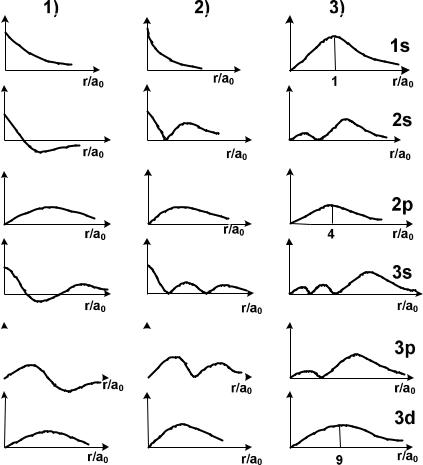
Приклади розподілу Rn, (r), Rn, 2(r) і 4 r2Rn, 2(r) для декількох квантових чисел n і наведені на рис. 8.5. Радіальна частина хви-
R10 |
R102 |
r2R102 |
R20 |
R202 |
r2R202 |
R21 |
R212 |
r2R212 |
R30 |
R302 |
r2R302 |
R31 R231
R231 r2R231
r2R231
R32 |
R322 |
r2R322 |
Рис.8.5. (1) - Rn, (r/а0) атома H, (2) - R2n, (r/а0) та (3) - r2R2n, (r/а0) .
льової функції може зменшуватись і змінювати знак, а густина радіального розподілу завжди позитивна і має характерні максимуми найбільш вірогідного знаходження електронної густини. На рис.8.6 радіальний розподіл електронної густини зображений у масштабі відстаней r.
Збільшення квантових чисел зсуває максимум електронної густини на більші відстані від ядра. Для того, щоб уявити собі повний просторовий розподіл електронної густини, користуються хвильовою
Находкін М.Г., Харченко Н.П., Атомна фізика |
208 |
Глава 8. Уявлення про будову атомів в квантовій механіці
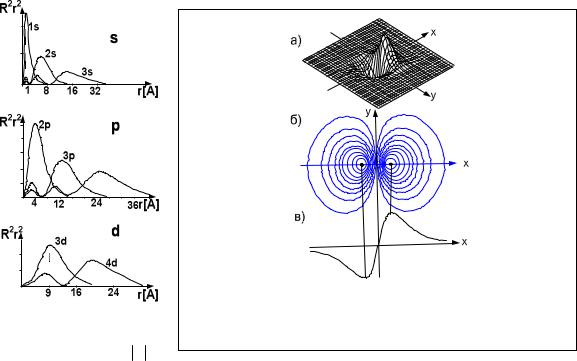
функцією (r, , ) = Rn, Y ,m( , ) і просторовий розподіл графічно зображають іншими способами. Один із прикладів такого зображення хвильової функції стану 2рх представлений на рис.8.7. Рис.8.7.а дає уявлення про трьохвимірний розподіл хвильової функції, а рис.8.7.б - про контурну карту хвильової функції, на якій кривими з’єднані точки з однаковими значеннями 2рх.
Видно, що просторовий розподіл електронної густини в стані 2рх направлений вздовж осі х. Це означає, що атомні р-орбіталі направлені вздовж певних осей.
На рис.8.7.в зображена залежність 2рх-хвильової функції від х. Вона змінює знак. Тому, при побудові атомних орбіталей їм приписують знак хвильової функції. Наприклад, на рис.8.7.б вздовж осі х > 0 атомній орбіталі приписують знак +, при х < 0 - знак мінус. 0
0
1
2
Рис.8.6. Радіальний розподіл електронної густи-
ни в атомі водню R 2 r2 .
Рис. 8.7. Радіальний розподіл електронної густини 2рх стану атому Н:
а)|R|2r2; б) контурна карта; в) псі-функція.
Находкін М.Г., Харченко Н.П., Атомна фізика |
209 |

Глава 8. Уявлення про будову атомів в квантовій механіці
8.9. Квантові числа та їх фізичний зміст
Нерелятивістська модель атома водню на основі рівняння Шредінгера визначає стаціонарні стани 3-ма квантовими числами n,
і m.
Головне квантове число n визначає енергію стаціонарного
стану
|
E |
n |
|
|
|
e 2 Z 2 |
, |
(8.69) |
|
|
|
2 a 0 n 2 |
|||||||
|
|
|
|
|
|
|
|||
|
|
a |
0 |
|
|
2 |
|
|
|
|
|
e 2 m 0 |
|
|
|||||
де |
|
|
|
|
|
, |
|
|
|
а n набуває значень: |
n = 1, 2, 3, 4,...... |
(8.70) |
|||||||
|
|
||||||||
|
Побічне або орбітальне квантове число визначає |
||||||||
квадрат моменту кількості руху |
|
L2 = [r,p]2 |
|
||||||
|
L2 = 2 |
( + 1) |
|
(8.71) |
|||||
і набуває таких дискретних значень 0 n-1 |
|
||||||||
|
= 0, 1, 2, 3, 4,....., n - 1 |
(8.72) |
|||||||
Воно подібне до числа n в моделі Бора-Зомерфельда, проте max=n -1. Так як енергія стану визначається лише головним квантовим числом,
то при даному n має місце n-кратне виродження - при даній енергії існує n станів руху з різними , тобто з різними моментами
кількості руху L 
 1 ).
1 ).
Магнітне квантове число m визначає проекцію моменту
кількості руху на вісь z |
|
Lz = m |
(8.73) |
і набуває 2 1 дискретних значень Lz, де |
|
m = 0; 1; 3; 4;..........., , |
(8.74). |
Таблиця 8.3. Кількість станів із різними значеннями квантового числа m в станах, що визначаються квантовим числом .
Стан |
s |
p |
d |
F |
|
|
|
|
|
|
0 |
1 |
2 |
3 |
2 +1 |
1 |
3 |
5 |
7 |
Находкін М.Г., Харченко Н.П., Атомна фізика |
210 |
Глава 8. Уявлення про будову атомів в квантовій механіці
При заданому значенні n може бути n2 станів із різними значеннями квантових чисел та m, тобто має місце n2 - кратне виродження. Дійсно:
n 1 |
|
1 {2 ( n 1) 1} |
|
|
|
( 2 1) |
|
n n 2 . |
(8.75) |
||
2 |
|||||
0 |
|
|
|
Таким чином, у сучасній атомній фізиці квантові числа відіграють дуже важливу роль. Вони визначають параметри стаціонарних електронних станів у атомі енергію, момент кількості руху та зв’язаний з ним магнітний момент. Квантові числа дозволяють визначати ці величини, а також можливу кількість станів та ступінь виродження енергетичних рівнів. Виродження енергетичних рівнів можна зняти за допомогою силових полів, а саме магнітного та електричного. Зняття виродження ми розглянемо в іншому розділі. Переходи між окремими стаціонарними станами супроводжуються випромінюванням квантів електромагнітних хвиль і, щоб знайти їх, потрібно використати правила відбору.
8.10. Правила відбору квантових чисел
Розглянемо перехід з одного стаціонарного стану з En і n до іншого з Eк і к. Хвильові функції цих стаціонарних станів мають вигляд
t , n , k |
n , k |
( x ) e x p |
|
|
E n , k |
|
|
|
|
i |
|
|
t |
(8.76) |
|||
|
|
|||||||
|
|
|
|
|
|
|
|
|
Знайдемо середнє значення <x> |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
x |
|
x t ,n ,k d x |
|
|
|
x n ,k d x . |
|
|
t ,n ,k |
n ,k |
(8.77) |
||||||
Зформули (8.71) видно, що в стаціонарних станах середнє значення <x> не залежить від часу. Тому й середній дипольний момент е<x> не залежить від часу. Незалежність дипольного моменту від часу означає, що в цьому випадку не відбувається випромінювання електромагнітних хвиль.
Уперехідному стані від стаціонарного стану із квантовим числом n до іншого з квантовим числом к виникає змішаний стан,
який є суперпозицією цих двох станів n і к із хвильовою функцією t
t Cn t,n Ck t,k , |
(8.78) |
Находкін М.Г., Харченко Н.П., Атомна фізика |
211 |
Глава 8. Уявлення про будову атомів в квантовій механіці
де |C*nCn| та |C*к Cк| - імовірності системи знаходитись в n або к станах. Умова нормування дає
|
С*n C*n |
+ C*к Cк = 1. |
|
(8.79) |
|||||
Обчислимо тепер середнє значення <x> для змішаного стану |
|||||||||
x |
|
|
|
|
|
|
|
||
|
|
|
|
|
|||||
(Cn t,n Ck t,n )x(Cn t,n Ck t,n )dx |
|
||||||||
|
|
|
|
|
|
|
|
||
Cn2 n x ndx Ck2 k2 x k dx |
|
(8.80) |
|||||||
|
i |
t |
( E |
E ) |
i |
t |
( E |
E |
) |
Ck Cn k x ne k |
n |
dx CnCk n x k e k |
n |
dx |
|||||
В окремому випадку зв’язаної системи із двома станами цю задачу можна спростити, бо для такої системи
*n к = *к n і |
С*n Cк = C*n Cк |
|
|||||
і формула (8.74) набуває вигляду |
|
|
|||||
x C n2 x n C k2 x k C n C k x n ,k (ei kn t e i kn t ) |
|
||||||
Cn2 x n Ck2 x k |
2C n Ck x nk |
cos kn t |
|
||||
де |
k n |
1 |
E k E n |
|
|
||
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
x k n |
|
k x n d x |
. |
(8.81) |
|||
|
|
|
|
|
|
|
|
Вираз (8.75) |
називається матричним елементом переходу |
||||||
електрона з одного стану із квантовим числом n до іншого стану з квантовим числом к. Якщо під час цього переходу матричний елемент <x>кn не дорівнює нулеві ( <x>к,n 0 ), то й дипольний момент е<x>к,n 0. Це означає, що при такому переході диполь випромінює електромагнітні хвилі із частотою, яка визначається за правилом частот Бора Ek En .
Таким чином, матричний елемент визначає дозволені й
заборонені переходи, тобто правила відбору: |
|
|
xkn 0 |
заборонені переходи; |
|
xkn 0 дозволені переходи . |
(8.82) |
|
Визначимо для прикладу правило відбору для магнітного числа |
||
m для дипольних або |
довгохвильових переходів |
(при умові |
Находкін М.Г., Харченко Н.П., Атомна фізика |
212 |
