
- •Міністерство освіти і науки україни
- •І. Обробка та оформлення результатів лабораторних робіт
- •Іі. Правила роботи в лабораторії з фізичної хімії і техніка безпеки
- •Ліквідація нещасних випадків і надання першої допомоги
- •Ііі. Агрегатний стан речовин
- •1. Визначення маси моля речовини вимірюванням її об’єму в газоподібному стані
- •2. Визначення в’язкості системи етиловий спирт – вода
- •I. Хімічна термодинаміка
- •1. Визначення теплоти згоріння речовин за допомогою калориметра юнкерса
- •Експериментальна частина
- •2. Визначення теплоти розчинення і теплоти гідратації солі
- •V. Поверхневі явища (поверхнева енергія, поверхневий натяг та адсорбція на межі розділу фаз)
- •1. Визначення поверхневого натягу розчинів методом відліку крапель (сталагмометричним методом)
- •Поверхневий натяг води в залежності від температури
- •Густина води в залежності від температури
- •Густина розчинів NaCl при 293 к
- •2. Визначення площі та довжини молекули поверхнево-активної речовини
- •3. Адсорбція оцтової кислоти на активованому вугіллі
- •Методика експерименту
- •4. Дослідження адсорбції забарвлених речовин із розчинів
- •5. Дослідження адсорбції ізоамілового спирту із розчину за допомогою активованого вугілля
- •6. Визначення повної обмінної ємності (оє) катіоніту
- •7. Визначення вмісту лікарської речовини (глюконату кальцію) в розчині методом йонообмінної адсорбції
- •8. Обезсолювання води за допомогою йонітів
- •VI. Розчини неелектролітів
- •1. Визначення критичної температури взаємного розчинення рідин
- •2. Визначення молекулярної маси розчиненої речовини кріоскопічним методом
- •VII. Розчини електролітів
- •1. Визначення електропровідності електролітів і обчислення ступеня дисоціації
- •Експериментальна частина
- •Робота на змінному струмові
- •2. Bизначення розчинності малорозчинних сполук
- •3. Визначення іонного добутку води
- •4.Визначення концентрації кислоти методом кондуктометричного титрування
- •5. Визначення вмісту лікарської речовини в розчині
- •Хід роботи
- •Обробка результатів експерименту
- •VIII. Гальванічні елементи та електродні потенціали
- •1. Вимірювання електрорушійних сил гальванічних елементів
- •2. Визначення водневого показникa потенціометричним методом
- •3. Потенціометричне визначення рН, розрахунок константи дисоціації слабкої кислоти
- •Іх. Хімічна кінетика і каталіз
- •1. Визначення швидкості розкладу тіосульфатної кислоти
- •Дослід 1. Залежність швидкості розкладу тіосульфатної кислоти від її молярної концентрації
- •Дослід 2. Залежність швидкості розкладу тіосульфатної кислоти від температури
- •Виконання роботи
- •Склад реакційної суміші
- •Результати титрування
- •3. Дослідження гідролізу крохмалю в присутності соляної кислоти
- •4. Дослідження гідролізу крохмалю в присутності ферментів і соляної кислоти при температурі 310 к
- •5. Визначення швидкості розкладу пероксиду водню газометричним методом
- •6. Фотохімічний розклад н2о2
- •Послідовність виконання роботи
- •Х. Фізикохім ія дисперсних систем.
- •1. Методи одержання колоїдних розчинів
- •2. Коагуляція колоїдних розчинів електролітами
- •3. Визначення величини електрокінетичного потенціалу методом електрофорезу
- •4. Вивчення ізоелектричної точки білків
- •5. Набухання гелів
- •Хід виконання роботи
- •Хі. Біогенні елементи
- •1. Аналітичні реакції на йони s-елементів
- •Визначення хлор-йонів Cl– в питних водах за методом Фольгарда
- •2. Аналітичні реакції на р-елементи та їх сполуки
- •Реакція на бор (ііі) по кольору полум’я
- •Реакція на йон з розведеними кислотами
- •Реакція на йон з реактивом Несслера
- •Реакція на йон із розчином хлориду барію
- •(Реакція л.А. Чугаєва)
- •Контрольні питання до колоквіумів іii. Агрегатний стан речовин
- •Іv. Хімічна термодинаміка та біоенергетика
- •V. Поверхневі явища (поверхнева енергія, поверхневий натяг та адсорбція на межі розділу фаз)
- •Vі. Розчини неелектролітів
- •Vіі. Розчини електролітів
- •Vііі. Гальванічні елементи та електродні потенціали
- •IX. Хімічна кінетика і каталіз
- •Х. Фізикохімія дисперсних систем
- •Хі. Біогенні елементи
- •Додатки
- •Деякі фізичні константи
- •Густина деяких речовин
- •Густина деяких газів (н.У.)
- •Співвідношення між позасистемними одиницями
- •Пояснювальна записка
- •Зміст дисципліни
- •Тема 1. Предмет фізичної хімії та її значення. Розділи фізичної хімії. Методи дослідження. Розвиток фізичної хімії в Україні.
- •Тема 7.
- •Тема 8.
- •Тема 9.
- •Тема 10.
- •Тема 11.
- •Тема 12.
- •Тема 13.
- •Тема 14.
- •Орієнтовний перелік питань до підсумкового контролю знань з дисципліни.
- •Cписок літератури
- •І. Обробка та оформлення результатів
- •Гомонай Василь Іванович
Поверхневий натяг води в залежності від температури
|
Т, К |
Поверхневий натяг води, Н/м10–2 |
|
273 |
75,64 |
|
283 |
74,22 |
|
293 |
72,75 |
|
303 |
71,18 |
|
313 |
69,56 |
|
323 |
67,91 |
|
333 |
66,18 |
Таблиця 3
Густина води в залежності від температури
|
Т, К |
Густина, кг/м3 |
Т, К |
Густина, кг/м3 |
Т, К |
Густина, кг/м3 |
|
277 |
1000,00 |
286 |
999,40 |
295 |
997,80 |
|
278 |
999,99 |
287 |
999,30 |
296 |
997,65 |
|
279 |
999,97 |
288 |
999,13 |
297 |
997,32 |
|
280 |
999,93 |
289 |
998,97 |
298 |
997,07 |
|
281 |
999,88 |
290 |
998,80 |
299 |
996,81 |
|
282 |
999,81 |
291 |
998,62 |
300 |
996,54 |
|
283 |
999,73 |
292 |
998,43 |
301 |
996,26 |
|
284 |
999,63 |
293 |
998,23 |
302 |
995,97 |
|
285 |
999,52 |
294 |
998,02 |
303 |
995,67 |
Таблиця 4
Густина розчинів NaCl при 293 к
|
Конц. NaCl, н. |
Густина, кг/м3 |
|
0,1 |
994,7 |
|
0,25 |
1003,1 |
|
0,5 |
1018,5 |
|
1,0 |
1032,8 |
2. Визначення площі та довжини молекули поверхнево-активної речовини
Для виконання роботи потрібно визначити поверхневий натяг декіль- кох розчинів поверхнево-активної речовини різної молярної концентрації (за вказівкою викладача). Вимірювання поверхневого натягу проводять сталагмометричним методом, як описано вище.
Для визначення величини адсорбції находять різницю величини по- верхневого натягу 2 і 1, які виміряли для двох сусідніх розчинів різної молярної концентрації с2(Х) і с1(Х) . Цю різницю 2 – 1 = і с2(Х) – с1(Х)=с(Х) підставляють у рівняння Гіббса:
![]() ,
,
де Г – величина адсорбції, моль/м2;
с(х) – молярна концентрація поверхнево-активної речовини, моль/м3;
R – газова стала, дорівнює 8,31 Дж/моль.К;
Т – абсолютна температура, К;
σ – поверхневий натяг, Дж/м2.
В цьому випадку в
якості с(х)
беруть середнє арифметичне
![]() .
Потім розраховуютьсср.(х)
і будують графік залежності
.
Потім розраховуютьсср.(х)
і будують графік залежності
![]() (вісь ординат) відсср.(х)
(вісь абсцис). Проводять пряму, за
тангенсом кута якої знаходять Г.
(вісь ординат) відсср.(х)
(вісь абсцис). Проводять пряму, за
тангенсом кута якої знаходять Г.
Одержані дані заносять в таку таблицю:
|
№№ п/п |
с(х), моль/м3 |
σ, Дж/м2 |
сср.(Х), моль/м3 |
Δс(Х), моль/м3 |
Δσ, Дж/м2 |
Г, моль/м2 |
сср.(Х) моль/м3 |
|
|
|
|
|
|
|
|
|
Розрахувати площу (S) і довжину (l) молекули поверхнево-активної речовини:
![]() ,
,
де N – постійна Авогадро, дорівнює 6,021023 моль–1;
Гmax – величина граничної адсорбції, моль/м2;
М(Х) – молярна маса ПАР, кг/моль;
ρ – густина ПАР, кг/м3.
3. Адсорбція оцтової кислоти на активованому вугіллі
Ізотерми адсорбції ряду речовин із розчину на поверхні твердого тіла в області середніх концентрацій задовільно описуються емпіричним рів- нянням Фрейндліха:
![]() ,
(1)
,
(1)
де Х – кількість адсорбтиву, ммоль;
m – маса адсорбенту, кг;
![]() –величини
адсорбції, кмоль/кг;
–величини
адсорбції, кмоль/кг;
К
і
![]() – емпіричні константи, залежні від
природи адсорбенту і адсорбативу;
– емпіричні константи, залежні від
природи адсорбенту і адсорбативу;
с – рівноважна молярна концентрація адсорбативу, моль/м3.
Величина адсорбції
![]() абоа
розраховується за формулою:
абоа
розраховується за формулою:
![]() .
(2)
.
(2)
Якщо прологарифмуємо рівняння (1), то воно набуде вигляду:
![]() .
(3)
.
(3)
Одержане рівняння є рівнянням прямої лінії.
Д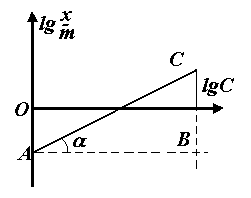 ля
визначенняК
і
ля
визначенняК
і
![]() находять логарифми значень с
і
находять логарифми значень с
і
![]() і будують графік (див. рисунок: по осі
абсцисlgc,
а по осі ординат lg
і будують графік (див. рисунок: по осі
абсцисlgc,
а по осі ординат lg![]() ).
Величина відрізкуАО
дорівнює lgK.
За значенням логарифму находять К.
Постійна
).
Величина відрізкуАО
дорівнює lgK.
За значенням логарифму находять К.
Постійна
![]() дорівнює tgα
або відношенню довжин відрізків СВ
і АВ,
тобто
дорівнює tgα
або відношенню довжин відрізків СВ
і АВ,
тобто
![]() .
.
