
- •Міністерство освіти і науки україни
- •І. Обробка та оформлення результатів лабораторних робіт
- •Іі. Правила роботи в лабораторії з фізичної хімії і техніка безпеки
- •Ліквідація нещасних випадків і надання першої допомоги
- •Ііі. Агрегатний стан речовин
- •1. Визначення маси моля речовини вимірюванням її об’єму в газоподібному стані
- •2. Визначення в’язкості системи етиловий спирт – вода
- •I. Хімічна термодинаміка
- •1. Визначення теплоти згоріння речовин за допомогою калориметра юнкерса
- •Експериментальна частина
- •2. Визначення теплоти розчинення і теплоти гідратації солі
- •V. Поверхневі явища (поверхнева енергія, поверхневий натяг та адсорбція на межі розділу фаз)
- •1. Визначення поверхневого натягу розчинів методом відліку крапель (сталагмометричним методом)
- •Поверхневий натяг води в залежності від температури
- •Густина води в залежності від температури
- •Густина розчинів NaCl при 293 к
- •2. Визначення площі та довжини молекули поверхнево-активної речовини
- •3. Адсорбція оцтової кислоти на активованому вугіллі
- •Методика експерименту
- •4. Дослідження адсорбції забарвлених речовин із розчинів
- •5. Дослідження адсорбції ізоамілового спирту із розчину за допомогою активованого вугілля
- •6. Визначення повної обмінної ємності (оє) катіоніту
- •7. Визначення вмісту лікарської речовини (глюконату кальцію) в розчині методом йонообмінної адсорбції
- •8. Обезсолювання води за допомогою йонітів
- •VI. Розчини неелектролітів
- •1. Визначення критичної температури взаємного розчинення рідин
- •2. Визначення молекулярної маси розчиненої речовини кріоскопічним методом
- •VII. Розчини електролітів
- •1. Визначення електропровідності електролітів і обчислення ступеня дисоціації
- •Експериментальна частина
- •Робота на змінному струмові
- •2. Bизначення розчинності малорозчинних сполук
- •3. Визначення іонного добутку води
- •4.Визначення концентрації кислоти методом кондуктометричного титрування
- •5. Визначення вмісту лікарської речовини в розчині
- •Хід роботи
- •Обробка результатів експерименту
- •VIII. Гальванічні елементи та електродні потенціали
- •1. Вимірювання електрорушійних сил гальванічних елементів
- •2. Визначення водневого показникa потенціометричним методом
- •3. Потенціометричне визначення рН, розрахунок константи дисоціації слабкої кислоти
- •Іх. Хімічна кінетика і каталіз
- •1. Визначення швидкості розкладу тіосульфатної кислоти
- •Дослід 1. Залежність швидкості розкладу тіосульфатної кислоти від її молярної концентрації
- •Дослід 2. Залежність швидкості розкладу тіосульфатної кислоти від температури
- •Виконання роботи
- •Склад реакційної суміші
- •Результати титрування
- •3. Дослідження гідролізу крохмалю в присутності соляної кислоти
- •4. Дослідження гідролізу крохмалю в присутності ферментів і соляної кислоти при температурі 310 к
- •5. Визначення швидкості розкладу пероксиду водню газометричним методом
- •6. Фотохімічний розклад н2о2
- •Послідовність виконання роботи
- •Х. Фізикохім ія дисперсних систем.
- •1. Методи одержання колоїдних розчинів
- •2. Коагуляція колоїдних розчинів електролітами
- •3. Визначення величини електрокінетичного потенціалу методом електрофорезу
- •4. Вивчення ізоелектричної точки білків
- •5. Набухання гелів
- •Хід виконання роботи
- •Хі. Біогенні елементи
- •1. Аналітичні реакції на йони s-елементів
- •Визначення хлор-йонів Cl– в питних водах за методом Фольгарда
- •2. Аналітичні реакції на р-елементи та їх сполуки
- •Реакція на бор (ііі) по кольору полум’я
- •Реакція на йон з розведеними кислотами
- •Реакція на йон з реактивом Несслера
- •Реакція на йон із розчином хлориду барію
- •(Реакція л.А. Чугаєва)
- •Контрольні питання до колоквіумів іii. Агрегатний стан речовин
- •Іv. Хімічна термодинаміка та біоенергетика
- •V. Поверхневі явища (поверхнева енергія, поверхневий натяг та адсорбція на межі розділу фаз)
- •Vі. Розчини неелектролітів
- •Vіі. Розчини електролітів
- •Vііі. Гальванічні елементи та електродні потенціали
- •IX. Хімічна кінетика і каталіз
- •Х. Фізикохімія дисперсних систем
- •Хі. Біогенні елементи
- •Додатки
- •Деякі фізичні константи
- •Густина деяких речовин
- •Густина деяких газів (н.У.)
- •Співвідношення між позасистемними одиницями
- •Пояснювальна записка
- •Зміст дисципліни
- •Тема 1. Предмет фізичної хімії та її значення. Розділи фізичної хімії. Методи дослідження. Розвиток фізичної хімії в Україні.
- •Тема 7.
- •Тема 8.
- •Тема 9.
- •Тема 10.
- •Тема 11.
- •Тема 12.
- •Тема 13.
- •Тема 14.
- •Орієнтовний перелік питань до підсумкового контролю знань з дисципліни.
- •Cписок літератури
- •І. Обробка та оформлення результатів
- •Гомонай Василь Іванович
V. Поверхневі явища (поверхнева енергія, поверхневий натяг та адсорбція на межі розділу фаз)
1. Визначення поверхневого натягу розчинів методом відліку крапель (сталагмометричним методом)
Для роботи необхідні: сталагмометр; пікнометр; стаканчик на 50 мл.
Вільна поверхнева енергія, вірніше, надлишок вільної енергії на одиницю площі поверхневого шару на межі розділу рідина – повітря, називається поверхневим натягом, а на межі розділу рідина – рідина – граничним натягом .
Одиницями виміру поверхневого натягу може бути Дж/м2 у випадку, коли його розглядають як надлишок вільної енергії поверхні розділу двох фаз, що накопичується на цій поверхні за рахунок нескомпенсованих міжмолекулярних сил, і в Н/м у випадку, якщо розглянути роботу утво- рення одиниці нової поверхні.
Існує декілька методів визначення поверхневого натягу.
Найбільш розповсюдженим методом є сталагмометричний (метод відліку крапель).
В основі методу лежить експериментально встановлене положення, що вага краплі, яка повільно відривається під дією сили тяжіння від кін- чика вертикальної трубки сталагмометра, буде тим більшою, чим більший поверхневий натяг рідини на межі з повітрям.
Вважається, що сила поверхневого натягу F, що діє вертикально по колу трубки, приблизно рівна F = 2r, підтримує краплю, зрівноважуючи її вагу P. У момент відриву краплі можна вважати ці сили рівними:
![]() ,
,
![]() ,
,
де F – сила поверхневого натягу; P – сила ваги краплі; – коефіцієнт пропорційності, який зв’язує силу поверхневого натягу з периметром (в даному випадку, з довжиною кола капіляру, з якого витікає рідина).
При
2r
= 0,01 м
коефіцієнт пропорційності рівний силі
поверхневого натягу, тобто
![]() .
.
Визначення радіусу капіляру зв’язане з деякими труднощами і тому практично визначають поверхневий натяг відносно стандартної рідини з відомим поверхневим натягом. Стандартною рідиною може бути тільки така рідина, яка утворює краплі, близькі по об’єму до крапель дослід- жуваної рідини.
При утворенні краплі сила поверхневого натягу досліджуваної речовини дорівнює F=2 r (якщо вимірювання проводиться в одному і тому ж сталагмометрі).
Силу поверхневого натягу визначити важко, тому при експеримен- тальних дослідженнях визначають вагу краплі, яка в момент відриву приблизно дорівнює силі поверхневого натягу.
Сила ваги одної краплі досліджуваної рідини
![]() ,
,
де Vр – об’єм рідини, що витікає з сталагмометра;
ρ – густина рідини;
n – число крапель досліджуваної рідини в об’ємі;
g – прискорення сили земного тяжіння.
Аналогічний вираз при одному і тому ж об’ємі приладу можна записати і для стандартної рідини
![]() .
.
Беруть співвідношення цих рівнянь
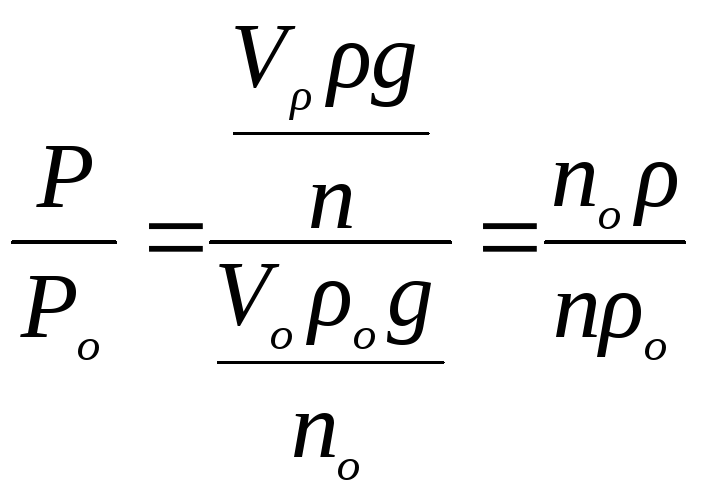 .
.
А так як
![]() ,
тоді
,
тоді
![]() .
.
Розв’язавши це рівняння відносно поверхневого натягу досліджуваної речовини, одержуємо розрахункову формулу:
![]() ,
,
де о, ρo – поверхневий натяг і густина стандартної рідини.
Якщо за стандартну рідину береться вода, то о при температурі дос- ліду беруть з табл. 2, що знаходиться в кінці опису. ρo для води приблизно дорівнює одиниці.
При досліджуванні розведених розчинів (розчини ізоамілового спирту) густину ρ також можна прийняти за 1.
Густина концентрованих розчинів хлористого натрію береться з табл. 4, а густина води в залежності від температури – з табл. 3.
При дослідженні чистих рідин їх густину необхідно визначити. n, no – число крапель стандартної і досліджуваної речовини, визначається з допо- могою сталагмометра.

Визначення поверхневого натягу зводиться до відліку кількості крапель, що витікають з капіляру.
Через каучукову трубку, що знаходиться на верхньому кінці втягують рідину вище мітки. Відлік крапель починають тоді, коли рідина проходить міт- ку. Відраховують число крапель від мітки до остан- ньої краплини.
Спочатку
проводять виміри із стандартною рідиною,
якщо це вода, то немає необхідності
сушити сталагмометр при переході до
водних розчинів. Визначення ведуть,
починаючи з розбав-
лених розчинів,
переходячи до більш концентрованих.
Для кожного роз-
чину визначення
кількості крапель проводять не менше
трьох разів і знаходять середню кількість
крапель. З одержаних даних розраховують
поверхневий натяг розчинів
поверхнево-активних і поверхнево-неактивних
речовин. Будують ізотерму поверхневого
натягу в координатах
![]() .
.
Результати досліду і розрахункові дані записуються в табл. 1.
Таблиця 1
|
Кількість крапель |
Густина, кг/м3 |
Поверхневий натяг, Н/м10-2 | |
|
Дослід |
Середнє значення | ||
|
1 |
|
|
|
|
2 |
|
|
|
|
3 |
|
|
|
Таблиця 2
