
- •Міністерство освіти і науки україни
- •І. Обробка та оформлення результатів лабораторних робіт
- •Іі. Правила роботи в лабораторії з фізичної хімії і техніка безпеки
- •Ліквідація нещасних випадків і надання першої допомоги
- •Ііі. Агрегатний стан речовин
- •1. Визначення маси моля речовини вимірюванням її об’єму в газоподібному стані
- •2. Визначення в’язкості системи етиловий спирт – вода
- •I. Хімічна термодинаміка
- •1. Визначення теплоти згоріння речовин за допомогою калориметра юнкерса
- •Експериментальна частина
- •2. Визначення теплоти розчинення і теплоти гідратації солі
- •V. Поверхневі явища (поверхнева енергія, поверхневий натяг та адсорбція на межі розділу фаз)
- •1. Визначення поверхневого натягу розчинів методом відліку крапель (сталагмометричним методом)
- •Поверхневий натяг води в залежності від температури
- •Густина води в залежності від температури
- •Густина розчинів NaCl при 293 к
- •2. Визначення площі та довжини молекули поверхнево-активної речовини
- •3. Адсорбція оцтової кислоти на активованому вугіллі
- •Методика експерименту
- •4. Дослідження адсорбції забарвлених речовин із розчинів
- •5. Дослідження адсорбції ізоамілового спирту із розчину за допомогою активованого вугілля
- •6. Визначення повної обмінної ємності (оє) катіоніту
- •7. Визначення вмісту лікарської речовини (глюконату кальцію) в розчині методом йонообмінної адсорбції
- •8. Обезсолювання води за допомогою йонітів
- •VI. Розчини неелектролітів
- •1. Визначення критичної температури взаємного розчинення рідин
- •2. Визначення молекулярної маси розчиненої речовини кріоскопічним методом
- •VII. Розчини електролітів
- •1. Визначення електропровідності електролітів і обчислення ступеня дисоціації
- •Експериментальна частина
- •Робота на змінному струмові
- •2. Bизначення розчинності малорозчинних сполук
- •3. Визначення іонного добутку води
- •4.Визначення концентрації кислоти методом кондуктометричного титрування
- •5. Визначення вмісту лікарської речовини в розчині
- •Хід роботи
- •Обробка результатів експерименту
- •VIII. Гальванічні елементи та електродні потенціали
- •1. Вимірювання електрорушійних сил гальванічних елементів
- •2. Визначення водневого показникa потенціометричним методом
- •3. Потенціометричне визначення рН, розрахунок константи дисоціації слабкої кислоти
- •Іх. Хімічна кінетика і каталіз
- •1. Визначення швидкості розкладу тіосульфатної кислоти
- •Дослід 1. Залежність швидкості розкладу тіосульфатної кислоти від її молярної концентрації
- •Дослід 2. Залежність швидкості розкладу тіосульфатної кислоти від температури
- •Виконання роботи
- •Склад реакційної суміші
- •Результати титрування
- •3. Дослідження гідролізу крохмалю в присутності соляної кислоти
- •4. Дослідження гідролізу крохмалю в присутності ферментів і соляної кислоти при температурі 310 к
- •5. Визначення швидкості розкладу пероксиду водню газометричним методом
- •6. Фотохімічний розклад н2о2
- •Послідовність виконання роботи
- •Х. Фізикохім ія дисперсних систем.
- •1. Методи одержання колоїдних розчинів
- •2. Коагуляція колоїдних розчинів електролітами
- •3. Визначення величини електрокінетичного потенціалу методом електрофорезу
- •4. Вивчення ізоелектричної точки білків
- •5. Набухання гелів
- •Хід виконання роботи
- •Хі. Біогенні елементи
- •1. Аналітичні реакції на йони s-елементів
- •Визначення хлор-йонів Cl– в питних водах за методом Фольгарда
- •2. Аналітичні реакції на р-елементи та їх сполуки
- •Реакція на бор (ііі) по кольору полум’я
- •Реакція на йон з розведеними кислотами
- •Реакція на йон з реактивом Несслера
- •Реакція на йон із розчином хлориду барію
- •(Реакція л.А. Чугаєва)
- •Контрольні питання до колоквіумів іii. Агрегатний стан речовин
- •Іv. Хімічна термодинаміка та біоенергетика
- •V. Поверхневі явища (поверхнева енергія, поверхневий натяг та адсорбція на межі розділу фаз)
- •Vі. Розчини неелектролітів
- •Vіі. Розчини електролітів
- •Vііі. Гальванічні елементи та електродні потенціали
- •IX. Хімічна кінетика і каталіз
- •Х. Фізикохімія дисперсних систем
- •Хі. Біогенні елементи
- •Додатки
- •Деякі фізичні константи
- •Густина деяких речовин
- •Густина деяких газів (н.У.)
- •Співвідношення між позасистемними одиницями
- •Пояснювальна записка
- •Зміст дисципліни
- •Тема 1. Предмет фізичної хімії та її значення. Розділи фізичної хімії. Методи дослідження. Розвиток фізичної хімії в Україні.
- •Тема 7.
- •Тема 8.
- •Тема 9.
- •Тема 10.
- •Тема 11.
- •Тема 12.
- •Тема 13.
- •Тема 14.
- •Орієнтовний перелік питань до підсумкового контролю знань з дисципліни.
- •Cписок літератури
- •І. Обробка та оформлення результатів
- •Гомонай Василь Іванович
Хід роботи
В 4–5 конічних колб вносять точні маси чистого препарату, до- дають із бюретки по 50 мл НСl визначеної концентрації. Маси розра- ховують так, щоб відношення концентрації речовини, що визначають, і реагенту знаходилось в межах 0,5–0,95. Розчини перемішують і вимірюють опір чистого реагенту НСl і всіх розчинів при Т=298 К. Таблетку неві- домого складу зважують, потім подрібнюють до порошку і вносять в чис- тий розчин реагенту (50 мл), повністю розчиняють (дозволяється каламут- ність нерозчинних домішок). Іноді потрібен підігрів розчину на водяній бані. Вимірюють опір одержаного розчину.
Обробка результатів експерименту
Для
кожного розчину розраховують за рівнянням
опір
![]() і зміну питомої електричної провідності
Δχ по рівнянню (1), будують залеж-
ність
і зміну питомої електричної провідності
Δχ по рівнянню (1), будують залеж-
ність![]() і методом найменших квадратів розраховують
коефі-
цієнтиа
і b
рівняння (3). Розраховують χ і Δχ у досліді
з таблеткою і за каліброваним графіком
або рівнянням (3) знаходять масу речовини
в таблетці, що аналізується. Оцінюють
похибку аналізу, підставивши у рівняння
(3) величини Δχ і зрівнявши взяті наважки
з розрахованими по рівнянню.
і методом найменших квадратів розраховують
коефі-
цієнтиа
і b
рівняння (3). Розраховують χ і Δχ у досліді
з таблеткою і за каліброваним графіком
або рівнянням (3) знаходять масу речовини
в таблетці, що аналізується. Оцінюють
похибку аналізу, підставивши у рівняння
(3) величини Δχ і зрівнявши взяті наважки
з розрахованими по рівнянню.
Результати досліду і розрахунки заносять у таблицю:
|
№п/п |
Маса наважки т, кг |
Опір R, Ом |
Питома електрична провідність χ, Ом–1м–1 |
Зміна питомої електричної провідності, Δχ, Ом–1м–1 |
|
|
|
|
|
|
VIII. Гальванічні елементи та електродні потенціали
1. Вимірювання електрорушійних сил гальванічних елементів
Для роботи необхідно: акумулятор на 1,2 V – Ак; гальванометр – Г; нормальний елемент Вестона Еп; елемент з невідомою ЕРС – Ех; реохорд АВ; ключ для вмикання К; перемикач на шість клем П; провідники струму; розчини CuSO4, ZnSO4; насичений розчин KCl.
Прилад, в якому відбувається перетворення хімічної енергії в елек- тричну, називається гальванічним елементом. Його можна зобразити схе- мою
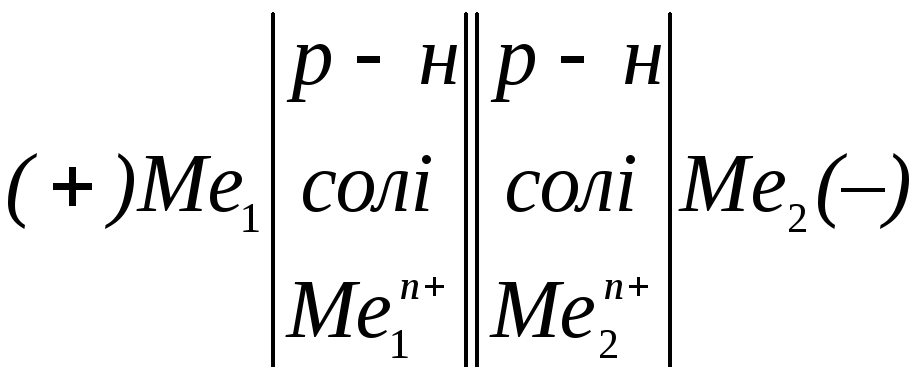
ЕРС такого елемента в більшості випадків виміряють двома мето- дами: ввімкненням у ланцюг чутливого вольтметра або компенсаційним методом. Перший з цих методів має деякі недоліки, зв’язані з проход- женням через прилад електричного струму. Ці недоліки усуваються при визначенні ЕРС компенсаційним методом, коли через елемент струм не проходить.
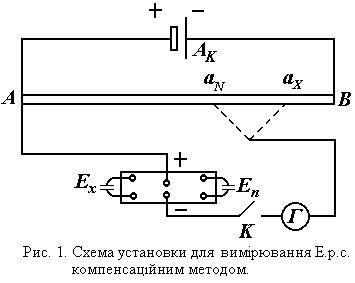
Схема установки для вимірювання ЕРС
компенсаційним методом.
Принцип методу компенсації полягає в тому, що до елемента з невідо- мою ЕРС приєднують інший елемент, ЕРС якого направлена назустріч (джерело струму). При цьому відбувається взаємна компенсація двох електрорушійних сил – досліджуваного елемента і джерела струму.
Схема
установки для компенсаційного методу
подана на рисунку. Акумулятор
АК замкнутий через дротину АВ, що
натягується вздовж шкали реохорду
довжиною 1 м. Дротина на всій довжині
реохорда однорідна і має однаковий
переріз, тому спад напруги на одиницю
довжини теж однаковий і рівний
![]() ,
а спад напруги на всій довжині реохорда
рівний:
,
а спад напруги на всій довжині реохорда
рівний:
|
|
|
(1) |
де І – сила струму;
r – опір одиниці довжини дротини (питомий опір).
Якщо в коло назустріч акумуляторові ввімкнули елемент з невідомою ЕРС, то, переміщуючи повзунок С по лінійці АВ, можна знайти таке положення, при якому стрілка гальванометра Г стає на нуль.
Це відбувається внаслідок того, що ЕРС гальванічного елемента Ех точно компенсується різницею потенціалів у межах між точками А і В. Якщо ця різниця потенціалів більша від ЕРС елемента, то стрілка галь- ванометра відхиляється в одну сторону. Якщо ЕРС гальванічного елемента більша за різницю потенціалів на лінійці, то спостерігається відхилення стрілки гальванометра в протилежну сторону.
Необхідно знати ці два положення, потім зменшувати інтервал між ними до того часу, поки стрілка гальванометра прийме нульове положення.
Якщо гальванометр знаходиться в нульовому положенні, а повзунок на віддалі ах, тоді
![]() ,
а
,
а
![]() .
.
Із співвідношення
![]() ,
,
знаходимо
|
|
|
(2) |
Але ЕРС акумулятора невідома і тим більше в процесі роботи вона може змінюватись. Тому перш ніж компенсувати Ех, в електричне коло замість досліджуваного елементу включають нормальний елемент Вестона ЕN, ЕРС якого відома.
При компенсації ЕN і ЕРС акумулятора одержуємо певне положення контакта аN, тоді
|
|
|
(3) |
Із співвідношення
|
|
|
|
знаходимо
|
|
|
(4) |
Підставивши рівняння (4) у рівняння (2), знаходимо ЕхЕРС дослід- жуваного елементу:
|
|
|
(5) |
Експериментальна частина роботи виконується у наступному по- рядку.
По наведеній схемі компенсують спочатку нормальний елемент Вес- тона, потім мідно-цинковий елемент і тільки після цього каломельно-цинковий. З одержаних даних по формулі (5) розраховують ЕРС дослід- жуваних елементів.
Із значення ЕРС каломельно-цинкового елементу розраховують по- тенціал цинкового електроду. Потенціал каломельного електроду по від- ношенню до цинкового буде позитивним. Значення його в залежності від температури подані на с. 51.
Величину потенціалу цинкового електроду обраховують, виходячи із співвідношення:
|
|
|
(6) |
Результати досліду і розрахункові дані записуються в таблицю:
|
Елемент |
Покази на лінійці |
ЕРС |
Електродний потенціал |
|
Норм. елемент Вестона |
|
|
|
|
|
|
|
|
|
|
|
|
-ПZn/Zn2+ |
