
- •Міністерство освіти і науки україни
- •І. Обробка та оформлення результатів лабораторних робіт
- •Іі. Правила роботи в лабораторії з фізичної хімії і техніка безпеки
- •Ліквідація нещасних випадків і надання першої допомоги
- •Ііі. Агрегатний стан речовин
- •1. Визначення маси моля речовини вимірюванням її об’єму в газоподібному стані
- •2. Визначення в’язкості системи етиловий спирт – вода
- •I. Хімічна термодинаміка
- •1. Визначення теплоти згоріння речовин за допомогою калориметра юнкерса
- •Експериментальна частина
- •2. Визначення теплоти розчинення і теплоти гідратації солі
- •V. Поверхневі явища (поверхнева енергія, поверхневий натяг та адсорбція на межі розділу фаз)
- •1. Визначення поверхневого натягу розчинів методом відліку крапель (сталагмометричним методом)
- •Поверхневий натяг води в залежності від температури
- •Густина води в залежності від температури
- •Густина розчинів NaCl при 293 к
- •2. Визначення площі та довжини молекули поверхнево-активної речовини
- •3. Адсорбція оцтової кислоти на активованому вугіллі
- •Методика експерименту
- •4. Дослідження адсорбції забарвлених речовин із розчинів
- •5. Дослідження адсорбції ізоамілового спирту із розчину за допомогою активованого вугілля
- •6. Визначення повної обмінної ємності (оє) катіоніту
- •7. Визначення вмісту лікарської речовини (глюконату кальцію) в розчині методом йонообмінної адсорбції
- •8. Обезсолювання води за допомогою йонітів
- •VI. Розчини неелектролітів
- •1. Визначення критичної температури взаємного розчинення рідин
- •2. Визначення молекулярної маси розчиненої речовини кріоскопічним методом
- •VII. Розчини електролітів
- •1. Визначення електропровідності електролітів і обчислення ступеня дисоціації
- •Експериментальна частина
- •Робота на змінному струмові
- •2. Bизначення розчинності малорозчинних сполук
- •3. Визначення іонного добутку води
- •4.Визначення концентрації кислоти методом кондуктометричного титрування
- •5. Визначення вмісту лікарської речовини в розчині
- •Хід роботи
- •Обробка результатів експерименту
- •VIII. Гальванічні елементи та електродні потенціали
- •1. Вимірювання електрорушійних сил гальванічних елементів
- •2. Визначення водневого показникa потенціометричним методом
- •3. Потенціометричне визначення рН, розрахунок константи дисоціації слабкої кислоти
- •Іх. Хімічна кінетика і каталіз
- •1. Визначення швидкості розкладу тіосульфатної кислоти
- •Дослід 1. Залежність швидкості розкладу тіосульфатної кислоти від її молярної концентрації
- •Дослід 2. Залежність швидкості розкладу тіосульфатної кислоти від температури
- •Виконання роботи
- •Склад реакційної суміші
- •Результати титрування
- •3. Дослідження гідролізу крохмалю в присутності соляної кислоти
- •4. Дослідження гідролізу крохмалю в присутності ферментів і соляної кислоти при температурі 310 к
- •5. Визначення швидкості розкладу пероксиду водню газометричним методом
- •6. Фотохімічний розклад н2о2
- •Послідовність виконання роботи
- •Х. Фізикохім ія дисперсних систем.
- •1. Методи одержання колоїдних розчинів
- •2. Коагуляція колоїдних розчинів електролітами
- •3. Визначення величини електрокінетичного потенціалу методом електрофорезу
- •4. Вивчення ізоелектричної точки білків
- •5. Набухання гелів
- •Хід виконання роботи
- •Хі. Біогенні елементи
- •1. Аналітичні реакції на йони s-елементів
- •Визначення хлор-йонів Cl– в питних водах за методом Фольгарда
- •2. Аналітичні реакції на р-елементи та їх сполуки
- •Реакція на бор (ііі) по кольору полум’я
- •Реакція на йон з розведеними кислотами
- •Реакція на йон з реактивом Несслера
- •Реакція на йон із розчином хлориду барію
- •(Реакція л.А. Чугаєва)
- •Контрольні питання до колоквіумів іii. Агрегатний стан речовин
- •Іv. Хімічна термодинаміка та біоенергетика
- •V. Поверхневі явища (поверхнева енергія, поверхневий натяг та адсорбція на межі розділу фаз)
- •Vі. Розчини неелектролітів
- •Vіі. Розчини електролітів
- •Vііі. Гальванічні елементи та електродні потенціали
- •IX. Хімічна кінетика і каталіз
- •Х. Фізикохімія дисперсних систем
- •Хі. Біогенні елементи
- •Додатки
- •Деякі фізичні константи
- •Густина деяких речовин
- •Густина деяких газів (н.У.)
- •Співвідношення між позасистемними одиницями
- •Пояснювальна записка
- •Зміст дисципліни
- •Тема 1. Предмет фізичної хімії та її значення. Розділи фізичної хімії. Методи дослідження. Розвиток фізичної хімії в Україні.
- •Тема 7.
- •Тема 8.
- •Тема 9.
- •Тема 10.
- •Тема 11.
- •Тема 12.
- •Тема 13.
- •Тема 14.
- •Орієнтовний перелік питань до підсумкового контролю знань з дисципліни.
- •Cписок літератури
- •І. Обробка та оформлення результатів
- •Гомонай Василь Іванович
2. Визначення водневого показникa потенціометричним методом
Для роботи необхідно: потенціометр; акумулятор; нормальний еле- мент Вестона; хінгідронно-каломельний елемент; гальванометр; провідни- ки; хінгідрон; досліджувані розчини.
Для визначення рН за допомогою хінгідронного електроду користу- ються хінгідронно-каломельним ланцюгом:
![]()
Вимірюють еРС цього ланцюга за допомогою потенціометра. рН розчину розраховують, виходячи з рівняння залежності потенціалу хін- гідронного електроду від концентрації водневих іонів:
![]() ,
,
![]()
або
![]() .
.
ЕРС хінгідронно-каломельного елементу набуває вигляду:
![]() .
.
Підставляючи в це рівняння значення Пхін і Пкал, одержуємо:
![]() .
.
Звідки дістаємо розрахункову формулу:
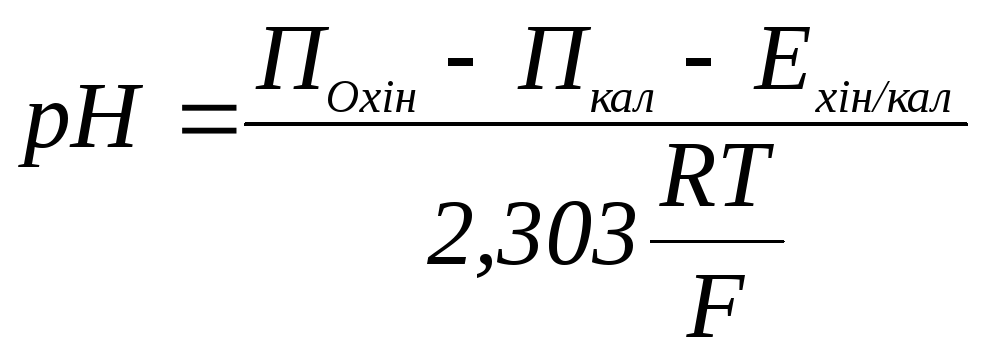 .
.
Значення
нормального потенціалу хінгідронного
електроду – ПОхін,
потенціалу насиченого каломельного
електроду – Пкал
в залежності від температури, а також
значення коефіцієнту
![]() беруть з таблиць, які знаходяться у
кінці опису.
беруть з таблиць, які знаходяться у
кінці опису.
Для визначення еРС хінгідронно-каломельного елементу до відпо- відних клем на потенціометрі приєднують: хінгідронно-каломельний еле- мент, нормальний елемент Вестона, гальванометр і джерело струму. Не- обхідно пам’ятати, що джерело струму при збиранні електричної схеми підключається останнім. Хінгідронний електрод готують таким чином.
У скляний посуд заливають досліджуваний розчин; туди ж додають хінгідрон до насичення.
Р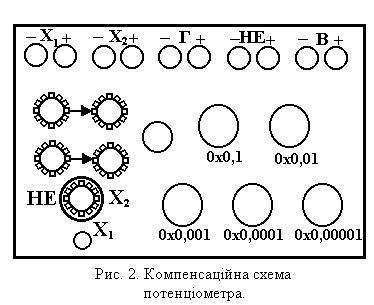 озчин
старанно перемішують і опускають
платиновий електрод. Приготовлений
хінгідронний електрод з’єднують за
допомогою солевих містків з каломельним.
озчин
старанно перемішують і опускають
платиновий електрод. Приготовлений
хінгідронний електрод з’єднують за
допомогою солевих містків з каломельним.
Компенсаційна схема потенціометра.
Готовий хінгідронно-каломельний елемент приєднують до приладу, зображеному на рисунку.
Якщо вимірювання проводяться з хінгідронним електродом, то кало- мельний електрод приєднується до клеми “мінус”, а з водневим – до “плюс”. Перед вимірюванням ЕРС хінгідронно-каломельного ланцюга спо- чатку проводять наладку потенціометра по нормальному елементу. Для цього ручка вмикача ставиться в положення “НЗ”, а реостатами, вмонто- ваними в лівій частині приладу, підбирають опір, починаючи з грубої наводки і кінчаючи більш плавною до тих пір, поки стрілка гальванометра покаже відсутність струму. Потім починають визначення ЕРС дослід- жуваного елементу. Для цього ручку вмикача ставлять в положення “Х” і реостатами, вмонтованими в правій частині приладу (починаючи з ручки 0,1 і закінчуючи 0,001 В), підбирають такий опір, при якому стрілка галь- ванометра покаже відсутність струму, тобто стане на нуль.
Cумарне значення показів кожного реостату відповідає значенню ЕРС хінгідронно-каломельного елемента. Маючи значення ЕРС хінгідронно-каломельного електрода, по розрахунковій формулі вираховують величину водневого показника.
Результати досліду записують у табл. 1.
Таблиця 1
|
Дослід. р-н |
Покази потенціо-метра, В |
ПОхін, В |
Пкал, В |
|
рН |
|
|
|
|
|
|
|
Значення потенціалу насиченого каломельного електроду при різних температурах наведені в табл. 2.
Таблиця 2
|
Темпера- тура, К |
Потен-ціал, В |
Темпера- тура, К |
Потен-ціал, В |
Темпера-тура, К |
Потен-ціал, В |
|
286 |
0,32 |
289 |
0,2517 |
292 |
0,2425 |
|
287 |
0,2525 |
290 |
0,2509 |
293 |
0,2488 |
|
288 |
0,2517 |
291 |
0,2503 |
294 |
0,2458 |
Значення потенціалу нормального хінгідронного електроду при температурі від 281 до 301 К наведені в табл. 3.
Таблиця 3
|
Температура, К |
ПОхін, В |
Температура, К |
ПОхін, В |
|
281 |
0,6866 |
292 |
0,6948 |
|
282 |
0,6874 |
293 |
0,6955 |
|
284 |
0,6888 |
294 |
0,6970 |
|
285 |
0,6896 |
295 |
0,6977 |
|
286 |
0,6903 |
296 |
0,6985 |
|
287 |
0,5911 |
297 |
0,6992 |
|
288 |
0,6918 |
298 |
0,6999 |
|
289 |
0,6925 |
299 |
0,7007 |
|
290 |
0,6933 |
300 |
0,7011 |
|
291 |
0,6940 |
301 |
0,7022 |
Значення
![]() для
різних температур наведені в табл. 4.
для
різних температур наведені в табл. 4.
Таблиця 4
|
Т, К
|
|
Т, К
|
|
|
283 |
0,0561 |
294 |
0,0583 |
|
284 |
0,0563 |
295 |
0,0585 |
|
285 |
0,0565 |
296 |
0,0587 |
|
286 |
0,0567 |
297 |
0,0589 |
|
287 |
0,0569 |
298 |
0,0591 |
|
288 |
0,0571 |
299 |
0,0593 |
|
289 |
0,0573 |
300 |
0,0595 |
|
290 |
0,0575 |
301 |
0,0597 |
|
291 |
0,0577 |
302 |
0,0599 |
|
292 |
0,0579 |
303 |
0,0601 |
|
293 |
0,0581 |
– |
– |
