
- •Федеральное агентство по образованию
- •Экологическая химия
- •Введение: предмет экологической химии, задачи экологической химии
- •1Основные понятия и определения
- •1.1 Загрязнение окружающей среды. Химическое загрязнение. Вредные вещества.
- •1.2 Предельно допустимые концентрации вредных веществ
- •2.1.1. Пдк вредных веществ в атмосфере
- •1.2.2 Пдк вредных веществ в водной среде
- •1.2.3Пдк вредных веществ в почве
- •1.3.2 Распространение в ос
- •1.3.3 Время жизни (устойчивость) загрязнителя
- •1.3.4 Склонность загрязнителя к деградации (биоразложению)
- •1.4 Термодинамический и кинетический подходы к изучению поведения загрязнителей в ос
- •1) Определять возможность самопроизвольного протекания химических реакций в том или ином направлении;
- •2) Определять условия, при которых устанавливается химическое равновесие.
- •При низких давлениях газы можно считать идеальными, и Ka ≈ Kp.
- •1) Рассчитать время достижения заданной степени превращения веществ (или опре- делить степень превращения вещества в заданный момент времени),
- •2) Найти условия, при которых время достижения заданной степени превращения ве- щества будет минимальным.
- •2. Физико-химические процессы в атмосфере
- •2.1 Состав и строение атмосферы
- •Qисточник и Qсток – скорости поступления и стока веществ соответственно для произвольного резервуара, атмосферы в целом или ее части;
- •2.1.1 Основные зоны атмосферы
- •2.1.2 Атмосферное давление
- •2.1.3 Солнечная радиация и вертикальная структура атмосферы
- •2.1.4 Тепловой баланс атмосферы и подстилающей ее поверхности
- •Процессы окисления примесей в тропосфере могут протекать:
- •1.3.4. Фотохимический смог в городской атмосфере
- •1.3.6Метан
- •В присутствии no общий результат окисления метана:
- •1.3.7.1 Номенклатура и особенности тропосферного аэрозоля
- •1.3.7.2 Время жизни (устойчивость) аэрозоля
- •Водородный цикл
- •Азотный цикл
- •Хлорный цикл
- •Физико-химические процессы в гидросфере
- •3. Биогенные вещества – главным образом соединения азота и фосфора. К биогенным элементам относят также соединения кремния и железа.
- •2.2. Классификация природных вод
- •1) Физико-географические (рельеф, климат…);
- •2.3.2 Процессы растворения твердых веществ в природныхводах
- •2.4 Кислотно-основное равновесие в природных водоемах
- •2.4.2 Растворимость карбонатов и рН подземных и поверхностных природных вод
- •2.5.1 Окислительно_восстановительное равновесие
- •2.5.2 Взаимосвязь между окислительно-восстановительны-ми и кислотно-основными характеристиками природных вод
- •2.6 Процессы самоочищения водных экосистем
- •2.6.1 Виды загрязнений и каналы самоочищения водной среды
- •2.6.3 Физико-химические процессы на границе разделафаз
- •1) В качестве окислителя участвуют ионы металлов в окисленной форме;
- •2) В окислении зв участвуют свободные радикалы и другие реакционноспособные частицы.
- •1) Рекомбинация и диспропорционирование
- •3) Присоединение по кратной связи
- •3 Физико-химические процессы в почвах
- •3.1 Гипергенез и почвообразование
- •3.3 Элементный и фазовый состав почв
- •3.4 Оганические вещества почвы
- •3.4.1 Классификация органических веществ почвы
- •3.5.2 Обменные катионы почв
- •3.7 Соединения азота в почве
- •3.6 Проблемы загрязнения почвенных экосистем
- •3.6.1 Проблема применения минеральных удобрений
- •3.6.2 Проблемы применения химическх средств защиты растений
- •3.6.3 Поведение пестицидов в ос
3.7 Соединения азота в почве
Основное количество соединений азота сосредоточено в верхнем почвенном горизонте и представлено главным образом органическими соединениями. В среднем на долю азота приходится около5% от массы органического вещества почвы, что составляет обычно 0,02-0,4% от массы пахотного слоя почв. Помимо органическихсоединений (гумусовые вещества и растительные остатки), азот впочве присутствует в виде неорганических компонентов в почвенном воздухе, почвенном растворе и в обменном или фиксированномсостоянии входит в состав твердой фазы почв.
Среди органических соединений азота от 20 до 50% составляют аминокислоты, присутствуют также амиды, аминосахара и гетероциклические соединения. Около 50% органических соединений азота остаются неидентифицированными. Все органические соеди-нения азота можно разделить на легко разлагаемую и стабильную фракции. На долю первой приходится обычно менее одной трети всего органического азота почвы.
Органические соединения азота, содержащиеся в почве, являются основным резервом для питания растений. В результате процессов химической и, преимущественно, биохимической трансформации этих соединений происходит образование доступных для растений веществ, протекает так называемый процесс мобилизации азота. Даже бедные почвы, например дерново-подзолистые, содержат в пахотном слое до 4 т/га азота. Этого количества при егополной мобилизации было бы достаточно для созревания урожая в течение 50-60 лет. Однако такая мобилизация азота привела бы к полному разрушению гумусовых веществ, и почвы утратили бы все свои агрономически ценные свойства.
Соединения азота всегда содержатся в поступающих в почву растительных остатках и мобилизуются в процессе их разложения. Особенно интенсивно этот процесс протекает на ранних стадиях распада растительных остатков, когда соотношение массы углерода и азота в них ниже 20. В дальнейшем скорость поступления соединений азота определяется скоростью разложения органического вещества почвы. Обычно в полевых условиях в результате процессов разложения в почву ежегодно переходит от 1 до 3% азота, содержащегося в органическом веществе почв.
В почвенном воздухе соединения азота представлены молекулярным азотом, аммиаком, оксидом азота (I), оксидом азота (II) и диоксидом азота.
При газовом обмене с атмосферным воздухом часть почвенного азота теряется. Так, по данным Б. Н. Макарова, например на дерново-подзолистых и суглинистых почвах, в среднем за период с мая по август на полях без внесения азотных удобрений теряется только в виде NO2 до 0,2 т азота на каждом гектаре. Внесение азотных удобрений увеличивает количество соединений азота, поступающих в атмосферу, что особенно заметно в первый год. В целом, если принять во внимание данные о возможном переходе 27% азота из удобрений в газовую фазу и считать доли молекулярного азота и N2О в газовой фазе одинаковыми, при внесении 90 кг азота на гектар почв в атмосферу может выделиться 12 кг N2, 19 кг N2О и 0,8 кг NO2.
Экспериментальные измерения состава приземного воздуха, проведенные Б. Н. Макаровым, показали, что в зависимости от гидротермических условий содержание диоксида азота в приземном слое колеблется от 0 до 8 ·10-7 % (об.) и в среднем составляет 4 ·10 -7 % (об.), доля аммиака изменяется от 0 до 9 · 10-6 %(об.).
Главными источниками образования газообразных соединений азота в почве являются протекающие при участии микроорганизмов процессы аммонификации, нитрификации и денитрификации.
Аммонификация – это процесс разложения органических веществ, протекающий с участием специфических аммонифицирующих микроорганизмов. В результате этого процесса в почвенном воздухе появляется газообразный аммиак, а в почвенном растворе – ионы аммония.
Ионы аммония вступают во взаимодействие с почвенно-поглощающим комплексом, причем часть ионов NH4+ в результате такого взаимодействия может потерять подвижность. Обычно в почвах содержание связанного с ППК обменного аммония на порядок выше, чем свободного. Поэтому концентрация ионов NH4+ в почвенном растворе невелика.
Процесс фиксации ионов аммония можно рассмотреть на примере связывания ионов аммония минералом иллитом. Расположенные на внешней поверхности кристалла и его сколах ионы NH4+ могут легко вступать в реакции замещения и являются обменными катионами. Ионы аммония и калия способны проникать и в области межпакетных промежутков. В этом случае они теряют способность к обмену и превращаются в катионы, фиксированные твердой фазой почв. Способность минералов фиксировать ионы NH4+ определяется их строением, степенью выветривания и степенью насыщения решетки катионами К+ и меняется от нескольких смоль (р+)/кг до 10-12 смоль (р+)/кг.
Неорганические соединения азота присутствуют в почве в виде NH4+ и NO3-, лишь в некоторых щелочных почвах могут встречаться небольшие количества ионов NО2-. Соотношение NH4+ / NO3- в почве определяется наличием условий для нитрификации, которая угнетается при низких значениях рН и анаэробных условиях в почве. Там, где нет препятствий для нитрификации, большая часть азота представлена нитратами, и их содержание в почвенном растворе изменяется от 50 до 150 мг/л.
Окисление аммиака микроорганизмами протекает в два этапа. На первом этапе под воздействием бактерий Nitromonas происходит окисление ионов NH4+ до ионов NO2-. Образующиеся на этой стадии соли азотистой кислоты подвергаются дальнейшему окислению, которое протекает с участием бактерий Nitrobacter. При этом ионы NO2- переходят в NO3-.
В процессе нитрификации в почву поступают ионы водорода:
NH+ + 2О2 → NО3- + Н2О + 2Н+.
Поэтому процессы нитрификации сопровождаются закислением почв, и при длительном применении аммонийных удобрений необходимо предусматривать компенсирующее известкование почв. ПриpH= 7, T = 298 К и достаточной аэрации почв, когда окислительно-восстановительный потенциал почвенного раствора составляет 0,4-0,5 В, скорость нитрификации аммония может достигать 10-20 кг/(га · сут). Если аэрация почв затруднена и окислительно-восстановительный потенциал ниже 0,35 В, нитрификация может прекратиться, и в почве начнутся процессы денитрификации.
Денитрификация – процесс восстановления, в результате которого происходит образование газообразных соединений азота, выделяющихся в атмосферу. Различают два пути денитрификации: косвенный, или химический, и прямой, или биологический. Косвенный процесс денитрификации связан с протеканием химических реакций:
R-NH2 + HNO2 → R-OH + N2 + Н2О
(NH2)2CO + 2HNO2 → 2N2 + CO2 + 3H2O
2HNO3 ↔ NO + NO2 + H2O + O2
3HNO2 ↔ 2NO + HNO3 + H2O, где
R — органические радикалы.
Разложение азотной и азотистой кислот следует отнести к основным процессам косвенной денитрификации в кислых почвах при рН < 5,5. Для таких почв отмечалось заметное увеличение содержания диоксида азота в почвенном воздухе, что указывает на преимущественное протекание процесса разложения ионов NО3-. Небиологическому восстановлению нитритов могут способствовать ионы Cu2+, Fe2+, Mn2+ и увеличение содержания органических компонентов с фенольными ОН-группами. В некоторых предварительно стерилизованных почвах в течение 10 дней содержание нитритного азота уменьшалось в результате процессов косвенной денитрификации в 3 раза. Однако, как отмечается многими исследователями, косвенная денитрификация играет значительно меньшую роль в процессах восстановления соединений азота, чем биохимическаяденитрификация.
Различают два типа процессов биохимической денитрификации: специфическую, или диссимиляторную, и неспецифическую денитрификацию. В процессе диссимиляторной денитрификации происходит восстановление нитратов до молекулярного азота, в результате переноса электронов с субстрата (донора электронов) на нитраты, при этом высвобождается необходимая для микроорганизмов энергия. Неспецифическая денитрификация не выполняет энергетических функций. В этом процессе нитраты восстанавливаются преимущественно до нитритов. К неспецифической относят и ассимиляторную денитрификацию, при которой нитраты восстанавливаются до аммония. Неспецифическую денитрификацию часто рассматривают как первую стадию процесса денитрификации, при которой нитраты восстанавливаются до нитритов. Дальнейшее восстановление происходит в результате диссимиляторной нитрификации и протекает при участии микроорганизмов из родов Pseudomonos, Achromobacter, Micrococcus, Bacillus, Thiobacillus. Эти бактерии используют нитраты как источник энергии в отсутствие кислорода. Энергетический эффект этого процесса оценивается в 1760 кДж/моль. Суммарно процесс можно представить уравнением:
C6H1206 + 4NO3- → 6CO2 + 6Н2О + 2N2.
Подавляющее большинство денитрифицирующих бактерий при высокой концентрации кислорода могут перейти на обычное дыхание. Поэтому процесс денитрификации протекает и в аэробных, и в анаэробных условиях. Однако наиболее интенсивно этот процесс протекает в плохо дренированных почвах при величине рН раствора, близкой к нейтральной, температуре около 25°С и окислительно-восстановительном потенциале почвенного раствора Еh < 0,35 В (ре- < 5,9).
Необходимо отметить, что в процессе денитрификации часто происходит образование заметных количеств оксида азота (I). Ежегодная эмиссия N2O из почв, по данным Д.С. Орлова, может достигать 20-50 г/га. Как известно, инертный в тропосфере, оксида азота (I), достигая стратосферы, разлагается с образованием оксида азота, нарушающего нулевой цикл озона. Поэтому увеличение количества образующегося в почве оксида азота (I), которое связано с ростом использования азотных удобрений, может оказать разрушающее влияние на озоновый слой планеты. Суммарно процесс трансформации неорганических соединений азота в почве можно представить схемой:
k1 k2
NH4+ → NO2- ↔ NO3-, где
↓ k4 k3
Г
k1, k2, k3, k4 – константы скоростей соответствующих реакций нитрификации и денитрификации; Г –сумма газов N2O, NO, NO2, N2.
Скорости соответствующих реакций зависят от температуры почв, рН, степени аэрации и, следовательно, окислительно-восстановительного потенциала почвенного раствора, содержания влаги, органических веществ и ингибиторов. Реакции нитрификации относятся к реакциям первого порядка, а реакции денитрификации имеют нулевой порядок, поэтому можно записать:
Для средних условий почв соответствующие константы скоростей реакций равны: k1 = 0,02 ч -1, k2 = 0,04 ч-1, k3 = 0,015 мг · кг-1(N) · ч-1, k4 = 0,01мг · кг-1(N) · ч-1. Константа скорости процесса окисления нитрит-ионов в нитрат-ионы k2 в 2 раза превосходит константу скорости образования нитрит-ионов k1, поэтому нитриты, как уже отмечалось, практически не накапливаются в почве. Значения констант kз и k4 в значительной степени зависят от окислительно-восстановительных условий и присутствия ингибиторов в почве.
Общие потери азота, удаляемого из почв в виде газообразных соединений, только с пахотных почв РФ составляют около 1,5 млн. т азота в год. Для уменьшения потерь азота в некоторых случаях используют ингибиторы скорости процессов денитрификации. В общем виде литосферную ветвь глобального кругооборота азота можно представить схемой, предложенной Д. С. Орловым (рис. 3.6). Природными источниками поступления соединений азота в почву являются соединения азота, присутствующие в атмосфере и поступающие с атмосферными осадками, азот атмосферы, фиксируемый бактериями, и азот, содержащийся в остатках живых организмов. К этим источникам все в больших количествах добавляются антропогенные поступления.
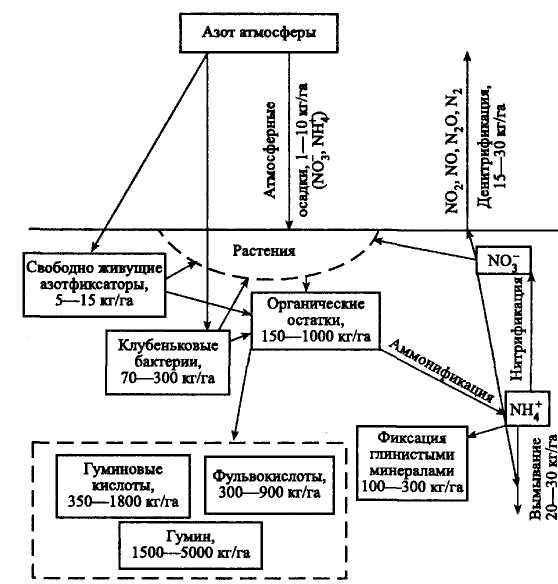
Рис. 3.6–Схема литосферной части глобального кругооборота азота
Органические остатки живых организмов подвергаются гумификации и аммонификации. Ионы NH4+ частично усваиваются растениями, частично участвуют в процессах гумификации или связываются почвенно-поглощающим комплексом. Часть ионов вымывается с инфильтрационной влагой или подвергается процессу нитрификации. Нитрат-ион активно поглощается растениями, частично подвергается денитрификации, замыкая тем самым биохимический цикл азота, а частично переходит в подземные воды, что во многих случаях приводит к их загрязнению.
СОЕДИНЕНИЯ ФОСФОРА В ПОЧВЕ
Общее количество фосфора в верхнем слое почвы в среднем составляет около 1000 кг/га. Главный источник его поступления – почвообразующие породы, некоторая незначительная часть поступает с атмосферными осадками. Ежегодно с урожаем сельскохозяйственных растений из почвы выносится от 10 до 40 кг/га фосфора. Поэтому значительные количества его соединений дополнительно вносятся в почву с органическими и минеральными удобрениями. Соединения фосфора в почве содержатся в почвенном растворе, находятся в адсорбированном состоянии на поверхности неорганических компонентов почвы, присутствуют в твердой фазе почв в виде аморфных и кристаллических минералов и входят в состав органических соединений почвы.
В зависимости от вида почв содержание фосфора в органических соединениях изменяется от 10-20% (дерново-подзолистые почвы) до 70-80% (черноземные почвы) от его общего содержания впочвенном слое. Основное количество (до 60%) органических соединений фосфора во многих почвах находится в виде инозитолфосфатов, которые представляют собой эфиры ортофосфорной кислоты и насыщенного шестиатомного циклического спирта — циклогексангексола, или инозита. В результате присоединения к инозиту шести молекул ортофосфорной кислоты образуется 12-основная инозитгексафосфорная кислота. При неполном фосфорилировании возникают пента-, тетра-, три-, ди- и моноинозитолфосфаты.
В составе гуминовых и фульвокислот может находиться от 2-3 до 50-80% всего фосфора, содержащегося в органической части почв. Его концентрация в гуминовых кислотах колеблется от 0,03-0,05 до 0,3-0,5%. Часть этого фосфора представлена также инозитолфосфатами.
Около 1% фосфора органической части почв сосредоточено в липидах, 2-3% —в нуклеиновых кислотах. Помимо этих соединений в почве идентифицированы фосфопротеины, сахарофосфаты и фосфорилированные карбоновые кислоты. Фосфаты принимают участие и в образовании органоминеральных соединений в почве, в этом случае ортофосфаты, например, могут быть связаны с органическими соединениями через катионные мостики железа, алюминия или кальция.
Минеральная часть твердой фазы почв представлена в основном ортофосфатами, преимущественно минералами апатитовой группы. Кроме них распространены минералы группы плюмбогумита РЬА13Н(ОН)6(РО4)2, на долю которых в некоторых видах почв приходится до 50% от всей массы минерального фосфора, вавеллита А1(РО4)4(ОН)6 · 5Н2О и вивианита Fe3(PO4)2 · 8Н2О. Все встречающиеся в почве ортофосфаты относятся к труднорастворимым соединениям. (табл. 3.10).
Трансформация соединений фосфора в почве связана с протеканием процессов минерализации органических фосфорсодержащих веществ, а также процессов иммобилизации, фиксации и мобилизации его неорганических соединений.
Минерализация – процесс превращения органических соединений фосфора в минеральные. Этот процесс протекает в почве в результате деятельности микроорганизмов. При этом под воздействием различных ферментов, например фитаз, происходит выделение из органических веществ остатков ортофосфорной кислоты. Последующие их превращения будут определяться свойствами почвенного раствора и составом твердой фазы почв.
Таблица З.10 –Основные представители ортофосфатов кальция в почвах
-
Вещество
Формула
рК = -lgK
Гидрортоофосфат кальция
СаНРО4
6,66
Ортофосфат кальция
 -Са3(РО4)2
-Са3(РО4)233,21
Тригидрат ортофосфата кальция
Са3(РО4)2 · ЗН2О
146,9
Гидроксилапатит
Са10(РО4)6(ОН)2
113,7
Фторапатит
Ca10(PO4)6F2
18,4
Иммобилизация — превращение неорганических соединений фосфора в органические формы в процессе развития живых организмов. При этом фосфор переходит, например, в молекулы фосфолипидов или нуклеиновых кислот микробных клеток и в форме органических фосфорсодержащих соединений становится недоступным для других организмов.
Фиксация фосфора — переход растворимых фосфорных соединений в менее растворимое состояние за счет образования прочных связей с минеральными компонентами почвы. Фиксация протекает в результате образования труднорастворимых минералов и в процессе хемосорбции фосфат-ионов из почвенного раствора. Хемосорбция осуществляется в результате связывания фосфат-ионов с ионами Al, Fe или Са, которые находятся на поверхности минералов. В случае взаимодействия фосфат-ионов с катионами железа, алюминия или кальция, присутствующими в растворе, возможно образование и выпадение малорастворимых соединений.
Мобилизация — увеличение подвижности соединений фосфора, связанное с превращением труднорастворимых соединений в более растворимые, или переход их в почвенный раствор. Для большинства почв главный путь мобилизации связан с переходом соединений кальция из ортофосфата в гидроортофосфат или дигидроортофосфат кальция:
Cа3(РО4)2 → СаНРО4 → Са(Н2РО4)2.
Эти превращения протекают в присутствии свободных кислот, образующихся, в частности, при трансформации компонентов почв. Для оценки возможного перехода фосфатов из твердой фазы почв в почвенный раствор на практике часто используют величину фосфатного потенциала почв (ФП). Фосфатный потенциал почв характеризует степень насыщения почвенного раствора по отношению к дигидроортофосфату кальция:
ФП = -1g[а(Са2+) ·а(H2PO4-)], или
ФП = 0,5 р(Са2+) + р(Н2РО4-), где
р(Са2+) = - lg а(Са2+), р(Н2РО4-) = - lg а(H2PO4-).
Сравнивая величину фосфатного потенциала с отрицательным логарифмом корня квадратного из произведения растворимости дигидроортофосфата кальция, можно сделать вывод о вероятном поведении соединений фосфора. Так, если для почв соблюдается неравенство
0,5 р(Са2+) + р(Н2РО4-) > -0,5 lg ПР[Ca(H2PO4)2],
то концентрация фосфат-ионов в растворе контролируется соединениями, более трудно растворимыми, чем Са(Н2РО4)2. Если наблюдается равенство
0,5 р(Са2+) + р(Н2РО4-) = - 0,5 lg ПР[Ca(H2PO4)2],
то растворяется преимущественно гидроортофосфат. Чем выше фосфатный потенциал, тем труднее переходит фосфор в почвенный раствор, тем менее благоприятные условия создаются для питания растений фосфором.
.
