
- •Федеральное агентство по образованию
- •Экологическая химия
- •Введение: предмет экологической химии, задачи экологической химии
- •1Основные понятия и определения
- •1.1 Загрязнение окружающей среды. Химическое загрязнение. Вредные вещества.
- •1.2 Предельно допустимые концентрации вредных веществ
- •2.1.1. Пдк вредных веществ в атмосфере
- •1.2.2 Пдк вредных веществ в водной среде
- •1.2.3Пдк вредных веществ в почве
- •1.3.2 Распространение в ос
- •1.3.3 Время жизни (устойчивость) загрязнителя
- •1.3.4 Склонность загрязнителя к деградации (биоразложению)
- •1.4 Термодинамический и кинетический подходы к изучению поведения загрязнителей в ос
- •1) Определять возможность самопроизвольного протекания химических реакций в том или ином направлении;
- •2) Определять условия, при которых устанавливается химическое равновесие.
- •При низких давлениях газы можно считать идеальными, и Ka ≈ Kp.
- •1) Рассчитать время достижения заданной степени превращения веществ (или опре- делить степень превращения вещества в заданный момент времени),
- •2) Найти условия, при которых время достижения заданной степени превращения ве- щества будет минимальным.
- •2. Физико-химические процессы в атмосфере
- •2.1 Состав и строение атмосферы
- •Qисточник и Qсток – скорости поступления и стока веществ соответственно для произвольного резервуара, атмосферы в целом или ее части;
- •2.1.1 Основные зоны атмосферы
- •2.1.2 Атмосферное давление
- •2.1.3 Солнечная радиация и вертикальная структура атмосферы
- •2.1.4 Тепловой баланс атмосферы и подстилающей ее поверхности
- •Процессы окисления примесей в тропосфере могут протекать:
- •1.3.4. Фотохимический смог в городской атмосфере
- •1.3.6Метан
- •В присутствии no общий результат окисления метана:
- •1.3.7.1 Номенклатура и особенности тропосферного аэрозоля
- •1.3.7.2 Время жизни (устойчивость) аэрозоля
- •Водородный цикл
- •Азотный цикл
- •Хлорный цикл
- •Физико-химические процессы в гидросфере
- •3. Биогенные вещества – главным образом соединения азота и фосфора. К биогенным элементам относят также соединения кремния и железа.
- •2.2. Классификация природных вод
- •1) Физико-географические (рельеф, климат…);
- •2.3.2 Процессы растворения твердых веществ в природныхводах
- •2.4 Кислотно-основное равновесие в природных водоемах
- •2.4.2 Растворимость карбонатов и рН подземных и поверхностных природных вод
- •2.5.1 Окислительно_восстановительное равновесие
- •2.5.2 Взаимосвязь между окислительно-восстановительны-ми и кислотно-основными характеристиками природных вод
- •2.6 Процессы самоочищения водных экосистем
- •2.6.1 Виды загрязнений и каналы самоочищения водной среды
- •2.6.3 Физико-химические процессы на границе разделафаз
- •1) В качестве окислителя участвуют ионы металлов в окисленной форме;
- •2) В окислении зв участвуют свободные радикалы и другие реакционноспособные частицы.
- •1) Рекомбинация и диспропорционирование
- •3) Присоединение по кратной связи
- •3 Физико-химические процессы в почвах
- •3.1 Гипергенез и почвообразование
- •3.3 Элементный и фазовый состав почв
- •3.4 Оганические вещества почвы
- •3.4.1 Классификация органических веществ почвы
- •3.5.2 Обменные катионы почв
- •3.7 Соединения азота в почве
- •3.6 Проблемы загрязнения почвенных экосистем
- •3.6.1 Проблема применения минеральных удобрений
- •3.6.2 Проблемы применения химическх средств защиты растений
- •3.6.3 Поведение пестицидов в ос
2.4.2 Растворимость карбонатов и рН подземных и поверхностных природных вод
Карбонаты широко распространены как в донных отложениях морей и океанов, так и на поверхности материков. Мощные толщи известняков, мергелей и других карбонатных пород встречаются практически повсеместно. Среди солей угольной кислоты (карбонатов) наиболее распространенным в природе является карбонат кальция.
Карбонат кальция в природе встречается в виде двух кристаллических форм – кальцита и арагонита. Кальцит распространен значительно шире и наиболее характерен для осадков, образующихся в холодной среде. Арагонит, образующийся в тропических морях, относится к метастабильной форме карбоната кальция и постепенно переходит в кальцит.
Процесс непосредственного растворения карбоната кальция по уравнению
СаСО3![]() Са2++ СО32-(116)
Са2++ СО32-(116)
практически не играет роли при переходе малорастворимых карбонатов в раствор. соли угольной кислоты в природных водоемах могут переходить в раствор и существовать в нем в заметных количествах только при наличии растворенного диоксида углерода:
СаСО3+ СО2 (р-р) + Н2О![]() Са2++ 2НСО3-.
(117)
Са2++ 2НСО3-.
(117)
Образующиеся при этом анионы включаются в общую систему карбонатных равновесий, существующих в природных водах, и оказывают существенное влияние на рН растворов.
Рассмотрим в качестве примера зависимость рН растворов карбоната кальция в воде от парциального давления диоксида углерода над системой при условии отсутствия других ионов в растворе.
В рассматриваемой системе карбонатных
равновесий имеем пять переменных:
[HCO3-], [CO32-],
[H+], [Ca2+]
и![]() .
Для описания системы взаимосвязанных
равновесий необходимо пять уравнений.
В их число входят:
.
Для описания системы взаимосвязанных
равновесий необходимо пять уравнений.
В их число входят:
I.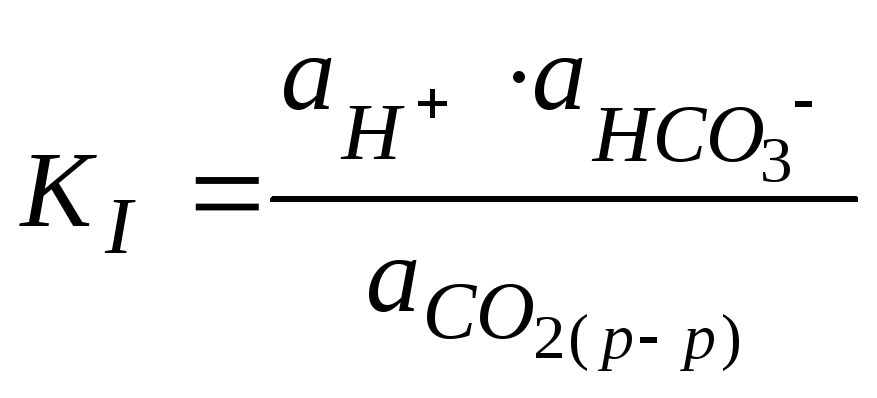 (101)
(101)
II.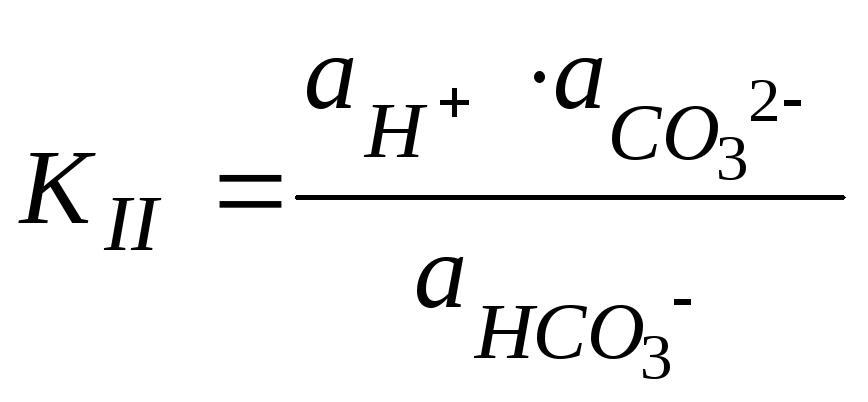 (103)
(103)
III.
![]() (из 116)
(из 116)
IV.
![]() (83)
(83)
Необходимое для решения системы пятое уравнение может быть получено из условия электронейтральности раствора:
[H+] + 2[Ca2+] = [HCO3-] + 2[CO32-] + [OH-]. (118)
Основываясь на экспериментальных данных о величине рН растворов СаСО3, будем рассматривать только область с рН<9. В этой области [H+]+[OH-]+[CO32-]<[Ca2+]+[HCO3-]. Поэтому уравнение электронейтральности раствора можно записать в виде:
2[Ca2+] = [HCO3-]. (119)
С учетом коэффициентов активности ионов Са2+и НСО3-можно записать
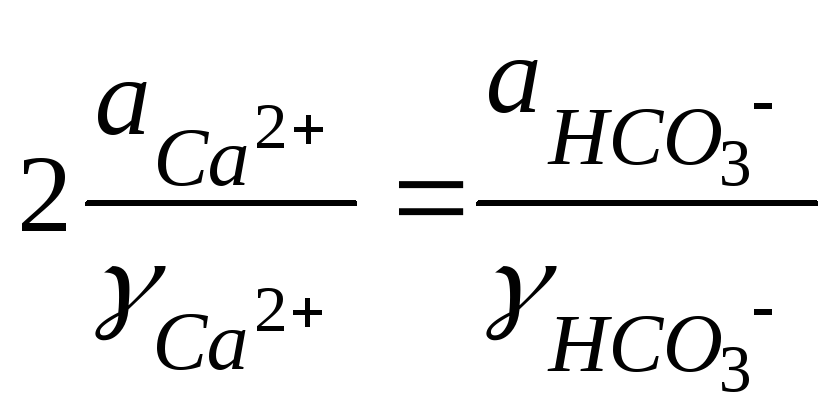 .
(119) Откуда
.
(119) Откуда
V.
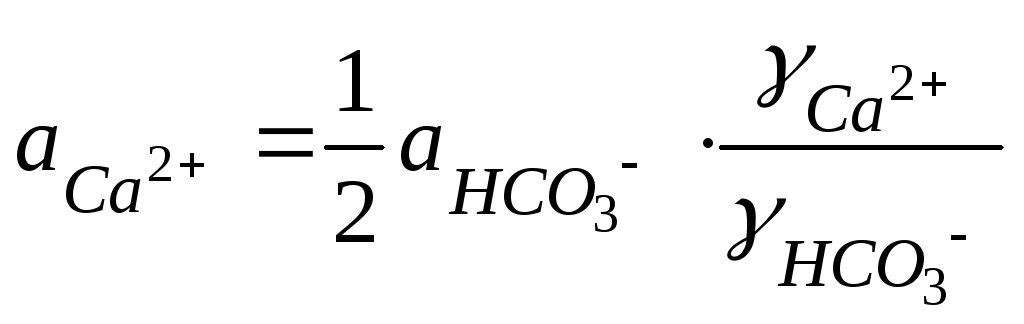 .
(120)
.
(120)
Решая систему из пяти перечисленных уравнений методом подстановки получим:
 .
(121)
.
(121)
Система уравнений решается следующим
образом. Из уравнения (101) выразим
![]() :
:
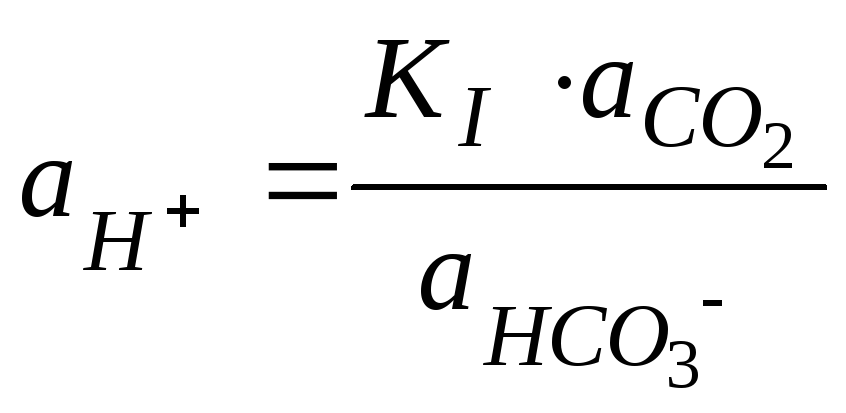 .
.
В
полученное уравнение подставим
![]() из (83):
из (83):
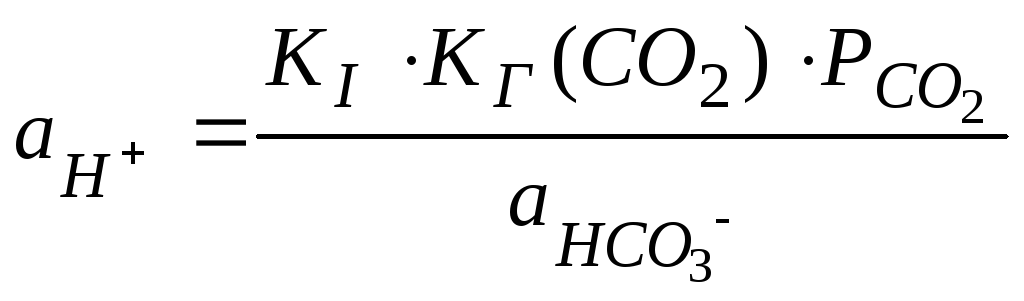 .
(122)
.
(122)
Выразим
![]() из (120) и подставим в уравнение (122):
из (120) и подставим в уравнение (122):
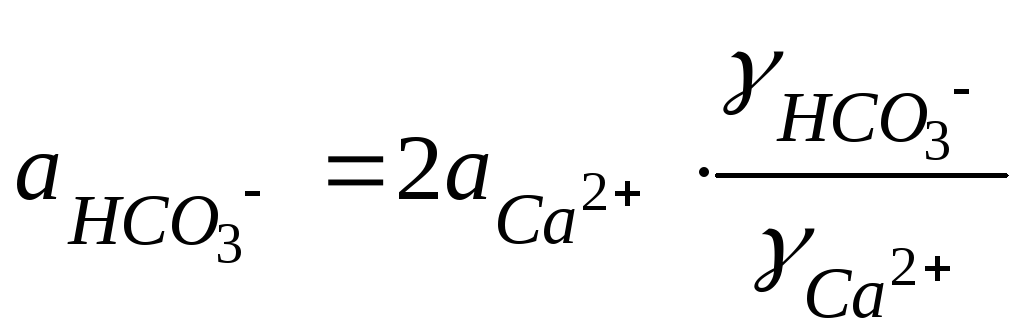 ,
,
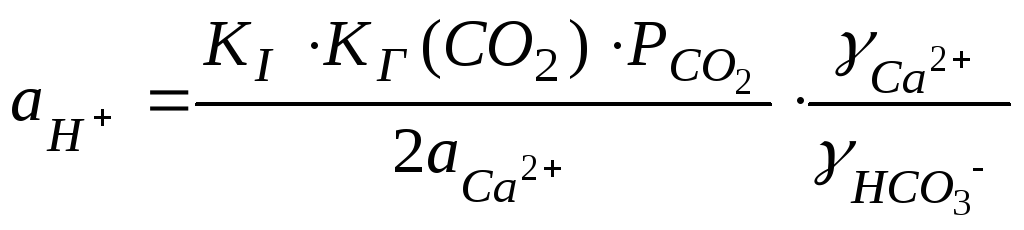 .
(123)
.
(123)
Выразим
![]() из уравнения для константы равновесия
процесса растворения СаСО3:
из уравнения для константы равновесия
процесса растворения СаСО3:
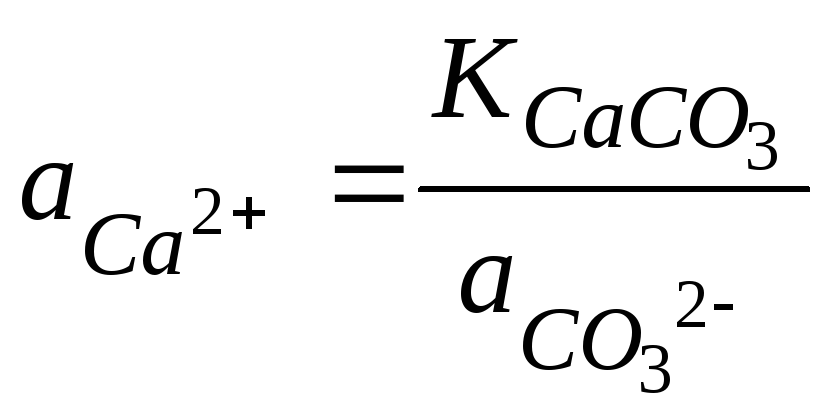
и подставим в (123), получим:
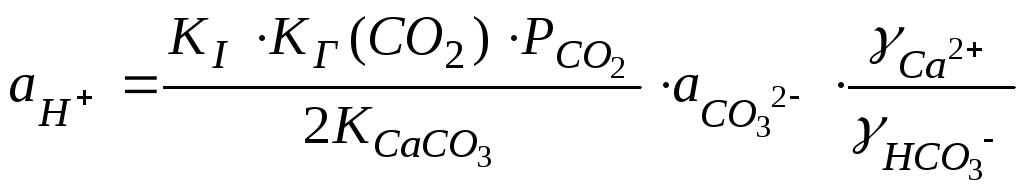 .
(124)
.
(124)
В уравнение (124) подставим
![]() из уравнения (103):
из уравнения (103):
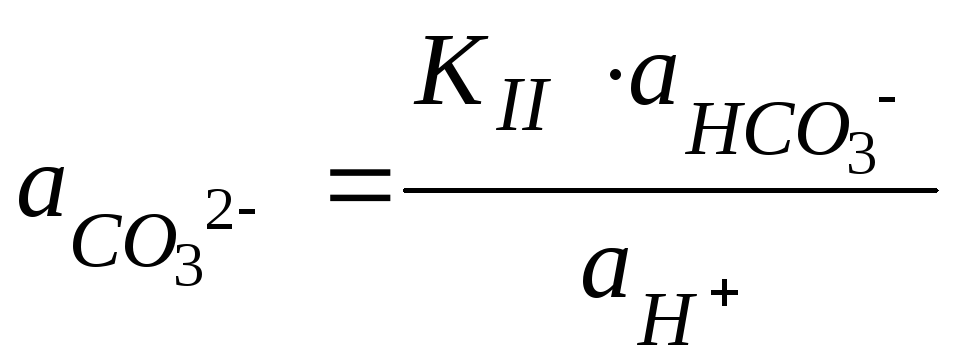 ,
,
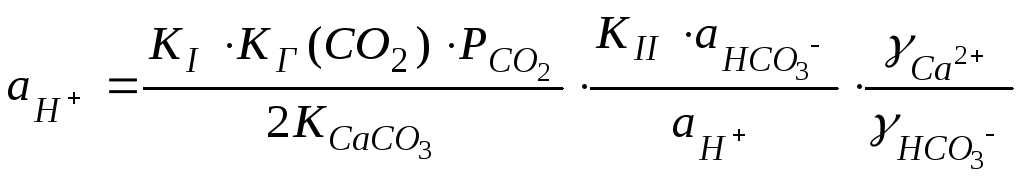 ,
,
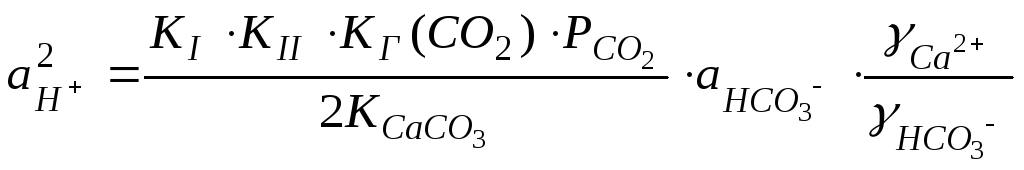 .
(125)
.
(125)
В уравнение (125) подставим
![]() ,
полученное из уравнения (122):
,
полученное из уравнения (122):
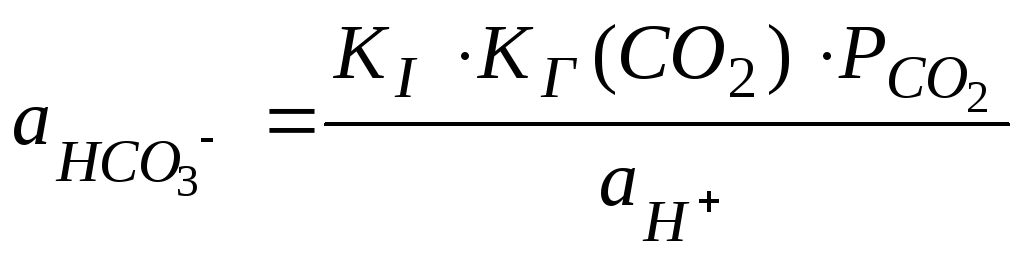 ,
,
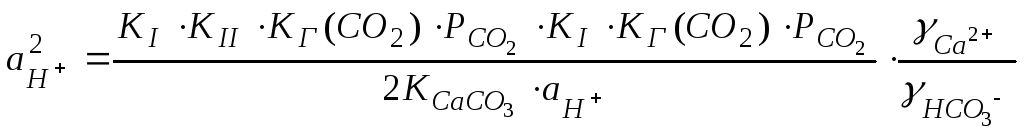 .
.
Откуда
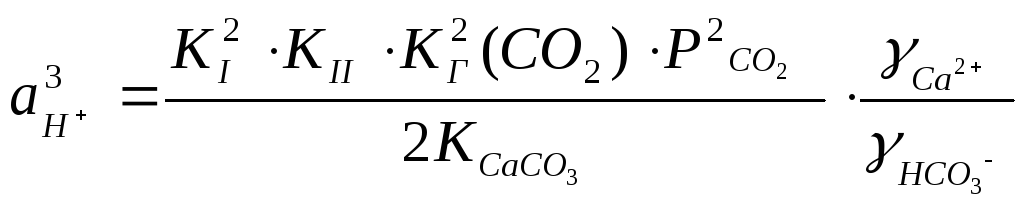 .
(126)
.
(126)
2.5 ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ В ГИДРОСФЕРЕ
Окислительно-восстановительные реакции играют исключительно важную роль в описании процессов, протекающих в природных водоемах. Состав природных вод в значительной степени зависят от вида окислительно-восстановительных реакций, их кинетических характеристик и величины окислительно-восстановительного потенциала, который соответствовал бы данной системе при установлении равновесия.
Для редокс-реакций в природных водах характерны две особенности. Во-первых, большинство наиболее редокс-реакций катализируется микроорганизмами (окисление органического вещества молекулярным кислородом, восстановление Fe(III) в Fe(II) и т. д.). Во-вторых, инициирование процессов окисления, протекающих в природных водах, в большинстве случаев, несмотря на крайне низкие значения концентраций, связано с присутствием в природных водах таких окислителей, как свободные радикалы, пероксид водорода, озон, и некоторых других сильных окислителей.
Далее будут обсуждены только общие подходы и рассмотрены лишь физико-химические основы окислительно-восстановительных процессов, протекающих в природных водах.
