
- •И. С. Колпащикова, а. Ф. Бетнев, е. М. Алов сборник задач по органической химии
- •150023, Ярославль, Московский пр., 88
- •150000, Ярославль, ул. Советская, 14а
- •1. Указания к выполнению домашней работы
- •2. Алканы
- •2.1. Изомерия
- •2.2. Конформации - изобразить проекции Ньюмена
- •2.3. Строение и температура кипения
- •2.4. Синтез Вюрца
- •2.5. Механизм радикального замещения: Механизм, расчет теплот реакций (2) и (3), медленная стадия – на примере углеводородов, которые в медленной стадии образуют один углеводородный радикал
- •2.6. Галогенирование высших алканов: строение радикалов, образующихся в медленной стадии, сравнение их устойчивости и легкости образования
- •2.7. Расчет процентного состава моногалогензамещенных, образующихся в реакции галогенирования алканов, или сравнение активностей алканов в реакции моногалогенирования
- •2.8. Цепочка превращений (сульфохлорирование, сульфоокисление, нитрование, электролиз, реакция Вюрца, галогенирование алканов
- •3. Алкены
- •3.1. Вывод структурных изомеров
- •3.2. Строение и устойчивость
- •3.3. Механизм электрофильного присоединения
- •3.4. Реакция электрофильного присоединения протекающая с перегруппировкой
- •3.5. Озонолиз
- •3.6. Полимеризация
- •3.7. Способы получения и химические превращения
- •3.8. Синтез алкенов и их химические превращения
- •3.9. Установление строения соединении по их свойствам
- •3.10. Задача на стехиометрический расчет
- •4. Диены. Алкины
- •4.1. Структурные изомеры диеновых углеводородов
- •4.2. Сравнение длины, энергий, дипольных моментов связей
- •4.3. Электрофильное присоединение к диенам
- •4.4. Полимеризация, озонолиз полимера
- •4.5. Реакция Дильса-Альдера
- •4.6. Свойства алкина как кислоты, реакция с солями более слабых кислот
- •4.7. Реакция гидратации алкинов
- •4.8. Способы получения и химические превращения
- •4.9. Сиетез алкинов
- •4.10. Установление строения соединений по их свойствам
- •5. Арены. Гетероциклы
- •5.1. Ароматичность, критерии ароматичнсти
- •5.2. Механизм электрофильного замещения в ядре
- •5.3. Расположить соединения с различными ориентантами в порядке изменения реакционной способности (4 соединения)
- •5.4. Объяснить механизм ориентирующего влияния определенной группы в seAr
- •5.5. Рассмотреть совместное влияние двух групп (согласованная и несогласованная ориентация)
- •5.6. Синтез замещенных аренов на основе бензола
- •5.7. Цепочка химических превращений
- •5.8. Электрофильное замещение в конденсированных многоядерных углеводородах
- •5.9. Реакции гетероциклов
- •5.10. Реакции гетероциклов
- •6. Галогеналканы. Галогенарены
- •6.1. 4 Реакции
- •6.2. Механизм sn
- •6.3. Cила нуклеофила
- •6.4. Растворитель
- •6.5. Уходящая группа
- •6.6. Стереохимия
- •6.7. Перегруппировка
- •6.8. Конкурирующие реакции
- •6.9. Элиминирование
- •6.10. Реакционная способность галогенов в соединениях, содержащих группировки
- •6.11. Цепочка
- •6.12. Осуществить превращение
- •6.13. Sn2 в ароматическом ядре
- •6.14. Стехиометрический расчет
- •7. Спирты. Фенолы. Простые эфиры
- •7.1. Спирты: строение - температура кипения
- •7.2. Спирты, фенолы: строение – кислотность
- •7.3. Магнийорганический синтез
- •7.4. Гидратация алкенов, гидролиз галогеналканов, гидроборирование
- •7.5. Магнийорганический синтез (подобрать исходные соединения), окисление спиртов
- •7.6. Превращение в простые эфиры
- •7.7. Превращение в сложные эфиры
- •7.8. Взаимодействие спиртов с галогенводородами
- •7.9. Элиминирование
- •7.10. Установить строение спирта
- •7.11. Реакция Вильямсона
- •7.12. Реакция расщепления простого эфира
- •7.13. Получение фенолов щелочным плавом, гидролизом галогенбензола, кумольный метод
- •7.14. Реакции фенолов в ароматическом ядре и в группе – он
- •7.15. Установить строение фенола
- •8. Карбонильные соединения
- •8.1. Получение ароматических альдегидов и кетонов
- •8.2. Получение алифатических альдегидов и кетонов
- •8.3. Реакция Кучерова, пиролиз солей карбоновых кислот
- •8.4. Подвижность α-водородного атома, нуклеофильное присоединение hcn, спиртов, гидросульфита натрия
- •8.5. Нуклеофильное присоединение производных аммиака, роль катализатора
- •8.6. Альдольная конденсация, другие реакции с участием карбанионов
- •8.7. Альдольная конденсация с участием соединений других классов
- •8.8. Получение спиртов с помощью альдольной конденсации
- •8.9. Реакция Канниццаро
- •8.10. Реакция окисления
- •8.11. Установить строение, провести превращение: а → карбонильное соединение или карбонильное соединение б
- •9. Карбоновые и сульфоновые кислоты
- •9.1. Окисление спиртов, превращение насыщенной кислоты в -амино, гидрокси, ненасыщенную или двухосновную кислоту через -галогензамещенную
- •9.2. Магнийорганический и нитрильный синтез
- •9.3. Алкилирование бензольного ядра и последующее окисление алкилароматического углеводорода
- •9.4. Строение и кислотность
- •9.5. Цепочка превращений, свойства кислот и их производных
- •9.6. Механизм реакций этерификации, гидролиза, реакционная способность
- •9.7. Сравнение поведения карбонильной группы карбоновой кислоты и кетона, сравнение реакционной способности ацильного и насыщенного углеродов
- •9.8. Получение и превращение сульфоновой кислоты
- •9.9. Установить строение карбоновой или сульфоновой кислоты
- •10. Амины
- •10.1. Получение алифатических аминов реакцией восстановления нитрилов, алкилированием аммиака и аминов и восстановительным аминированием
- •10.2. Строение и основность
- •10.3. Получение ароматических аминов и их превращение
- •10.4. Превращение аминов в соли диазония и реакции солей диазония с выделением азота
- •10.5. Превращение аминов в соли диазония и реакции солей диазония с выделением азота
- •10.6. Получение азокрасителя
- •10.7. Подобрать исходные соединения для синтеза азокрасителя
- •Библиографический список
- •И. С. Колпащикова, а. Ф. Бетнев,
9.5. Цепочка превращений, свойства кислот и их производных
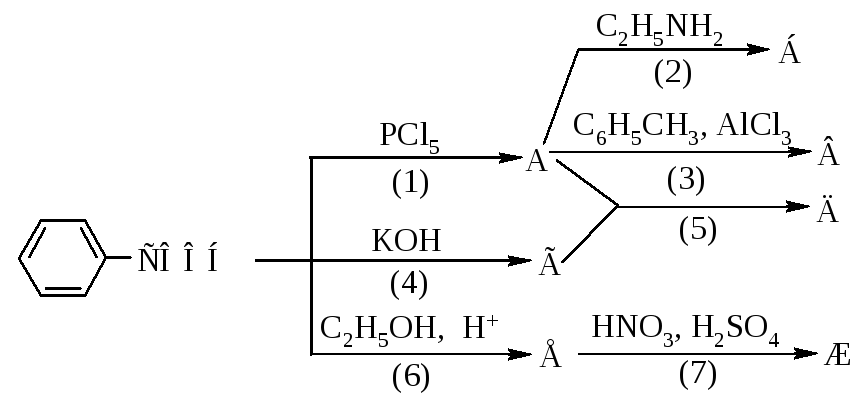
1231. Напишите уравнения реакций, назовите продукты, укажите механизмы реакций, рассмотрите механизмы реакций (1) и (3).
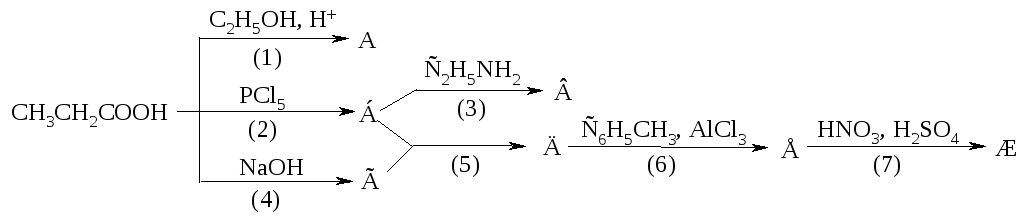
1232. Напишите уравнения реакций, назовите продукты, укажите механизмы реакций, рассмотрите механизмы реакций (2) и (7).
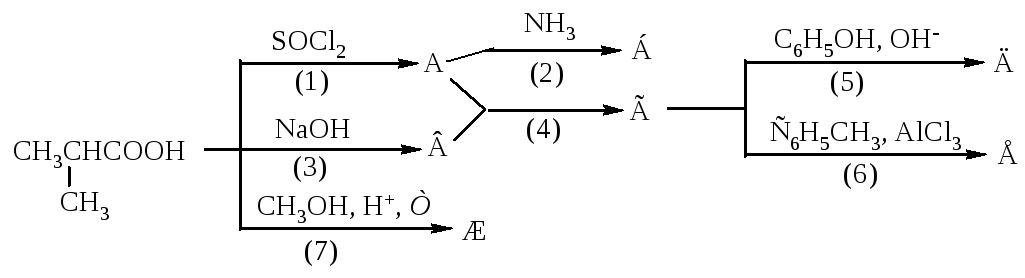
1233. Напишите уравнения реакций, назовите продукты, укажите механизмы реакций, рассмотрите механизмы реакций (2) и (3).
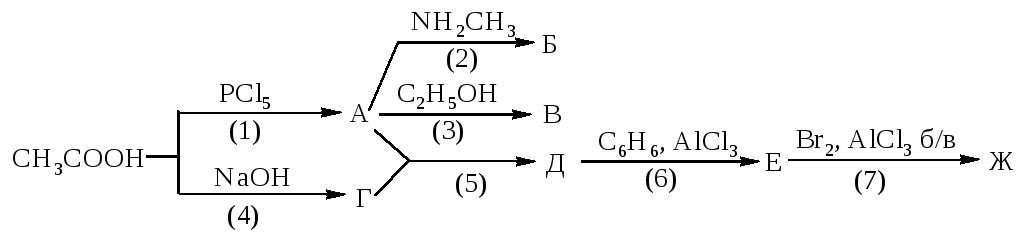
1234. Напишите уравнения реакций, назовите продукты, укажите механизмы реакций, рассмотрите механизмы реакций (3) и (6).
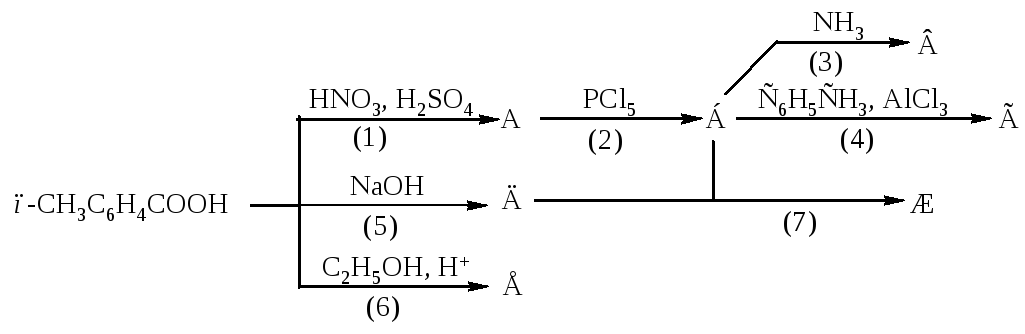
1235. Напишите уравнения реакций, назовите продукты, укажите механизмы реакций, рассмотрите механизмы реакций (2) и (7).
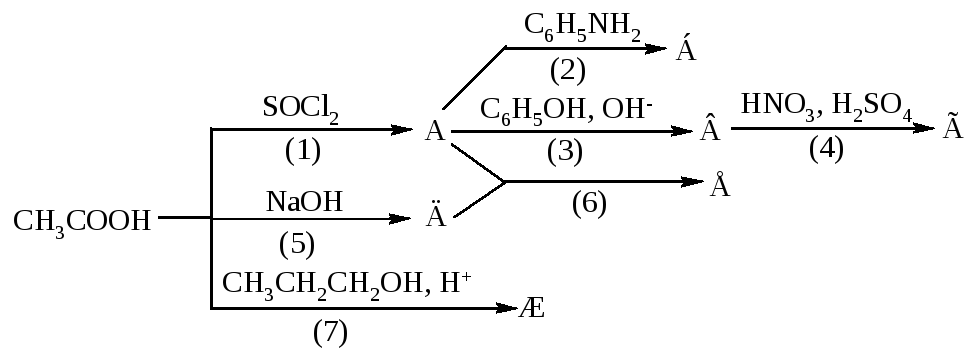
1236. Напишите уравнения реакций, назовите продукты, укажите механизмы реакций, рассмотрите механизмы реакций (4) и (7).

1237. Напишите уравнения реакций, назовите продукты, укажите механизмы реакций, рассмотрите механизмы реакций (1) и (6).
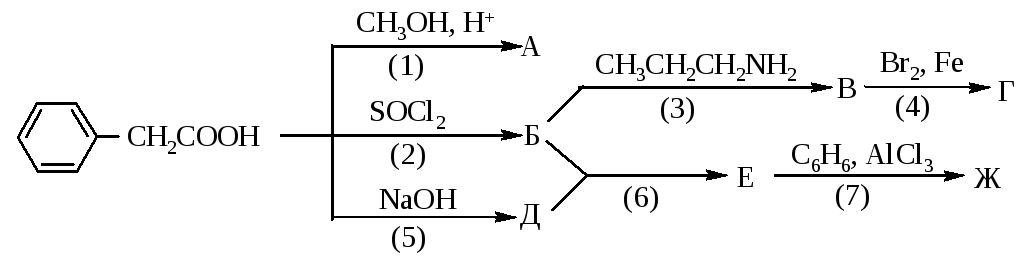
1238. Напишите уравнения реакций, назовите продукты, укажите механизмы реакций, рассмотрите механизмы реакций (2) и (7).
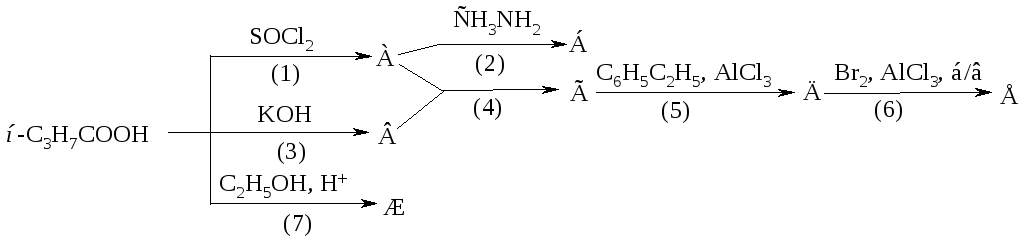
1239. Напишите уравнения реакций, назовите продукты, укажите механизмы реакций, рассмотрите механизмы реакций (1) и (5).
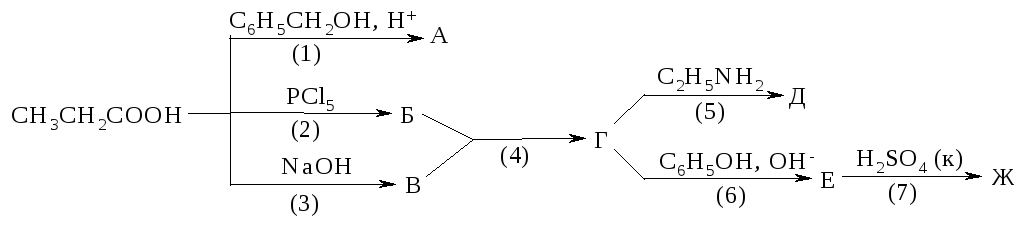
1240. Напишите уравнения реакций, назовите продукты, укажите механизмы реакций, рассмотрите механизмы реакций (2) и (6).
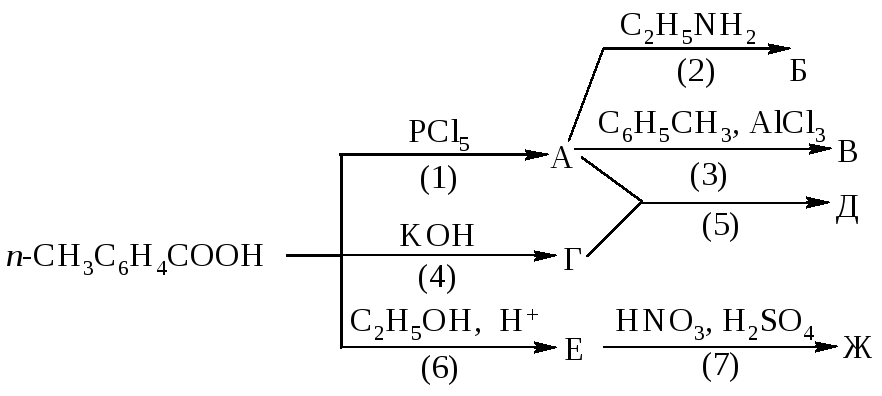
1241. Напишите уравнения реакций, назовите продукты, укажите механизмы реакций, рассмотрите механизмы реакций (2) и (7).
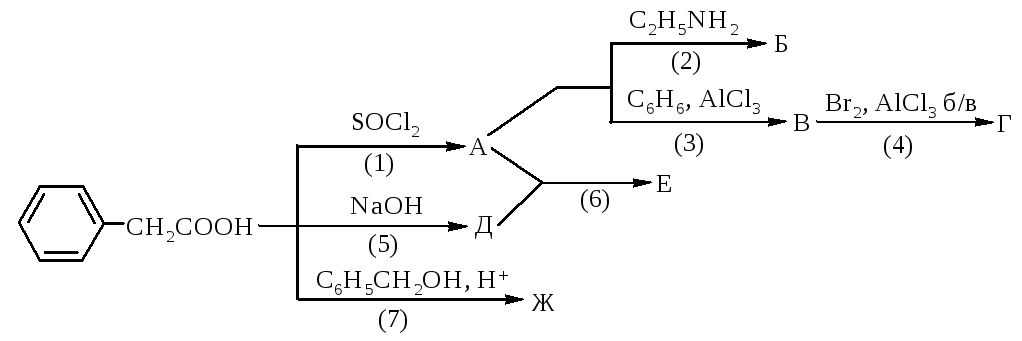
1242. Напишите уравнения реакций, назовите продукты, укажите механизмы реакций, рассмотрите механизмы реакций (3) и (7).
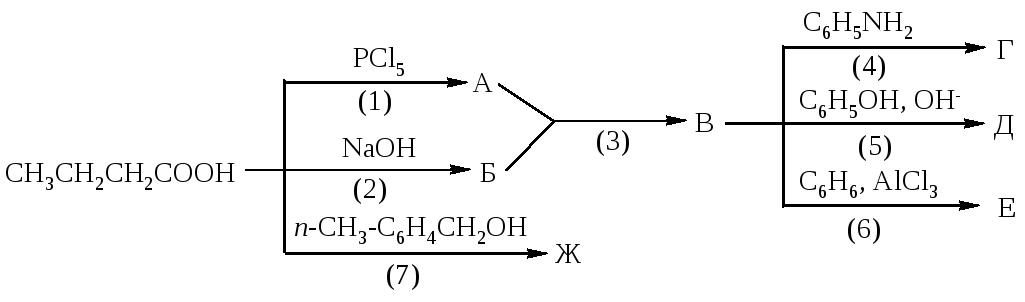
1243. Напишите уравнения реакций, назовите продукты, укажите механизмы реакций, рассмотрите механизмы реакций (1) и (3).
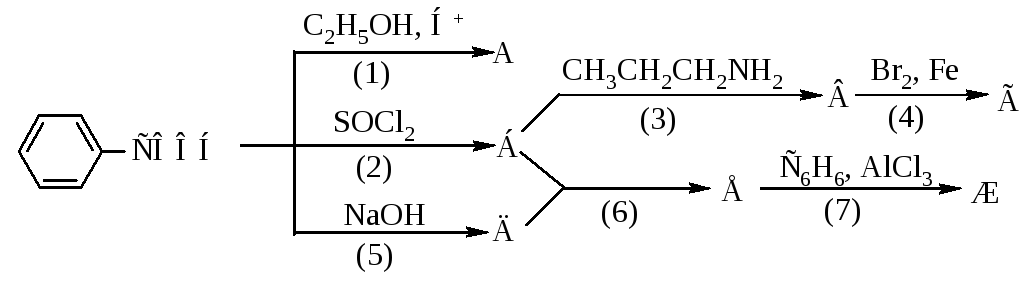
1244. Напишите уравнения реакций, назовите продукты, укажите механизмы реакций, рассмотрите механизмы реакций (2) и (4).

1245. Напишите уравнения реакций, назовите продукты, укажите механизмы реакций, рассмотрите механизмы реакций (5) и (6).
9.6. Механизм реакций этерификации, гидролиза, реакционная способность
1246. Напишите стадии, объясняющие обмен изотопом 18О между этилацетатом СН3С18ООС2Н5 и водой в кислом растворе. Кислотный гидролиз трет-бутилацетата в воде, обогащенной 18О, приводит к трет-бутиловому спирту, обогащенному 18О, и уксусной кислоте, содержащей обычный кислород. Как Вы объясните этот результат?
1247. Кислотный гидролиз ацетата оптически активного 3,7-диметилоктанола-3 дает спирт гораздо меньшей оптической чистоты, чем исходный спирт. Объясните этот результат.
1248. Относительные скорости щелочного гидролиза этиловых эфиров п-замещенных бензойных кислот п-Х-С6Н4-СООС2Н5 равны:
Х = - NO2 > - Cl > - H > - CH3 > - OCH3
110 4 1 0,5 0,2
Относительные скорости щелочного гидролиза алкилацетатов CH3COOR равны:
R = -CH3 > -C2H5 > -CH(CH3)2 > -C(CH3)3
1 0,6 0,15 0,008
Объясните такой порядок изменения реакционной способности.
1249. Как объяснить, что скорости реакций этерификации этиловым спиртом уксусной, пропионовой и пивалиновой (триметилуксусной) кислот уменьшаются в том порядке, в каком перечислены кислоты?
1250. Для получения трет-бутиловых эфиров карбоновых кислот часто используют следующий метод: карбоновую кислоту прибавляют к раствору изобутилена в хлористом метилене, взятому в избытке по отношению к кислоте, после чего к смеси добавляют концентрированную серную кислоту массой, равной 3-5 % массы карбоновой кислоты. Рассмотрите механизм протекающих превращений.
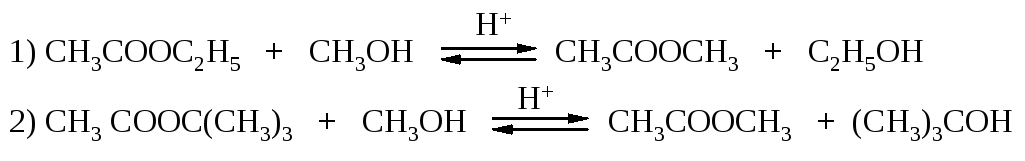
1251. Напишите механизмы для реакций переэтерификации, катализируемых кислотами (механизмы различны, во втором случае образуется значительное количество метил-трет-бутилового эфира):
1252. Скорости щелочного гидролиза этиловых эфиров триметилуксусной и трихлоруксусной кислот соотносятся как 1:107. Скорости кислотного гидролиза эфиров (СН3)3ССН2СООС2Н5 и НСООС2Н5 соотносятся как 1:105. Объясните причину такого различия.
1253. Рассмотрите механизмы реакций переэтерификации. Каков будет стереохимический результат реакций в первом и во втором случаях?
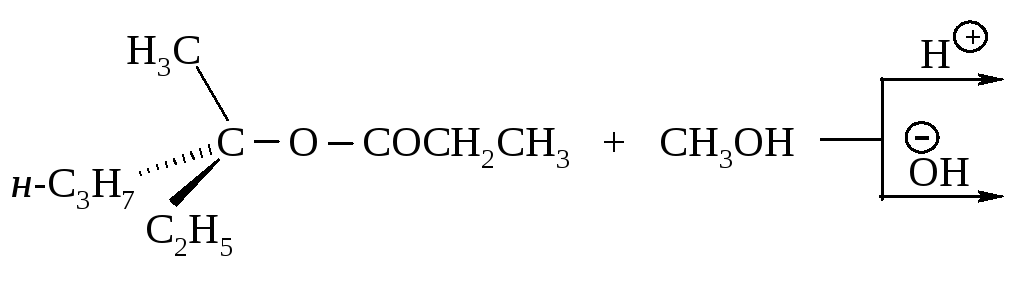
1254. Гидролиз трифенилметилбензоата в воде не нуждается в присутствии кислоты или основания. Добавление небольших количеств кислоты или основания не оказывает почти никакого влияния на скорость гидролиза. Рассмотрите механизм реакции, объясните наблюдаемые факты.
1255. Если ввести в реакцию с обычной бензойной кислотой меченный метиловый спирт СН3 18О, то образующийся метилбензоат будет содержать 18О, в то время как вода не будет содержать изотопной метки. Рассмотрите механизм реакции, объясните наблюдаемые факты.
1256. Расположите соединения каждой группы в порядке возрастания реакционной способности в реакциях этерификации:
а) реакция бензойной кислоты со следующими спиртами: метиловый, трет-пентиловый, н-пропиловый;
б) реакция этилового спирта со следующими кислотами: бензойная, 2,6-диметилбензойная, 4-толуиловая.
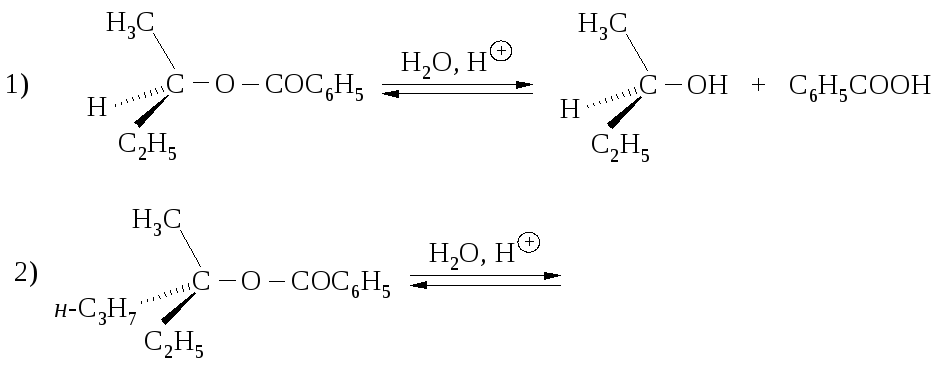
1257. Гидролиз втор-бутилбензоата протекает, как показано на схеме (1). Рассмотрите механизм реакции, покажите, что предложенный Вами механизм подтверждается стереохимическим результатом реакции. Предскажите стереохимический результат реакции (2).
1258. Напишите схему переэтерификации этилацетата метанолом. Приведите механизмы в условиях кислотного (Н2SO4) и основного (CH3ONa) катализа.
1259. Приведите схемы и механизмы кислотного и щелочного гидролиза этилпропионата. Объясните, почему щелочи катализируют только гидролиз сложных эфиров, но не их образование.
1260. Напишите схему этерификации пропионовой кислоты метиловым спиртом в присутствии серной кислоты. Приведите механизм и с его помощью объясните следующие факты: а) в отсутствие минеральной кислоты реакция практически не идет; б) высокая концентрация серной кислоты приводит к снижению скорости этерификации; в) использование меченого метанола СН318ОН приводит к эфиру, содержащему изотоп кислорода; г) добавление воды уменьшает выход эфира.
