
- •И. С. Колпащикова, а. Ф. Бетнев, е. М. Алов сборник задач по органической химии
- •150023, Ярославль, Московский пр., 88
- •150000, Ярославль, ул. Советская, 14а
- •1. Указания к выполнению домашней работы
- •2. Алканы
- •2.1. Изомерия
- •2.2. Конформации - изобразить проекции Ньюмена
- •2.3. Строение и температура кипения
- •2.4. Синтез Вюрца
- •2.5. Механизм радикального замещения: Механизм, расчет теплот реакций (2) и (3), медленная стадия – на примере углеводородов, которые в медленной стадии образуют один углеводородный радикал
- •2.6. Галогенирование высших алканов: строение радикалов, образующихся в медленной стадии, сравнение их устойчивости и легкости образования
- •2.7. Расчет процентного состава моногалогензамещенных, образующихся в реакции галогенирования алканов, или сравнение активностей алканов в реакции моногалогенирования
- •2.8. Цепочка превращений (сульфохлорирование, сульфоокисление, нитрование, электролиз, реакция Вюрца, галогенирование алканов
- •3. Алкены
- •3.1. Вывод структурных изомеров
- •3.2. Строение и устойчивость
- •3.3. Механизм электрофильного присоединения
- •3.4. Реакция электрофильного присоединения протекающая с перегруппировкой
- •3.5. Озонолиз
- •3.6. Полимеризация
- •3.7. Способы получения и химические превращения
- •3.8. Синтез алкенов и их химические превращения
- •3.9. Установление строения соединении по их свойствам
- •3.10. Задача на стехиометрический расчет
- •4. Диены. Алкины
- •4.1. Структурные изомеры диеновых углеводородов
- •4.2. Сравнение длины, энергий, дипольных моментов связей
- •4.3. Электрофильное присоединение к диенам
- •4.4. Полимеризация, озонолиз полимера
- •4.5. Реакция Дильса-Альдера
- •4.6. Свойства алкина как кислоты, реакция с солями более слабых кислот
- •4.7. Реакция гидратации алкинов
- •4.8. Способы получения и химические превращения
- •4.9. Сиетез алкинов
- •4.10. Установление строения соединений по их свойствам
- •5. Арены. Гетероциклы
- •5.1. Ароматичность, критерии ароматичнсти
- •5.2. Механизм электрофильного замещения в ядре
- •5.3. Расположить соединения с различными ориентантами в порядке изменения реакционной способности (4 соединения)
- •5.4. Объяснить механизм ориентирующего влияния определенной группы в seAr
- •5.5. Рассмотреть совместное влияние двух групп (согласованная и несогласованная ориентация)
- •5.6. Синтез замещенных аренов на основе бензола
- •5.7. Цепочка химических превращений
- •5.8. Электрофильное замещение в конденсированных многоядерных углеводородах
- •5.9. Реакции гетероциклов
- •5.10. Реакции гетероциклов
- •6. Галогеналканы. Галогенарены
- •6.1. 4 Реакции
- •6.2. Механизм sn
- •6.3. Cила нуклеофила
- •6.4. Растворитель
- •6.5. Уходящая группа
- •6.6. Стереохимия
- •6.7. Перегруппировка
- •6.8. Конкурирующие реакции
- •6.9. Элиминирование
- •6.10. Реакционная способность галогенов в соединениях, содержащих группировки
- •6.11. Цепочка
- •6.12. Осуществить превращение
- •6.13. Sn2 в ароматическом ядре
- •6.14. Стехиометрический расчет
- •7. Спирты. Фенолы. Простые эфиры
- •7.1. Спирты: строение - температура кипения
- •7.2. Спирты, фенолы: строение – кислотность
- •7.3. Магнийорганический синтез
- •7.4. Гидратация алкенов, гидролиз галогеналканов, гидроборирование
- •7.5. Магнийорганический синтез (подобрать исходные соединения), окисление спиртов
- •7.6. Превращение в простые эфиры
- •7.7. Превращение в сложные эфиры
- •7.8. Взаимодействие спиртов с галогенводородами
- •7.9. Элиминирование
- •7.10. Установить строение спирта
- •7.11. Реакция Вильямсона
- •7.12. Реакция расщепления простого эфира
- •7.13. Получение фенолов щелочным плавом, гидролизом галогенбензола, кумольный метод
- •7.14. Реакции фенолов в ароматическом ядре и в группе – он
- •7.15. Установить строение фенола
- •8. Карбонильные соединения
- •8.1. Получение ароматических альдегидов и кетонов
- •8.2. Получение алифатических альдегидов и кетонов
- •8.3. Реакция Кучерова, пиролиз солей карбоновых кислот
- •8.4. Подвижность α-водородного атома, нуклеофильное присоединение hcn, спиртов, гидросульфита натрия
- •8.5. Нуклеофильное присоединение производных аммиака, роль катализатора
- •8.6. Альдольная конденсация, другие реакции с участием карбанионов
- •8.7. Альдольная конденсация с участием соединений других классов
- •8.8. Получение спиртов с помощью альдольной конденсации
- •8.9. Реакция Канниццаро
- •8.10. Реакция окисления
- •8.11. Установить строение, провести превращение: а → карбонильное соединение или карбонильное соединение б
- •9. Карбоновые и сульфоновые кислоты
- •9.1. Окисление спиртов, превращение насыщенной кислоты в -амино, гидрокси, ненасыщенную или двухосновную кислоту через -галогензамещенную
- •9.2. Магнийорганический и нитрильный синтез
- •9.3. Алкилирование бензольного ядра и последующее окисление алкилароматического углеводорода
- •9.4. Строение и кислотность
- •9.5. Цепочка превращений, свойства кислот и их производных
- •9.6. Механизм реакций этерификации, гидролиза, реакционная способность
- •9.7. Сравнение поведения карбонильной группы карбоновой кислоты и кетона, сравнение реакционной способности ацильного и насыщенного углеродов
- •9.8. Получение и превращение сульфоновой кислоты
- •9.9. Установить строение карбоновой или сульфоновой кислоты
- •10. Амины
- •10.1. Получение алифатических аминов реакцией восстановления нитрилов, алкилированием аммиака и аминов и восстановительным аминированием
- •10.2. Строение и основность
- •10.3. Получение ароматических аминов и их превращение
- •10.4. Превращение аминов в соли диазония и реакции солей диазония с выделением азота
- •10.5. Превращение аминов в соли диазония и реакции солей диазония с выделением азота
- •10.6. Получение азокрасителя
- •10.7. Подобрать исходные соединения для синтеза азокрасителя
- •Библиографический список
- •И. С. Колпащикова, а. Ф. Бетнев,
4.5. Реакция Дильса-Альдера
331. Получите по реакции ДильсаАльдера следующее соединение:

Изобразите пространственное строение исходного диенофила.
332. Получите по реакции ДильсаАльдера следующее соединение:

333. Получите по реакции Дильса-Альдера аддукт, исходя из соединений: СН2=СН-СН=СН2 и цис-СН3-СО-СН=СН-С6Н5. Изобразите пространственное строение аддукта.
334. Получите по реакции ДильсаАльдера следующее соединение:

Изобразите пространственное строение исходного диенофила.
335. По реакции Дильса-Альдера получите аддукт

Изобразите пространственное строение исходного диенофила.
336. Получите по реакции Дильса-Альдера

337. Какие из перечисленных диенов будут реагировать с диэтилмалеатом Н5С2ООС–СН = СН–СООС2Н5? Напишите структурные формулы продуктов реакции.

338. Получите по реакции Дильса-Альдера

Изобразите пространственное строение исходного диенофила.
339. Получите по реакции Дильса-Альдера
![]()
340. Получите по реакции Дильса-Альдера

Изобразите пространственное строение исходного диенофила.
341. Получите по реакции Дильса-Альдера

342. Какие из перечисленных диенов будут реагировать с метилакрилатом СН2 = СН–СООСН3? Напишите структурные формулы продуктов реакции.
343. Получите по реакции Дильса-Альдера аддукт, исходя из соединений СН2=СН-СН=СН2 и СН3ООС-С≡С-СООСН3 в мольном соотношении 2:1.
344. По реакции Дильса-Альдера получите аддукт, исходя из следующих соединений:
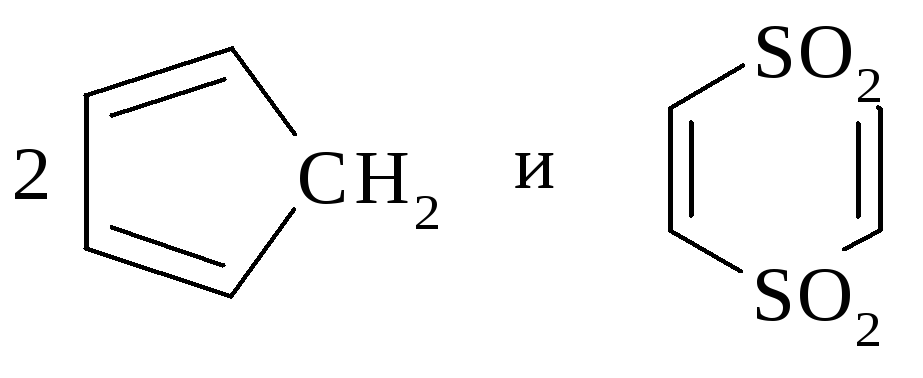
345. По реакции Дильса-Альдера получите аддукт, исходя из следующих соединений:
![]()
Изобразите пространственное строение аддукта.
4.6. Свойства алкина как кислоты, реакция с солями более слабых кислот
346. С какими из соединений 1-бутин будет реагировать как кислота: NaH, KNH2, CH3COONa? Напишите уравнения реакций. Укажите более слабые и более сильные кислоты и основания.
347. С какими из соединений 1-пентин будет реагировать как
кислота: NaNH2, KCl, NaOH? Напишите уравнения реакций. Укажите более слабые и более сильные кислоты и основания.
348. Расположите в порядке уменьшения кислотности соединения С2Н5ОН, С3Н8, СН3ССН. Какие из них будут реагировать с н-C4Н9Li? В этих реакциях укажите более сильные и более слабые кислоты и основания.
349. Среди перечисленных соединений найдите наиболее сильную СН-кислоту: пропин, 1-бутен, пропан. Напишите для нее реакцию с бутиллитием, укажите более сильные и более слабые кислоты и основания.
350. Среди перечисленных соединений найдите наиболее сильную СН-кислоту: бутан, 2-бутин, пропин. Напишите уравнение реакции этой кислоты с NaNH2, укажите более сильные и более слабые кислоты и основания.
351. Среди приведенных соединений укажите те, которые будут взаимодействовать с бутиллитием: пропан, пропин, этиловый спирт. Напишите уравнения реакций, укажите более сильные и более слабые кислоты и основания.
352. Какие из соединений могут вступать в реакцию с С2Н5MgI: СН3–СН3, СН3–СН2ОН, СН3–ССН? Напишите уравнения реакций, укажите более слабые и более сильные кислоты и основания.
353. Среди указанных соединений найдите наиболее сильную СН-кислоту: н-С4Н10, СН3–СС–СН3, СН3–СН2–ССН. Напишите для нее реакцию с NaNH2. Укажите более слабые и более сильные кислоты и основания.
354. С какими соединениями 1-пентин будет реагировать как кислота: бутиллитий, хлорид калия, этоксид натрия? Напишите уравнения реакций, укажите более сильные и более слабые кислоты и основания.
355. С какими соединениями 1-бутин будет реагировать как кислота: гидрид натрия, бутоксид натрия, гидроксид калия? Напишите уравнения реакций, укажите более сильные и более слабые кислоты и основания.
356. С какими соединениями 3-метил-1-пентин будет реагировать как кислота: ацетат натрия, бутиллитий, гидрид натрия? Напишите уравнения реакций, укажите более сильные и более слабые кислоты и основания.
357. Среди перечисленных соединений найдите наиболее сильные кислоты: 1-гексен, 1-гексин, гексан. Напишите уравнение реакции этих кислот с NaNH2, укажите более сильные и более слабые кислоты и основания.
358. Среди перечисленных соединений найдите наиболее сильную СН-кислоту: 2-бутин, 1-гептин, гексан. Напишите уравнение реакции этой кислоты с бутиллитием, укажите более сильные и более слабые кислоты и основания.
359. Среди указанных соединений найдите наиболее сильную СН-кислоту: пентан, 2-пентин, 1-пентин. Напишите для нее реакцию с С2Н5MgI. Укажите более слабые и более сильные кислоты и основания.
360. Среди указанных соединений найдите наиболее сильные кислоты: изопентан, 1-пропанол, 3-метил-1-бутин. Напишите для них реакции с гидридом натрия. Укажите более слабые и более сильные кислоты и основания.
