
- •И. С. Колпащикова, а. Ф. Бетнев, е. М. Алов сборник задач по органической химии
- •150023, Ярославль, Московский пр., 88
- •150000, Ярославль, ул. Советская, 14а
- •1. Указания к выполнению домашней работы
- •2. Алканы
- •2.1. Изомерия
- •2.2. Конформации - изобразить проекции Ньюмена
- •2.3. Строение и температура кипения
- •2.4. Синтез Вюрца
- •2.5. Механизм радикального замещения: Механизм, расчет теплот реакций (2) и (3), медленная стадия – на примере углеводородов, которые в медленной стадии образуют один углеводородный радикал
- •2.6. Галогенирование высших алканов: строение радикалов, образующихся в медленной стадии, сравнение их устойчивости и легкости образования
- •2.7. Расчет процентного состава моногалогензамещенных, образующихся в реакции галогенирования алканов, или сравнение активностей алканов в реакции моногалогенирования
- •2.8. Цепочка превращений (сульфохлорирование, сульфоокисление, нитрование, электролиз, реакция Вюрца, галогенирование алканов
- •3. Алкены
- •3.1. Вывод структурных изомеров
- •3.2. Строение и устойчивость
- •3.3. Механизм электрофильного присоединения
- •3.4. Реакция электрофильного присоединения протекающая с перегруппировкой
- •3.5. Озонолиз
- •3.6. Полимеризация
- •3.7. Способы получения и химические превращения
- •3.8. Синтез алкенов и их химические превращения
- •3.9. Установление строения соединении по их свойствам
- •3.10. Задача на стехиометрический расчет
- •4. Диены. Алкины
- •4.1. Структурные изомеры диеновых углеводородов
- •4.2. Сравнение длины, энергий, дипольных моментов связей
- •4.3. Электрофильное присоединение к диенам
- •4.4. Полимеризация, озонолиз полимера
- •4.5. Реакция Дильса-Альдера
- •4.6. Свойства алкина как кислоты, реакция с солями более слабых кислот
- •4.7. Реакция гидратации алкинов
- •4.8. Способы получения и химические превращения
- •4.9. Сиетез алкинов
- •4.10. Установление строения соединений по их свойствам
- •5. Арены. Гетероциклы
- •5.1. Ароматичность, критерии ароматичнсти
- •5.2. Механизм электрофильного замещения в ядре
- •5.3. Расположить соединения с различными ориентантами в порядке изменения реакционной способности (4 соединения)
- •5.4. Объяснить механизм ориентирующего влияния определенной группы в seAr
- •5.5. Рассмотреть совместное влияние двух групп (согласованная и несогласованная ориентация)
- •5.6. Синтез замещенных аренов на основе бензола
- •5.7. Цепочка химических превращений
- •5.8. Электрофильное замещение в конденсированных многоядерных углеводородах
- •5.9. Реакции гетероциклов
- •5.10. Реакции гетероциклов
- •6. Галогеналканы. Галогенарены
- •6.1. 4 Реакции
- •6.2. Механизм sn
- •6.3. Cила нуклеофила
- •6.4. Растворитель
- •6.5. Уходящая группа
- •6.6. Стереохимия
- •6.7. Перегруппировка
- •6.8. Конкурирующие реакции
- •6.9. Элиминирование
- •6.10. Реакционная способность галогенов в соединениях, содержащих группировки
- •6.11. Цепочка
- •6.12. Осуществить превращение
- •6.13. Sn2 в ароматическом ядре
- •6.14. Стехиометрический расчет
- •7. Спирты. Фенолы. Простые эфиры
- •7.1. Спирты: строение - температура кипения
- •7.2. Спирты, фенолы: строение – кислотность
- •7.3. Магнийорганический синтез
- •7.4. Гидратация алкенов, гидролиз галогеналканов, гидроборирование
- •7.5. Магнийорганический синтез (подобрать исходные соединения), окисление спиртов
- •7.6. Превращение в простые эфиры
- •7.7. Превращение в сложные эфиры
- •7.8. Взаимодействие спиртов с галогенводородами
- •7.9. Элиминирование
- •7.10. Установить строение спирта
- •7.11. Реакция Вильямсона
- •7.12. Реакция расщепления простого эфира
- •7.13. Получение фенолов щелочным плавом, гидролизом галогенбензола, кумольный метод
- •7.14. Реакции фенолов в ароматическом ядре и в группе – он
- •7.15. Установить строение фенола
- •8. Карбонильные соединения
- •8.1. Получение ароматических альдегидов и кетонов
- •8.2. Получение алифатических альдегидов и кетонов
- •8.3. Реакция Кучерова, пиролиз солей карбоновых кислот
- •8.4. Подвижность α-водородного атома, нуклеофильное присоединение hcn, спиртов, гидросульфита натрия
- •8.5. Нуклеофильное присоединение производных аммиака, роль катализатора
- •8.6. Альдольная конденсация, другие реакции с участием карбанионов
- •8.7. Альдольная конденсация с участием соединений других классов
- •8.8. Получение спиртов с помощью альдольной конденсации
- •8.9. Реакция Канниццаро
- •8.10. Реакция окисления
- •8.11. Установить строение, провести превращение: а → карбонильное соединение или карбонильное соединение б
- •9. Карбоновые и сульфоновые кислоты
- •9.1. Окисление спиртов, превращение насыщенной кислоты в -амино, гидрокси, ненасыщенную или двухосновную кислоту через -галогензамещенную
- •9.2. Магнийорганический и нитрильный синтез
- •9.3. Алкилирование бензольного ядра и последующее окисление алкилароматического углеводорода
- •9.4. Строение и кислотность
- •9.5. Цепочка превращений, свойства кислот и их производных
- •9.6. Механизм реакций этерификации, гидролиза, реакционная способность
- •9.7. Сравнение поведения карбонильной группы карбоновой кислоты и кетона, сравнение реакционной способности ацильного и насыщенного углеродов
- •9.8. Получение и превращение сульфоновой кислоты
- •9.9. Установить строение карбоновой или сульфоновой кислоты
- •10. Амины
- •10.1. Получение алифатических аминов реакцией восстановления нитрилов, алкилированием аммиака и аминов и восстановительным аминированием
- •10.2. Строение и основность
- •10.3. Получение ароматических аминов и их превращение
- •10.4. Превращение аминов в соли диазония и реакции солей диазония с выделением азота
- •10.5. Превращение аминов в соли диазония и реакции солей диазония с выделением азота
- •10.6. Получение азокрасителя
- •10.7. Подобрать исходные соединения для синтеза азокрасителя
- •Библиографический список
- •И. С. Колпащикова, а. Ф. Бетнев,
3.6. Полимеризация
196. Для стирола возможна как анионная, так и катионная полимеризация вследствие наличия сопряжения -электронной системы бензольного ядра в конце цепи. Приведите механизм реакции катионной полимеризации.
197. Приведите механизм реакции свободнорадикальной полимеризации стирола с инициатором пероксидом бензоила. Почему стирол полимеризуется очень быстро?
198. Рассмотрите механизм полимеризации н-пропилвинилового эфира CН3СН2СН2-О-СН=СН2 в присутствии BF3 (кислота Льюиса).
199. Рассмотрите механизм полимеризации пропилвинилового эфира СН3СН2СН2-О-СН=СН2 в присутствии BF3 (кислота Льюиса).
200. Из какого
мономера был получен полимер ![]() ?
Приведите механизм реакции полимеризации
по стадиям. Почему для данного мономера
не применяют катионную полимеризацию?
?
Приведите механизм реакции полимеризации
по стадиям. Почему для данного мономера
не применяют катионную полимеризацию?
201. Из какого
мономера получен полимер ![]() ?
Приведите
механизм реакции по стадиям.
Приведите структурные формулы полимеров,
которые могут быть получены в присутствии
инициатора Al(C2H5)3
+ TiCl4.
?
Приведите
механизм реакции по стадиям.
Приведите структурные формулы полимеров,
которые могут быть получены в присутствии
инициатора Al(C2H5)3
+ TiCl4.
202. Приведите
механизм реакции анионной полимеризации
метилметакрилата
![]() .
Почему для этого алкена
пригоден данный тип полимеризации?
.
Почему для этого алкена
пригоден данный тип полимеризации?
203. Из какого
мономера можно получить полимер
![]() ?
?

Приведите механизм реакции полимеризации по стадиям.
204. Приведите
механизм реакции анионной полимеризации
бутилметакрилата
 .
Почему для этого алкена невозможна
катионная полимеризация?
.
Почему для этого алкена невозможна
катионная полимеризация?
205. Полимеризация тетрафторэтилена обычно проводится при 70-100 оС и давлении 4-10 МПа (40-100 атм) в присутствии инициаторов. Приведите механизм реакции полимеризации по стадиям.
206. Полимеризация винилиденхлорида СН2=ССl2 в промышленности инициируется пероксидами и проводится при температуре 30-60 оС “голова к хвосту”. Приведите механизм реакции полимеризации по стадиям.
207. Полимеризацию простых виниловых эфиров проводят под действием кислот и катализаторов Фриделя-Крафтса (AlCl3, BF3). Приведите механизм реакции полимеризации этилвинилового эфира (СН2=СН-ОС2Н5).
208. Для стирола возможна как анионная, так и катионная полимеризация вследствие наличия сопряжения -электронной системы бензольного ядра в конце цепи. Приведите механизм реакции анионной полимеризации.
209.
Приведите
механизм
реакции
свободнорадикальной полимеризации
хлорвинила CH2=CHCl
с инициатором динитрилом азоизомасляной
кислоты .
Почему для
этого мономера не применяют катионную
полимеризацию?
.
Почему для
этого мономера не применяют катионную
полимеризацию?
210. Приведите механизм реакции катионной полимеризации метилпропена. Почему для этого алкена пригоден данный тип полимеризации?
3.7. Способы получения и химические превращения
211. Напишите уравнения реакций, назовите все соединения, укажите механизмы реакций:

Сформулируйте правило, по которому протекает реакция дегидрогалогенирования.
212. Напишите уравнения реакций, назовите все соединения, укажите механизмы реакций:

Сформулируйте правило, по которому протекает реакция дегидрогалогенирования.
213. Напишите уравнения реакций, назовите все соединения, укажите механизмы реакций:
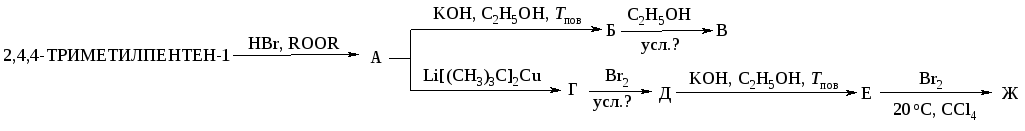
Сформулируйте правило, по которому протекает реакция дегидрогалогенирования.
214. Напишите уравнения реакций, назовите все соединения, укажите механизмы реакций:

Сформулируйте правило, по которому протекают реакции дегидратации и дегидрогалогенирования.
215. Напишите уравнения последовательных реакций
![]()
Сформулируйте правило Зайцева, укажите механизмы реакции.
216. Какими реакциями и какие алкены можно получить из следующих соединений: а) 2-метилпентан, б) 2-пентанол, в) 2-бром-3-метилпентан? Алкен, полученный из соединения (а), превратите во вторичный спирт. Напишите уравнения реакций, назовите все соединения, укажите механизмы реакций, сформулируйте правило Зайцева.
217. Из каких спиртов и каких галогеналканов можно получить 2,4-диметил-2-пентен? Напишите уравнения. Сформулируйте правило Зайцева. Как полученный алкен будет реагировать а) с водным раствором перманганата калия на холоду; б) с раствором перманганата калия в присутствии H2SO4 при нагревании; в) с бромоводородом в присутствии пероксида?
218. Продукт бромирования 2-метилпентана обработали спиртовым раствором щелочи, а полученное соединение ввели в реакцию а) с водным раствором перманганата калия на холоду; б) с раствором перманганата калия в присутствии H2SO4 при нагревании; в) с ВН3, а затем с Н2О2(ОНө). Напишите уравнения реакций. Сформулируйте правило Зайцева.
219. Напишите уравнения реакций, назовите все соединения, укажите механизмы реакций:

Сформулируйте правило, по которому протекает реакция дегидрогалогенирования.
220. Напишите уравнения реакций, назовите все соединения, укажите механизмы реакций:
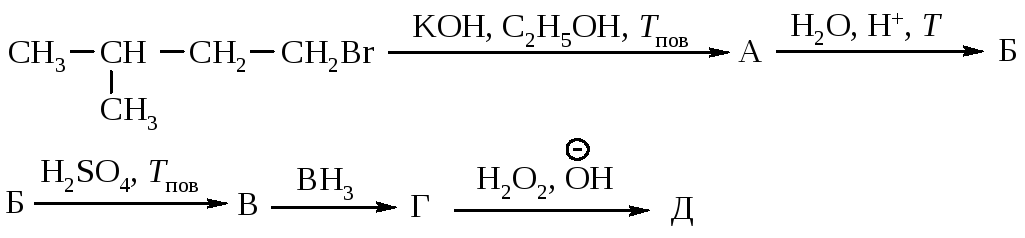
Сформулируйте правило, по которому протекает реакция дегидратации.
221. Напишите уравнения реакций, назовите все соединения, укажите механизмы реакций:
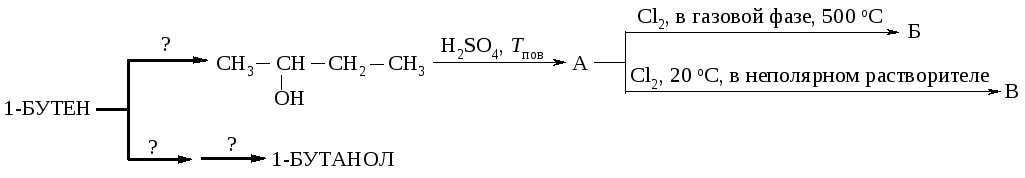
Сформулируйте правило, по которому протекает реакция дегидратации.
222. Напишите уравнения реакций, назовите все соединения, укажите механизмы реакций:
![]()
Сформулируйте правило, по которому протекает реакция дегидратации.
223. Напишите уравнения реакций, назовите все соединения, укажите механизмы реакций:

Приведите правило, по которому протекает реакция дегидрогалогенирования.
224. Из какого спирта и какого галогеналкана можно получить 3,4-диметил-3-гексен? Как полученный алкен будет реагировать а) с водным раствором перманганата калия (с массовой долей 2 %) на холоду; б) с раствором перманганата калия в присутствии H2SO4 при нагревании; в) с бромом; г) с бромоводородом в присутствии пероксида? Напишите уравнения всех реакций. Сформулируйте правило Зайцева.
225. Продукт бромирования 2,2,5-триметилгексана обработали спиртовым раствором щелочи при нагревании, а затем ввели в реакции а) с бромоводородом в присутствии пероксида; б) с раствором КмnO4 (с массовой долей 2 %) при 20 оС; в) с гидропероксидом бензоила С6Н5С(О)ООН. Сформулируйте правило Зайцева. Напишите уравнения реакций, укажите условия и механизмы реакций.
