
6 курс / Эндокринология / Endokrinologia_-_2013
.pdf
150 |
Вепрена |
|
|
|
|
|
|
|
Глава 2 |
|||
тонинами млекопитающих), его дей, |
ФАРМАКОКИНЕТИКА. |
Всасыва/ |
||||||||||
ствие выражено в наибольшей степе, |
ние. Препарат быстро всасывается че, |
|||||||||||
ни как по силе, так и по продолжите, |
рез слизистую оболочку носа, Cmax |
в |
||||||||||
льности. |
|
|
|
|
плазме достигается в течение первого |
|||||||
Кальцитонин |
лосося подавляет ак, |
часа (в среднем, около 10 мин). Биодо, |
||||||||||
тивность остеокластов за счет воздей, |
ступность — 3–5%. При применении |
|||||||||||
ствия на специфические рецепторы, |
препарата в дозах, превышающих ре, |
|||||||||||
существенно снижает скорость обме, |
комендованные, |
повышается |
AUC, |
|||||||||
на костной ткани до нормального |
при этом биодоступность не увеличи, |
|||||||||||
уровня при состояниях с повышен, |
вается. |
|
|
|
|
|
||||||
ной скоростью резорбции (при остео, |
Определение концентрации кальци, |
|||||||||||
порозе). |
|
|
|
|
тонина лосося в плазме, как и концен, |
|||||||
Кальцитонин обладает анальгетиче, |
траций других полипептидных гормо, |
|||||||||||
ской активностью при болях костно, |
нов, представляется малоценным, по, |
|||||||||||
го происхождения, которая обуслов, |
скольку по уровню концентраций не, |
|||||||||||
лена непосредственным воздействи, |
льзя |
предсказать терапевтическую |
||||||||||
ем на ЦНС. |
|
|
|
эффективность |
препарата. |
|
Актив, |
|||||
Уже после однократного применения |
ность препарата оценивают по клини, |
|||||||||||
препарата отмечается |
клинически |
ческим показателям эффективности. |
||||||||||
значимая ответная реакция, которая |
Кальцитонин лосося не проникает |
|||||||||||
проявляется повышением экскреции |
через плацентарный барьер. |
|
|
|
||||||||
с мочой кальция, фосфора и натрия |
Метаболизм. T1/2 составляет около 20 |
|||||||||||
(за счет снижения их канальцевой ре, |
минут, при повторном применении |
|||||||||||
абсорбции) и снижением экскреции |
кумуляции не отмечается. |
|
|
|
||||||||
гидроксипролина. |
|
|
ПОКАЗАНИЯ |
|
|
|
|
|||||
По известным данным, при продол, |
|
|
|
|
||||||||
жительном применении кальцитони, |
• лечение постменопаузного остеопо, |
|||||||||||
на достигается значительное и стой, |
роза; |
|
|
|
|
|
|
|||||
• боли в костях, связанные с остеоли, |
||||||||||||
кое снижение уровня биохимических |
||||||||||||
маркеров костного обмена, таких как |
зом и/или остеопенией; |
|
|
|
||||||||
• болезнь Педжета (деформирующий |
||||||||||||
сывороточные С,телопептиды и ко, |
||||||||||||
стные изоферменты ЩФ. |
|
остеит); |
|
|
|
|
|
|||||
Применение препарата |
приводит к |
• нейродистрофические заболевания |
||||||||||
статистически |
значимому |
повыше, |
(в т.ч. алгонейродистрофия, атро, |
|||||||||
нию минеральной плотности кости в |
фия Зудека) различной этиологии, |
|||||||||||
поясничных |
позвонках, |
которое |
обусловленные различными пред, |
|||||||||
определяется уже на первом году ле, |
располагающими факторами, в т.ч. |
|||||||||||
чения и сохраняется до 5 лет; обеспе, |
такими как посттравматический ос, |
|||||||||||
чивает |
поддержание |
минеральной |
теопороз, |
рефлекторная |
дистро, |
|||||||
плотности бедренной кости. |
|
фия, |
плечелопаточный |
синдром, |
||||||||
Применение препарата в дозе 200 |
каузалгии, |
лекарственные |
нейро, |
|||||||||
ME/сут в комбинации с препаратами |
трофические нарушения. |
|
|
|
||||||||
витамина D и кальция приводит к |
ПРОТИВОПОКАЗАНИЯ |
|
|
|
||||||||
статистически и клинически значи, |
• повышенная |
чувствительность |
к |
|||||||||
мому снижению риска развития но, |
синтетическому кальцитонину ло, |
|||||||||||
вых переломов позвонков и сниже, |
сося или любому другому компо, |
|||||||||||
нию частоты множественных перело, |
ненту препарата; |
|
|
|
||||||||
мов позвонков. |
|
|
• препарат |
не |
рекомендуется для |
|||||||
Кальцитонин |
снижает |
желудочную |
применения у детей в возрасте до 18 |
|||||||||
секрецию и экзокринную функцию |
лет в связи с отсутствием данных по |
|||||||||||
поджелудочной железы. |
|
эффективности и безопасности. |
|
|||||||||

|
|
|
|
|
|
|
|
Вепрена |
151 |
||
ПРИМЕНЕНИЕ ПРИ БЕРЕМЕН0 |
ях в начале лечения может потребо, |
||||||||||
НОСТИ |
И |
КОРМЛЕНИИ |
ГРУ0 |
ваться доза 400 МЕ/сут, назначаемая |
|||||||
ДЬЮ. Кальцитонин не оказывает эм, |
в несколько введений. |
|
|
||||||||
бриотоксического и |
тератогенного |
При болезни Педжета продолжите, |
|||||||||
действия, не проникает через плацен, |
льность лечения должна составлять |
||||||||||
тарный барьер, согласно эксперимен, |
от нескольких месяцев до нескольких |
||||||||||
тальным данным. |
|
|
|
лет. На фоне лечения отмечается су, |
|||||||
Клинических данных по безопасно, |
щественное снижение концентрации |
||||||||||
сти применения препарата в период |
ЩФ в крови и экскреции гидроксип, |
||||||||||
беременности нет. В связи с этим пре, |
ролина с мочой, иногда до нормаль, |
||||||||||
парат не следует применять у жен, |
ных значений. В отдельных случаях |
||||||||||
щин в период беременности. |
|
после начального снижения значения |
|||||||||
В период терапии препаратом реко, |
этих показателей, возможно их повы, |
||||||||||
мендуется отказаться |
от |
кормления |
шение. В этих случаях врач, руковод, |
||||||||
грудью, т.к. неизвестно, проникает ли |
ствуясь клинической картиной, дол, |
||||||||||
кальцитонинлососявгрудноемолоко. |
жен решить, следует ли отменять ле, |
||||||||||
СПОСОБ ПРИМЕНЕНИЯ И ДО0 |
чение и когда его можно возобновить. |
||||||||||
Через один или несколько месяцев |
|||||||||||
ЗЫ. Интраназально, в один из носо, |
после отмены лечения нарушения ме, |
||||||||||
вых ходов. |
|
|
|
|
таболизма костной ткани могут воз, |
||||||
Для лечения остеопороза: рекоменду, |
|||||||||||
никнуть вновь; в этом случае потре, |
|||||||||||
емая доза — 200 МЕ/сут. |
|
|
буется проведение нового курса. |
||||||||
Одновременно с применением наза, |
Нейродистрофические заболевания: в |
||||||||||
льного спрея рекомендуется назначе, |
суточной дозе 200 МЕ, ежедневно в |
||||||||||
ние адекватных доз кальция и вита, |
течение 2–4 нед. Возможно дополни, |
||||||||||
мина D. Лечение следует проводить в |
тельное назначение по 200 МЕ через |
||||||||||
течение длительного времени. |
|
день в течение 6 нед в зависимости от |
|||||||||
При болях в костях, связанных с ос/ |
динамики состояния пациента. |
||||||||||
теолизом и/или остеопенией: суточ, |
Применение у пациентов пожилого воз/ |
||||||||||
ная |
доза |
препарата |
составляет |
раста и отдельных групп пациентов |
|||||||
200–400 |
МЕ |
ежедневно. Суточная |
По известным |
данным, |
пациентам |
||||||
доза, составляющая 200 МЕ, может |
пожилого возраста и больным со сни, |
||||||||||
быть введена за 1 раз. Более высокие |
жением функции почек или печени |
||||||||||
дозы следует разделять на несколько |
нет необходимости изменять режим |
||||||||||
введений. Дозу следует корректиро, |
дозирования препарата. |
|
|
||||||||
вать с учетом индивидуальных по, |
Правила применения |
|
|
||||||||
требностей больного. Для достиже, |
1. Никогда не следует встряхивать |
||||||||||
ния |
полного |
анальгетического эф, |
флакон, т.к. это может привести к |
||||||||
фекта может потребоваться несколь, |
образованию |
пузырьков |
воздуха |
||||||||
ко дней. При проведении длительной |
внутри флакона, что повлечет за со, |
||||||||||
терапии |
начальную |
суточную |
дозу |
бой неправильное дозирование пре, |
|||||||
обычно уменьшают и/или увеличи, |
парата. |
|
|
|
|||||||
вают интервал между введениями. |
2. Необходимо снять защитный кол, |
||||||||||
Продолжительность лечения состав, |
пачок. |
|
|
|
|||||||
ляет минимум 3 мес, при необходи, |
3. При первом применении, удержи, |
||||||||||
мости она может быть больше. Суточ, |
вая устройство одной или двумя ру, |
||||||||||
ную дозу следует корректировать с |
ками строго вертикально, надавить на |
||||||||||
учетом |
индивидуальных |
потребно, |
поршень 3 раза, что позволит воздуху |
||||||||
стей больного. |
|
|
|
выйти из трубочки. Это надо сделать |
|||||||
Болезнь Педжета: суточная доза пре, |
только однажды для |
приведения |
|||||||||
парата — 200 МЕ. В некоторых случа, |
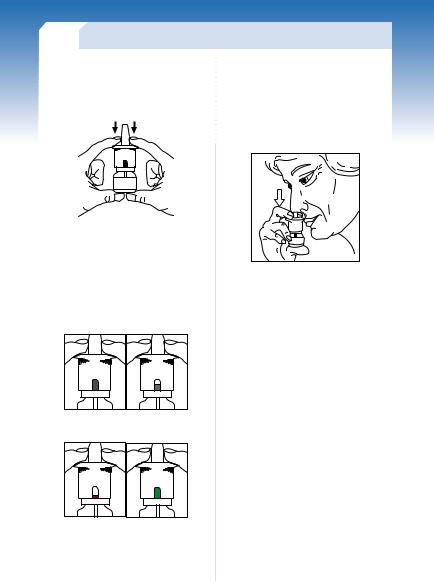
устройства в рабочее состояние (рис. |
||||||||||
152 |
Вепрена |
Глава 2 |
1). Не следует беспокоиться, если |
Убедиться, что наконечник распола, |
|
вместе с воздухом произойдет раз, |
гается на одной линии с носовым хо, |
|
брызгивание незначительного коли, |
дом, что обеспечит более равномер, |
|
чества раствора (это предусмотрено и |
ное распределение раствора. Нажать |
|
не влияет на последующее количест, |
на поршень один раз. Вынуть нако, |
|
во доз). |
|
нечник из носа и сделать несколько |
|
|
энергичных вдохов носом для преду, |
|
|
преждения вытекания препарата |
|
|
(рис. 3). |
Рисунок |
1. Методика приведения |
|
|
|
устройства в рабочее состояние. |
|
|
||
4. Следует обратить внимание, что |
|
|
||
после каждого последовательного на, |
|
|
||
жатия на поршень цвет окошка счет, |
Рисунок 3. Методика использова0 |
|||
чика доз будет меняться от черного до |
ния назального спрея. |
|
||
зеленого. После четвертого нажатия |
Не следует прочищать нос сразу по, |
|||
окошко должно стать зеленого цвета, |
сле применения препарата. Если врач |
|||
что означает готовность устройства к |
назначил 2 введения за 1 прием, то |
|||
работе (рис. 2.1 и 2.2). |
второе введение следует сделать в |
|||
|
|
другой носовой ход. |
|
|
|
|
После использования |
наконечник |
|
|
|
следует аккуратно протереть чистой |
||
|
|
сухой тканью и надеть защитный |
||
|
|
колпачок на наконечник. |
|
|
|
|
Проверка счетчика доз |
|
|
|
|
1. Перед и после использования спрея |
||
Рисунок |
2.1. Изменение цвета |
следует проверять цифру в окошке |
||
счетчика доз. |
|
|||
окошка счетчика. |
2. После каждого использования на, |
|||
|
|
зального спрея цифра в окошке будет |
||
|
|
меняться. |
|
|
|
|
3. Если за один раз вводится 1 доза, то |
||
|
|
предыдущее значение увеличивается |
||
|
|
на 1. |
|
|
|
|
4. Назальный спрей содержит 14 |
||
|
|
полных доз. Поскольку всегда пре, |
||
Рисунок 2.2 Изменение цвета окош0 |
дусмотрен остаток раствора во фла, |
|||
коне, то возможно получение еще |
||||
ка счетчика. |
двух дополнительных доз. Когда в |
|||
Методика использования назального |
||||
окошке появится цифра 16 красного |
||||
спрея |
|
цвета, это будет означать, что лекар, |
||
1. Слегка наклонить голову вперед и |
ственный препарат |
закончился |
||
вставить наконечник в носовой ход. |
(рис. 4). |
|
||

|
|
|
Вепрена |
153 |
|
|
|
|
(≥1/10000, <1/1000), включая отде, |
||
|
|
|
льные сообщения. |
|
|
|
|
|
Со стороны иммунной системы: ред, |
||
|
|
|
ко — гиперчувствительность; очень |
||
|
|
|
редко — анафилактические или ана, |
||
|
|
|
филактоидные реакции, анафилакти, |
||
|
|
|
ческий шок. |
|
|
Рисунок 4. Проверка количества доз. |
Со стороны ЦНС: часто — головная |
||||
боль, головокружение, . |
|
||||
На дне флакона можно заметить |
Со стороны органов чувств: часто — |
||||
очень незначительный остаток рас, |
вкусовые нарушения; иногда — зри, |
||||
твора; он не подлежит использова, |
тельные нарушения. |
|
|||
нию, это предусмотрено. |
|
Со стороны ССС: часто — приливы |
|||
Дополнительные предупреждения |
|||||
крови к лицу; иногда — артериальная |
|||||
1. Никогда не следует пытаться уве, |
|||||
гипертензия. |
|
||||
личить отверстие распылителя с по, |
Со стороны дыхательной системы: |
||||
мощью иглы или других острых пред, |
очень часто — болезненность в носо, |
||||
метов. Это приведет к полному нару, |
вой полости, застойные явления, отек |
||||
шению работы устройства. |
|
слизистой носа, чихание, ринит, в т.ч. |
|||
2. Не разбирать насос. При возникно, |
|||||
аллергический, сухость в |
полости |
||||
вении каких,либо сомнений, в работе |
носа, эритема слизистой носа, раздра, |
||||
устройства, необходимо проконсуль, |
жение, неприятный запах, образова, |
||||
тироваться у специалиста в месте |
ние экскориаций в носовой полости; |
||||
приобретения препарата. |
|
часто — носовые кровотечения, сину, |
|||
3. Для обеспечения правильного от, |
сит, язвенный ринит, фарингит; ино, |
||||
меривания доз следует хранить и пе, |
гда — кашель. |
|
|||
реносить флакон в вертикальном по, |
Со стороны пищеварительной систе/ |
||||
ложении. |
|
|
мы: часто — тошнота, боль в животе, |
||
4. Не встряхивать флакон. |
|
диарея; иногда — рвота. |
|
||
5. Избегать резких перепадов темпе, |
Со стороны кожных покровов: ред, |
||||
ратуры. |
|
|
ко — генерализованная сыпь. |
|
|
6. Открытый флакон должен храни, |
Со стороны опорно/двигательного ап/ |
||||
ться при комнатной температуре. Он |
парата: часто — артралгии; иногда — |
||||
годен для применения максимум в те, |
боль в костях и мышцах. |
|
|||
чение 4 нед. |
|
|
Со стороны мочевыделительной сис/ |
||
ПОБОЧНЫЕ ДЕЙСТВИЯ. Сообща, |
темы: редко — полиурия. |
|
|||
лось о таких нежелательных эффектах |
Общие расстройства и нарушения в |
||||
как тошнота, рвота, головокружение, |
месте введения: часто — повышенная |
||||
незначительные |
приливы крови к |
утомляемость; иногда — гриппопо, |
|||
лицу, артралгии. Возможно развитие |
добный синдром, отеки лица, перифе, |
||||
полиурии и озноба, которые обычно |
рические и генерализованные отеки, |
||||
исчезают самостоятельно и лишь в от, |
редко — озноб; реакции в месте введе, |
||||
дельных случаях требуют временного |
ния препарата (зуд). Если любые из |
||||
снижения дозы препарата. |
|
указанных в инструкции побочных |
|||
Частота развития нежелательных яв, |
эффектов усугубляются или пациент |
||||
лений, возможно связанных с приме, |
заметил любые другие побочные эф, |
||||
нением препарата, оценивается сле, |
фекты, не указанные в инструкции, |
||||
дующим образом: очень |
часто |
следует сообщить об этом врачу. |
|||
(≥1/10); часто (≥1/100, <1/10); ино, |
ВЗАИМОДЕЙСТВИЕ. При одновре, |
||||
гда (≥1/1000, |
<1/100); |
редко |
менном назначении кальцитонина и |
||

154 |
Виктоза® |
|
|
|
Глава 2 |
|||
препаратов лития может возникнуть |
ном влиянии Вепрены на способ, |
|||||||
необходимость в коррекции дозы по, |
ность водить автомобиль и управлять |
|||||||
следнего, т.к. возможно |
|
снижение |
механизмами отсутствуют. Тем не |
|||||
плазменной концентрации лития. |
менее, учитывая, что применение |
|||||||
ПЕРЕДОЗИРОВКА. Симптомы: в |
препарата может привести к разви, |
|||||||
отдельных случаях — тошнота, рвота, |
тию таких побочных эффектов как |
|||||||
приливы крови к лицу, головокруже, |
головокружение, повышенная утом, |
|||||||
ляемость и зрительные нарушения, |
||||||||
ние. Возможно развитие гипокальци, |
||||||||
емии с такими симптомами как паре, |
рекомендуется соблюдать осторож, |
|||||||
стезии, подергивание мышц. |
|
ность при вождении автомобиля или |
||||||
|
работе с механизмами. |
|||||||
Лечение: симптоматическое, при раз, |
||||||||
витии гипокальциемии — введение |
ФОРМА ВЫПУСКА. Спрей назаль, |
|||||||
кальция глюконата. |
|
|
|
ный дозированный, 200 МЕ/доза. |
||||
Имеются сообщения о применении |
По 2 мл (14 доз) препарата во флако, |
|||||||
кальцитонина в дозе до 1600 МЕ од, |
нах из бесцветного стекла с навинчи, |
|||||||
нократно и в дозе 800 МЕ/сут в тече, |
вающимся распыляющим дозирую, |
|||||||
ние 3 дней, при этом не было отмече, |
щим устройством. По 1 или 2 флако, |
|||||||
но никаких |
серьезных нежелатель, |
на в картонной пачке. |
||||||
ных явлений. |
|
|
|
|
|
УСЛОВИЯ ОТПУСКА ИЗ АПТЕК. |
||
ОСОБЫЕ УКАЗАНИЯ. Кальцито, |
По рецепту. |
|||||||
нин лосося — пептид, поэтому сущест, |
ВИКТОЗА® (VICTOZA®) |
|||||||
вует вероятность возникновения сис, |
|
|||||||
темных аллергических реакций. Име, |
Лираглутид* . . . . . . . . . . . . . . . . . . 361 |
|||||||
ются сообщения об аллергических ре, |
Novo Nordisk (Дания) |
|||||||
акциях, |
включая |
отдельные |
случаи |
|||||
анафилактического шока, |
которые |
|
||||||
имели место у больных, получавших |
|
|||||||
кальцитонин |
в |
форме |
назального |
|
||||
спрея. |
|
|
|
|
|
|
|
|
При подозрении |
на повышенную |
|
||||||
чувствительность больного к кальци, |
|
|||||||
тонину лосося до начала лечения пре, |
|
|||||||
паратом следует обратиться к врачу. |
|
|||||||
При длительной терапии возможно |
|
|||||||
образование антител к кальцитонину, |
|
|||||||
однако на клиническую эффектив, |
|
|||||||
ность это, как правило, не влияет. |
|
|||||||
У пациентов с болезнью Педжета, по, |
|
|||||||
лучающих длительную терапию, фе, |
|
|||||||
номен привыкания может быть след, |
|
|||||||
ствием насыщения мест связывания |
|
|||||||
и очевидно не имеет отношения к об, |
|
|||||||
разованию антител. Терапевтический |
|
|||||||
эффект препарата восстанавливается |
|
|||||||
после перерыва в лечении. |
|
|
|
|||||
Влияние |
на |
способность |
|
управлять |
ЛЕКАРСТВЕННАЯ ФОРМА И |
|||
автомобилем или выполнять работы, |
||||||||
требующие |
повышенной |
|
скорости |
СОСТАВ |
||||
физических и психических реакций. В |
Раствор для подкожного |
|||||||
настоящее время данные о возмож, |
введения. . . . . . . . . . . . . . . . . . 1 мл |
|||||||

|
|
|
|
|
|
|
|
Виктоза® |
155 |
||||
активное вещество: |
|
|
действия со специфическими рецеп, |
||||||||||
лираглутид. . . . . . . . . . . . . . . . . . 6 мг |
торами ГПП,1, в результате чего по, |
||||||||||||
(1 шприц,ручка (3 мл) содержит |
вышается уровень цАМФ. |
|
|
||||||||||
лираглутида 18 мг) |
|
|
Под действием лираглутида происхо, |
||||||||||
вспомогательные вещества: на, |
дит |
глюкозозависимая |
стимуляция |
||||||||||
трия гидрофосфата дигидрат — |
секреции |
инсулина |
и |
улучшение |
|||||||||
1,42 мг; пропиленгликоль — 14 |
функции |
бета,клеток |
|
поджелудоч, |
|||||||||
мг; фенол — 5,5 мг; кислота хло, |
ной железы. Одновременно лираглу, |
||||||||||||
ристоводородная/натрия |
гидро, |
тид |
подавляет |
излишне |
высокую |
||||||||
ксид — q.s. до достижения необ, |
глюкозозависимую секрецию глюка, |
||||||||||||
ходимого значения pH; вода для |
гона. Таким образом, при повышении |
||||||||||||
инъекций — до 1 мл |
|
|
концентрации глюкозы крови проис, |
||||||||||
ОПИСАНИЕ |
ЛЕКАРСТВЕННОЙ |
ходит стимуляция секреции инсули, |
|||||||||||
ФОРМЫ. Бесцветный или почти бес, |
на и подавление секреции глюкагона. |
||||||||||||
цветный прозрачный раствор. |
С другой стороны, во время гипогли, |
||||||||||||
кемии лираглутид снижает секрецию |
|||||||||||||
ФАРМАКОДИНАМИКА. |
Меха/ |
||||||||||||
инсулина, но не подавляет секрецию |
|||||||||||||
низм действия |
|
|
|
глюкагона. |
Механизм |
|
снижения |
||||||
Лираглутид представляет собой ана, |
|
||||||||||||
уровня гликемии включает также не, |
|||||||||||||
лог человеческого глюкагоноподобно, |
большую задержку опорожнения же, |
||||||||||||
го пептида,1 (ГПП,1), произведенный |
лудка. Лираглутид снижает |
массу |
|||||||||||
методом биотехнологии рекомбинант, |
тела и уменьшает жировую ткань при |
||||||||||||
ной ДНК с использованием штамма |
помощи |
механизмов, |
вызывающих |
||||||||||
Saccharomyces cerevisiae, имеющий 97% |
уменьшение чувства голода и сниже, |
||||||||||||
гомологичности |
с |
человеческим |
ние расхода энергии. |
|
|
|
|
||||||
ГПП,1,которыйсвязываетсяиактиви, |
Исследования |
на эксперименталь, |
|||||||||||
рует рецепторы ГПП,1 у человека. Ре, |
|||||||||||||
цептор ГПП,1 служит мишенью для |
ных животных моделях с предиабе, |
||||||||||||
нативного ГПП,1 — эндогенного гор, |
том показали, что лираглутид замед, |
||||||||||||
ляет |
развитие |
сахарного |
диабета. |
||||||||||
мона инкретина, вызывающего стиму, |
|||||||||||||
ляцию глюкозозависимой |
секреции |
Диагностика in vitro показала, что ли, |
|||||||||||
инсулина в бета,клетках поджелудоч, |
раглутид является мощным факто, |
||||||||||||
ной железы. В отличие от нативного |
ром специфической стимуляции про, |
||||||||||||
ГПП,1, фармакокинетический и фар, |
лиферации бета,клеток поджелудоч, |
||||||||||||
макодинамический профили лираглу, |
ной железы и предупреждает образо, |
||||||||||||
тида позволяют вводить его пациентам |
вание цитокинов и свободных жир, |
||||||||||||
ежедневно 1 раз в сутки. |
|
|
ных кислот, индуцирующих гибель |
||||||||||
|
|
бета,клеток (апоптоз). In vivo лираг, |
|||||||||||
Профиль длительного действия ли, |
|||||||||||||
раглутида при п/к инъекции обеспе, |
лутид повышает биосинтез инсулина |
||||||||||||
и увеличивает массу бета,клеток на |
|||||||||||||
чивается тремя механизмами: само, |
|||||||||||||
ассоциацией, в |
результате |
которой |
модели диабета у эксперименталь, |
||||||||||
происходит замедленное всасывание |
ных животных. Когда уровень глюко, |
||||||||||||
препарата; связыванием с альбуми, |
зы нормализуется, лираглутид пере, |
||||||||||||
ном и более высоким уровнем фер, |
стает наращивать массу бета,клеток |
||||||||||||
ментативной стабильности по отно, |
поджелудочной железы. |
|
|
|
|||||||||
шению к дипептидилпептидазе,4 |
Лираглутид |
обладает |
|
длительным |
|||||||||
(ДПП,4) и ферменту |
нейтральной |
24,часовым |
действием |
и |
улучшает |
||||||||
эндопептидазе (НЭП), за счет чего |
гликемический контроль путем сни, |
||||||||||||
обеспечивается длительный T1/2 пре, |
жения концентрации глюкозы крови |
||||||||||||
парата из плазмы. Действие лираглу, |
натощак и после еды у пациентов с са, |
||||||||||||
тида осуществляется за счет взаимо, |
харным диабетом типа 2. |
|
|
||||||||||

156 |
Виктоза® |
|
|
|
|
|
|
|
|
|
|
Глава 2 |
||
Глюкозозависимая секреция инсулина. |
да наблюдается более низкая выра, |
|||||||||||||
При возрастании концентрации глю, |
ботка эндогенной глюкозы. |
|
|
|||||||||||
козы в крови лираглутид увеличивает |
Опорожнение |
|
желудка. Лираглутид |
|||||||||||
секрецию инсулина. При применении |
вызывает небольшую задержку в опо, |
|||||||||||||
поэтапной инфузии глюкозы секре, |
рожнении желудка, снижая таким об, |
|||||||||||||
ция инсулина после введения одно, |
разом |
интенсивность |
поступления |
|||||||||||
кратной дозы лираглутида пациентам |
постпрандиальной глюкозы в кровь. |
|||||||||||||
с сахарным диабетом типа 2 возраста, |
Масса тела, состав тела и расход |
|||||||||||||
ет до уровня, сопоставимого с тако, |
энергии. У субъектов с повышенной |
|||||||||||||
вым у здоровых субъектов (рис. 1). |
массой тела, включенных в долго, |
|||||||||||||
|
|
|
|
|
|
срочные клинические исследования |
||||||||
|
|
|
|
|
|
лираглутида, |
|
последний |
вызывает |
|||||
|
|
|
|
|
|
значительное снижение веса. Скани, |
||||||||
|
|
|
|
|
|
рование при помощи методов компь, |
||||||||
|
|
|
|
|
|
ютерной томографии (КТ) и двух, |
||||||||
|
|
|
|
|
|
энергетической рентгеновской абсор, |
||||||||
|
|
|
|
|
|
бциометрии |
(ДЭРА) |
показало, что |
||||||
|
|
|
|
|
|
потеря веса произошла в первую оче, |
||||||||
Рисунок 1. |
|
|
|
редь из,за потери жировой клетчатки |
||||||||||
|
|
|
пациентов. Эти результаты объясня, |
|||||||||||
Функция |
бета/клеток |
поджелудоч/ |
ются тем, что во время терапии лираг, |
|||||||||||
ной |
железы. Лираглутид улучшает |
лутидом |
у |
пациентов |
снижаются |
|||||||||
функцию |
бета,клеток |
поджелудоч, |
ощущение голода и расход энергии. |
|||||||||||
ной железы, что подтверждается пер, |
Электрофизиология |
сердца |
(ЭФс). |
|||||||||||
вой и второй фазой инсулинового от, |
Действие лираглутида на процесс ре, |
|||||||||||||
вета и максимальной секреторной ак, |
поляризации в сердце было протести, |
|||||||||||||
тивностью бета,клеток. Фармакоди, |
ровано в исследовании ЭФс. Приме, |
|||||||||||||
намические исследования пациентов |
нение |
лираглутида |
в |
равновесной |
||||||||||
с сахарным диабетом типа 2 показали |
концентрации в ежедневной дозе до |
|||||||||||||
восстановление первой фазы секре, |
1,8 мг не вызывает пролонгацию пе, |
|||||||||||||
ции инсулина (в/в введение инсули, |
риода |
реполяризации |
по |
|
данным |
|||||||||
на), улучшение второй фазы секре, |
ЭФс. |
|
|
|
|
|
|
|
|
|||||
ции инсулина (гипергликемический |
Клиническая |
|
эффективность. 3992 |
|||||||||||
клэмп,тест) и максимальную секре, |
пациента с диабетом типа 2 были ран, |
|||||||||||||
торную активность |
инсулина (тест |
домизированы в 5 двойных слепых |
||||||||||||
стимуляции аргинином). В ходе |
клинических исследованиях по безо, |
|||||||||||||
52,недельной |
терапии |
препаратом |
пасности и эффективности, осущест, |
|||||||||||
Виктоза® |
произошло |
улучшение |
вленных в целях оценки влияния |
|||||||||||
функции |
бета,клеток |
поджелудоч, |
препарата |
Виктоза® |
на гликемиче, |
|||||||||
ной |
железы, |
что |
подтверждается |
ский контроль. Терапия препаратом |
||||||||||
оценкой |
гомеостатической модели |
Виктоза® вызывает клинически и ста, |
||||||||||||
функции |
бета,клеток |
поджелудоч, |
тистически значимое улучшение по, |
|||||||||||
ной железы (НОМА,индекс) и соот, |
казателя HbA1с, глюкозы натощак и |
|||||||||||||
ношением инсулина к проинсулину. |
постпрандиальной глюкозы по срав, |
|||||||||||||
Секреция |
глюкагона. |
Лираглутид, |
нению с плацебо. |
|
|
Препарат |
||||||||
стимулируя секрецию инсулина и по, |
Гликемический |
контроль. |
||||||||||||
давляя секрецию глюкагона, умень, |
Виктоза® в виде монотерапии в тече, |
|||||||||||||
шает уровень глюкозы в крови. Ли, |
ние 52 недель вызывает статистически |
|||||||||||||
раглутид не подавляет глюкагоновый |
значимое (p<0,0014) и продолжитель, |
|||||||||||||
ответ на низкую концентрацию глю, |
ное снижение показателя HbA1с по |
|||||||||||||
козы. Кроме того, на фоне лираглути, |
сравнению с этим же показателем у па, |
|||||||||||||

|
|
|
|
|
|
|
|
|
|
Виктоза® |
157 |
|||||
циентов, получающих терапию глиме, |
чение |
52,недельного |
исследования |
|||||||||||||
пиридом. При этом отмеченное сниже, |
число пациентов, достигших уровня |
|||||||||||||||
ниеHbA1с нижеуровня7%сохраняется |
НbА1с <7%, статистически значимо |
|||||||||||||||
на протяжении 12 мес (рис. 2). |
|
выросло (р≤0,0007) по сравнению с |
||||||||||||||
|
|
|
|
|
|
числом пациентов, получающих гли, |
||||||||||
|
|
|
|
|
|
мепирид. На 26,й неделе применения |
||||||||||
|
|
|
|
|
|
препарата Виктоза® |
в |
сочетании с |
||||||||
|
|
|
|
|
|
метформином, препаратами произ, |
||||||||||
|
|
|
|
|
|
водных |
|
сульфонилмочевины |
или |
|||||||
|
|
|
|
|
|
комбинацией метформина с тиазоли, |
||||||||||
|
|
|
|
|
|
диндионами число пациентов, |
|
до, |
||||||||
|
|
|
|
|
|
стигших уровня НbА1с |
≤6,5%, стати, |
|||||||||
|
|
|
|
|
|
стически значимо (р≤0,0001) вырос, |
||||||||||
Рисунок 2. |
|
|
|
|
ло по отношению к числу пациентов, |
|||||||||||
|
|
|
|
которые получали терапию одними, |
||||||||||||
У пациентов с HbA1с выше уровня |
||||||||||||||||
|
|
|
|
|
|
|
|
|
® |
|||||||
без добавления препарата Виктоза , |
||||||||||||||||
9,5% в исходной точке исследования |
||||||||||||||||
гипогликемическими препаратами. |
|
|||||||||||||||
данный показатель снизился на 2,1% |
В группах пациентов, не достигших |
|||||||||||||||
на фоне |
монотерапии препаратом |
|||||||||||||||
® |
, в то время как у пациентов, |
адекватного гликемического контро, |
||||||||||||||
Виктоза |
ля терапией препаратом Виктоза |
® |
и |
|||||||||||||
участвующих |
в |
комбинированных |
|
|||||||||||||
клинических |
исследованиях |
препа, |
метформином, процентное соотно, |
|||||||||||||
шение пациентов, достигших целево, |
||||||||||||||||
|
|
® |
, средний уровень |
|||||||||||||
рата Виктоза |
го уровня HbA1с |
(<7 и |
≤6,5%) было |
|||||||||||||
HbA1с снизился на 1,1–2,5%. |
|
значительно выше при терапии инсу, |
||||||||||||||
Препарат Виктоза® в течение 26,не, |
||||||||||||||||
дельной комбинированной терапии с |
лин детемир + лираглутид 1,8 мг + |
|||||||||||||||
метформином, препаратами сульфо, |
метформин, по сравнению с терапией |
|||||||||||||||
лираглутид |
1,8 |
мг |
+ |
метформин |
||||||||||||
нилмочевины |
или метформином и |
|||||||||||||||
тиазолидиндионом вызывает стати, |
(р≤0,0001/р=0,0016). |
|
|
|
|
|
||||||||||
стически значимое (р<0,0001) и про, |
В ходе 26,недельного исследования |
|||||||||||||||
должительное |
|
|
снижение |
уровня |
комбинированного применения пре, |
|||||||||||
НbА1с по сравнению с таковым у па, |
парата |
Виктоза® |
удалось достичь |
|||||||||||||
циентов, получающих плацебо. У па, |
уровня НЬА1с <7,0% у большего числа |
|||||||||||||||
циентов, не достигших адекватного |
пациентов, |
получавших препарат |
в |
|||||||||||||
гликемического контроля на терапии |
виде комбинированной терапии, по |
|||||||||||||||
препаратом Виктоза® и метформи, |
сравнению с числом пациентов, полу, |
|||||||||||||||
ном, добавление инсулина детемир |
чавших его в виде заместительной те, |
|||||||||||||||
обеспечило б ольшую эффективность рапии. |
|
|
|
|
|
|
|
|
|
|||||||
по сравнению с терапией препаратом |
Уровень гликемии натощак. Уровень |
|||||||||||||||
Виктоза® |
и метформином после 26 |
глюкозы |
|
натощак |
снизился |
|
на |
|||||||||
недель лечения |
(снижение |
уровня |
13–43,5 мг% (0,72–2,42 ммоль/л) на |
|||||||||||||
HbA1с на 0,52%). Было доказано, что |
фоне приема препарата Виктоза® как |
|||||||||||||||
эффективность препарата Виктоза® в |
в виде монотерапии, так и в комбина, |
|||||||||||||||
дозе 0,6 мг в комбинации с препарата, |
ции с одним или двумя пероральны, |
|||||||||||||||
ми сульфонилмочевины или метфор, |
ми гипогликемическими средствами. |
|||||||||||||||
мином превосходит плацебо, но в то |
Это снижение наблюдалось уже в те, |
|||||||||||||||
же время является более низкой, по |
чение первых двух недель от начала |
|||||||||||||||
сравнению с дозировками 1,2 и 1,8 мг. |
лечения. |
|
|
|
|
|
|
|
|
|||||||
Соотношение пациентов, достигших |
Постпрандиальный уровень гликемии. |
|||||||||||||||
снижения уровня HbA1с. На фоне мо, |
Применение препарата Виктоза® в те, |
|||||||||||||||
нотерапии препаратом Виктоза® в те, |
чение 3 |
дней приема |
стандартной |
|||||||||||||

158 |
|
Виктоза® |
|
|
|
|
|
|
|
|
Глава 2 |
|||
пищи |
помогло |
снизить концентра, |
на (ингибитор ДПП,4, в дозе 100 мг) у |
|||||||||||
цию постпрандиальной глюкозы на |
пациентов, не достигших адекватного |
|||||||||||||
31–49 мг% (1,68–2,71 ммоль/л). |
контроля на терапии метформином, |
|||||||||||||
Масса тела. 52,недельная монотера, |
после 26 недель лечения доказано |
|||||||||||||
пия препаратом Виктоза® ассоцииро, |
лучшее снижение |
|
уровня |
HbA |
на |
|||||||||
валась с устойчивым снижением мас, |
препарате Виктоза® |
|
|
1с |
|
|||||||||
в обеих дозах по |
||||||||||||||
сы тела. На протяжении всего перио, |
сравнению с ситаглиптином (,1,24, |
|||||||||||||
да |
клинического |
|
исследования |
,1,5% по сравнению с ,0,9%, р<0,0001). |
||||||||||
устойчивое снижение массы тела на |
Значительно большее число пациен, |
|||||||||||||
1–2,8 кг также ассоциировалось с ис, |
тов достигает уровня НbА |
ниже 7% |
||||||||||||
пользованием препарата Виктоза® в |
|
|
|
|
|
1с |
|
|
||||||
на препарате Виктоза® по сравнению с |
||||||||||||||
комбинации с метформином и в соче, |
ситаглиптином (43,7 и 56% по сравне, |
|||||||||||||
тании с комбинациями метформина с |
нию с 22%, р<0,0001). Снижение веса |
|||||||||||||
производными сульфонилмочевины |
у пациентов, получающих препарат |
|||||||||||||
или метформина с тиазолиндионом. |
Виктоза®, было значительно больше, |
|||||||||||||
Снижение массы тела у пациентов, |
по сравнению с пациентами, получаю, |
|||||||||||||
получающих препарат Виктоза® в |
щими ситаглиптин (,2,9 и |
,3,4 кг в |
||||||||||||
комбинации с метформином, также |
сравнении с ,1 кг, р<0,0001). |
|
|
|||||||||||
наблюдалось после добавления инсу, |
По сравнению с пациентами, получа, |
|||||||||||||
лина детемир. |
|
|
|
ющими ситаглиптин, пациенты |
на |
|||||||||
Наибольшее снижение массы тела |
||||||||||||||
препарате Виктоза |
® |
чаще жаловались |
||||||||||||
наблюдалось у пациентов, имевших в |
|
|||||||||||||
исходной точке исследования повы, |
на присутствие побочного эффекта |
|||||||||||||
(тошнота). Однако |
тошнота была |
|||||||||||||
шенный индекс массы тела (ИМТ). |
преходящей. Частота случаев легкой |
|||||||||||||
Монотерапия препаратом Виктоза® в |
||||||||||||||
течение 52 недель вызвала уменьше, |
гипогликемии незначительно отли, |
|||||||||||||
ниесреднегообъематалиина3–3,6см. |
чалась при лечении препаратом Вик, |
|||||||||||||
тоза |
® |
и ситаглиптином (0,178 и 0,161 |
||||||||||||
Снижение массы тела наблюдалось у |
|
|||||||||||||
всех пациентов, получавших терапию |
в сравнении с 0,106 случая/пациента |
|||||||||||||
препаратом Виктоза |
, независимо от |
в год). Снижение уровня НbА1с и пре, |
||||||||||||
имущество препарата Виктоза® |
по |
|||||||||||||
|
|
|
® |
|
|
|
|
|
|
|
|
|
|
|
того, испытывали они или нет побоч, |
сравнению с ситаглиптином наблю, |
|||||||||||||
ную реакцию в виде тошноты. |
далось после 26,й |
|
®недели |
лечения |
||||||||||
Препарат Виктоза® в составе комби, |
|
|||||||||||||
нированной терапии с метформином |
препаратом Виктоза |
(1,2 и 1,8 мг) и |
||||||||||||
снизил |
объем |
подкожно,жировой |
подтверждалась после 52,й недели |
|||||||||||
лечения (,1,29 и ,1,51% в сравнении с |
||||||||||||||
клетчатки на 13–17%. |
|
,0,88%, р<0,0001). Через 52 недель |
||||||||||||
Неалкогольный жировой стеатоз пе/ |
||||||||||||||
чени. Лираглутид сокращает стеатоз |
применения ситаглиптина пациенты |
|||||||||||||
печени у пациентов с сахарным диа, |
были переведены на препарат Викто, |
|||||||||||||
бетом типа 2. |
|
|
|
за®, что привело к дополнительному и |
||||||||||
Показатели АД. Долгосрочные кли, |
статистически значимому снижению |
|||||||||||||
нические исследования показали, что |
уровня НbА1с на 78,й неделе лечения |
|||||||||||||
препарат Виктоза® снижает показате, |
(0,24 и 0,45%, 95 С1: от 0,41 до 0,07 и |
|||||||||||||
ли сАД в среднем на 2,3–6,7 мм рт.ст. |
от ,0,67 до 0,23). |
|
|
|
|
|
||||||||
в первые 2 недели лечения. Сниже, |
В сравнительном исследовании эф, |
|||||||||||||
ние сАД наступило до начала умень, |
фективности и безопасности препа, |
|||||||||||||
шения массы тела. |
|
|
рата Виктоза® (в дозе 1,8 мг) и эксена, |
|||||||||||
Другие клинические данные. В сравни, |
тида (в дозе 10 мкг 2 раза в день) у па, |
|||||||||||||
тельном |
исследовании |
эффективно, |
циентов, не достигших адекватного |
|||||||||||
сти и безопасности препарата Викто, |
контроля на терапии метформином |
|||||||||||||
за® (в дозах 1,2 и 1,8 мг) и ситаглипти, |
и/или производными сульфонилмо, |
|||||||||||||

|
|
|
|
|
|
Виктоза® |
|
159 |
||
чевины, после 26 недель лечения пре, |
дозе. После введения лираглутида в |
|||||||||
парат Виктоза® показал лучшее сни, |
однократной |
дозе |
внутрипопуляци, |
|||||||
жение уровня HbA1с по сравнению с |
онный |
коэффициент вариации для |
||||||||
эксенатидом (,1,12% в сравнении с |
AUC |
составляет |
11%. |
Абсолютная |
||||||
,0,79%, р<0,0001). |
|
биодоступность |
лираглутида |
|
после |
|||||
Значительно большее количество па, |
п/к введения составляет приблизите, |
|||||||||
циентов достигает уровня НbА ниже |
льно 55%. |
|
|
|
|
|
|
|
||
|
1с |
Распределение. Vss лираглутида в тка, |
||||||||
7% на терапии препаратом Виктоза® |
||||||||||
по сравнению с эксенатидом (54,2% по |
нях после п/к введения — 11–17 л. |
|||||||||
сравнению с 43,4%, р=0,0015). Обе те, |
Средний Vd |
лираглутида после в/в |
||||||||
рапии показали среднюю потерю мас, |
введения — 0,07 л/кг. Лираглутид в |
|||||||||
сы тела приблизительно 3 кг. Количе, |
значительной степени связывается с |
|||||||||
ство пациентов, сообщавших о побоч, |
белками плазмы крови (>98%). |
|
||||||||
ном явлении (тошнота), было ниже в |
Метаболизм. На протяжении 24 ч по, |
|||||||||
группе пациентов, получающих пре, |
сле введения здоровым |
доброволь, |
||||||||
парат Виктоза®, по сравнению с эксе, |
цам однократной дозы меченного ра, |
|||||||||
натидом. Частота случаев легкой ги, |
диоактивным изотопом (3H),лираг, |
|||||||||
погликемии была значительно ниже в |
лутида главным компонентом плаз, |
|||||||||
группе пациентов, получающих пре, |
мы оставался неизмененный лираг, |
|||||||||
парат Виктоза®, по сравнению с эксе, |
лутид. Были обнаружены два метабо, |
|||||||||
натидом (1932 в сравнении с 2600 слу, |
лита в плазме (≤9 и |
≤5% от уровня об, |
||||||||
чая/пациента в год, р=0,01). Через 26 |
щей радиоактивности в плазме кро, |
|||||||||
недель применения эксенатида паци, |
ви). Лираглутид |
метаболизируется |
||||||||
енты были переведены на препарат |
подобно крупным белкам, без учас, |
|||||||||
Виктоза®, что привело к дополнитель, |
тия какого,либо специфического ор, |
|||||||||
ному снижению уровня HbA1с |
на 40,й |
гана в качестве пути выведения. |
||||||||
неделе лечения (,0,32%, р<0,0001), |
Выведение. |
|
После |
введения |
дозы |
|||||
13% пациентов удалось достичь уров, |
(3H),лираглутида неизмененный ли, |
|||||||||
ня HbA1с ниже 7%. |
|
раглутид не определялся в моче или |
||||||||
Терапия препаратом Виктоза® в тече, |
кале. |
Лишь |
незначительная |
|
часть |
|||||
ние 52 недель улучшила инсулино, |
введенной |
радиоактивности |
в |
виде |
||||||
чувствительность по сравнению с та, |
связанных с лираглутидом метаболи, |
|||||||||
ковой у препаратов сульфонилмоче, |
тов (6 и 5% соответственно) выводи, |
|||||||||
вины, что было выявлено при помо, |
лась почками или через кишечник. |
|||||||||
щи гомеостатической модели оценки |
Радиоактивные |
вещества почками |
||||||||
инсулинорезистентности HOMA,IR. |
или через кишечник выводятся в |
|||||||||
ФАРМАКОКИНЕТИКА. |
Абсорб/ |
основном, в течение первых 6–8 дней |
||||||||
ция. Всасывание лираглутида после |
после введения дозы препарата и |
|||||||||
п/к введения происходит медленно, |
представляют собой три метаболита. |
|||||||||
Tmax в плазме — 8–12 ч после введения |
Средний клиренс из организма после |
|||||||||
дозы препарата. Cmax лираглутида в |
п/к введения лираглутида в одно, |
|||||||||
плазме после п/к инъекции в одно, |
кратной дозе составляет приблизите, |
|||||||||
кратной дозе 0,6 мг составляет 9,4 |
льно 1,2 л/ч с элиминационным T1/2 — |
|||||||||
нмоль/л. При введении лираглутида в |
примерно 13 ч. |
|
|
|
|
|
||||
дозе 1,8 мг средний показатель его |
Особые группы пациентов |
|
|
|||||||
равновесной концентрации в плазме |
Пожилой возраст: данные фармако, |
|||||||||
(AUCt/24) достигает приблизительно |
кинетических исследований в группе |
|||||||||
34 нмоль/л. Экспозиция лираглутида |
здоровых |
добровольцев |
и |
анализ |
||||||
(процесс воздействия препарата) уси, |
фармакокинетических данных, полу, |
|||||||||
ливается пропорционально введенной |
ченных в популяции пациентов от 18 |
|||||||||
