
- •12.Характеристика простых и сложных белков. Характеристика классов сложных белков: нуклеопротеиды, липопротеиды, гликопротеиды, фосфопротеиды, хромопротеиды, металлопротеиды, флавопротеиды.
- •15. Методы выделения и очистки белков.
- •17. Скорость химических реакций и сущность явления катализа. Теоретические основы и особенности ферментативного катализа. Термодинамические и кинетические характеристики ферментативного катализа.
- •18.Классификация и номенклатура ферментов. Химическая природа ферментов, их функциональные группы. Активный и аллостерический центры.
- •19. Коферменты, простетические группы. Роль витаминов, металлов и других кофакторов в функционировании ферментов.
- •22. Влияние ингибиторов на ферментативную активность. Множественные формы ферментов. Изоферменты.
- •23. Общие представления о механизме ферментативного катализа. Количественная характеристика ферментативных реакций.
- •24. Принципы регуляции ферментативных процессов в клетке и регуляция метаболизма. Регуляция ферментативных процессов количеством субстрата и фермента. Локализация ферментов в клетке.
- •25. Роль нуклеиновых кислот в формировании и свойствах живой материи. Основной постулат молекулярной биологии. Строение нуклеиновых кислот. Пуриновые и пиримидиновые основания. Углеводные компоненты.
- •26. Нуклеозиды и нуклеотиды. Нуклеотидный состав днк. Правила Чаргаффа. Нуклеозиды, нуклеотиды
- •27. Первичная, вторичная и третичная структура днк. Функциональная организация
- •28. Общая характеристика рнк. Виды рнк. Особенности структуры, синтеза и функции м-рнк, т-рнк и р-рнк..
- •30. Регуляция синтеза белка у прокариот Мутации, их виды и последствия.
- •31.Ферментативный гидролиз белков. Протеолитические ферменты, их специфичность, активация.
- •32. Общая схема источников и расходования аминокислот в организме. Незаменимые аминокислоты. Общие пути катаболизма аминокислот.
- •34. Образование аммиака. Транспорт аммиака. Восстановительное аминирование. Амиды и их физиологическое значение.
- •35. Особенности обмена отдельных аминокислот и их роль в образовании важнейших биологически активных веществ.
- •36. Биосинтез мочевины. Орнитиновый цикл мочевинообразования.
- •37. Азотистые небелковые вещества (биогенные амины), их синтез, распад и биологическая роль. Нарушения структуры и обмена белков. Наследственные заболевания.
- •38. Алкалоиды, их роль у растений и значение в медицине
- •39. Углеводы и их биологическая роль, классификация и номенклатура.
- •40. Структура, свойства и распространение в природе основных представителей моносахаридов и полисахаридов. Гликопротеины и гликолипиды. Взаимопревращения моносахаридов.
- •4 1. Анаэробный и аэробный распад углеводов. Энергетическая характеристика аэробной и анаэробной фазы углеводного обмена.
- •42. Гликолиз. Спиртовое брожение.
- •43 Биосинтез полисахаридов. Гликозил-трансферазные реакции. Гликогенез
- •44. Окислительное декарбоксилирование пировиноградной кислоты. Пируватдегидрогеназный комплекс.
- •45. Цикл трикарбоновых кислот. Окислительное фосфорилирование на уровне субстрата. Прямое окисление глюкозо-6-фосфата.
- •47.Макроэргические соединения. Нуклеозидфосфаты, атф, креатинфосфат и аргининфосфат. Пути образования атф и других макроэргических соединений.
- •48.Окислительное фосфорилирование. Окислительно-востановительные процессы.
- •49. Цепь переноса водорода и электронов (дыхательная цепь).
- •52. Окислительное фосфорилирование в дыхательной цепи. Представление о механизмах сопряжения окисления и фосфорилирования в дыхательной цепи.
- •55. Жирные кислоты, их классификация и номенклатура. Простагландины.
- •56.Ферментативный распад и синтез липидов. Окисление жирных кислот, биосинтез жирных кислот. Мультиферментные комплексы синтеза жирных кислот.
- •57. Кетоновые тела, структура, синтез, утилизация в тканях.
- •60.Хим природа и физиол роль важнейших гормонов, их роль в регуляции обмена в-в и синтеза белков.
- •62. Связь между обменом белков, углеводов и липидов. Обмен веществ как единая система процессов.
17. Скорость химических реакций и сущность явления катализа. Теоретические основы и особенности ферментативного катализа. Термодинамические и кинетические характеристики ферментативного катализа.
Скорость химической реакции, величина, характеризующая интенсивность реакции химической. Скоростью образования продукта реакции называется количество этого продукта, возникающее в результате реакции за единицу времени в единице объёма (если реакция гомогенна) или на единице площади поверхности (если реакция гетерогенна). Для исходных веществ аналогичным образом определяется скорость их расходования. Количества веществ выражают в молях. Катализ - изменение скорости химических реакций в присутствии веществ (катализаторов), вступающих в промежуточное химическое взаимодействие с реагирующими веществами, но восстанавливающих после каждого цикла промежуточных взаимодействий свой химический состав. Реакции с участием катализаторов называются каталитическими. Основным фактором, определяющим скорость химического превращения, является энергия активации (Е) — разность энергий активного комплекса и исходных реагирующих молекул. Если предположить, что реакция не нарушает равновесного распределения энергии между молекулами, то вероятность образования активного комплекса, а следовательно, и скорость реакции в первом приближении пропорциональна exp (—E/RT), где R — газовая постоянная, Т — абсолютная температура. Отсюда следует, что скорость реакции тем больше, чем меньше Е, и вследствие экспоненциальной зависимости возрастает значительно даже при небольшом снижении Е.
ФЕРМЕНТАТИВНЫЙ КАТАЛИЗ (биокатализ), ускорение биохим. р-ций при участии белковых макромолекул, называемых ферментами (энзимами). Ферментативный катализ- разновидность катализа, хотя термин "ферментация" (брожение)известен с давних времен, когда еще не было понятия хим. катализа. В простейшем случае ур-ние р-ции с участием фермента имеет вид: E+S-->ES-->E+P где E - фермент, S - субстрат, ES - фермент-субстратный комплекс (т. наз. комплекс Михаэлиса), P- продукт р-ции.
![]()
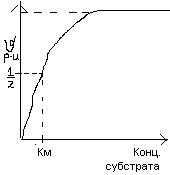 Км
– константа Михаэлиса.
Км
– константа Михаэлиса.
Общие свойства ферментов и химических катализаторов небелковой природы:
1) Ф. не входят в состав конечных продуктов реакции и не тратятся в процессе катализа, выходя из реакции в неизменном виде; 2) Ф. только ускоряют реакции протекающие и без них, не могут возбудить реакций, противоречащих законам термодинамики; 3) Ф. не смещают положение равновесия, а лишь ускоряют его достижение. Отличительные признаки ферментативного и химического катализа:
1) Скорость ферментативных реакций на много порядков выше, чем у небиологических катализаторов. 2) Ферменты обладают высокой специфичностью; 3) Ферментативные процессы не дают побочных реакций, для них характерен 100% выход целевого продукта. 4) Ферменты катализируют реакции в мягких условиях организма (р, t°, рН), однако весьма чувствительны к сдвигам рН среды и изменению температуры. 5) Белки-ферменты термолабильны и чувствительны к денатурирующим агентам; 5) Активность ферментов контролируется (генетически на уровне строения и различными биорегуляторами), они могут изменять свою активность под воздействием ряда факторов, изменяя количественные выходы продуктов. 6) В организме, как правило, действуют полиферментные системы.
