
- •12.Характеристика простых и сложных белков. Характеристика классов сложных белков: нуклеопротеиды, липопротеиды, гликопротеиды, фосфопротеиды, хромопротеиды, металлопротеиды, флавопротеиды.
- •15. Методы выделения и очистки белков.
- •17. Скорость химических реакций и сущность явления катализа. Теоретические основы и особенности ферментативного катализа. Термодинамические и кинетические характеристики ферментативного катализа.
- •18.Классификация и номенклатура ферментов. Химическая природа ферментов, их функциональные группы. Активный и аллостерический центры.
- •19. Коферменты, простетические группы. Роль витаминов, металлов и других кофакторов в функционировании ферментов.
- •22. Влияние ингибиторов на ферментативную активность. Множественные формы ферментов. Изоферменты.
- •23. Общие представления о механизме ферментативного катализа. Количественная характеристика ферментативных реакций.
- •24. Принципы регуляции ферментативных процессов в клетке и регуляция метаболизма. Регуляция ферментативных процессов количеством субстрата и фермента. Локализация ферментов в клетке.
- •25. Роль нуклеиновых кислот в формировании и свойствах живой материи. Основной постулат молекулярной биологии. Строение нуклеиновых кислот. Пуриновые и пиримидиновые основания. Углеводные компоненты.
- •26. Нуклеозиды и нуклеотиды. Нуклеотидный состав днк. Правила Чаргаффа. Нуклеозиды, нуклеотиды
- •27. Первичная, вторичная и третичная структура днк. Функциональная организация
- •28. Общая характеристика рнк. Виды рнк. Особенности структуры, синтеза и функции м-рнк, т-рнк и р-рнк..
- •30. Регуляция синтеза белка у прокариот Мутации, их виды и последствия.
- •31.Ферментативный гидролиз белков. Протеолитические ферменты, их специфичность, активация.
- •32. Общая схема источников и расходования аминокислот в организме. Незаменимые аминокислоты. Общие пути катаболизма аминокислот.
- •34. Образование аммиака. Транспорт аммиака. Восстановительное аминирование. Амиды и их физиологическое значение.
- •35. Особенности обмена отдельных аминокислот и их роль в образовании важнейших биологически активных веществ.
- •36. Биосинтез мочевины. Орнитиновый цикл мочевинообразования.
- •37. Азотистые небелковые вещества (биогенные амины), их синтез, распад и биологическая роль. Нарушения структуры и обмена белков. Наследственные заболевания.
- •38. Алкалоиды, их роль у растений и значение в медицине
- •39. Углеводы и их биологическая роль, классификация и номенклатура.
- •40. Структура, свойства и распространение в природе основных представителей моносахаридов и полисахаридов. Гликопротеины и гликолипиды. Взаимопревращения моносахаридов.
- •4 1. Анаэробный и аэробный распад углеводов. Энергетическая характеристика аэробной и анаэробной фазы углеводного обмена.
- •42. Гликолиз. Спиртовое брожение.
- •43 Биосинтез полисахаридов. Гликозил-трансферазные реакции. Гликогенез
- •44. Окислительное декарбоксилирование пировиноградной кислоты. Пируватдегидрогеназный комплекс.
- •45. Цикл трикарбоновых кислот. Окислительное фосфорилирование на уровне субстрата. Прямое окисление глюкозо-6-фосфата.
- •47.Макроэргические соединения. Нуклеозидфосфаты, атф, креатинфосфат и аргининфосфат. Пути образования атф и других макроэргических соединений.
- •48.Окислительное фосфорилирование. Окислительно-востановительные процессы.
- •49. Цепь переноса водорода и электронов (дыхательная цепь).
- •52. Окислительное фосфорилирование в дыхательной цепи. Представление о механизмах сопряжения окисления и фосфорилирования в дыхательной цепи.
- •55. Жирные кислоты, их классификация и номенклатура. Простагландины.
- •56.Ферментативный распад и синтез липидов. Окисление жирных кислот, биосинтез жирных кислот. Мультиферментные комплексы синтеза жирных кислот.
- •57. Кетоновые тела, структура, синтез, утилизация в тканях.
- •60.Хим природа и физиол роль важнейших гормонов, их роль в регуляции обмена в-в и синтеза белков.
- •62. Связь между обменом белков, углеводов и липидов. Обмен веществ как единая система процессов.
34. Образование аммиака. Транспорт аммиака. Восстановительное аминирование. Амиды и их физиологическое значение.
БИОГЕННЫЕ АМИНЫ Образуются при декарбоксилировании аминокислот. Биогенные амины (БА) являются непептидными азотсодержащими производными аминокислот. К ним относятся гормоны надпочечников (адреналин, норадреналин), щитовидной железы (тироксин, трийодтиронин), медиаторы ЦНС (ацетилхолин, ГАМК, дофамин), медиатор воспаления (гистамин), этаоламин, аминопропанол и др. Некоторые из этих соединений являются составными частями других биомолекул.
![]()
Амины, образовавшиеся при декарбоксилировании аминокислот, часто являются биоактивными веществами.
Серотонин – нейромедиатор проводящих путей. Образуется в надпочечниках и ЦНС.
-Аминомасляная кислота (ГАМК). В нервных клетках декарбоксилирование глутамата приводит к образованию ГАМК, которая служит основным тормозным медиатором высших отделов мозга.
Содержание ГАМК в головном мозге в десятки раз выше других нейромедиаторов. Она увеличивает проницаемость постсинаптических мембран для ионов , что вызывает торможение нервного импульса; повышает дыхательную активность нервной ткани; улучшает кровоснабжение головного мозга.
Аминомасляная кислота (ГАМК). В нервных клетках декарбоксилирование глутамата приводит к образованию ГАМК, которая служит основным тормозным медиатором высших отделов мозга.
Содержание ГАМК в головном мозге в десятки раз выше других нейромедиаторов. Она увеличивает проницаемость постсинаптических мембран для ионов , что вызывает торможение нервного импульса; повышает дыхательную активность нервной ткани; улучшает кровоснабжение головного мозга.
Гистамин выполняет в организме человека следующие функции: --стимулирует секрецию желудочного сока, слюны; --повышает проницаемость капилляров, вызывает отеки, снижает АД; --сокращает гладкую мускулатуру легких, вызывает удушье; --участвует в формировании воспалительной реакции – вызывает расширение сосудов, покраснение кожи, отечность ткани; – вызывает аллергическую реакцию; -выполняет роль нейромедиатора; -является медиатором боли.
Образующийся
в результате реакций дезаминирования
аммиак является токсичным для организма.
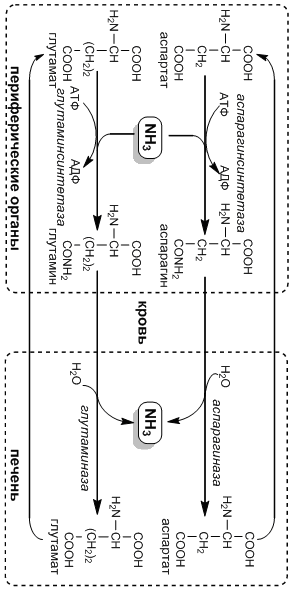 Его
дезактивация с образованием нетоксичных
мочевины и креатина происходит в печени,
куда он предварительно должен быть
транспортирован кровью. Трансортными
формами аммиака являются аспарагин и
глутамин, образующиеся амидированием
аспартата и глутамата. Реакции
катализируются аспарагин- и
глутаминсинтетазой. В печени аспарагиназа
и глутаминаза отщепляют амидную группу
в виде аммиака.
Его
дезактивация с образованием нетоксичных
мочевины и креатина происходит в печени,
куда он предварительно должен быть
транспортирован кровью. Трансортными
формами аммиака являются аспарагин и
глутамин, образующиеся амидированием
аспартата и глутамата. Реакции
катализируются аспарагин- и
глутаминсинтетазой. В печени аспарагиназа
и глутаминаза отщепляют амидную группу
в виде аммиака.
В печени аммиак карбоксилируется с образованием карбамоилфосфата, который вовлекается в орнитиновый цикл. На последнем этапе этого процесса образуется аргинин, который распадается на орнитин и мочевину, либо преобразуется в креатин. В мышцах креатин фосфорилируется и используется в качестве донора фосфатной группы при регенерировании АТФ из АДФ. Образовавшиеся креатинин и мочевина выводятся из организма.
реакция в обмене аминок-т рис13
Восстановительное аминирование - это превращение кетонов в соответствующие им амины.
