
- •12.Характеристика простых и сложных белков. Характеристика классов сложных белков: нуклеопротеиды, липопротеиды, гликопротеиды, фосфопротеиды, хромопротеиды, металлопротеиды, флавопротеиды.
- •15. Методы выделения и очистки белков.
- •17. Скорость химических реакций и сущность явления катализа. Теоретические основы и особенности ферментативного катализа. Термодинамические и кинетические характеристики ферментативного катализа.
- •18.Классификация и номенклатура ферментов. Химическая природа ферментов, их функциональные группы. Активный и аллостерический центры.
- •19. Коферменты, простетические группы. Роль витаминов, металлов и других кофакторов в функционировании ферментов.
- •22. Влияние ингибиторов на ферментативную активность. Множественные формы ферментов. Изоферменты.
- •23. Общие представления о механизме ферментативного катализа. Количественная характеристика ферментативных реакций.
- •24. Принципы регуляции ферментативных процессов в клетке и регуляция метаболизма. Регуляция ферментативных процессов количеством субстрата и фермента. Локализация ферментов в клетке.
- •25. Роль нуклеиновых кислот в формировании и свойствах живой материи. Основной постулат молекулярной биологии. Строение нуклеиновых кислот. Пуриновые и пиримидиновые основания. Углеводные компоненты.
- •26. Нуклеозиды и нуклеотиды. Нуклеотидный состав днк. Правила Чаргаффа. Нуклеозиды, нуклеотиды
- •27. Первичная, вторичная и третичная структура днк. Функциональная организация
- •28. Общая характеристика рнк. Виды рнк. Особенности структуры, синтеза и функции м-рнк, т-рнк и р-рнк..
- •30. Регуляция синтеза белка у прокариот Мутации, их виды и последствия.
- •31.Ферментативный гидролиз белков. Протеолитические ферменты, их специфичность, активация.
- •32. Общая схема источников и расходования аминокислот в организме. Незаменимые аминокислоты. Общие пути катаболизма аминокислот.
- •34. Образование аммиака. Транспорт аммиака. Восстановительное аминирование. Амиды и их физиологическое значение.
- •35. Особенности обмена отдельных аминокислот и их роль в образовании важнейших биологически активных веществ.
- •36. Биосинтез мочевины. Орнитиновый цикл мочевинообразования.
- •37. Азотистые небелковые вещества (биогенные амины), их синтез, распад и биологическая роль. Нарушения структуры и обмена белков. Наследственные заболевания.
- •38. Алкалоиды, их роль у растений и значение в медицине
- •39. Углеводы и их биологическая роль, классификация и номенклатура.
- •40. Структура, свойства и распространение в природе основных представителей моносахаридов и полисахаридов. Гликопротеины и гликолипиды. Взаимопревращения моносахаридов.
- •4 1. Анаэробный и аэробный распад углеводов. Энергетическая характеристика аэробной и анаэробной фазы углеводного обмена.
- •42. Гликолиз. Спиртовое брожение.
- •43 Биосинтез полисахаридов. Гликозил-трансферазные реакции. Гликогенез
- •44. Окислительное декарбоксилирование пировиноградной кислоты. Пируватдегидрогеназный комплекс.
- •45. Цикл трикарбоновых кислот. Окислительное фосфорилирование на уровне субстрата. Прямое окисление глюкозо-6-фосфата.
- •47.Макроэргические соединения. Нуклеозидфосфаты, атф, креатинфосфат и аргининфосфат. Пути образования атф и других макроэргических соединений.
- •48.Окислительное фосфорилирование. Окислительно-востановительные процессы.
- •49. Цепь переноса водорода и электронов (дыхательная цепь).
- •52. Окислительное фосфорилирование в дыхательной цепи. Представление о механизмах сопряжения окисления и фосфорилирования в дыхательной цепи.
- •55. Жирные кислоты, их классификация и номенклатура. Простагландины.
- •56.Ферментативный распад и синтез липидов. Окисление жирных кислот, биосинтез жирных кислот. Мультиферментные комплексы синтеза жирных кислот.
- •57. Кетоновые тела, структура, синтез, утилизация в тканях.
- •60.Хим природа и физиол роль важнейших гормонов, их роль в регуляции обмена в-в и синтеза белков.
- •62. Связь между обменом белков, углеводов и липидов. Обмен веществ как единая система процессов.
27. Первичная, вторичная и третичная структура днк. Функциональная организация
Первичная структура ДНК. Представляет собой цепочку последовательно связанных нуклеотидов. Эта последовательность несет информацию о структуре белковых молекул. Для первичной структуры ДНК установлены следующие закономерности (закономерности Чаргаффа): молярное соотношение аденина к тимину равно 1; молярное соотношение гуанина к цитозину равно 1; сумма пуриновых нуклеотидов равна сумме пиримидиновых нуклеотидов; в ДНК из разных источников соотношение Г+Ц/А+Т неодинаково (коэффициент специфичности).
Вторичная структура ДНК. Представляет собой двухцепочечную правозакрученную спираль из комплементарных друг другу полинуклеотидных цепей. Комплементраность достигается за счет образования водородных связей между парами азотистых оснований A-T и G-C. При этом пары комплементарных оснований одинаковы по размеру и по форме.
Третичная структура ДНК эукариот образуется путем суперспирализации комплексов вторичной структуры с белком хромосом. При этом сначала взаимодействием ДНК с белками-гистонами образуются нуклеосомы. Затем из нуклеосомной нити образуется хроматиновая фибрилла, которая укладывается в петли, фиксируемые негистоновыми белками. Каждая петля представляет собой домен ДНК.
Структура и функции РНК.В цитоплазме клеток содержатся три основных вида РНК: матричная РНК (мРНК) выполняет роль матрицы при синтезе белка. Имеет сложную вторичную структуру. В целом линейная молекула мРНК имеет несколько двухспиральных шпилек, на концах которых располагаются «знаки» инициации и терминации трансляции транспортная РНК (тРНК) выполняет функцию посредника в ходе трансляции мРНК, транспортирует аминокислоту на рибосому. Вторичная структура имеет форму клеверного листа; рибосомная РНК (рРНК) формируют основу, с которой связываются специфические белки при образовании рибосомы.
Также в ядре клетки обнаружена ядерная РНК (яРНК), являющаяся предшественницей мРНК и тРНК.
Основные функции ДНК: хранение запаса генетической информации, необходимой для кодирования структуры всех белков и РНК каждого вида организма; регуляция во времени и пространстве биосинтез компонентов клеток и тканей; определение деятельности организма в течение его жизненного цикла; обеспечение индивидуальности данного организма.
28. Общая характеристика рнк. Виды рнк. Особенности структуры, синтеза и функции м-рнк, т-рнк и р-рнк..
РНК - нуклеиновые кислоты, полимеры нуклеотидов, в состав которых входят остаток ортофосфорной кислоты, рибоза (в отличие от ДНК, содержащей дезоксирибозу) и азотистые основания — аденин, цитозин, гуанин и урацил (в отличие от ДНК, содержащей вместо урацила тимин). Эти молекулы содержатся в клетках всех живых организмов, а также в некоторых вирусах. РНК принимают участие во всех стадиях процесса генной экспрессии и биосинтеза белка
С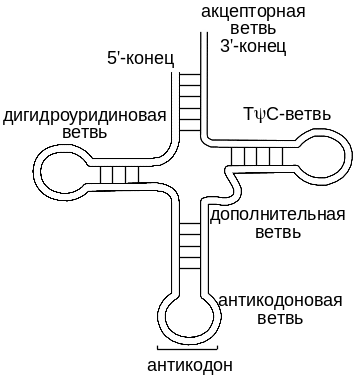 труктура
и функции РНК.В цитоплазме клеток
содержатся три основных вида РНК:
матричная РНК (мРНК) выполняет роль
матрицы при синтезе белка. Имеет сложную
вторичную структуру. В целом линейная
молекула мРНК имеет несколько
двухспиральных шпилек, на концах которых
располагаются «знаки» инициации и
терминации трансляции транспортная
РНК (тРНК) выполняет функцию посредника
в ходе трансляции мРНК, транспортирует
аминокислоту на рибосому. Вторичная
структура имеет форму клеверного листа;
рибосомная РНК (рРНК) формируют основу,
с которой связываются специфические
белки при образовании рибосомы.
труктура
и функции РНК.В цитоплазме клеток
содержатся три основных вида РНК:
матричная РНК (мРНК) выполняет роль
матрицы при синтезе белка. Имеет сложную
вторичную структуру. В целом линейная
молекула мРНК имеет несколько
двухспиральных шпилек, на концах которых
располагаются «знаки» инициации и
терминации трансляции транспортная
РНК (тРНК) выполняет функцию посредника
в ходе трансляции мРНК, транспортирует
аминокислоту на рибосому. Вторичная
структура имеет форму клеверного листа;
рибосомная РНК (рРНК) формируют основу,
с которой связываются специфические
белки при образовании рибосомы.
Также в ядре клетки обнаружена ядерная РНК (яРНК), являющаяся предшественницей мРНК и тРНК.
Синтез РНК (транскрипция).1. Инициация. σ-Субединица РНК-полимеразы связывается с промотором – специальным участком ДНК. К σ-субединице присоединяется кофермент, цепи ДНК раскручиваются и образуется открытый транскрипционный комплекс. Первым нуклеотидом с 5’-конца является гуанин, который метилируется (кэпируется), эта стартовая точка гена называется кэп-сайт. 2. Элонгация. Происходит синтез комплементарной цепи. При этом пройденные участки из 15-20 нуклеотидов вновь спирализуются. 3. Терминация. Синтез РНК замедляется по достижении стоп-сигнала. Затем синтезируется цепь по коду дополнительного сигнала и еще 15 следующих за ним нуклеотидов. В процессе отделения РНК от матрицы экзонуклеаза отщепляет терминальные 15 нуклеотидов, а полиА-полимераза достраивает 150-200 полиА-нуклеотидов. 4. Процессинг РНК.
В отличие от ДНК, РНК не образуют двойных спиралей, но содержат короткие участки со спаренными основаниями. Это приводит к образованию субструктур, которые при двумерном изображении напоминают «шпильки» и петли, образующие фигуру типа «кленового листа». В таких структурах двухцепочечные участки соединены петлями. Матричная РНК переносит генетическую информацию из клеточного ядра в цитоплазму. Так как мРНК считывается на рибосоме кодон за кодоном она не должна складываться в стабильную третичную структуру. Спариванию оснований препятствуют белки, ассоциированные с мРНК. Для мРНК характерно короткое время жизни, так как они быстро распадаются после трансляции. В сплайсинге предшественников мРНКпринимают участие малые ядерные РНК
Транспортные РНК участвуют в процессе трансляции в качестве промежуточного связующего звена между нуклеиновыми кислотами и белками. Это небольшие молекулы РНК из 70-90 нуклеотидов, которые с помощью своих антикодонов "узнают" за счет спаривания оснований определенные кодоны на мРНК. По функциональному значению РНК делят на следующие виды: 1. транспортные РНК (тРНК) осуществляют кодирование аминокислот и перенос их в рибосомальный аппарат клетки в процессе биосинтеза белка. ТРНК локализованы в ядерном соке, митохондриях. 2. рибосомальные РНК (рРНК) являются структурной основой рибосом и выполняют в них разнообразные функции. 3. информационные или матричные РНК (мРНК) выполняют роль матрицы в процессе сборки полипептидных цепей в рибосомальном аппарате клетки. 4. вирусные РНК являются составными частями вирусных и фаговых рибонуклеопротеинов и несут всю информацию, необходимую для размножения вируса в клетках хозяина.
29. Рибосомы. Генетический код и его свойства. Трансляция. Рибосома состоят из двух частей и представляют собой нуклеопротеины, состоящие из рРНК и белка в соотношении 1:1. Биологическая роль рРНК – являются структурной основой рибосом, взаимодействует с мРНК и тРНК в процессе биосинтеза белка, принимает участие в процессе сборки полипептидной цепи. У эукариот обнаружено 4 типа рРНК с различным коэф. седиментации: 18S(в малой части рибосомы), а 28S, 5,8S и 5S (сведбергов) – в большой части рибосомы.. Они различаются молекулярной массой (35 000-1 600 000) и локализацией в рибосомах. Вторичная структура рРНК характеризуется спирализацией цепи самой на себя, третичная – ее компактной укладкой. Рибосомы служат для биосинтеза белка из аминокислот по заданной матрице на основе генетической информации, предоставляемой матричной РНК (трансляция). Нередко с одной молекулой мРНК ассоциировано несколько рибосом, такая структура называется полирибосомой. Синтез рибосом у эукариот происходит в специальной внутриядерной структуре — ядрышке.
Генети́ческий код — свойственный всем живым организмам способ кодирования аминокислотной последовательности белков при помощи последовательности нуклеотидов. Информация о строении белка закодирована в ДНК с помощью генетического кода, который является линейным, непрерывным, триплетным, выражденным. Он является универсальным. В ДНК используется четыре нуклеотида — аденин (А), гуанин (G), цитозин (С), тимин (T). Эти буквы составляют алфавит генетического кода. В РНК используются те же нуклеотиды, за исключением тимина, который заменён похожим нуклеотидом — урацилом, который обозначается буквой U. В молекулах ДНК и РНК нуклеотиды выстраиваются в цепочки и, таким образом, получаются последовательности генетических букв. Для построения белков в природе используется 20 различных аминокислот. Каждый белок представляет собой цепочку или несколько цепочек аминокислот в строго определённой последовательности. Эта последовательность определяет строение белка, а, следовательно, все его биологические свойства. Набор аминокислот также универсален почти для всех живых организмов.Реализация генетической информации в живых клетках (то есть синтез белка) осуществляется при помощи двух матричных процессов: транскрипции (то есть синтеза мРНК на матрице ДНК) и трансляции генетического кода в аминокислотную последовательность (синтез полипептидной цепи на мРНК). Для кодирования 20 аминокислот, а также сигнала «стоп», означающего конец белковой последовательности, достаточно трёх последовательных нуклеотидов. Набор из трёх нуклеотидов называется триплетом. Принятые сокращения, соответствующие аминокислотам и кодонам. Свойства:1Триплетность — значащей единицей кода является сочетание трёх нуклеотидов (триплет, или кодон).2Непрерывность — между триплетами нет знаков препинания, то есть информация считывается непрерывно.3Неперекрываемость — один и тот же нуклеотид не может входить одновременно в состав двух или более триплетов (не соблюдается для некоторых перекрывающихся генов вирусов, митохондрий и бактерий, которые кодируют несколько белков, считывающихся со сдвигом рамки).4Однозначность (специфичность) — определённый кодон соответствует только одной аминокислоте (однако, кодон UGA у Euplotes crassus кодирует две аминокислоты — цистеин и селеноцистеин)[1]5Вырожденность (избыточность) — одной и той же аминокислоте может соответствовать несколько кодонов.7Универсальность — генетический код работает одинаково в организмах разного уровня сложности — от вирусов до человека (на этом основаны методы генной инженерии; есть ряд исключений, показанный в таблице раздела «Вариации стандартного генетического кода» ниже).8Помехоустойчивость — мутации замен нуклеотидов, не приводящие к смене класса кодируемой аминокислоты, называют консервативными; мутации замен нуклеотидов, приводящие к смене класса кодируемой аминокислоты, называют радикальными.
