
- •Часть 1. Компьютерное моделирование электронной структуры фуллерена с60
- •Введение
- •Лабораторная работа №1 «Основы работы в редакторе GaussView пакета Gaussian03»
- •1.1 Теоретическая часть
- •1.1.1 Программный комплекс Gaussian03
- •1.1.2 Редактор GaussView
- •1.2 Практическая часть
- •1.2.1 Построение молекул c использованием библиотек редактора GaussView
- •1.2.2. Примеры задания конфигурации молекул в редакторе GaussView
- •Вопросы
- •Лабораторная работа №2 «Численное моделирование электронной структуры молекул с использованием пакета Gaussian03»
- •2.1 Теоретическая часть
- •2.1.1 Основные методы расчета молекулярных структур
- •2.1.2 Неэмпирические методы расчета
- •2.1.2.1 Метод Хартри-Фока
- •2.1.2.2 Метод теории функционала плотности
- •2.1.3 Основные квантово- механические базисы
- •2.2 Практическая часть
- •2.2.1 Использование Gaussian Calculation Setup для установки параметров расчетов
- •2.2.2 Контрольный пример. Расчет характеристик молекулы кислорода o2
- •2.2.2.1 Визуализация электронной структуры атома кислорода
- •2.2.2.2 Зависимость полной энергии двух атомов кислорода от расстояния между ними
- •2.2.2.3 Расчет равновесного расстояния молекулы кислорода
- •Лабораторная работа №3 «Молекулярное строение и электронная структура молекулы фуллерена с60»
- •3.1 Теоретическая часть
- •3.1.1 Молекулярное строение фуллеренов c60
- •3.1.2 Получение фуллеренов
- •3.1.3 Свойства фуллеренов
- •3.1.4 Применение фуллеренов
- •3.1.5 Фуллериты
- •3.1.6 Электронная структура фуллеренов с60
- •3.2 Практическая часть
- •3.2.1 Электронная структура молекулы фуллерена с60
- •Вопросы
- •Лабораторная работа №4 «ик- спектр изолированной молекулы фуллерена с60»
- •4.1 Теоретическая часть
- •4.1.2 Колебательный спектр двухатомной молекулы
- •4.1.3 Колебания многоатомных молекул
- •4.2 Практическая часть
- •4.2.1 Расчет нормальных колебательных мод в Gaussian
- •4.2.2 Расчет структуры и колебательного спектра молекулы воды
- •Вопросы:
- •Лабораторная работа №5 «ик- спектр молекулы фуллерена с60 в растворах»
- •5.1 Теоретическая часть
- •5.1.1 Типы растворов
- •5.1.2 Растворимость фуллеренов
- •5.2 Практическая часть
- •5.2.1 Учет эффектов сольватации при расчетах в Gaussian03
- •Вопросы:
- •Литература
- •Глоссарий терминов.
- •Приложение 1. Панель меню и панель команд редактора GaussView.
- •Приложение 2. Настройки параметров расчетов Gaussian03.
- •Приложение 3. Справочная информация о неорганических молекулах
- •Приложение 4. Справочная информация об органических молекулах
- •Приложение 5. Правила оформления лабораторных работ
4.1.2 Колебательный спектр двухатомной молекулы
Спектральные характеристики (положения максимумов полос, их полуширина, интенсивность) индивидуальной молекулы зависят от масс составляющих ее атомов, геометрического строения, особенностей межатомных сил, распределения заряда и др. Рассмотрим простейший случай двухатомной молекулы AB.
Молекулу можно представить в виде двух шариков с массами mA и mB, связанных между собой упругой связью с равновесным расстоянием re (рис. 4.1). При смещении шариков A и B из положения равновесия на расстояние Δr возникает возвращающая сила f (рис. 4.2), стремящаяся вернуть систему в исходное равновесное положение. Сила f описывается с помощью закона Гука:
![]() (4.1)
(4.1)
Δr=r-re – изменение длины связи, k- силовая постоянная связи.
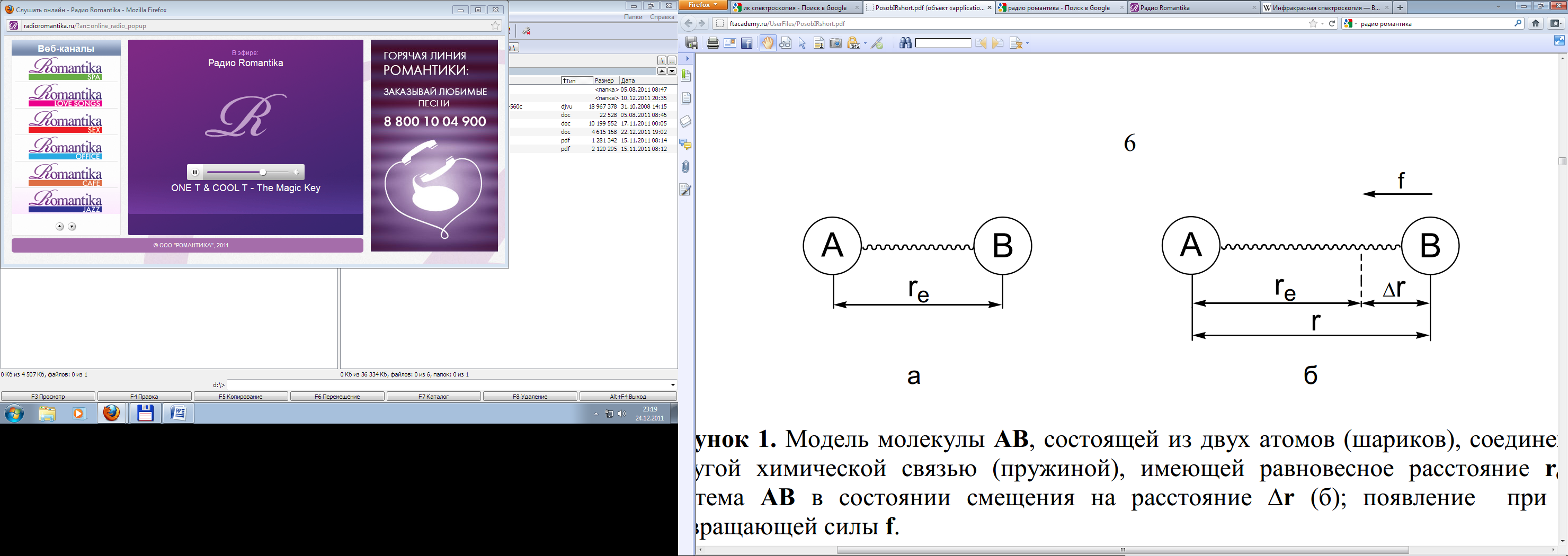
Рис.4.1 Модель двухатомной молекулы AB с равновесным расстоянием re (а) и возникновение возвращающей силы f при изменении расстояния между атомами на Δr
Движение, происходящее после смещения шариков A и B из положения равновесия называется простым гармоническим колебанием. Потенциальная энергия Vгарм системы гармонического осциллятора, состоящего из двух атомов, связанных упругой химической связью, определяется выражением:
![]() (4.2)
(4.2)
Функция V(r) представляет собой симметричную параболу, проходящую через точку минимума, соответствующую равновесному межъядерному расстоянию re (рис.4.2).
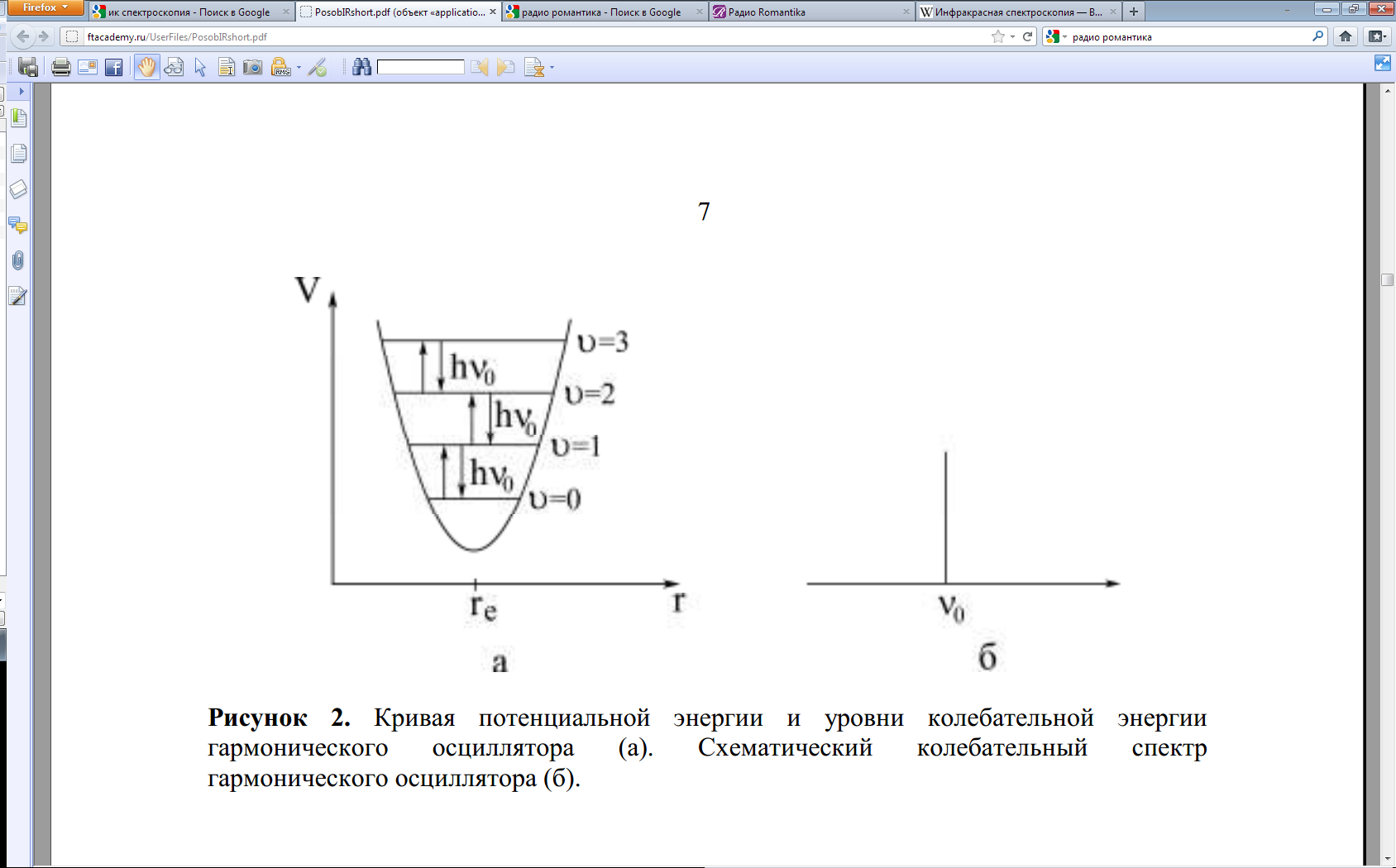
Рис.4.2 Кривая потенциальной энергии и уровни колебательной энергии гармонического осциллятора (а). Схематический колебательный спектр гармонического осциллятора (б).
Колебательная
энергия гармонического осциллятора
![]() квантуется
по закону:
квантуется
по закону:
![]() (4.3)
(4.3)
h- постоянная Планка, n=0, 1, 2, …- колебательное квантовое число, ν0 – частота колебаний гармонического осциллятора, описываемая уравнением:
![]() (4.4)
(4.4)
k – силовая постоянная связи, M=mAmB/(mA+mB) – приведенная масса двухатомной системы AB.
В результате квантования энергии гармонический осциллятор характеризуется набором равноотстоящих энергетических уровней, отличающихся друг от друга на одинаковую величину hν0 (рис.4.2). Разрешенными являются только переходы между соседними уровнями, т.е. правило отбора для перехода между колебательными уровнями гармонического осциллятора имеет вид:
Δn=±1 (4.4)
В результате колебательный спектр гармонического осциллятора представляет собой только одну линию с частотой ν0.
В отличие от модели гармонического осциллятора колебания реальных молекул ангармоничны. Потенциальная энергия ангармонического осциллятора Vангарм описывается функцией Морзе:
![]() (4.5)
(4.5)
D – энергия диссоциации связи, ∆r- смещение атомов из положения равновесия, a- постоянная, определяемая выражением:
![]() (4.6)
(4.6)
ν0 – частота осциллятора, M – приведенная масса.
Колебательная энергия ангармонического осциллятора квантуется согласно закону:
![]() (4.7)
(4.7)
По мере увеличения квантового числа n колебательные уровни будут постепенно сближаться (рис.4.3а). В случае ангармонического осциллятора (реальной молекулярной системы) могут реализовываться переходы не только между соседними колебательными уровнями с ∆n=1, но и переходы с ∆n=2, 3, … Это приводит к появлению в колебательном спектре нескольких полос с частотами ν, ν1, ν2.(рис. 4.3б).

Рис. 4.3 Кривая потенциальной энергии и уровни колебательной энергии ангармонического осциллятора (а). Схематический колебательный спектр ангармонического осциллятора (б)
Полоса спектра, отвечающая переходу между колебательными уровнями n=0 →1 (∆n=1) называется основной частотой. Колебательный переход между уровнями с n=0 →2 (ν1) называется первым обертоном, n=0→3 (ν2) вторым обертоном.
