
- •Часть 1. Компьютерное моделирование электронной структуры фуллерена с60
- •Введение
- •Лабораторная работа №1 «Основы работы в редакторе GaussView пакета Gaussian03»
- •1.1 Теоретическая часть
- •1.1.1 Программный комплекс Gaussian03
- •1.1.2 Редактор GaussView
- •1.2 Практическая часть
- •1.2.1 Построение молекул c использованием библиотек редактора GaussView
- •1.2.2. Примеры задания конфигурации молекул в редакторе GaussView
- •Вопросы
- •Лабораторная работа №2 «Численное моделирование электронной структуры молекул с использованием пакета Gaussian03»
- •2.1 Теоретическая часть
- •2.1.1 Основные методы расчета молекулярных структур
- •2.1.2 Неэмпирические методы расчета
- •2.1.2.1 Метод Хартри-Фока
- •2.1.2.2 Метод теории функционала плотности
- •2.1.3 Основные квантово- механические базисы
- •2.2 Практическая часть
- •2.2.1 Использование Gaussian Calculation Setup для установки параметров расчетов
- •2.2.2 Контрольный пример. Расчет характеристик молекулы кислорода o2
- •2.2.2.1 Визуализация электронной структуры атома кислорода
- •2.2.2.2 Зависимость полной энергии двух атомов кислорода от расстояния между ними
- •2.2.2.3 Расчет равновесного расстояния молекулы кислорода
- •Лабораторная работа №3 «Молекулярное строение и электронная структура молекулы фуллерена с60»
- •3.1 Теоретическая часть
- •3.1.1 Молекулярное строение фуллеренов c60
- •3.1.2 Получение фуллеренов
- •3.1.3 Свойства фуллеренов
- •3.1.4 Применение фуллеренов
- •3.1.5 Фуллериты
- •3.1.6 Электронная структура фуллеренов с60
- •3.2 Практическая часть
- •3.2.1 Электронная структура молекулы фуллерена с60
- •Вопросы
- •Лабораторная работа №4 «ик- спектр изолированной молекулы фуллерена с60»
- •4.1 Теоретическая часть
- •4.1.2 Колебательный спектр двухатомной молекулы
- •4.1.3 Колебания многоатомных молекул
- •4.2 Практическая часть
- •4.2.1 Расчет нормальных колебательных мод в Gaussian
- •4.2.2 Расчет структуры и колебательного спектра молекулы воды
- •Вопросы:
- •Лабораторная работа №5 «ик- спектр молекулы фуллерена с60 в растворах»
- •5.1 Теоретическая часть
- •5.1.1 Типы растворов
- •5.1.2 Растворимость фуллеренов
- •5.2 Практическая часть
- •5.2.1 Учет эффектов сольватации при расчетах в Gaussian03
- •Вопросы:
- •Литература
- •Глоссарий терминов.
- •Приложение 1. Панель меню и панель команд редактора GaussView.
- •Приложение 2. Настройки параметров расчетов Gaussian03.
- •Приложение 3. Справочная информация о неорганических молекулах
- •Приложение 4. Справочная информация об органических молекулах
- •Приложение 5. Правила оформления лабораторных работ
Лабораторная работа №3 «Молекулярное строение и электронная структура молекулы фуллерена с60»
Цель работы: проведение расчетов электронной структуры молекулы фуллерена С60 с использованием метода DFT программного комплекса Gaussian03.
3.1 Теоретическая часть
3.1.1 Молекулярное строение фуллеренов c60
Молекула С60 представляет собой полиэдр с наиболее высокой симметрией Ih - симметрией усеченного икосаэдра (рис. 3.1а). Эта фигура формируется двадцатью шестиугольниками и двенадцатью пятиугольниками и подчиняется уравнению Эйлера для различных поверхностей:
![]() (3.1)
(3.1)
где n – размерность многоугольников, Nn – число многоугольников размерности n , s – характеристика кривизны поверхности (s = 1 для сферы и s = 0 для плоскости) из формулы 3.1 следует, что для образования сферической поверхности необходимо 12 пентагонов n = 5 и сколь угодно гексагонов (n=6).
Полиэдры с большим числом вершин сложно представить наглядно в виде пространственной фигуры. Поэтому при описании высших фуллеренов используют плоские графы - диаграммы Шлегеля. Диаграмма Шлегеля, представляющая молекулу С60, изображена на рис.3.1б.
Усеченный икосаэдр обладает 6 осями пятого порядка, проходящими через 12 противоположно лежащих пятиугольников, 10 осями третьего порядка, проходящими через 20 противоположно лежащих шестиугольников, 30 осями второго порядка, проходящими через противоположно лежащие шестьдесят ребер шестиугольник-шестиугольник. Существует также несколько типов плоскостей симметрии пятого, третьего и второго порядков.
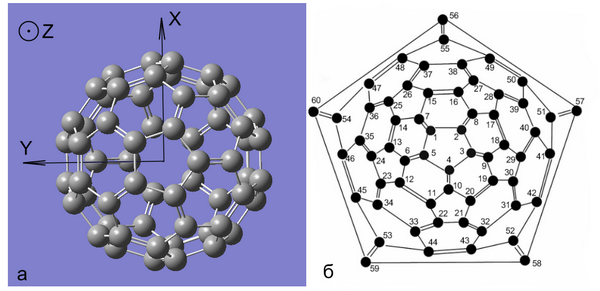
Рис. 3.1. Структура фуллерена С60 (а)и диаграмма Шлегеля (б).
В молекуле фуллерена С60 каждый шестиугольник граничит с тремя шестиугольниками и тремя пятиугольниками, а каждый пятиугольник граничит только с шестиугольниками, так называемое правило изолированного пентагона. Таким образом, каждый атом углерода в молекуле С60 находится в вершинах двух шестиугольников и одного пятиугольника и принципиально неотличим от других атомов углерода, что подтверждается спектром ядерного магнитного резонанса: для чистого образца С60 регистрируется единственный пик.
Существенной особенностью фуллеренов, определяющей как электронные свойства, так и способность к формированию связей между молекулами, является чередование ковалентных связей. Длины связей С–С и С=С составляют ~ 0.139 и 0.144 нм соответственно. Радиус молекулы С60, составляет ~ 0.357 нм. Средняя энергия С–С-связи в молекуле С60 составляет ~448.78 кДж⋅моль–1 [5].
В отличие от молекул С60, спектр ядерного магнитного резонанса молекул С70 состоит из пяти пиков. Данный факт хорошо согласуется с представлением о структуре молекулы С70, которая отличается от С60 введением в последнюю 10 атомов углерода в экваториальную область сферы с последующим ее растяжением. В данной структуре имеется восемь различных типов С–С-связей, отличающихся своим месторасположением и длиной. Длина связей, составляющих пятиугольники, близка к 0.146 нм, в то время как длина связей, соединяющих вершины двух пятиугольников, близка к 0.137 нм. Связь, не искаженная близостью пятиугольников, аналогична С–С-связи в слое графита. Связь, соединяющая вершины пятиугольника и шестиугольника в экваториальной области молекулы С70, имеет длину 0.139 нм, промежуточную между длинами связей, соединяющих два шестиугольника и два пятиугольника соответственно. Большая полуось молекулы С70 ~0.39 нм, малая полуось ~ 0.347нм. Средняя энергия одной С–С-связи в молекуле С70 составляет 436.26 кДж⋅моль–1.
