
- •I . Борівська теорія атома
- •1.1. Закономірність в атомних спектрах
- •1.2. Модель атома Томсона
- •1.3. Досліди по розсіянню -частинок. Ядерна модель атома
- •1.4. Постулати Бора. Дослід Франка і Герца
- •1.5. Елементарна борівська теорія водневого атома
- •II. Елементи квантової механіки
- •2.1. Гіпотеза Луї де Бройля. Корпускулярно-хвильовий дуалізм
- •2.2. Співвідношення невизначеностей Гейзенберга
- •2.3. Рівняння Шредінгера
- •2.4. Фізичний зміст псі-функції
- •2.5. Квантування енергії
- •2.6. Рух вільної частинки
- •2.7. Частинка в нескінченно глибокій потенціальній ямі
- •2.8. Гармонічний осцилятор
- •2.9. Проходження частинки крізь потенціальний бар’єр
- •2.10. Квантування моменту імпульсу
- •III. Квантова теорія атомів і молекул
- •3.1. Квантова теорія атома водню
- •3.2. Багатоелектронні атоми
- •3.2.1. Спектри лужних металів
- •3.2.2. Нормальний ефект Зеємана
- •3.2.3 Мультиплетність спектрів і спін електрона
- •3.2.4 Механічний та магнітний моменти багатоелектонного атома
- •3.2.5. Розподіл електронів в атомі за станами. Періодична система елементів д.І. Менделєєва
- •3.2.6. Рентгенівські спектри
- •3.2.7. Енергія молекули
- •3.2.8. Молекулярні спектри
- •3. 2. 9 Комбінаційне розсіювання світла
- •3. 2.10. Вимушене випромінювання. Лазери
- •I. Борівська теорія атома………………………………………………………..…3
Міністерство освіти і науки України
Національний технічний університет України
“Київський політехнічний інститут”
Фізика
Методичні вказівки
до вивчення дисципліни
Розділ “Фізика атомів і молекул”
для студентів усіх форм навчання
Київ
НТУУ “КПІ”
2011
Фізика: Метод. вказівки до вивч.дисципліни. Розділ “Фізика атомів і молекул” для студ. усіх форм навч./ Уклад.: В.А. Горбатюк, Т.В. Печерська. – К.; НТУУ “КПІ”, 2009. – 75с.
Фізика
Методичні вказівки
до вивчення дисципліни
Розділ “Фізика атомів і молекул”
для студентів усіх форм навчання
Рекомендовано кафедрою ЗФ та ФТТ НТУУ “КПІ”
Протокол № 08-10 від 30 серпня 2010 р.
Укладачі: Горбатюк Василь Архипович, канд. техн. наук
Печерська Тетяна Вікторівна
Відповідальний
редактор Л.П. Гермаш, д-р. техн. наук, проф.
Рецензент А.О. Снарський, д-р. фіз.-мат. наук, проф.
За редакцією укладачів
Надруковано з оригінал – макета замовника
I . Борівська теорія атома
1.1. Закономірність в атомних спектрах
Якщо ізольованим атомам у вигляді газів або парів металів надати певну енергію (наприклад нагріти), то вони випромінюють різні кванти енергії, сукупності яких утворюють окремі спектральні лінії. У відповідності з цим спектр випромінювання окремих атомів називають лінійчастим. Лінії в спектрах атомів розташовані не хаотично, а об’єднуються в групи, які назвали серіями ліній; для кожної серії довжини хвиль визначаються за певними закономірностями.
Так, в 1885 р. швейцарський фізик Й. Я. Бальмер (1825 - 1899) встановив, що довжини хвиль серії видимого спектра атомів водню виражаються формулою
![]() ,
(1.1)
,
(1.1)
де
![]() - стала величина, n
– ціле
число,
що приймає значення 3, 4, 5…
- стала величина, n
– ціле
число,
що приймає значення 3, 4, 5…
У спектроскопії прийнято характеризувати спектральні лінії величиною, зворотною довжині хвилі
![]() ,
(1.2)
,
(1.2)
яку
називають
хвильовим
числом (не слід
змішувати
з
хвильовим
числом ![]() ).
Виконавши
незначні
математичні
перетворення,
отримаємо:
).
Виконавши
незначні
математичні
перетворення,
отримаємо:
![]() ,
(1.3)
,
(1.3)
де
![]() R=4/λ0=10973731,77м-1
≈ 1,1∙107
м-1
R=4/λ0=10973731,77м-1
≈ 1,1∙107
м-1
Враховуючи
те, що ν′
=1/λ=ν/c
,
де с – швидкість світла в вакуумі,
![]() -частота
коливань, на підставі формули (1.3)
отримаємо:
-частота
коливань, на підставі формули (1.3)
отримаємо:
![]() ,
(1.4)
,
(1.4)
де
![]() ≈3,29∙1015
с-1
≈3,29∙1015
с-1
Зважаючи
на
те, що ![]() ,
на підставі формули
(1.4) маємо:
,
на підставі формули
(1.4) маємо:
![]() .
(1.5)
.
(1.5)
де R= 20,648∙1015с-1≈20,7∙1015 с-1
Формули (1.1), (1.2), (1.3), (1.4), (1.5) називають формулами Бальмера, а величини R – на честь шведського спектроскопіста - сталою Рідберга (іноді сталою Бальмера-Рідберга [1]).
Сукупність ліній, що описуються формулою Бальмера, дістала назву серії Бальмера.
Згодом у спектрі атома водню було виявлено низку інших серій, подібних до серії Бальмера. В ультрафіолетовій частині спектра знаходиться серія Лаймана . Інші серії знаходяться в інфрачервоній області спектра. Лінії цих серій можна представити у вигляді формул, аналогічних формулі (1.5):
серія
Лаймана 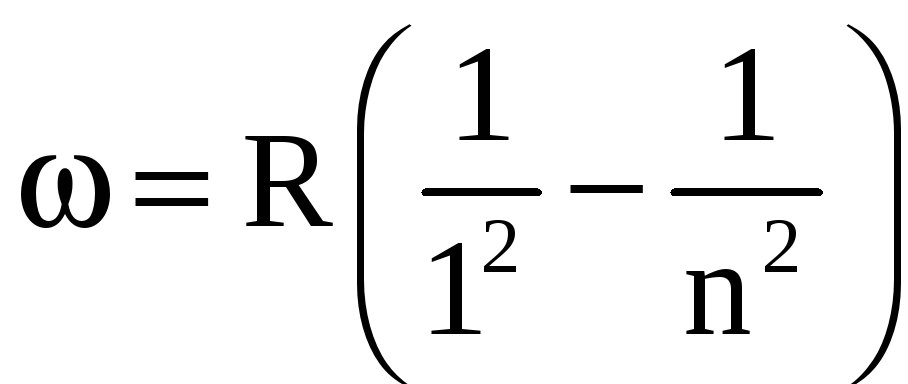
![]() ,
,
серія
Пашена 
![]() ,
,
серія
Бреккета

![]() ,
,
серія
Пфунда
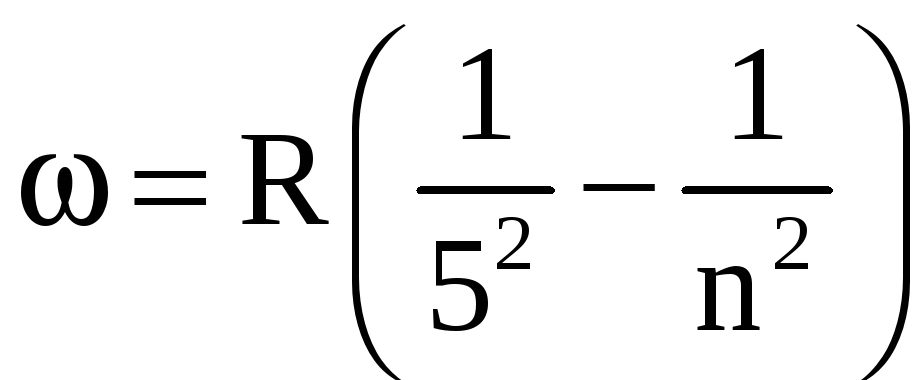
![]() ,
,
серія
Хемфрі 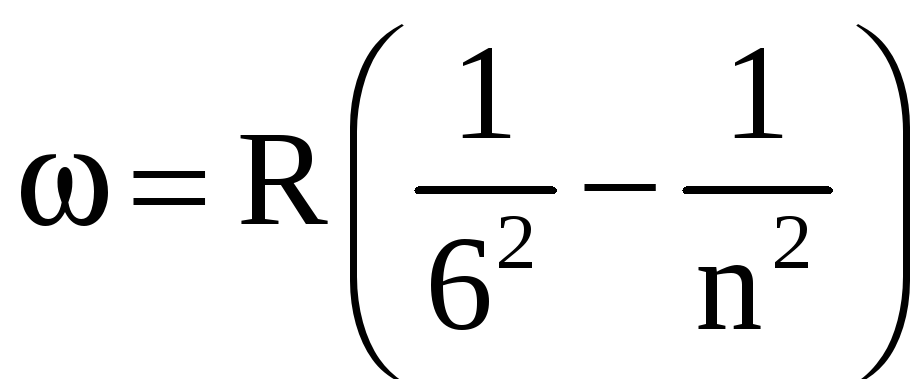
![]() .
.
Частоту всіх ліній спектра атома водню можна представити загальною формулою:
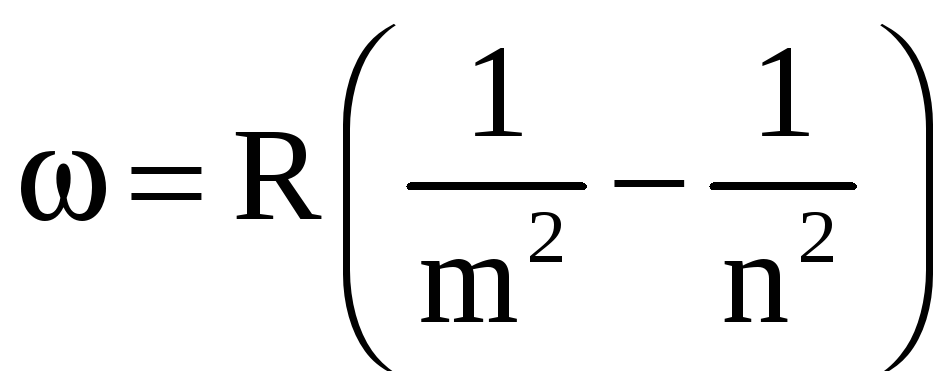 ,
(1.6)
,
(1.6)
де m має значення 1 для серії Лаймана, 2 – для серії Бальмера і т.д. При заданому m число n приймає всі цілі значення, починаючи з m+1. Формулу (1.6) називають об’єднаною формулою Бальмера.
При
зростанні n
частота лінії в кожній серії спектра
прагне до граничного значення ![]() ,
яке називають межею
серії.
,
яке називають межею
серії.
Розглянемо
ряд значень виразу ![]()
![]() ,
,
![]() ,
,
![]() ,…
(1.7)
,…
(1.7)
Частота будь-якої лінії спектра водню може бути представленою у вигляді різниці двох чисел ряду (1.7). Ці числа називають спектральними термами або просто термами. Так, наприклад, частота першої лінії Бальмера дорівнює T(2) - T(3), другої лінії серії Пфунда Т(5) – Т(7) і т.д.
Дослідження показали, що частоти ліній спектрів інших атомів можуть бути представленні у вигляді різниці двох термів:
![]() .
(1.8)
.
(1.8)
Однак терм Т(n) має більш складний вигляд, ніж для атома водню. Окрім того, перший і другий члени формули (1.8) беруться з різних рядів термів.
