
Кислотно-основное_состояние
.pdf
Какая теория используется на
практике?
•Проще других – Bronsted-Lowry.
Использовать Н2СО3 вместо СО2
•На практике большинство из нас понимают кислоту, как:
-[Н+] в растворе (Аррениус)
-донор [Н+] (Bronsted-Lowry)
-и даже СО2, как «кислоту» (Льюис)

Важно! Н+ - «символ метафоры» (Стюарт)
•Н+ в «чистом виде» в р-ре не существуют!
•Протоны связываются и реагируют с окружающими их молекулами Н2О = Н3О+ - ион гидрония
•Или, ещѐ точнее - {Н:(Н2О)n}+
•Крайне неудобно и непривычно – возвращаемся к «метафорическому» Н+

рН
•Нелинейная трансформация концентрации Н+ -
отрицательный логарифм [Н+]. ↓рН = ↑ [Н+]
•Логарифмическое выражение объѐма,
способного вместить 1 Eq [Н+] (для плазмы с
рН=7.4, этот объѐм составляет 25.000.000 л)
•Для сравнения – концентрация Na+ в плазме –
140 meq/L; концентрация Н+ - 0.00004 meq/L
(pH – 7.4)
•Безразмерная величина

pH = - log10[Н+]
• Для Н2О при 22 С:
[Н+] = [ОН-] = 1 10-7 моль/л
• рН (Н2О) = - log (1 10-7) = - (-7.0)= 7.00
•Поскольку основание log = 10 (log10), именения рН на 1 ед. соответствуют
изменению [Н+] в 10 раз (в обратную
сторону):
Р-р с рН 3 содержит [Н+] в 10 раз больше,
чем р-р с рН 4

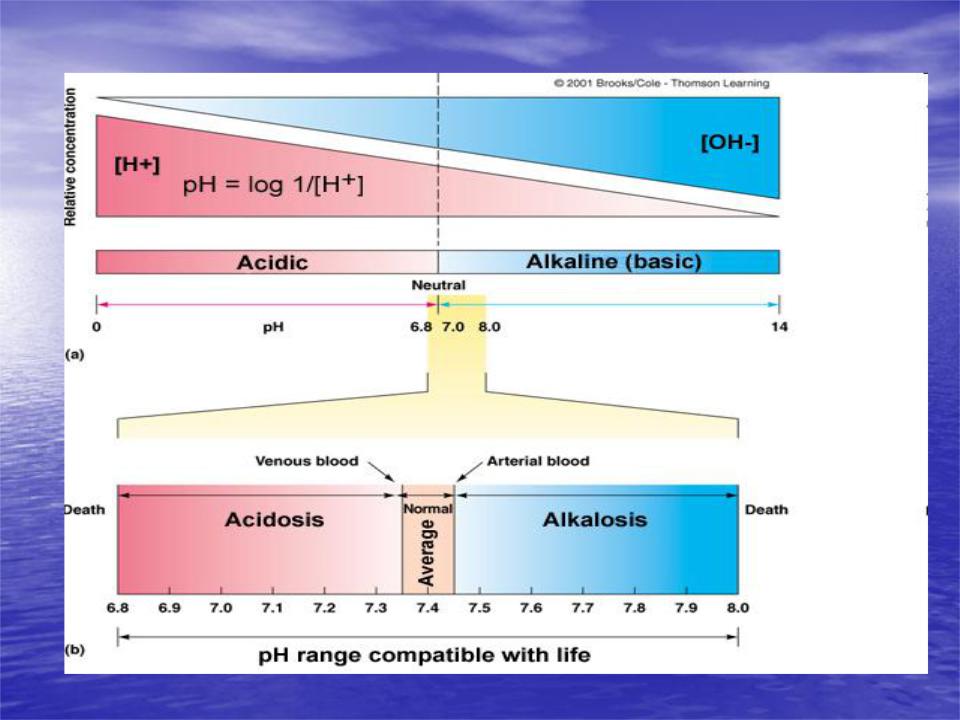
Шкала рН (0-14) и [Н+] ммоль/л

pH = - log10[Н+] или pН = - log10(aH+)?
•ax = g . [x], где
ах – активность в-ва х в р-ре g – коэффициент активности х
[x] – концентрация х в р-ре
•Активность отражает степень взаимодействия
молекул р-ра и растворимого в-ва друг с
другом. Она выше при повышении их
концентрации и степени ионизации.
•Для разбавленных р-ров (рН 0-14) не имеет
значения (?), поэтому в организме: pH = - log10[Н+] = - log10(aH+)

Соотношение [Н+] (у) и рН (х) нелинейно!

Преимущества использования рН
•Традиционный, широкоупотребляемый символ
•Отражает активность Н+, а не концентрацию (см. устройство рНэлектрода далее) – реальное св-во физиологических систем
•Н+ не присутствуют в р-рах в чистом виде

Недостатки рН
•Производное, отражающее двойную нелинейную трансформацию [Н+] (т.е. 1.
отрицательный 2. логарифм)
•Трудно понять и запомнить
•Недооценивает степень изменения концентрации [Н+]
