
- •Биосинтез белка
- •Тема 21. Современные методы молекулярной биологии
- •Тема 22. Гормоны. Общий механизм действия гормонов
- •Механизм действия гормонов, взаимодействующих
- •Механизм действия гормонов, взаимодействующих с 1-тмс-рецепторами
- •Механизм действия гормонов, взаимодействующих с внутриклеточными рецепторами
- •Тема 23. Гормоны — производные белков, пептидов и аминокислот гормоны гипоталамуса
- •Гормоны гипоталамуса
- •Гормоны аденогипофиза Это гормоны белково-пептидной природы (табл. 23.2).
- •Гормоны аденогипофиза
- •Гормоны задней доли гипофиза
- •Гормоны поджелудочной железы
- •Выделяют две формы диабета:
- •1) Инсулин-зависимый сахарный диабет (диабет 1-го типа), развивается вследствие дефицита инсулина, вызываемого аутоиммунным разрушением β-клеток поджелудочной железы;
- •2) Инсулин-независимый сахарный диабет (диабет 2-го типа), характеризуется устойчивостью к инсулину и его сниженной секрецией. Он встречается чаще, развивается у пожилых лиц.
- •Тема 24. Стероидные гормоны
- •2. Окисление и изомеризация прегненолона в прогестерон. Прегненолон является предшественником всех стероидных гормонов.
- •Половые гормоны
- •Тема 25. Биохимия питания. Макро- и микроэлементы
- •Макроэлементы
- •Концентрация электролитов вне и внутри клетки существенно различается: натрий и кальций преобладают во внеклеточном пространстве, калий и магний — внутри клетки. Кальций
- •Кальцитонин
- •Паратирин (паратгормон)
- •Витамин д (кальциферол), антирахитический
- •Микроэлементы Железо
- •Тема 26. Биохимия питания. Витамины и другие незаменимые факторы питания. Синдром недостаточного питания
- •Витамины
- •Клинические формы недостаточности питания
- •Тема 27. Биохимия соединительных тканей и органов полости рта (костная и хрящевая ткани, зубы)
- •Неколлагеновые белки костной ткани и их роль в процессах минерализации
- •Химический состав тканей зуба и кости (весовые %)
- •Тема 28. Биохимия ротовой жидкости
- •Химический состав ротовой жидкости
- •Скорость саливации и характер секрета слюны из протоков слюнных желез
- •Функции ротовой жидкости
- •Белки ротовой жидкости и их роль
- •Ферменты ротовой жидкости и их роль
- •Поверхностные образования на эмали
- •Фтор (f) и его роль в организме
- •Виды фтор-профилактики
- •Тема 29. Биохимия печени
- •Функции печени
- •Тема 30. Биохимия мышечной ткани
- •Миофибриллярные (сократительные) белки
- •Молекулярный механизм мышечного сокращения
- •Источники энергии мышечного сокращения
- •Механизмы энергообеспечения мышечного сокращения
- •Литература
- •Оглавление
- •Биологическая химия
- •220030, Г. Минск, ул. Ленинградская, 6.
Фтор (f) и его роль в организме
1. 99 % фтора в виде фторапатита входит в состав костей и зубов, придает им прочность и кислотоустойчивость.
2. Стимулирует реминерализацию костей и зубов (поступление в них кальция и фосфора).
3. Стимулирует синтез костной ткани, иммунитет (в том числе полости рта), гемопоэз.
4. Блокирует енолазу микроорганизмов (прекращается синтез лактата, который снижает рН ротовой жидкости) и синтез микроорганизмами внеклеточных полисахаридов.
5. Изменяет электрический потенциал поверхности эмали и препятствует адгезии бактерий к эмали.
Концентрация F выражается в мг/л и ppm (parts per million): 1 мг/л = 1 ppm; 1 % = 10 000 ppm.
Рекомендации Всемирной организации здравоохранения (ВОЗ), 1994 г.:
за оптимум принято количество F, приближающееся к 4 мг/сут (1,5–4 мг/сут);
1,2 мг F — из воды (30 %); 2,0 мг — из пищи (50 %); 0,8 мг — из воздуха (20 %);
в жарких странах F в воде должно быть 0,5–0,8 мг/л, с умеренным климатом — 0,8–1,0 мг/л, в северных — 1,0–1,2 мг/л.
Больше всего фтора содержится в морепродуктах, зеленом и черном чае, красном вине. Много F в районах комбинатов по выпуску фосфорных удобрений, сжигания каменного угля.
В Республике Беларусь фтора содержится в воде 0,2 ppm (мг/л), в употребляемых продуктах — 0,6 ppm, из воздуха — 0,5 мг. В среднем мы получаем (0,6 + 0,8 + 0,5) мг = 1,9 мг фтора. Виды фтор-профилактики представлены в таблице 28.3.
Таблица 28.3
Виды фтор-профилактики
|
Системная (эндогенная) |
Местная (экзогенная) |
|
Фторирование питьевой воды, поваренной соли, молока, таблетки «Витафтор» |
Фторсодержащие пасты, растворы, гели, лаки, герметики фиссур |
В зубной пасте для взрослых фтора должно быть 1500 ppm , для детей — 500 ppm.
Недостаток фтора вызывает кариес, избыток — флюороз: «крапчатая», «пятнистая» эмаль зубов; минерализация хрящей и связок, остеосклероз скелета; раннее старение; снижение иммунитета и гормональной активности.
Тема 29. Биохимия печени
Печень играет центральную роль в обмене веществ. Масса печени у взрослого человека составляет ≈ 1,5 кг, при этом на долю воды приходится 70–75 % . Из сухого остатка более 50 % составляют белки. 90 % этих белков — глобулины. В печени много ферментов, липидов, гликогена.
Функции печени
1. Гомеостатическая. Поддерживает постоянный состав крови (гомеостаз). Питательные вещества в желудочно-кишечном тракте всасываются периодически. Их концентрации в портальном кровотоке в разные периоды времени существенно различаются, но благодаря гомеостатической функции печени концентрации важнейших метаболитов в большом круге кровообращения практически постоянны.
2. Роль печени в обмене белков. Освобождающиеся в процессе пищеварения аминокислоты попадают с током крови в печень и используются:
для синтеза белков плазмы крови (альбуминов, глобулинов, факторов свёртывания крови);
образования α-кетокислот путём трансаминирования или окислительного дезаминирования аминокислот;
глюконеогенеза;
синтеза кетоновых тел;
получения энергии, подвергаясь превращениям в цикле трикарбоновых кислот;
синтеза мочевины;
для синтеза креатина, холина.
3. Роль в обмене липидов. Печень играет ключевую роль в метаболизме липидов:
в ней синтезируются, распадаются, удлиняются и укорачиваются жирные кислоты, поступающие с пищей или образующиеся при распаде простых и сложных липидов;
распадаются и синтезируются триацилглицеролы;
синтезируется большинство липопротеинов и 90 % из общего количества холестерола в организме;
в печени из холестерола синтезируются желчные кислоты, которые входят в состав желчи, необходимой для переваривания липидов в кишечнике;
печень — единственный орган, в котором синтезируются кетоновые тела;
в печени синтезируются витамин А и 25-гидроксихолекальциферол (предшественник витамина D3), запасается (!) витамин В12.
4. Роль печени в обмене углеводов. Основная роль печени в метаболизме углеводов — это поддержание нормальной концентрации глюкозы в крови благодаря тому, что в печени имеются:
ферменты синтеза и распада гликогена;
ферменты глюконеогенеза;
ферменты, превращающие другие гексозы (галактозу и фруктозу) в глюкозу.
5. Антитоксическая функция. Поступающие в организм ксенобиотики (чужеродные вещества) и образующиеся в самом организме токсичные или непригодные для дальнейших превращений продукты метаболизма обезвреживаются в печени следующими способами:
метилированием (никотиновая кислота);
ацетилированием (сульфаниламидные препараты);
окислением (алкоголь, ароматические углеводороды, катехоламины, биогенные амины);
восстановлением (нитробензол);
путём синтеза мочевины (аммиак);
конъюгацией, т. е. связыванием с сильно полярными, отрицательно заряженными молекулами — активными формами глюкуроновой или серной кислот — УДФ-глюкуроновой кислотой и ФАФС (фосфоаденозинфосфосульфатом). Так метаболизируются стероидные гормоны, билирубин, продукты гниения белков в кишечнике, фенолы, желчные кислоты;
с помощью микросомной системы монооксигеназ (лекарственные препараты и канцерогены) и редуктаз (кетоны, альдегиды, красители);
с помощью ферментов пероксисомного окисления — оксидаз и каталаз (мочевая кислота, аминокислоты, лактат, пероксид водорода).
6. Роль печени в обмене желчных пигментов. Эритроциты живут приблизительно 120 дней, а затем разрушаются, главным образом, в печени, селезёнке и костном мозге, при этом разрушается и гемоглобин. Распад гемоглобина протекает в клетках макрофагов, в частности, в звёздчатых ретикулоэндотелиоцитах, а также в гистиоцитах соединительной ткани любого органа.
 НАДФН∙Н+;
О2глобинНАДФН∙Н+
НАДФН∙Н+;
О2глобинНАДФН∙Н+
гемоглобинвердоглобинбиливердинбилирубин
вит. С; цит. Р450; Fe биливердинредуктаза
гемоксигеназа
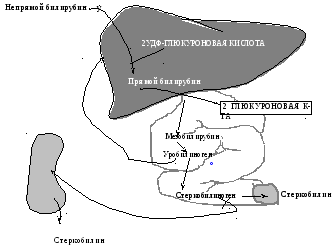
Рис. 29.1. Метаболизм желчных пигментов
Образующийся при распаде гемоглобина билирубин поступает в кровь и связывается альбуминами плазмы — это непрямой билирубин (рис. 29.1). В отличие от прямого билирубина, непрямой не даёт цветную реакцию с диазореактивом Эрлиха, пока альбумины плазмы крови не осаждены спиртом. Непрямой билирубин называется такжесвободным, поскольку его связь с альбуминами плазмы не химическая (не ковалентная), а адсорбционная. Попадая впечень, билирубин ковалентно связывается с двумя молекулами УДФ-глюкуроновой кислоты, образуя диглюкуронид билирубина, который называетсясвязанным билирубином. Связанный билирубин называется такжепрямым, поскольку он легко даёт цветную реакцию с диазореактивом Эрлиха. Прямой и небольшая часть непрямого билирубина вместес желчью поступают в тонкий кишечник, где от прямого билирубина отщепляется глюкуроновая кислота и при этом образуетсямезобилирубин. Последний в конечных отделах тонкого кишечника под воздействием микроорганизмов восстанавливается вуробилиноген, часть которого всасывается по мезентериальным сосудам и поступает в печень, где разрушается до пиррольных соединений.
Большая часть уробилиногена поступает втолстый кишечник. Уробилиноген в толстом кишечнике восстанавливается встеркобилиноген. 80 % стеркобилиногена выделяется с калом и под влиянием кислорода воздуха окисляется встеркобилин, придающий характерную окраску стулу.Меньшаячасть стеркобилиногена всасывается по нижней и средней геморроидальным венам и попадает вбольшой круг кровообращения, поступает впочки, которыми и выделяется. Под влиянием кислорода воздуха стеркобилиноген мочи также окисляется до стеркобилина. Нередко стеркобилин мочи называют уробилином (stercorous — каловый,urinary— мочевой), однако это неправильно. В норме в моче уробилин отсутствует.
Норма общего билирубина в крови — 8,55–20,52 мкмоль/л, из них более 80 % приходится на долю свободного билирубина. При повышении концентрации общего билирубина в крови более 25 мкмоль/л у человека желтеют кожные покровы, слизистые оболочки и склеры. Такое состояние называется«желтуха» (icterus)и требует врачебного вмешательства.
7. Синтез гемоглобина. Гемоглобин — сложный белок, состоящий из белка глобина и небелковой части — гема. Глобин синтезируется как обычный белок, а синтез гема представляет собой сложный многостадийный процесс, поэтому мы выделим в нём только основные этапы (рис. 29.2). Все клетки, имеющие ядро, могут синтезировать гем, но в количественном плане наиболее интенсивно синтез гема протекает в печени и костном мозге.
1
1 .
Сукцинил ~
SКоА
+ глицин δ-аминолевулиновая кислота
(δ-АЛК)
.
Сукцинил ~
SКоА
+ глицин δ-аминолевулиновая кислота
(δ-АЛК)
КоА — SН + СО2
1 = δ-аминолевулинатсинтаза (δ-АЛС)
2
2 .
2 δ-АЛК порфобилиноген ( ПБГ)
.
2 δ-АЛК порфобилиноген ( ПБГ)
2Н2О
2 = δ-аминолевулинатдегидратаза (δ-АЛД)
3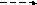 .
4 ПБГ протопорфиринIX
(ПП IX)
через ряд промежуточных стадий
.
4 ПБГ протопорфиринIX
(ПП IX)
через ряд промежуточных стадий
3
4 .
ППIX
+ Fe2
гем
.
ППIX
+ Fe2
гем
вит. В12; Cu2+
3 = гемсинтаза (феррохелатаза)
Рис. 29.2. Этапы синтеза гема
Регуляция синтеза гема. Фермент, лимитирующий скорость синтеза гема, — δ-АЛС. Она ингибируется гемом по принципу обратной связи, а активируется стероидными гормонами. Также ингибируется гемом δ-АЛД и гемсинтаза. Последняя к тому же очень чувствительна к свинцу, а δ-АЛД — вообще ко всем тяжёлым металлам.
Гем + белок → гемопротеины: гемоглобин, миоглобин, цитохромы
8. Экскреторная функция. Из печени различные вещества эндо- и экзогенного происхождения или поступают в желчные протоки и выводятся с желчью (более 40 соединений), или попадают в кровь, откуда выводятся почками.
