
- •Биосинтез белка
- •Тема 21. Современные методы молекулярной биологии
- •Тема 22. Гормоны. Общий механизм действия гормонов
- •Механизм действия гормонов, взаимодействующих
- •Механизм действия гормонов, взаимодействующих с 1-тмс-рецепторами
- •Механизм действия гормонов, взаимодействующих с внутриклеточными рецепторами
- •Тема 23. Гормоны — производные белков, пептидов и аминокислот гормоны гипоталамуса
- •Гормоны гипоталамуса
- •Гормоны аденогипофиза Это гормоны белково-пептидной природы (табл. 23.2).
- •Гормоны аденогипофиза
- •Гормоны задней доли гипофиза
- •Гормоны поджелудочной железы
- •Выделяют две формы диабета:
- •1) Инсулин-зависимый сахарный диабет (диабет 1-го типа), развивается вследствие дефицита инсулина, вызываемого аутоиммунным разрушением β-клеток поджелудочной железы;
- •2) Инсулин-независимый сахарный диабет (диабет 2-го типа), характеризуется устойчивостью к инсулину и его сниженной секрецией. Он встречается чаще, развивается у пожилых лиц.
- •Тема 24. Стероидные гормоны
- •2. Окисление и изомеризация прегненолона в прогестерон. Прегненолон является предшественником всех стероидных гормонов.
- •Половые гормоны
- •Тема 25. Биохимия питания. Макро- и микроэлементы
- •Макроэлементы
- •Концентрация электролитов вне и внутри клетки существенно различается: натрий и кальций преобладают во внеклеточном пространстве, калий и магний — внутри клетки. Кальций
- •Кальцитонин
- •Паратирин (паратгормон)
- •Витамин д (кальциферол), антирахитический
- •Микроэлементы Железо
- •Тема 26. Биохимия питания. Витамины и другие незаменимые факторы питания. Синдром недостаточного питания
- •Витамины
- •Клинические формы недостаточности питания
- •Тема 27. Биохимия соединительных тканей и органов полости рта (костная и хрящевая ткани, зубы)
- •Неколлагеновые белки костной ткани и их роль в процессах минерализации
- •Химический состав тканей зуба и кости (весовые %)
- •Тема 28. Биохимия ротовой жидкости
- •Химический состав ротовой жидкости
- •Скорость саливации и характер секрета слюны из протоков слюнных желез
- •Функции ротовой жидкости
- •Белки ротовой жидкости и их роль
- •Ферменты ротовой жидкости и их роль
- •Поверхностные образования на эмали
- •Фтор (f) и его роль в организме
- •Виды фтор-профилактики
- •Тема 29. Биохимия печени
- •Функции печени
- •Тема 30. Биохимия мышечной ткани
- •Миофибриллярные (сократительные) белки
- •Молекулярный механизм мышечного сокращения
- •Источники энергии мышечного сокращения
- •Механизмы энергообеспечения мышечного сокращения
- •Литература
- •Оглавление
- •Биологическая химия
- •220030, Г. Минск, ул. Ленинградская, 6.
Элонгация: наращивание цепи РНК осуществляет коровая полимераза.
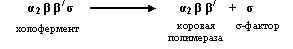
Т ерминация:
в гене имеются терминирующие
последовательности; белковый ρ (ро)-фактор
вызывает отсоединение РНК-полимеразы
от матрицы. Образовавшаяся молекула
РНК у прокариот содержит информацию о
нескольких белках (полицистронный
транскрипт) и сразу же подвергается
трансляции.
ерминация:
в гене имеются терминирующие
последовательности; белковый ρ (ро)-фактор
вызывает отсоединение РНК-полимеразы
от матрицы. Образовавшаяся молекула
РНК у прокариот содержит информацию о
нескольких белках (полицистронный
транскрипт) и сразу же подвергается
трансляции.
В ядре у эукариот имеется 3 типа РНК полимераз (I — синтезирует рРНК, II — для иРНК, III — для тРНК). Все виды РНК синтезируются в виде предшественников и нуждаются в процессинге (созревании). После процессинга РНК транспортируется из ядра в цитоплазму.
Созревание иРНК (рис. 20.4). Во время синтеза пре-иРНК происходит модификация концов молекулы — кэпирование на 5/-конце и полиаденилирование на 3/-конце. Кэп («шапочка» из трифосфометилгуанозина) и полиадениловый «хвост» защищают иРНК от действия нуклеаз. Следующим этапом созревания РНК является сплайсинг — удаление интронов (неинформативных вставок) и сшивание экзонов (информативных участков). В сплайсинге участвует малая ядерная РНК, которая содержит последовательности, комплементарные интронам.
Созревание тРНК. От предшественника тРНК отщепляются дополнительные олигонуклеотиды на 3’- и 5’-концах, вырезаются интроны, достраивается акцепторный участок (ЦЦА), формируется петля антикодона, проводится модификация нуклеотидов (образуются псевдоуридин, дигидроуридин и т. п.).
Созревание рРНК. рРНК синтезируется в виде крупных предшественников, из которых затем удаляются интроны, молекулы разрезаются на фрагменты разного размера, метилируются, объединяются с белками (образуются малая и большая субъединицы рибосом).
Ингибиторы транскрипции:
актиномицинД — препятствует раскручиванию ДНК и продвижению РНК-поли-меразы;
рифампицин — ингибирует РНК-полимеразу прокариот на этапе инициации;
α-аманитин (токсин бледной поганки) — ингибирует РНК полимеразу II эукариот.
Биосинтез белка
Трансляция — биосинтез белка на матрице иРНК. Участники трансляции: иРНК, рибосомы, белковые факторы инициации, элонгации и терминации, ГТФ, аминоацил-тРНК.
Последовательность нуклеотидов иРНК определяет последовательность включения аминокислот в синтезируемый белок. При этом одну аминокислоту кодирует последовательность из трех нуклеотидов (триплет, кодон). Существует 43 = 64 кодона (3 из них не кодируют аминокислоты — бессмысленные или нонсенс-кодоны). Общий набор кодонов составляет генетический код. Свойства генетического кода: триплетность; специфичность (1 кодон — 1 аминокислота); вырожденность (или избыточность, 61 кодон для 20 аминокис-лот); однонаправленность; неперекрывае-мость; отсутствие знаков препинания; универсальность.
Роль тРНК в биосинтезе белка: 1) транспорт аминокислот на рибосомы; 2) адапторная функция, т. е. тРНК является посредником при переводе с языка нуклеиновых кислот (последовательность нуклеотидов) на язык белков (последовательность аминокислот). Адапторная функция осуществляется благодаря наличию в структуре тРНК акцепторного участка для аминокислоты и антикодона для связи с иРНК.
Рекогниция — процесс узнавания аминокислотой своей тРНК. Специфичность связывания обеспечивает фермент АРСаза (аминоацил-тРНК-синтетаза), который катализирует 2 реакции:
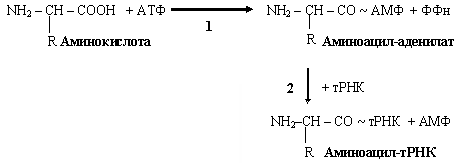

Собственно трансляция проходит в три этапа: инициация, элонгация и терминация.
Инициация: иРНК поступает на малую субъединицу рибосомы 5/-концом, к инициирующему кодону (АУГ) присоединяется первая аминоацил-тРНК (мет-тРНК), и комплекс «закрывается» большой субъединицей рибосомы. В образовании инициирующего комплекса (рис. 20.5) участвуют белковые факторы инициации (IF-1, 2, 3) и используется энергия ГТФ.
 Элонгация:
в аминоацильный участок поступает
следующая аминоацил-тРНК. Фермент
пептидилтрансфераза образует пептидную
связь между активированной карбоксильной
группой первой аминокислоты и аминогруппой
второй аминокислоты (рис. 20.6). Образованный
при этом дипептид «зависает» в
аминоацильном центре. Затем с помощью
транслоказы и энергии ГТФ рибосома
перемещается по иРНК на один кодон,
аминоацильный участок освобождается,
туда поступает новая аминокислота.
Элонгация:
в аминоацильный участок поступает
следующая аминоацил-тРНК. Фермент
пептидилтрансфераза образует пептидную
связь между активированной карбоксильной
группой первой аминокислоты и аминогруппой
второй аминокислоты (рис. 20.6). Образованный
при этом дипептид «зависает» в
аминоацильном центре. Затем с помощью
транслоказы и энергии ГТФ рибосома
перемещается по иРНК на один кодон,
аминоацильный участок освобождается,
туда поступает новая аминокислота.
Терминация наступает тогда, когда в аминоацильном участке оказывается один из терминирующих (нонсенс) кодонов. К таким кодонам присоединяются специальные белки (рилизинг-факторы), которые высвобождают синтезированный пептид и вызывают диссоциацию субъединиц рибосомы.
Многие белки синтезируются в неактивном виде (в виде предшественников) и после схождения с рибосом подвергаются постсинтетической модификации. Виды модификации белков:
частичный протеолиз (удаление N-концевого мет и сигнального пептида, образование активных форм ферментов и гормонов);
объединение протомеров и формирование четвертичной структуры белков;
образование внутри- и межцепочечных S–S связей;
ковалентное присоединение кофакторов к ферментам (пиридоксальфосфат, биотин);
гликозилирование (гормоны, рецепторы);
модификация остатков аминокислот:
гидроксилирование про и лиз (коллаген);
йодирование тир (тиреоидные гормоны);
карбоксилирование глу (факторы свертывания крови);
фосфорилирование (казеин молока, регуляция активности ферментов);
ацетилирование (гистоны);
пренилирование (G-белки).
Регуляция биосинтеза белка в клетке
Синтез белка в клетке можно регулировать на этапе транскрипции, созревания иРНК, транспорта ее из ядра в цитоплазму, изменяя стабильность иРНК, в процессе трансляции и посттрансляционной модификации. Регуляция на самых ранних этапах (на уровне экспрессии генов) является наиболее выгодной и потому широко используется.
П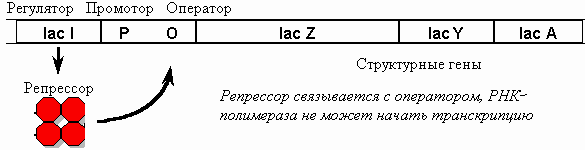 римером
регуляции экспрессии генов является
работаlac-оперона
у E.
coli.
Lac-опе-рон
содержит 3 структурных гена ферментов,
участвующих в метаболизме лактозы. В
отсутствие лактозы оперон заблокирован
белком репрессором (рис. 20.7).
римером
регуляции экспрессии генов является
работаlac-оперона
у E.
coli.
Lac-опе-рон
содержит 3 структурных гена ферментов,
участвующих в метаболизме лактозы. В
отсутствие лактозы оперон заблокирован
белком репрессором (рис. 20.7).
Рис. 20.7. Работа lac-оперона в отсутствие лактозы
В присутствии индуктора (лактозы) репрессор меняет свою конформацию и отсоединяется от ДНК. Однако если в этот момент в среде имеется глюкоза (более доступный источник энергии), транскрипция не идет. В том случае, если глюкоза отсутствует, в клетке увеличивается уровень цАМФ (сигнал «голода») и цАМФ в комплексе со специальным белком (catabolite activator protein) связывается с промотором. Только в присутствии этого белка РНК-полимераза может образовать прочную связь с промотором и начать транскрипцию (рис. 20.8).
Белковые факторы, которые способствуют связыванию РНК-полимеразы с промотором, называются факторами транскрипции.
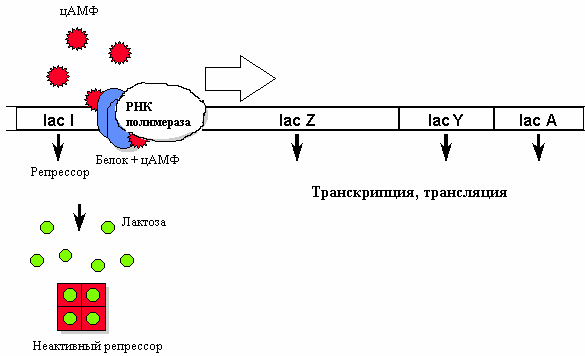
Рис. 20.8. Работа lac-оперона при наличии лактозы и в отсутствие глюкозы
Регуляторная часть генов эукариот устроена более сложно. Имеются энхансеры (элементы, усиливающие транскрипцию), сайленсеры (ослабляющие), адапторные элементы. Факторы транскрипции могут связываться с любым из этих элементов, тем самым регулировать функции генов. В качестве индукторов биосинтеза белка на генетическом уровне могут выступать не только субстраты (лактоза для лактазы), но и стероидные гормоны, жирорастворимые витамины, тиреоидные гормоны, ионы металлов и др.
