
6 курс / Кардиология / Карпов_Р_С_,_Дудко_В_А_Атеросклероз_патогенез,_клиника,_функциональная
.pdf
1.2. Липиды и липопротеины плазмы крови |
31 |
1.2.1. Дислипопротеинемия как основной патогенетический фактор атеросклероза
На первых порах главную причину накопления липидов в артери альной стенке видели только в гиперхолестеринемии, поэтому опреде лению уровня холестерина в крови придавали (и до сих пор придают) главенствующее значение в клинике при лабораторной диагностике ате росклероза. В дальнейшем было получено множество доказательств, что липиды, в том числе холестерин и его эфиры, внутри и вокруг клеток
Таблица 1.2
Фенотипирование гиперлипопротеинемий и их возможные причины [38].
Фенотип |
Уровень каких |
Первичные |
Вторичные |
|
ЛП повышен |
причины |
причины |
|
|
|
|
I |
Хиломикроны |
Дефицит |
Системная красная |
|
|
липопротеинлипазы, |
волчанка (редко) |
|
|
дефицит апо С П |
|
|
|
|
|
II а |
ЛПНП |
Семейная |
Пониженная функция |
|
|
гиперхолистеринемия |
щитовидной железы |
II б |
ЛПНП и ЛПОНП |
Комбинированная семейная |
Диабет, нефротический |
|
|
гиперхолистеринемия |
синдром, анорексия |
|
|
|
|
III |
Ремнанты |
Семейная гиперлипо |
Пониженная функция |
|
хиломикронов |
протеинемия III типа |
щитовидной железы, |
|
и ЛППП |
|
диабет, ожирение |
|
|
|
|
IV |
ЛПОНП |
Комбинированная |
Диабет, хронические |
|
|
гиперлипидемия, семейная |
заболевания почек |
|
|
гипертриглицеридемия |
|
|
|
|
|
V |
Хиломикроны |
Семейная |
Алкоголь, бета блокаторы, |
|
и ЛПОНП |
гипертриглицеридемия, |
диуретики, гормональные |
|
|
дефицит апо С П |
контрацептивы |
|
|
|
|
интимы и медии артерий происходят из липопротеинов плазмы, инфиль трующих сосудистую стенку [34 36].
В табл. 1.1 приведены показатели липидов и липопротеинов крови здоровых людей. Однако необходимо иметь в виду, что в эпидемиоло гических исследованиях только использование стандартных методов по зволяет получить сравнимые значения уровней липидов и липопротеи нов, которые определяют верхние и нижние значения показателей, со ответствующих их нормативам в репрезентативных выборках мужчин и женщин в данной географической зоне [37].
Первой и весьма успешной попыткой систематизации отклонений от нормы в липопротеиновом спектре крови явилась классификация ги
32 |
ГЛАВА 1 |
перлипопротеинемий (ГЛП), разработанная американскими учеными [38] и одобренная комитетом экспертов ВОЗ (табл. 1.2).
Из таблицы видно, что I тип ГЛП выражается в гипертриглицериде мии при избытке хиломикронов. При II типе повышается уровень холе стерина ЛПНП, а при типе IIб это дополняется умеренной формой ги пертриглицеридемии за счет возрастания ЛПОНП. Накопление ремнан тов хиломикронов и ЛПП при III м типе ГЛП приводит к увеличению содержания холестерина и триглицеридов в сыворотке. Повышение со держания триглицеридов в крови пациентов с IV типом ГЛП обусловле но накоплением ЛПОНП, часто сопровождающимся умеренной гипер холестеринемией при нормальном холестерине ЛПНП. Причиной вы раженной гипертриглицеридемии при V типе ГЛП является избыток и хиломикронов, и ЛПОНП.
Каждый из названных фенотипов может быть как первичным, так и вторичным. Генетические факторы взаимодействуют с факторами ок ружающей среды, включающими образ питания, интеркуррентные за болевания и прием лекарств. Наследственные компоненты часто явля ются полигенными и плохо поддаются определению, но тем не менее описаны три чисто наследственных нарушения – семейная гиперхоле стеринемия, семейная комбинированная гиперлипидемия и семейная гипертриглицеридемия [4,31,39].
Семейная гиперхолестеринемия вызывается доминантными мутаци ями гена, контролирующего синтез ЛПНП рецепторов, а поскольку 75% рецепторов к ЛПНП сосредоточено в печени, то именно в ней происхо дят главные изменения метаболизма липопротеинов. Отсутствие ЛПНП рецепторов существенно не сказывается на регуляции содержания хо лестерина в периферических клетках, так как в них компенсаторно ус коряется синтез холестерина. В печени же ЛПНП рецепторы использу ются, главным образом, для выведения избытка ЛПНП из кровотока. Одновременно в печени усиливается синтез холестерина и ЛПОНП. Биохимические нарушения у гетерозиготов варьируются от тяжелой ги перхолестеринемии до легких сдвигов в спектре липопротеинов, что определяет различия в скорости и тяжести клинических проявлений атеросклероза. Важно, что в случае дефицита ЛПНП рецепторов в орга низме возникает “порочный кругооборот” холестерина, так как накоп ление в печеночных клетках атерогенных ЛПНП и ЛПОНП, насыщен ных холестерином, блокирует активность ЛПНП рецепторов и выведе ние холестерина через печень. В этой ситуации организм активирует вы ведение избытка холестерина альтернативными путями – через сосуди стую стенку и клетки ретикуло эндотелиальной системы [2,4]. Гомози готная форма семейной гиперхолестеринемии лечится методом транс плантации печени в связи с почти абсолютной резистентностью к ле карственному лечению.
1.2.1. Дислипопротеинемия ... |
33 |
Семейная комбинированная гиперлипидемия вызывается одиноч ным доминантным аутосомным геном. Приблизительно треть больных имеет фенотип IIа гиперлипопротеинемии, вторая треть имеет IV й фенотип, остальные 30 40% больных имеют смешанный IIб фенотип ГЛП. Среди людей с ускоренным развитием атеросклероза на долю се мейной комбинированной гиперлипидемии приходится 15% случаев. У этих пациентов фракция ЛПНП гетерогенна по плотности, размерам частиц, спектру антигенных эпитопов, реакции с клеточными рецепто рами и скорости выведения этих частиц из кровотока. Фракции ЛПНП у таких больных имеют более высокий атерогенный потенциал и способ ны вызывать накопление липидов и эфиров холестерина в клетках, чаще всего в макрофагах [40].
Семейная гипертриглицеридемия – третье из наиболее распростра ненных генетических заболеваний, вызывающих ускоренное развитие атеросклероза через расстройства обмена липопротеинов. На долю это го генетического нарушения, которое обнаруживается лишь по дости жении полового созревания, но не выявляется у детей, приходится око ло 5% случаев ускоренного развития атеросклероза. При этом мутация аутосомно доминантного гена проявляется в значительном повышении уровня ЛПОНП и снижении уровня ЛПВП, тогда как концентрация ЛПНП в плазме крови остается нормальной.
Здесь же надо подчеркнуть, что существует лишь ограниченное чис ло дислипопротеинемий, запускающих атеросклероз. Другие мутации в сис теме обмена липидов и липопротеинов вызывают неврологические и другие расстройства [41].
Несомненное достоинство классификации Фредриксона заключалось в том, что она высветила связь нарушений обмена липопротеинов с раз витием атеросклероза и ИБС, выделив наиболее атерогенные типы ГЛП. Однако, к сожалению, в указанной классификации не были приняты во внимание сдвиги во фракции ЛПВП, полиморфизм аполипопротеинов и достаточно атерогенный самостоятельный фенотип липопротеина ЛП
(а) [4,42].
Обнаружение антиатерогенной роли ЛПВП [4,43,44], – пожалуй, одно из наиболее ярких открытий в области атеросклероза, – способ ствовало расширению представлений о нарушениях в обмене липопро теинов и привело к формированию нового понятия о дислипопротеи немиях (ДЛП) [2,43].
Дислипопротеинемия – это отклонения от нормы в липопротеино вом спектре крови, встречающиеся у человека и проявляющиеся в из менении содержания (увеличении, снижении, отсутствии) одного или более классов липопротеинов [2].
Классификация ДЛП, предложенная А.Н.Климовым [2,34], представ ляется, безусловно, более прогрессивной по сравнению с классифика
34 |
ГЛАВА 1 |
цией ГЛП, поскольку она охватывает значительно большее число вари антов отклонений от нормы в спектре липопротеинов крови и создает предпосылки для изучения более многообразных связей между наруше ниями липидного обмена, атеросклерозом и ИБС.
Необходимо подчеркнуть, что ДЛП может быть специфическим пер вичным проявлением нарушений в обмене липидов и липопротеинов, имеющих генетическую природу. Однако семейная предрасположен ность прослеживается лишь у 5 7% лиц, имеющих ДЛП, поэтому зна чительную часть составляют вторичные нарушения обмена липопроте инов, связанные с воздействием факторов внешней среды. Наряду с этим, даже при генетических нарушениях, как бы глубоки они ни были, течение и выраженность семейных ДЛП также подвержены влиянию факторов внешней и внутренней среды (алиментарных, нейрогенных, гормональных). Кроме того, ДЛП может встречаться и как сопутствую щий синдром при некоторых заболеваниях внутренних органов. Это так называемые вторичные ДЛП, выраженность которых зависит от харак тера основного заболевания, и при успешном лечении этого заболева ния показатели обмена липидов и липопротеинов нормализуются без применения гиполипидемических препаратов [34].
Среди ДЛП следует различать варианты, связанные с нарушениями обмена апо В содержащих липопротеинов (хиломикронов, ЛПОНП и ЛПНП), а также варианты, связанные с нарушением апо А содержа щих ЛПВП [2]. Кроме того, необходимо иметь в виду, что гликопроте ин содержащий липопротеин ЛП (а), имеющий не только атерогенные, но и тромбогенные свойства [22,23,42], является самостоятельным эти опатогенетическим фактором атеросклероза.
На сегодняшний день фенотипирование ДЛП является адекватным подходом в диагностике нарушений обмена липидов и липопротеинов, позволяющим выявлять среди населения лиц, предрасположенных к раз витию атеросклероза. При этом следует еще раз отметить, что наличие ДЛП, сопровождающихся повышением уровня ЛПНП и ЛПОНП, либо снижением уровня ЛПВП в крови, способствует развитию атеросклероза и ИБС [45 47].
Развитие атеросклероза и его клинических проявлений (ИБС, пере межающаяся хромота, преходящая ишемия мозга и др.) зависит не толь ко от абсолютного уровня тех или иных классов липопротеинов, но и от соотношения атерогенных и антиатерогенных липопротеинов в крови и от наличия липопротеинов, модифицированных с атерогенной направ ленностью. Для оценки соотношения атерогенных и антиатерогенных липопротеинов предложен ряд расчетных коэффициентов. Наиболее простым и в то же время достаточно информативным показателем яв ляется так называемый холестериновый индекс атерогенности (ИА), предложенный А.Н.Климовым [2] и рассчитываемый на основании оп

1.2.1. Дислипопротеинемия ... |
35 |
ределения общего холестерина (ОХС) и холестерина ЛПВП:
ИА, усл.ед. = (ОХС – ХС ЛПВП) / ХС ЛПВП.
Этот индекс практически отражает отношение содержания атероген ных липопротеинов к содержанию антиатерогенных ЛПВП в плазме крови. У новорожденных индекс атерогенности не превышает единицу,
к
20 30 годам у здоровых людей он увеличивается до 2,2 2,5 ед. У мужчин 40 60 лет без клинических проявлений атеросклероза этот показатель составляет 3 3,5 ед., а у больных ИБС – более 4 ед., достигая нередко 5 6 ед. и выше.
Соотношение между атерогенными и антиатерогенными липопро теинами может быть также оценено на основании определения содер жания в крови апопротеинов А I и В и расчета отношений апо А I к апо В или апо В к А I [4,24].
Следует отметить, что могут быть случаи, когда у пациентов с явны ми проявлениями атеросклероза содержание липидов, липопротеинов, апо протеинов и величины индекса атерогенности не выходят за пре делы нормы. В этих случаях атерогенная ситуация, очевидно, вызвана появлением модифицированных липопротеинов и изменением прони цаемости артериальной стенки [48,49].
Было бы, однако, неправильным сводить все представление об эти ологии и патогенезе атеросклероза только к одной ДЛП атерогенного характера. В целом вопрос о том, быть или не быть атеросклерозу, опре деляется взаимоотношениями липопротеинов с артериальной стенкой. При этом для формирования атеросклеротической бляшки не имеет зна чения, какие причины вызвали развитие ДЛП и привели к нарушению проницаемости стенки сосудов, – важен сам факт наличия этих сдви гов.
1.2.2.Другие факторы риска атеросклероза и ИБС
В1981 году американские ученые сделали попытку собрать воедино все факторы, которые могут влиять на возникновение и течение ИБС, и
вмировой литературе набралось 246 (!) таких факторов [50].
Внастоящее время в научную и популярную литературу прочно во шел термин “факторы риска”. К ним относятся факторы, причинно свя занные с заболеванием, влияние которых можно проследить в популя ционных исследованиях. Применительно к атеросклерозу и ИБС, по мимо гиперхолестеринемии, гипертриглицеридемии и гипоальфалипоп ротеинемии (ЛПВП), о которых было сказано выше, к факторам риска относятся следующие: 1) возраст; 2) принадлежность к мужскому полу; 3) артериальная гипертония; 4) курение; 5) сахарный диабет, нарушение

36 ГЛАВА 1
толерантности к глюкозе; 6) ожирение; 7) недостаточная физическая ак тивность; 8) особенности личности и поведения; 9) наследственные фак торы; 10) подагра; 11) мягкость питьевой воды [45,46,51].
О факторах риска написано немало книг, обзоров и статей [2,4,34,45 47,50]. Тем не менее следует, хотя бы в краткой форме, рассмотреть воз можную роль этих факторов, не как самостоятельно и независимо дей ствующих, а как способствующих развитию атеросклероза с патогене тических позиций.
С возрастом абсолютный риск развития ИБС увеличивается, и в 65 лет он значительно выше, чем в 35. Однако относительный риск воз никновения ИБС с повышением уровня холестерина в сыворотке более возрастает у 35 летних, чем у 65 летних.
У мужчин риск ИБС примерно в 3 раза выше, чем у женщин того же возраста при одинаковом уровне холестерина. Точный механизм боль шей защищенности женщин от ИБС пока не полностью ясен, возмож но, это связано с протекторной ролью эстрогенов и с более низкими по сравнению с мужчинами значениями концентрации триглицеридов и более высоким уровнем ЛПВП [2,4]. Относительная устойчивость жен щин к атеросклерозу и ИБС становится менее выраженной после мено паузы [52].
Артериальная гипертония относится к числу ведущих и твердо уста новленных факторов риска, способствующих развитию атеросклероза, а также ИБС и преходящей ишемии мозга. Специальные исследования показали, что чем выше артериальное давление, тем интенсивнее про никают липопротеины в стенку аорты и артерий. Это связано, во пер вых, с механическим повреждением эндотелиального покрова артерий и, во вторых, с гипертоническим утолщением интимы, в которой легче задерживаются и накапливаются липопротеиновые частицы [15,53]. Если имеется сочетание ДЛП атерогенного характера с гипертонией, то вероятность развития ИБС и атеросклеротических поражений артерий мозга увеличивается в несколько раз.
Курение сигарет, представляющее собой независимый фактор, дей ствует синергично с другими факторами риска – ДЛП и гипертонией. Установлено, что никотин повышает проницаемость эндотелия артерий для липопротеинов, вызывает спазм коронарных и периферических со судов и, наконец, увеличивая адгезию тромбоцитов, способствует тром бообразованию. Кроме того, в эксперименте показано, что окись угле рода, содержащаяся в табачном дыме, вызывает увеличение содержа ния холестерина в тканях [54].
Сахарный диабет, особенно его инсулиннезависимая форма, проте кает на фоне резкого увеличения синтеза холестерина и мобилизации свободных жирных кислот из жировых депо. Это ведет к повышению содержания в крови триглицеридов, ЛПОНП и к появлению высоко
1.2.2. Другие факторы риска атеросклероза и ИБС |
37 |
атерогенных модифицированных липопротеинов – гликозилированных ЛПНП [55,56]. При сахарном диабете не только возрастает заболевае мость атеросклерозом, но и отмечается его развитие в более молодом возрасте, причем утрачивается обычно присущая молодым женщинам устойчивость к ИБС [57]. Если у больного диабетом имеется еще и арте риальная гипертония, то риск возникновения мозгового инсульта воз растает примерно в 6 раз по сравнению со здоровыми людьми. Увели чивается также риск развития инфаркта миокарда и других осложнений со стороны сердечно сосудистой системы.
Ожирение (избыточная масса тела) ведет к повышению уровня ате рогенных липопротеинов в крови (особенно ЛПОНП) и очень часто – к снижению содержания антиатерогенных ЛПВП. Кроме того, ожире ние способствует развитию артериальной гипертонии, сахарного диа бета, желчнокаменной болезни и других состояний, прямо или косвен но влияющих на развитие атеросклероза [58].
Недостаточная физическая активность определяет относительную за медленность метаболических процессов, в том числе – обмена липидов и липопротеинов. Показательно, что физическая нагрузка повышает ак тивность в крови липопротеинлипазы и ЛХАТ, что приводит к ускорен ному катаболизму ЛПОНП и нарастанию уровня ЛПВП [59]. Кроме того, физические нагрузки в целом способствуют поддержанию нор мальной массы тела и снижению артериального давления, препятству ют развитию сахарного диабета.
Особенности личности и поведения определяют индивидуальную ре акцию на эмоциональные и стрессовые ситуации. Нервное напряжение, как известно, сопровождается выбросом в кровь большого количества катехоламинов. Это приводит, с одной стороны, к повышению прони цаемости эндотелия для плазменных апо В содержащих липопротеи нов, а с другой, – к активации липолиза в жировой ткани и к мобилиза ции неэстерифицированных жирных кислот, усилению синтеза тригли церидов и ЛПОНП в печени.
По наследственной линии могут передаваться: 1) тот или иной тип нарушения липопротеинового обмена; 2) предрасположенность к дру гим факторам риска, например – артериальной гипертонии, диабету; 3) уязвимость в отношении атеросклероза. И все же, одной лишь наслед ственностью поколений вряд ли можно объяснить широкое распрост ранение атеросклероза в наши дни.
Гиперурикемия (подагра) условно относится к факторам риска ате росклероза в связи с выявленной прямой корреляцией между уровнем мочевой кислоты и содержанием триглицеридов в крови [34,46].
Мягкость воды обусловливается недостаточным содержанием мик роэлементов, а дефицит ванадия, магния, марганца и хрома способствует развитию атеросклероза, который встречается у населения чаще и про
38 |
ГЛАВА 1 |
текает тяжелее, чем в районах, где употребляют жесткую воду. Резюмируя данные, изложенные в этом разделе, следует указать, что,
чем больше факторов риска одновременно воздействует на одного че ловека, тем выше вероятность развития у него атеросклероза и связан ных с ним осложнений. Согласно исследованию, проведенному в США [59], комбинация трех факторов, таких, как гиперхолестеринемия (уро вень общего холестерина более 6,5 ммоль/л, или 250 мг/дл), повышен ное диа столическое давление (выше 90 мм рт.ст.) и курение сигарет, увеличивает число случаев смерти от коронарной недостаточности в 8 раз, комбинация из двух факторов – в 4 раза и наличие одного фактора
– в 2 раза по сравнению с контрольной группой лиц того же возраста, не имеющей упомянутых выше факторов риска. Надо полагать, что при наличии четырех факторов риска и более синергизм действия возраста ет в еще большей степени. Это ставит на повестку дня организацию мно гофакторной профилактики атеросклероза в широком популяционном плане.
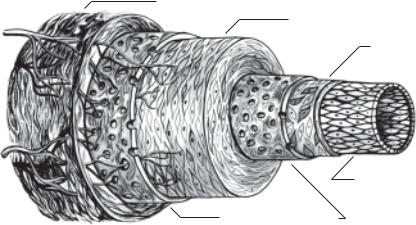
Адвентиция
Медия
Интима
Эндотелий
Эластические
пластины
Рис. 1.1. Строение стенки артерии эластического типа.

1.3. Функциональная морфология сосудистой стенки... |
39 |
1.3. ФУНКЦИОНАЛЬНАЯ МОРФОЛОГИЯ СОСУДИСТОЙ СТЕНКИ, ПУТИ ПРОНИК+ НОВЕНИЯ И ТКАНЕВОЙ ОБМЕН ЛИПИДОВ
Для правильного понимания сложных и во многом неясных патоло гических процессов, происходящих в стенке артерий при атеросклеро зе, необходимо иметь хотя бы общее представление о некоторых мор фологических и функциональных особенностях артериальных сосудов.
Общее строение стенки крупных артерий, наиболее часто и резко по ражаемых при атеросклерозе, представлено на рис. 1.1. В артериях эла стического типа, к которым относятся крупные сосуды, отчетливо вы деляются три слоя: внутренняя оболочка (интима), средняя (медия) и наружная (адвентиция), разделенные между собой эластическими пла стинами.
Внутренняя оболочка ограничена со стороны просвета сосуда одним непрерывным слоем эндотелиальных клеток, которые сцеплены друг с другом с помощью ряда контактных комплексов различных типов, за висящих от локализации и калибра сосуда. Клетки слегка перекрывают друг друга по краям, что обеспечивает некоторый клеточный резерв для поддержания непрерывности слоя при чрезмерном расширении сосуда или при других механических воздействиях, связанных с нормальной пульсацией.
С внешней стороны интима ограничена внутренней эластической мембраной – перфорированным круговым слоем эластической ткани. Отверстия диаметром 2 5 мкм во внутренней эластической мембране, по видимому, образуют специальные проходы для миграции клеток из средней оболочки в субэндотелиальное пространство. Эта точка зрения подтверждается результатами многочисленных работ, в которых пока зана морфологическая связь между фиброзно мышечной гиперплази ей внутренней оболочки, характерной для атеросклероза, и разрывами внутренней эластической мембраны.
Между эндотелием и внутренней эластической мембраной располо жено большое количество свободных компонентов соединительной тка ни, в том числе тонкая сеть соединительнотканных волокон, или ба зальный слой, который довольно слабо развит. В отдельных точках этот слой прикрепляется к эндотелию через полудесмосомы. Обычно в су бэндотелиальном пространстве между двумя слоями, ограничивающи ми интиму, лишь изредка удается обнаружить гладкомышечные клетки. Однако с увеличением возраста и в местах утолщения эндотелия (обыч но возле разветвлений сосудов) количество гладкомышечных клеток нарастает.
Средняя оболочка артерии (медия) состоит преимущественно из гладкомышечных клеток, организованных в виде множества концент
40 |
ГЛАВА 1 |
рических ламеллярных единиц. Коллаген, эластические волокна, гли козаминогликаны, окружающие гладкомышечные клетки, очевидно, вырабатываются самими клетками. Гладкомышечная клетка мультипо тентна, способна к миграции, пролиферации и синтезу веществ, что обусловливает утолщение интимы при атеросклерозе [60]. Внешняя (дальняя от просвета сосуда) поверхность средней оболочки образована наружной эластической мембраной, которая не является сплошной, а в некоторых местах может и вовсе отсутствовать. Наличие эластической ткани существенно для механической адаптации артериальной стенки
кповышению напряжения в фазе систолы и для эластического возврата
кпрежнему состоянию в фазе диастолы, что способствует более эффек тивному продвижению крови к дистальным сосудам и обеспечивает по степенное затухание пульсации потока крови в мелких сосудах.
Внешний слой стенки артерии (адвентиция) состоит из рыхлой со единительной ткани, образованной пучками коллагеновых и эластичес ких волокон вперемежку с гладкомышечными клетками и фиброблас тами. Последние являются доминирующим типом клеток в этом слое. Здесь же выявляются собственные кровеносные сосуды (vasa vasorum), проникающие внутрь стенки, приблизительно до двух третей медии. В верхнем слое медии и в адвентиции расположены периваскулярные не рвы и их окончания.
Характерными чертами крупных и средних артерий являются следу ющие. 1) Интима и внутренняя треть медии не содержат капилляров. Такая структура является уникальной для человеческого организма, она исключает возможность прямого обмена между кровью и тканями. 2) Через артериальную стенку в направлении адвентиции осуществляется постоянный, хотя и медленный, ток плазмы крови вместе с макромоле кулярными соединениями, в том числе липопротеинами. 3) Главным препятствием для прохождения макромолекулярных соединений через артериальную стенку являются эндотелиальный слой и внутренняя эла стическая мембрана. Кроме того, в артериальной стенке, в отличие от венозной, плазма крови проходит через мощные слои эластических, со единительнотканных и мышечных волокон. 4) Основная часть макро молекулярных соединений, проникших в стенку, легко метаболизирует или покидает ее через систему паравазального сосудистого русла адвен тиции. 5) В артериальной стенке, в отличие от венозной, легко созда ются условия для накопления липопротеинов. 6) Липопротеины сами по себе не оказывают повреждающего действия на сосудистую стенку, пока не произойдет их распад и высвобождение холестерина. 7) Инти ма артерий обладает высоким сродством к плазменным липопротеинам и способна накапливать их в концентрациях, превышающих таковые в плазме крови. 8) Холестерин – единственный липид, неметаболизируе мый в артериальной стенке, оказывает на нее прямое повреждающее
