
- •1. Предметы и методы химической термодинамики. Термодинамические системы, параметры, функции.
- •2. Первое начало термодинамики. Внутренняя энергия. Энтальпия. Закон Гесса и термохимические расчеты.
- •3. Второе начало термодинамики. Энтропия. Энергия Гиббса.
- •4. Химический потенциал. Термодинамические условия равновесия, прогнозирование направления самопроизвольных процессов. Энтальпийный и энтропийный факторы.
- •Внутренняя энергия
- •Энтальпия
- •Энергия Гельмгольца
- •Энергия Гиббса
- •5. Обратимые и необратимые по направлению реакции. Понятие о химическом равновесии. Константа химического равновесия и способы ее выражения. Принцип Ле-Шателье.
- •6. Роль растворов в жизнедеятельности организмов. Термодинамика растворения: энтропийный и энтальпийный факторы растворения, их связь с механизмом растворения.
- •7. Растворимость газов в жидкостях. Законы Дальтона, Генри, Сеченова. Растворимость газов в крови.
- •Роль диффузии в процессах переноса веществ в биологических системах
- •8. Слабые электролиты. Константа и степень диссоциации. Закон разведения Оствальда.
- •9. Основные положения теории сильных электролитов. Активность и коэффициент активности. Ионная сила раствора. Электролиты в организме человека.
- •10. Коллигативные свойства растворов. Закон Рауля. Осмос и осмотическое давление. Закон Вант-Гоффа.
- •Температура кипения разбавленных растворов
- •Криоскопическая и эбулиоскопическая константы
- •Осмос. Осмотическое давление разбавленных растворов
- •11. Коллигативные свойства растворов электролитов. Изотонический коэффициент, его физический смысл. Гипо-, гипер- и изотонические растворы. Роль осмоса в биосистемах. Плазмолиз и гемолиз.
- •12. Ионное произведение воды. Водородный показатель рН.
- •13. Буферные системы, их классификация и механизм действия. Уравнение Гендерсона-Гассельбаха. Буферная емкость.
- •I и II типы буферных систем
- •14. Буферные системы крови и сравнительная величина их буферной емкости. Понятие о кислотно-щелочном равновесии.
- •Кислотно-щелочное состояние.
- •15. Комплексные соединения, их изомерия, классификация и номенклатура.
- •1)По заряду комплекса: катионные, анионные и нейтральные комплексы.
- •2)По количеству комплексообразователей
- •3)По типу лиганда
- •4)По химическим свойствам: кислоты, основания, соли, неэлектролиты:
- •5)По количеству мест, занимаемых лигандом в координационной сфере
- •17. Предмет и методы химической кинетики. Скорость и константа скорости химической реакции. Закон действующих масс. Зависимость скорости реакции от температуры.
- •18. Простые и сложные реакции. Виды сложных реакций. Цепные фотохимические реакции. Роль фотохимических реакций в биологии и медицине.
- •19. Молекулярность и порядок химической реакции. Кинетические уравнения для реакции 0- и 1-го порядка. Энергия активации. Уравнение Аррениуса и энергетическая диаграмма реакции.
- •20. Основные положение теории активных соударений и теории переходного комплекса.
- •21. Гомогенный и гетерогенный катализ. Кислотно-основный катализ и роль в процессах метаболизма. Стадии гетерогенного катализа.
- •22. Ферментативный катализ.
- •23. Электродные потенциалы и механизм их возникновения. Строение двойного электрического слоя.
- •24. Уравнение Нернста для электродного потенциала и гальванического элемента.
- •25. Гальванический элемент Даниэля-Якоби. Принцип действия, эдс.
- •26. Классификация электродов. Электроды сравнения и определения. Водородный, хлорсеребряный и ионоселективные (стеклянные) электроды. Принцип их действия и электродные реакции.
- •27. Окислительно-восстановительный потенциал. Уравнение Нернста-Петерса.
- •28. Диффузный и мембранный потенциалы. Механизм действия и их роль в генерации биопотенциалов в организме.
- •29. Потенциометрия. Сущность метода и области применения в химических и медико-биологических исследованиях.
- •30. Вольтамперометрия (полярография), сущность метода и области применения в медико-биологических исследованиях.
- •31. Электропроводность растворов. Скорость движения ионов. Закон Кольрауша. Удельная и эквивалентная электропроводность.
- •32. Кондуктометрия, основные положения и область применения. Электропроводность тканей, применение в физиотерапии.
- •Органическая химия
- •33. Теория строения органических соединений а.М. Бутлерова.
- •34. Электронное строение атома углерода и виды гибридизации.
- •35. Классификация и номенклатура органических соединений.
31. Электропроводность растворов. Скорость движения ионов. Закон Кольрауша. Удельная и эквивалентная электропроводность.
Количественная характеристика электропроводности – молярная электрическая проводимость раствора λ (лямбда) – мера электрической проводимости всех ионов, образующихся при диссоциации 1 моль электролита при данной концентрации. Она численно равна электрической проводимости объема V (м3) раствора, заключенного между двумя параллельными электродами, с расстоянием между электродами 1 м, причем каждый электрод имеет такую площадь, чтобы в этом объеме содержался1 моль растворенного вещества.
Молярная и удельная электропроводности связаны соотношением:
![]()
где λ – молярная электрическая проводимость, См.м2/моль; Х – удельная электрическая проводимость, См/м; V – разведение раствора, м3/моль; C – концентрация, моль/м3.
Для практических расчетов используют уравнение:
![]()
Общий характер изменения молярной электрической проводимости с концентрацией для сильных и слабых электролитов выражен кривыми.
С увеличением разведения молярная электрическая проводимость возрастает и в области больших разведений стремится к предельному значению λ0.
Эквивалентная электропроводность λэ получается путем замены в формуле молярной электропроводности молярной концентрации на эквивалентную молярную концентрацию (нормальность):
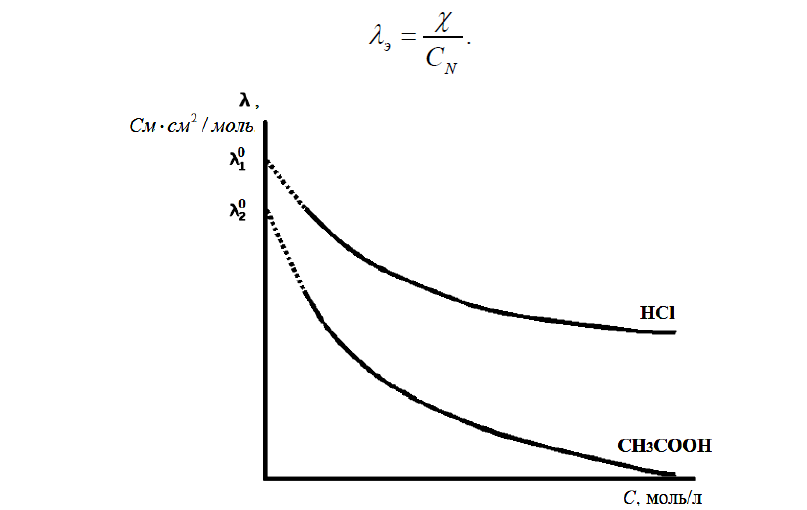
Для растворов слабых электролитов эквивалентная электрическая проводимость остается небольшой вплоть до очень низких концентраций, по достижении которых она резко поднимается до значений, сравнимых с λ сильных электролитов. Это происходит за счет увеличения степени диссоциации, которая, согласно классической теории электролитической диссоциации, растет с разбавлением и в пределе стремится к 1.
Отношение λ/λо у слабых электролитов характеризует его степень диссоциации α при данной концентрации раствора: α = λ/λо.
Закон Кольрауша
Ф. Кольрауш показал, что в молярную электропроводность бесконечно разбавленных растворов электролитов каждый из ионов вносит свой независимый вклад, и сформулировал закон независимости движения ионов: предельная молярная электрическая проводимость данного электролита равна сумме предельных молярных проводимостей ионов, входящих в его состав:
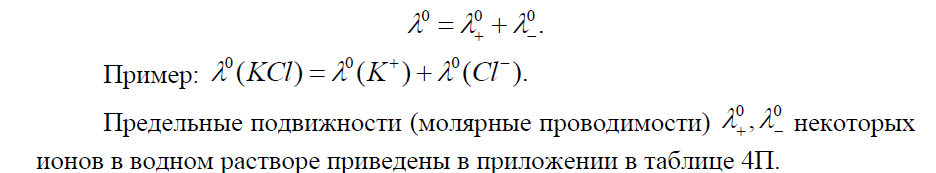
32. Кондуктометрия, основные положения и область применения. Электропроводность тканей, применение в физиотерапии.
Кондуктометрия – электрохимический метод анализа, основанный на измерении электрической проводимости растворов.
Электропроводность – это величина, обратная сопротивлению:
![]()
где R – сопротивление, Ом.
Единицей измерения электропроводности является Ом-1 или См (Сименс).
Согласно закону Ома, электрическое сопротивление проводника прямо пропорционально его длине l и обратно пропорционально площади поперечного сечения S:
![]()
где ρ – удельное сопротивление, характеризующее природу проводника
и выражаемое в Ом·м.
Поэтому
![]()
В качестве количественной меры способности раствора электролита проводить электрический ток используют обычно удельную электропроводность Х (каппа) – величину, обратную удельному сопротивлению (то есть величину, обратную сопротивлению столба раствора между электродами площадью 1 см2, находящимися на расстоянии 1 см):
![]()
Величина удельной электропроводности электролита зависит от:природы электролита, температуры, концентрации раствора.
Чем полнее диссоциация электролита, тем больше в растворе частиц, переносящих электрические заряды, и тем выше его проводимость. При повышении температуры удельная электропроводность растворов электролитов возрастает, что вызвано увеличением скорости движения ионов за счёт понижения вязкости раствора и уменьшения сольватированности ионов.
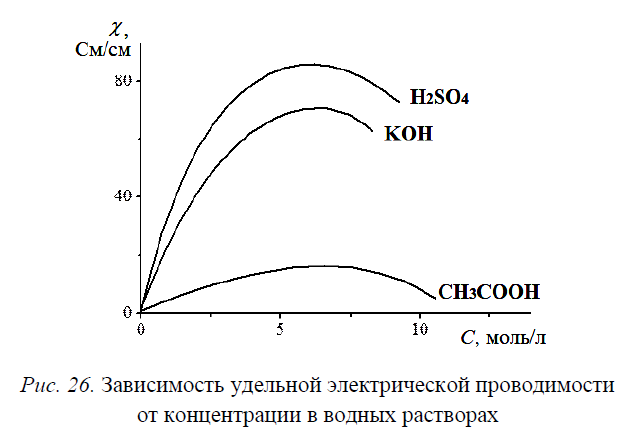
При равных концентрациях растворов проводимость растворов сильных электролитов значительно выше, чем слабых. С увеличением концентрации удельная электропроводность сначала растёт, достигает максимума и в области высоких концентраций начинается уменьшение удельной электропроводности. Для сильных электролитов это связано с увеличением вязкости растворов и усилением электростатического взаимодействия между ионами, что уменьшает скорость их движения и, соответственно, удельную электропроводность. Для слабых электролитов – с уменьшением степени диссоциации и, следовательно, уменьшением количества ионов.
Электропроводимость Биологические ткани и органы являются довольно разнородными образованиями с различными электрическими сопротивлениями, которые могут изменяться при действии электрического тока. Это обуславливает трудности измерения электрического сопротивления живых биологических систем. Электропроводимость отдельных участков организма, находящихся между электродами, наложенными непосредственно на поверхность тела, существенно зависит от сопротивления кожи и подкожных слоев. Внутри организма ток распространяется в основном по кровеносным и лимфатическим сосудам, мышцам, оболочкам нервных стволов. Сопротивление кожи, в свою очередь, определяется ее состоянием: толщиной, возрастом, влажностью и т.п. Электропроводность тканей и органов зависит от их функционального состояния и, следовательно, может быть использована как диагностический показатель. Так, например, при воспалении, когда клетки набухают, уменьшается сечение межклеточных соединений и увеличивается электрическое сопротивление. Непрерывный постоянный ток напряжением 60-80 В используют как лечебный метод физиотерапии(гальванизация). Постоянный ток используют в лечебной практике также и для введения лекарственных веществ через кожу или слизистые оболочки. Этот метод получил название электрофореза лекарственных веществ. Для этой цели поступают так же, как и при гальанизации, но прокладку активного электрода смачивают раствором соответствующего лекарственного вещества. Лекарство вводят с того полюса, зарядом которого оно обладает: анионы вводят с катода, катионы с анода.
